Documente Academic
Documente Profesional
Documente Cultură
Anexa 1 PROGRAME OLIMP 2014 2015
Anexa 1 PROGRAME OLIMP 2014 2015
Încărcat de
Anonymous B1v10EcSd0 evaluări0% au considerat acest document util (0 voturi)
2 vizualizări2 paginiolimpiade
Titlu original
Anexa_1_PROGRAME_OLIMP_2014_2015
Drepturi de autor
© © All Rights Reserved
Formate disponibile
PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentolimpiade
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
2 vizualizări2 paginiAnexa 1 PROGRAME OLIMP 2014 2015
Anexa 1 PROGRAME OLIMP 2014 2015
Încărcat de
Anonymous B1v10EcSdolimpiade
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 2
PROGRAMELE PENTRU OLIMPIADA DE CHIMIE
AN ŞCOLAR 2014 – 2015
Anexa 1 CLASELE a VIII-a, a IX-a, a X-a, a XI-a, a XII-a
PERIOADA PROGRAMA
DE
ETAPA
DESFĂŞU- a VIII-a a IX-a a X-a a XI-a a XII-a
RARE
Hidrogenul, Structura învelişului electronic pentru Formule brute. Izomeria Termochimie : Entalpie de
oxigenul, carbonul, elementele din perioadele 1, 2, 3, 4. Formule compuşilor reacţie. Căldură de combustie -
sulful, aluminiul, Corelaţii între structura învelişului moleculare. organici ( de arderea combustibililor
fierul şi cuprul – electronic, poziţia în tabelul periodic şi Structura constituţie, Căldură de neutralizare (acid
proprietăţi fizice şi proprietăţi ale elementelor. Variaţia sterică) tare – bază tare);Legea Hess;
compuşilor
chimice, utilizări. proprietăţilor periodice ale elementelor, Compuşi Căldură de dizolvare.
Oxizi ai în grupele principale şi în perioadele 1, organici. halogenaţi. Cinetica chimică: Viteză de
nemetalelor şi 2, 3,4. Alcani. Compuşi reacţie. Legea vitezei;
Ianuarie
locală metalelor- Legătura ionică. Legătura covalentă Alchene. hidroxilici. Catalizatori. Inhibitori;
2015 proprietăţi fizice şi polară şi nepolară. Legătura Diene. Amine. Acizi Influenţa concentraţiei,
chimice, utilizări. coordinativă. Legătura de hidrogen. Alchine. carboxilici. temperaturii, catalizatorilor
Forţe van der Waals. Legile gazelor. asupra vitezei de reacţie;
Ecuatia de stare a gazului ideal. ecuaţia Arrhenius.
Densitatea absolută si relativă a Reacții redox. Potenţiale
gazelor. standard de reducere. Pile
electrice. Electroliza soluțiilor
apoase și a topiturilor.
Hidrogenul, Structura învelişului electronic pentru Formule brute. Izomeria Termochimie : Entalpie de
oxigenul, carbonul, elementele din perioadele 1, 2, 3, 4. Formule compuşilor reacţie. Căldură de combustie -
sulful, aluminiul, Corelaţii între structura învelişului moleculare. organici ( de arderea combustibililor
fierul şi cuprul – electronic, poziţia în tabelul periodic şi Structura constituţie, Căldură de neutralizare (acid
proprietăţi fizice şi proprietăţi ale elementelor. Variaţia sterică) tare – bază tare); Legea Hess;
compuşilor
chimice, utilizări. proprietăţilor periodice ale elementelor, Compuşi Căldură de dizolvare;
Oxizi ai în grupele principale și secundare şi în organici. halogenaţi. Energia în sistemele biologice.
21 februarie nemetalelor şi perioadele 1, 2, 3,4. Alcani. Compuşi Rolul ATP şi ADP. Arderea
judeţeană metalelor- Legătura ionică. Legătura covalentă Cicloalcani. hidroxilici. zaharurilor și lipidelor;
2015 proprietăţi fizice şi polară şi nepolară. Legătura Alchene. Amine. Acizi Cinetica chimică: Viteză de
chimice, utilizări. coordinativă. Legătura de hidrogen. Diene. carboxilici. reacţie. Legea vitezei; ordinul
Acizi - proprietăţi Forţe van der Waals. Dizolvarea şi Alchine. Compuşi reacțiilor
fizice şi chimice, factorii care influenţează dizolvarea. Arene. carbonilici. Catalizatori. Inhibitori;
utilizări. Solubilitatea. Soluţii apoase . Influenţa concentraţiei,
Concentraţia molară. Cristalohidraţi. temperaturii, catalizatorilor
Legile gazelor. Ecuatia de stare a asupra vitezei de reacţie;
1
gazului ideal. Densitatea absolută si ecuaţia Arrhenius.
relativă a gazelor. Reacții redox. Potenţiale
standard de reducere. Pile
electrice. Electroliza soluțiilor
apoase și topiturilor.
Hidrogenul, Structura învelişului electronic pentru Formule brute. Izomeria Termochimie : Entalpie de
oxigenul, carbonul, elementele din perioadele 1, 2, 3, 4. Formule compuşilor reacţie. Căldură de combustie -
sulful, aluminiul, Corelaţii între structura învelişului moleculare. organici ( de arderea combustibililor
fierul şi cuprul – electronic, poziţia în tabelul periodic şi Structura constituţie, Căldură de neutralizare (acid
proprietăţi fizice şi proprietăţi ale elementelor. Variaţia sterică) tare – bază tare);
compuşilor
chimice, utilizări. proprietăţilor periodice ale elementelor, Compuşi Legea Hess;
Oxizi ai în grupele principale şi în perioadele 1, organici. halogenaţi. Căldură de dizolvare;
nemetalelor şi 2, 3,4. Alcani. Compuşi Energia în sistemele
metalelor- Legătura ionică. Legătura covalentă Cicloalcani. hidroxilici. biologice. Rolul ATP şi ADP.
proprietăţi fizice şi polară şi nepolară. Legătura Alchene. Amine. Acizi Arderea zaharurilor și
chimice, utilizări. coordinativă. Legătura de hidrogen. Diene. carboxilici. lipidelor;
Acizi - proprietăţi Forţe van der Waals. Dizolvarea şi Alchine.Arene. Compuşi Cinetica chimică: Viteză de
fizice şi chimice, factorii care influenţează dizolvarea. Alcooli. Acizi carbonilici. reacţie. Legea vitezei; ordinul
utilizări. Solubilitatea. Soluţii apoase. carboxilici. Derivaţi reacțiilor
5– 11 aprilie Hidroxizi - Concentraţia molară. Cristalohidraţi. funcţionali ai Catalizatori. Inhibitori;
naţională 2015 proprietăţi fizice şi Legile gazelor. Ecuatia de stare a compuşilor Influenţa concentraţiei,
chimice, utilizări. gazului ideal. Densitatea absolută şi carboxilici. temperaturii, catalizatorilor
Galați Săruri - proprietăţi relativă a gazelor. Soluţii apoase de Compuși asupra vitezei de reacţie;
fizice şi chimice, acizi (tari şi slabi) şi baze (tari şi organici cu ecuaţia Arrhenius.
utilizări. slabe); pH-ul soluţiilor apoase. Reacții funțiuni mixte. Reacții redox. Potenţiale
Identificarea redox și aplicații ale acestora. Efecte standard de reducere. Pile
cationilor şi Identificarea cationilor şi anionilor. electronice. electrice. Electroliza soluțiilor
anionilor. Titrări acido-bazice. Mecanisme de apoase și topiturilor.
reacţie. Soluţii apoase de acizi (tari şi
slabi) şi baze (tari şi slabe);
pH-ul soluţiilor apoase
Combinațiii complexe. Titrări
acido-bazice. Titrări bazate pe
reacții de precipitare. Titrări
redox.
Notă : Subiectele de la fiecare etapă pot conţine teme din clasele anterioare.
Inspector general,
Daniela Bogdan
S-ar putea să vă placă și
- Fisa de Citate MaraDocument2 paginiFisa de Citate MaraCristina Ciortan84% (45)
- AlcaniDocument6 paginiAlcaniLaura Bajan100% (1)
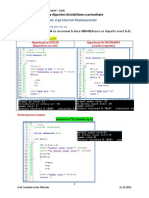
- Fisa10-Algoritmi Divizibilitate Si Prelucrari FundamentaleDocument6 paginiFisa10-Algoritmi Divizibilitate Si Prelucrari FundamentaleLaura BajanÎncă nu există evaluări
- Fisa Citate Borges, Arghezi, SimionescuDocument1 paginăFisa Citate Borges, Arghezi, SimionescuLaura BajanÎncă nu există evaluări