Documente Academic
Documente Profesional
Documente Cultură
Sindrome Hiperglucemico Hiperosmolar No Cetosico
Încărcat de
Analeticia Mendoza0 evaluări0% au considerat acest document util (0 voturi)
202 vizualizări5 paginiDrepturi de autor
© Attribution Non-Commercial (BY-NC)
Formate disponibile
PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Attribution Non-Commercial (BY-NC)
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
202 vizualizări5 paginiSindrome Hiperglucemico Hiperosmolar No Cetosico
Încărcat de
Analeticia MendozaDrepturi de autor:
Attribution Non-Commercial (BY-NC)
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 5
SÍNDROME HIPERGLUCÉMICO HIPEROSMOLAR
NO CETÓSICO
Autores Dr. Douglas Espinosa González
Dr. David Lozano Valdés
Dr. René Zamora Marín
Dr. Edmundo Rivero Arias
Dra. Miriam González Sánchez
Servicio Unidad de Cuidados Intensivos-8 (UCI-8)
Participan Endocrinología, Laboratorio Clínico, Imagenología
INTRODUCCIÓN
El síndrome hiperglucémico hiperosmolar (SHH) descrito por primera vez hace ya
más de un siglo por Dreschfeld, recibió poca atención hasta la segunda mitad del
siglo pasado cuando Sament y Schwarts informaron su experiencia con un
síndrome diabético caracterizado por alteraciones de la conciencia, hiperglucemia
marcada e hiperosmolaridad plasmática en ausencia de cetosis.
A pesar de algunas diferencias clínicas y epidemiológicas, hoy día existe una
tendencia universal de estudiar este síndrome asociado con la cetoacidosis
diabética (CAD) como parte indisoluble de un trastorno metabólico que comparte
un sustrato común (el déficit de insulina); ejemplo de ello es la serie de Watchel y
col. donde 22 % de los pacientes con crisis hiperglucémicas tenían CAD, 45 %
tenían SHH y 32 % compartían aspectos clínicos de ambas.
La mayoría de los pacientes que sufren un SHH son adultos entre 55-75 años de
edad, con una diabetes mellitus tipo II no diagnosticada. Si tenemos en cuenta
además la tendencia actual de la población cubana a alcanzar una esperanza de
vida superior a los 70 años, con un incremento de la incidencia de las
enfermedades crónicas no transmisibles, entre las que se encuentra la diabetes
mellitus, de la que el 0,05 % de todas las internaciones hospitalarias por esta
entidad cumple con los criterios de un SHH que acarrea una mortalidad que oscila
entre 5-35 % según las series(muy superior que la de la CAD), tendremos una idea
del problema al cual se enfrentan los servicios de salud y en especial los cuidados
progresivos con elevados costos, que se derivan del proceso asistencial; es por ello
que se precisa protocolizar la actuación clínica ante esta entidad con el objetivo de
estandarizar normas lo cual redunda en una mejor atención médica.
OBJETIVOS
• Reducir la mortalidad por SHH en 25 %.
• Disminuir la estadía hospitalaria por SHH.
• Racionar los recursos disponibles en el proceso de la atención médica.
• Obtener una reducción global de los costos por paciente en 10 %.
DESARROLLO
Definición
Se define este síndrome en presencia de alteraciones del sensorio acompañadas de
hiperglucemias > 600 mg/dL (33.3 mMol/L), hiper osmolaridad plasmática>de 320
mosM/kg agua, nivel de bicarbonato sérico > 15 mEq/L y pH >7,30 en ausencia o
escasa presencia de cuerpos cetónicos.
Tratamiento
Dada la gravedad de este síndrome así como la alta mortalidad que acarrea el
mismo estos pacientes deben ser trasladados de inmediato a una unidad de
cuidados progresivos que permita un monitoreo intensivo.
Medidas generales
• Establecer de inmediato una línea venosa preferentemente central.
• Monitorizar frecuentemente la presión venosa central (PVC).
• En caso de coma ó convulsiones generalizadas, proceder a la protección de
la vía aérea, para prevenir la broncoaspiración.
• Colocar una sonda Foley con el objetivo de monitorear la diuresis.
• Realizar balance hídrico cada 12 horas.
• Establecer seguimiento controlando la glucosa en sangre.
• Balance de ingresos y egresos cada una hora.
• Cada dos horas dosificar gases e iones en sangre.
• Monitoreo de los parámetros vitales horarios.
• Realizar Rx tórax y ECG el cual se repetirá según criterio medico.
• Sonda nasogástrica con el objetivo de descomprimir el estómago.
• En caso de alta sospecha clínica de sepsis o presencia de fiebre: recolectar
muestras para análisis bacteriológicos en sangre y orina.
• Soporte ventilatorio. (ver protocolo de ventilación mecánica).
• Administrar: sucralfato (tab-1 g/sobres 1g) 1 g cada 6 h.
• Como alternativas, utilizar medicamentos con acción anti-H2 como la
ranitidina (amp-50 mg) a dosis de 150 mg EV cada 12 h ó cimetidina (amp
300 mg), administrar 300 mg cada 6 u 8 h o en su defecto, inhibidores de
la bomba de protones de H, como el omeprazol (bulbos de 40 mg y
cápsulas de 20 mg), dosis de 20-60 mg-día.
• Utilizar medidas antiescaras cuando proceda.
• Se realizará profilaxis del tromboembolismo pulmonar, mediante el uso de
medios mecánicos y/o anticoagulación con heparinas de bajo peso
molecular (ver protocolo de profilaxis de tromboembolismo).
Reposición de fluidos
La mayoría de los pacientes con SHH muestran signos clínicos de una
deshidratación severa con déficit estimados de 8-12 litros. La fluidoterapia inicial se
debe comenzar con:
• Solución salina fisiológica (ClNa 0,9 %) a razón de 500-1 000 mL/h durante
una o dos horas.
En pacientes con una hipertonicidad extrema e inestabilidad hemodinámica
comenzar con:
• Solución salina fisiológica (ClNa 0,45 %)
Una vez estabilizada la tensión arterial se debe continuar con:”
• ClNa 0,45% a razón de 200-500 mL/h tratando de reponer la mitad del
déficit estimado en las primeras 12-24 h.
Para calcular el déficit de agua, hacerlo en base a los niveles de Na plasmático
según la fórmula:
ACT1 X Na1 = ACT2 X Na2
Dónde:
ACT1= (agua corporal ideal) 60 % del peso basal (kg) expresado en litros
Na1 = Na ideal (140 mEq/L)
Na2 = Na actual
ACT2= Agua actual
Ejemplo: Paciente 70 kg con Na actual de 150 mEq/L ∴
ACT1= 60 % X 70 Kg / 100 %
ACT1= 42 L
ACT2= ACT1 X Na1/ Na2
ACT2= 42 L X 140 mEq/150 mEq
ACT2= 39,2 L
Déficit de agua =ACT1 – ACT2
Déficit de agua = 42 L – 39,2 L= 2,8 L
Tratamiento con insulina
• Bolo inicial de insulina simple 0,1-0,2 U/kg
• Continuar con 0,1 U/kg/h en infusión continua, hasta
glucosa en 250 mg/dL (13,8 mMol/L)
• Entonces reducir infusión a 0,05 U/kg/h
(Comenzar a administrar dextrosa 5 % para prevenir la hipoglucemia)
Esta estrategia se mantendrá hasta obtener concentraciones de glucosa en sangre
de 200 mg/dL (11,1 mMol/L).
De no obtenerse una disminución o incluso de aumentar los niveles de glucosa:
• Duplicar la dosis de insulina a intervalos de dos horas.
• Mantener la infusión de insulina hasta que el paciente esté hemodinámica
mente estable, se alimente por vía oral y tenga un buen nivel de conciencia.
• Algunos autores preconizan el uso de insulina subcutánea una vez que se
ha alcanzado glucemias de 250 mg/dL.
Reposición de electrolitos
• Potasio: se estima que el déficit de potasio total oscila alrededor de los 5
mEq/kg de peso corporal. La reposición de potasio se debe comenzar tan
pronto se restituya la diuresis y la concentración plasmática de potasio baje
a 5 mEq/L a razón de 20-30 mEq/h, manteniendo los niveles entre 4-5
mEq/L. Evitar mediante el monitoreo del potasio en sangre descensos
bruscos del mismo.
• Fosfato: el fosfato se mantiene falsamente dentro de valores normales, a
pesar del déficit existente que se estima en 1 mEq/L. En caso de
hipofosfatemias severas, se debe agregar 20-30 mEq/L de fosfato de potasio
a los líquidos de reposición. Es necesario en este caso monitorizar
cuidadosamente los niveles séricos de Ca que pueden descender
súbitamente durante el tratamiento con fosfato.
EVALUACIÓN Y CONTROL
Indicadores de estructura Plan % Bueno Regular Malo
Recursos Personal que compone el grupo
95 95 -- < 80
humanos de trabajo asistencial
Aseguramiento instrumental y
95 95 -- < 80
equipos médicos según PA
Recursos Disponer de los medicamentos
95 95 -- < 80
materiales expuestos en el PA
Disponer de los recursos para la
95 95 -- < 80
aplicación de investigaciones
Disponibilidad diseño organizati-
95 95 -- < 80
Organiza- vo para aplicar el PA
tivos Planilla recogida datos del PA 100 100 - <100
Base de datos electrónica 100 100 - <100
Indicadores de procesos Plan % Bueno Regular Malo
% pacientes con diagnóstico de CHH/Pacien-
≥ 95 ≥ 95 85-95 < 85
tes con sospecha de CHHA
% pacientes cuyos datos fueron vinculados
≥ 95 ≥ 95 85-95 < 85
con el score APACHE
% pacientes con estadia según plan ≥ 95 ≥ 95 85-95 < 85
% pacientes interconsultados c/Endocrinolo-
≥ 95 ≥ 95 85-95 < 85
gía según necesidad/pacientes con CHH
Indicadores de resultados Plan % Bueno Regular Malo
% tasa de infecciones <5 <5 5-10 > 10
% tasa de fallecidos por SHH <5 <5 - >5
Información a pacientes y familiares
• Se informará a los familiares, el estado de los pacientes con una frecuencia
de dos veces por día.
• Se incluirá, en la medida de lo posible, en estas entrevistas criterios
pronósticos sobre cada caso.
• Cuando se considere pertinente, se le ofrecerá una información adecuada al
paciente de forma ética y profesional.
• En caso de algún proceder que ponga potencialmente en peligro la vida del
paciente, se utilizará un protocolo de consentimiento informado
confeccionado al efecto.
Bibliografía
1. Lobesio C: Síndrome hiperglucémico hiperosmolar. Texto de medicina
Intensiva. 5ta Ed. 2000; 95:1050-54.
2. Jiménez Murillo J, Barca C de la, Romero M, Montero F J. Coma hiperosmolar
en Medicina de urgencia. En: Jiménez Murillo J, Montero F J. Guía diagnóstica y
protocolo de actuación.2da. Ed. Madrid: Harcourt, 1999: 403-5.
3. Remuñan C, Álvarez JL: Coma Hiperosmolar. Rev Cubana Med 2001;
40(3):189-94.
4. Shoemaker LW: Critical Care Medicine. 3era Ed. Text Book of Critical Care.
Philadelphia Saunders. 2000; 71:783-85
5. Soler Morejón C: Coma hiperosmolar en: Temas Actualizados en: Rev Cubana
Med 1999; 38(3):183-7.
Villanueva V. Complicaciones agudas de la diabetes mellitas. Rev de postgrado de
la VI Cátedra de Medicina, 2003; 130:19-24.
S-ar putea să vă placă și
- Metabolismo CerebralDocument14 paginiMetabolismo CerebralJosurer NrtÎncă nu există evaluări
- ENDOCRINOLOGIADocument11 paginiENDOCRINOLOGIAvanessaÎncă nu există evaluări
- Estado Hiperosmolar No Cetósico (HHS)Document12 paginiEstado Hiperosmolar No Cetósico (HHS)Gloria Pg Montze100% (1)
- Hipogonadismo MasculinoDocument8 paginiHipogonadismo MasculinoHI CAÎncă nu există evaluări
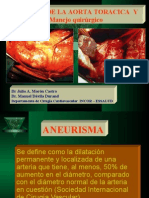
- Aneurisma de Aorta Toracica - AbdominalDocument61 paginiAneurisma de Aorta Toracica - Abdominaljft842Încă nu există evaluări
- Insuficiencia Renal AgudaDocument9 paginiInsuficiencia Renal AgudaAlexandra PiñeroÎncă nu există evaluări
- Hipertensión Portal para SeminarioDocument70 paginiHipertensión Portal para SeminarioCiro Calviño EstradaÎncă nu există evaluări
- Esteatohepatitis No AlcoholicaDocument7 paginiEsteatohepatitis No AlcoholicaJesus LunaÎncă nu există evaluări
- Endometriosis 100317220928 Phpapp01Document39 paginiEndometriosis 100317220928 Phpapp01Herssel Ciro Huamanquispe Tunque100% (1)
- 5 CRISIS HIPERTENSIVAS AzulDocument42 pagini5 CRISIS HIPERTENSIVAS AzulEloisa HernandezÎncă nu există evaluări
- Enfermdedad de CushingDocument20 paginiEnfermdedad de CushingYESICA YESSENIA ACEBEDO AMASIFUENÎncă nu există evaluări
- Sd. MieloproliferativosDocument8 paginiSd. MieloproliferativosCarlos Astete BórquezÎncă nu există evaluări
- 11 Linfangioma e Higroma Quc3adstico Del CuelloDocument77 pagini11 Linfangioma e Higroma Quc3adstico Del Cuellojorge138Încă nu există evaluări
- Resumen. Hiper e Hipoparatiroidismo PDFDocument15 paginiResumen. Hiper e Hipoparatiroidismo PDFGarcía PérezÎncă nu există evaluări
- Enfermedad Hipertensiva Del Embarazo2Document36 paginiEnfermedad Hipertensiva Del Embarazo2Alejandra FordÎncă nu există evaluări
- Hipo e HiperparatiroidisimoDocument10 paginiHipo e HiperparatiroidisimoVerónica Duménez JofréÎncă nu există evaluări
- PALS 2.en - EsDocument36 paginiPALS 2.en - EsalexaÎncă nu există evaluări
- Tetralogía de FallotDocument5 paginiTetralogía de FallotJose Carlos Sanchez ArvizuÎncă nu există evaluări
- Tumor de WarthinDocument6 paginiTumor de WarthinAndyRamosLopezÎncă nu există evaluări
- PropedeuticaDocument43 paginiPropedeuticaAndryk ZazuetaÎncă nu există evaluări
- Estado Hiperglicemico HiperosmolarDocument34 paginiEstado Hiperglicemico HiperosmolarDrkruyÎncă nu există evaluări
- 11 Protocolo Diagnóstico de Las Adenopatías CervicalesDocument4 pagini11 Protocolo Diagnóstico de Las Adenopatías CervicalesAnthony Salazar RodríguezÎncă nu există evaluări
- EapDocument33 paginiEapsofistanleyÎncă nu există evaluări
- Anemias PresentacionDocument15 paginiAnemias PresentacionKren Ciisf GuerreroÎncă nu există evaluări
- HIPOPITUITARISMODocument64 paginiHIPOPITUITARISMODämon CastroÎncă nu există evaluări
- Un Paciente Con Adenopatías CervicalesDocument10 paginiUn Paciente Con Adenopatías CervicalesDiego Ferrer MonteroÎncă nu există evaluări
- HTA, Crisis Hipertensiva y ArritmiasDocument82 paginiHTA, Crisis Hipertensiva y ArritmiasAny Armenta100% (1)
- Evc IsquemicoDocument8 paginiEvc IsquemicoAldo EscsanÎncă nu există evaluări
- Caso SIRADocument3 paginiCaso SIRAMimee MBÎncă nu există evaluări
- Sifilis GestacionalDocument5 paginiSifilis GestacionalAnyelii08Încă nu există evaluări
- Enfermedades Suprarrenales 2010-I Seccion A PubDocument22 paginiEnfermedades Suprarrenales 2010-I Seccion A Pubpablo88pazexÎncă nu există evaluări
- Edema Pulmonar Cardiogenico CuadrosDocument4 paginiEdema Pulmonar Cardiogenico CuadrosboobaluuuÎncă nu există evaluări
- HIPOPARATIROIDISMODocument5 paginiHIPOPARATIROIDISMOAndrés Sebastián González Hidalgo100% (1)
- Cor PulmonaleDocument12 paginiCor Pulmonaledel_piero7399336Încă nu există evaluări
- Insuficiencia Renal AgudaDocument31 paginiInsuficiencia Renal AgudaJosé María PalaciosÎncă nu există evaluări
- Hemorragia Uterina Anormal Expo de ClaseDocument16 paginiHemorragia Uterina Anormal Expo de ClaseMaria Paula Cano RomeroÎncă nu există evaluări
- Vih y Embarazo AngelaDocument11 paginiVih y Embarazo AngelaJULIAN DARIO AGUILERA TERCEROÎncă nu există evaluări
- Clase 6 - Insuficiencia CoronariaDocument70 paginiClase 6 - Insuficiencia CoronariaMario Chappa0% (1)
- Crisis Hipertensiva Maicol CortezDocument38 paginiCrisis Hipertensiva Maicol CortezMaicolCortezSandovalÎncă nu există evaluări
- Intoxicacion Por AcetaminofenDocument24 paginiIntoxicacion Por AcetaminofenJose QuinteroÎncă nu există evaluări
- Trombocitopatias PDFDocument11 paginiTrombocitopatias PDFGregory LeonÎncă nu există evaluări
- Caso Clinico - Cancer de ColonDocument11 paginiCaso Clinico - Cancer de ColonGarcia Yepez Stephanie GraceÎncă nu există evaluări
- Alteraciones Del Fosforo Hipo e HiperfosfatemiaDocument23 paginiAlteraciones Del Fosforo Hipo e HiperfosfatemiaMiguel Angel Mamani AlanocaÎncă nu există evaluări
- Nefropatia DiabeticaDocument37 paginiNefropatia DiabeticaCesia Angelica CarrascoÎncă nu există evaluări
- Intoxicación Por Metanol y EtanolDocument25 paginiIntoxicación Por Metanol y EtanolMaria Alejandra Casañas CorreaÎncă nu există evaluări
- Otorrino Otitis MediaDocument44 paginiOtorrino Otitis MediaJulio CedeñóÎncă nu există evaluări
- Tromboembolia PulmonarDocument24 paginiTromboembolia PulmonarAnnia Valdivia100% (1)
- Polirradiculoneuritis Aguda 2018 X Dr. Cristian Carpio BazánDocument43 paginiPolirradiculoneuritis Aguda 2018 X Dr. Cristian Carpio BazánCristian Carpio100% (1)
- EPOC en UrgenciasDocument46 paginiEPOC en Urgenciaswww.pacourgencias.blogspot.com/Încă nu există evaluări
- HTA en Pediatria en 2021Document52 paginiHTA en Pediatria en 2021Spike BuffayÎncă nu există evaluări
- Trastornos Hipertensivos en El EmbarazoDocument28 paginiTrastornos Hipertensivos en El EmbarazoBruno Guerrero ArismendizÎncă nu există evaluări
- Sindrome EdematosoDocument32 paginiSindrome EdematosoGeancarlo Vásquez MartinezÎncă nu există evaluări
- Trauma de ExtremidadesDocument17 paginiTrauma de ExtremidadesLizette Trochez LinceÎncă nu există evaluări
- Nefritis LúpicaDocument33 paginiNefritis LúpicaCeleste Caldera EscobarÎncă nu există evaluări
- ChoqueDocument25 paginiChoqueJoely OcampoÎncă nu există evaluări
- Síndrome de CushingDocument2 paginiSíndrome de CushingAndreaÎncă nu există evaluări
- GluconeogénesisDocument10 paginiGluconeogénesisSandra RiveraÎncă nu există evaluări
- Sindrome Hiperglucemico Hiperosmolar No CetosicoDocument5 paginiSindrome Hiperglucemico Hiperosmolar No CetosicoHeiser LlanosÎncă nu există evaluări
- IAP Personalizar CuidadosDocument9 paginiIAP Personalizar CuidadosAdleys CoraspeÎncă nu există evaluări
- InfectologiaDocument48 paginiInfectologiaJoel HuazoÎncă nu există evaluări
- Soporte Vital Básico Pediátrico, Embarazo y TraumaDocument23 paginiSoporte Vital Básico Pediátrico, Embarazo y TraumaManuel MontalvoÎncă nu există evaluări
- Guía de Estudio de Bioetica Colome UasdDocument3 paginiGuía de Estudio de Bioetica Colome UasdYamiley CarmelleRenaudÎncă nu există evaluări
- SVCA Síndromes Coronarios Agudos y Accidente CerebrovascularDocument9 paginiSVCA Síndromes Coronarios Agudos y Accidente CerebrovascularAbraham VillarÎncă nu există evaluări
- 2011-3.3.2-11. Presentacion de MelaDocument13 pagini2011-3.3.2-11. Presentacion de MelaJass SÎncă nu există evaluări
- Terminología ObstétricaDocument27 paginiTerminología ObstétricaVictor Castro0% (2)
- Formato ProfesiogramaDocument1 paginăFormato ProfesiogramaJose Lozano Joven100% (3)
- SEMANA 11 - Campos Laborales de Desempeño Del Q.F.Document12 paginiSEMANA 11 - Campos Laborales de Desempeño Del Q.F.miguel angelÎncă nu există evaluări
- Bacterias Gram Positivas y Gram NegativasDocument5 paginiBacterias Gram Positivas y Gram NegativasGleyrim Germán100% (1)
- Colombia Impone La Primera Demanda A Nivel Andino Contra Laboratorios Por La Venta de VacunasDocument71 paginiColombia Impone La Primera Demanda A Nivel Andino Contra Laboratorios Por La Venta de VacunasKaren HernándezÎncă nu există evaluări
- Aseo de UnidadDocument2 paginiAseo de UnidadJuan Pablo Hermosa88% (16)
- FamiliaDocument10 paginiFamiliaLore LeónÎncă nu există evaluări
- AterosclerosisDocument3 paginiAterosclerosisFALLBACK THRONEÎncă nu există evaluări
- GineDocument17 paginiGineVaban NJÎncă nu există evaluări
- Importancia Del Cuidado Integral en El Adulto Mayor Art. CientificoDocument7 paginiImportancia Del Cuidado Integral en El Adulto Mayor Art. CientificoPatricia Andrea RiveraÎncă nu există evaluări
- Informe Lista de ChequeoDocument4 paginiInforme Lista de ChequeoAlejandra GarcésÎncă nu există evaluări
- Tarea - 4 - Trabajo Colaborativo - Seguridad - Del - PacienteDocument56 paginiTarea - 4 - Trabajo Colaborativo - Seguridad - Del - PacienteLEIDY TATIANAÎncă nu există evaluări
- Antialergicos y Descongestivos OcularesDocument4 paginiAntialergicos y Descongestivos OcularesCesar Alex Vera CariÎncă nu există evaluări
- Tarea 4 PsicobiologiaDocument17 paginiTarea 4 PsicobiologiaDavis AlfonsoÎncă nu există evaluări
- El Niño Burbuja Análisis InmunológicoDocument4 paginiEl Niño Burbuja Análisis InmunológicoRodrigo Del OlmoÎncă nu există evaluări
- Trabajo MASTER - T. Aquiles, Sergio BandilaDocument27 paginiTrabajo MASTER - T. Aquiles, Sergio Bandilasergio bÎncă nu există evaluări
- Comunidad Tema 15 Mci 2022 20Document45 paginiComunidad Tema 15 Mci 2022 20Sergio Muñoz CabreraÎncă nu există evaluări
- 2 - AiepiDocument20 pagini2 - AiepiEvelyn Mercedes Peralta100% (1)
- Https WWW - Unitru.edu - Pe Publicaciones Admision 2020 II-EXA SUM 2020-I CEPUNT IDocument53 paginiHttps WWW - Unitru.edu - Pe Publicaciones Admision 2020 II-EXA SUM 2020-I CEPUNT Irobison juarezÎncă nu există evaluări
- CclavveeeDocument31 paginiCclavveeeAda Abigail Rojas GuerreroÎncă nu există evaluări
- RinosinusopatiasDocument4 paginiRinosinusopatiasAndrus152Încă nu există evaluări
- Guía MED-316L-104 (R3-2020)Document1 paginăGuía MED-316L-104 (R3-2020)Brenda Inmaculada MatosÎncă nu există evaluări
- RABIADocument1 paginăRABIAYeisonÎncă nu există evaluări