Documente Academic
Documente Profesional
Documente Cultură
Hielo Su Comportamiento
Încărcat de
Florentino Rodriguez ChaviraTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Hielo Su Comportamiento
Încărcat de
Florentino Rodriguez ChaviraDrepturi de autor:
Formate disponibile
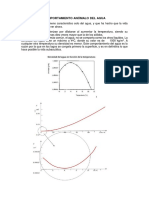
El comportamiento unico del hielo.
Un punto importante a considerar es que a nivel fsico-qumico, mientras en la mayora de las sustancias la densidad aumenta a medida que la temperatura disminuye, en el caso del agua esto se cumple slo hasta bajar a 4 C. Cuando el agua se contina enfriando por debajo de esta temperatura, la densidad disminuye. Es por ello que el hielo flota en el agua lquida. Este comportamiento, aparentemente anmalo del hielo, se debe a que la estructura generada por interacciones llamadas puentes o enlaces de hidrgeno en estado slido tiene un volumen molar mayor que aquel que posee en estado lquido. En las figuras se muestran, esquemticamente, estos enlaces en ambas fases. Para formar puentes de hidrgeno es necesario que las molculas posean tomos con electrones no compartidos (como los oxgenos del agua) y que estos tomos sean muy electronegativos y de pequeo tamao, como el oxgeno, el flor y el nitrgeno. A pesar de que un puente de hidrgeno no es tan fuerte como un enlace covalente, es suficientemente resistente para determinar ciertas propiedades de un estado de la materia intermedio entre el slido y el gaseoso, como lo es el estado lquido. Efectivamente, el agua se presenta en estado lquido, a presin atmosfrica en el intervalo de temperatura conocido, porque sus molculas estn unidas entre s por enlaces de hidrgeno, tal como fue sugerido por Linus Pauling . Estos puentes favorecen la unin de las molculas y, como resultado, el agua lquida tiene una estructura relativamente ordenada, y muy estable en un intervalo de temperaturas amplio. Los puentes de hidrgeno se forman y se rompen de manera continua a una velocidad que oscila entre una milmillonsima de segundo (un picosegundo) y una billonsima de segundo (un femtosegundo). Cuando el agua pasa al estado slido, es decir cuando se convierte en hielo, por efecto de la disminucin de la temperatura las molculas se organizan en una estructura que a pesar de ser compacta tiene un mayor volumen. Tal como observas en la imagen, cada molcula de agua se enlaza con otras cuatro a travs de puentes de hidrgeno. Por lo tanto, en un volumen dado de hielo hay menos molculas de agua que en el mismo volumen de agua lquida. Este es el motivo por el cual cuando el agua se congela su volumen aumenta y como consecuencia el hielo formado al congelarse el agua a 0 C flota sobre sta. Es tambin por esta razn que se rompen los envases de vidrio cuando se congelan botellas completamente llenas de agua. El puente de hidrgeno y el agua Interesante Gracias a la particularidad de que el hielo flota sobre el agua es que muchas especies vivas pueden sobrevivir bajo mares congelados en aquellos pases donde las temperaturas descienden considerablemente en invierno. En los mares y lagos se congela primero la capa superficial de las aguas, quedando por debajo del hielo agua lquida, cuya temperatura aumenta con la profundidad, llegando a ser de 4 C en el fondo. Durante los meses invernales, este fenmeno permite el mantenimiento de la vida vegetal y animal en el agua.
S-ar putea să vă placă și
- AguaDocument6 paginiAguaGrecia AlvarezÎncă nu există evaluări
- Propiedades físico-químicas del aguaDocument5 paginiPropiedades físico-químicas del aguaISRAELÎncă nu există evaluări
- Fisica Ii - Semana3-Kenya AncheytaDocument3 paginiFisica Ii - Semana3-Kenya AncheytaKenya VergaraÎncă nu există evaluări
- Fisica Ii - Semana3-Kenya AncheytaDocument3 paginiFisica Ii - Semana3-Kenya AncheytaKenya VergaraÎncă nu există evaluări
- Tarea de Hidraulica Por Que Flota El HieloDocument4 paginiTarea de Hidraulica Por Que Flota El HieloFranz QuisbertÎncă nu există evaluări
- El Agua Caracteristicas GeneralesDocument9 paginiEl Agua Caracteristicas GeneralesGuido AutoreÎncă nu există evaluări
- Dilatacion Anomala Del AguaDocument8 paginiDilatacion Anomala Del AguaIvan SailemaÎncă nu există evaluări
- El AguaDocument6 paginiEl AguaErika PerezÎncă nu există evaluări
- GlaciaresDocument6 paginiGlaciaresMarcelo VendetoÎncă nu există evaluări
- Agua Importancia FisiologicaDocument8 paginiAgua Importancia FisiologicaAmbrosio Salazar Aranza ZinayÎncă nu există evaluări
- Tratamiento de Agua IndustrialDocument145 paginiTratamiento de Agua Industrialchorch_correa100% (1)
- Porque Los Lagos Se Congelan Solo en La SuperficieDocument2 paginiPorque Los Lagos Se Congelan Solo en La SuperficieAbdías Alonso YuickÎncă nu există evaluări
- Comportamiento Anomalo Del AguaDocument6 paginiComportamiento Anomalo Del AguaErick Bryan Rodriguez Rosario100% (1)
- Tema 2. El AguaDocument13 paginiTema 2. El Aguasara rodriguezÎncă nu există evaluări
- Propiedades Del AguaDocument17 paginiPropiedades Del AguaBelphRam Joestar AbaddonÎncă nu există evaluări
- Puentes de Hidrógeno en El AguaDocument27 paginiPuentes de Hidrógeno en El AguaLuz CasteleyroÎncă nu există evaluări
- Lectura 5 - 3º Cyt - III UnidadDocument2 paginiLectura 5 - 3º Cyt - III UnidadIsabel Espino PaucarÎncă nu există evaluări
- Caracteristicas Del AguaDocument2 paginiCaracteristicas Del AguaMonica Perez100% (1)
- Propiedades y funciones del agua en el cuerpo humanoDocument11 paginiPropiedades y funciones del agua en el cuerpo humanosarengoÎncă nu există evaluări
- Fiq AguaDocument39 paginiFiq Aguarichard diegoÎncă nu există evaluări
- Propiedades Del AguaDocument51 paginiPropiedades Del AguaCRozilJ.EspinozaGanozaÎncă nu există evaluări
- Caracter BipolarDocument3 paginiCaracter BipolarDavid Cruz TorresÎncă nu există evaluări
- El Agua 2.1Document10 paginiEl Agua 2.1ERICK MALDONADOÎncă nu există evaluări
- Propiedades Físico Químicas Del AguaDocument6 paginiPropiedades Físico Químicas Del AguaSabrina Hernández GuianceÎncă nu există evaluări
- Agua, Propiedades FisicasDocument2 paginiAgua, Propiedades FisicasJEFRIT ALAN VIDAL ORTIZÎncă nu există evaluări
- 1 AguaDocument7 pagini1 AguaGabriela CatalánÎncă nu există evaluări
- Comportamiento Anómalo Del AguaDocument4 paginiComportamiento Anómalo Del AguaGiselle Escobedo CortijoÎncă nu există evaluări
- Comportamiento Anómalo Del AguaDocument4 paginiComportamiento Anómalo Del AguaGiselle Escobedo CortijoÎncă nu există evaluări
- AguaDocument7 paginiAguaInsecto ToxicoÎncă nu există evaluări
- Propiedades Fisicas Del AguaDocument4 paginiPropiedades Fisicas Del AguaMaria Jose Barrero ValleÎncă nu există evaluări
- Estados de La Materia y Transformaciones de FaseDocument20 paginiEstados de La Materia y Transformaciones de FaseCristianÎncă nu există evaluări
- Resumen Diagrama de Fases.Document14 paginiResumen Diagrama de Fases.Catalina CastroÎncă nu există evaluări
- Luisa Fernanda HoyosDocument5 paginiLuisa Fernanda HoyosNéstor Arias LoaizaÎncă nu există evaluări
- Propiedades Fisicas Del Agua HidraulicaDocument5 paginiPropiedades Fisicas Del Agua HidraulicaRony Condeña Manchego100% (1)
- Presentacion 2 Estructura Del AguaDocument13 paginiPresentacion 2 Estructura Del AguaMau Rojua RezÎncă nu există evaluări
- Estructura Física Del AguaDocument24 paginiEstructura Física Del AguaOrianny GraterolÎncă nu există evaluări
- Misterios Del AguaDocument2 paginiMisterios Del AguaDario Quimis SantanaÎncă nu există evaluări
- Caracter Bipolar y Estructura Intermolecular Del AguaDocument4 paginiCaracter Bipolar y Estructura Intermolecular Del Aguaalejandra370% (1)
- AguaDocument4 paginiAguakattherine rojas capchaÎncă nu există evaluări
- Propiedades Del AguaDocument3 paginiPropiedades Del AguaNéstor Walter Barrera RomeroÎncă nu există evaluări
- Agua Curtis y BarnesDocument2 paginiAgua Curtis y BarnesSusana SantellánÎncă nu există evaluări
- Características Físicoquimicas Del AguaDocument10 paginiCaracterísticas Físicoquimicas Del AguaJota Jota JotaÎncă nu există evaluări
- Comportamiento anómalo del aguaDocument3 paginiComportamiento anómalo del aguaCesar Vasquez PerezÎncă nu există evaluări
- El Fenómeno Anómalo Del AguaDocument1 paginăEl Fenómeno Anómalo Del AguaKeiko Uriol ReyesÎncă nu există evaluări
- Resumen de Bioquimica de Los Alimentos (Fennema)Document12 paginiResumen de Bioquimica de Los Alimentos (Fennema)Christian Alexander Mendoza EsquivelÎncă nu există evaluări
- Propiedades y estructura del aguaDocument32 paginiPropiedades y estructura del aguaSharon E. Chauca MontesinosÎncă nu există evaluări
- Biomoléculas Inorgánicas. Estados de La MateriaDocument16 paginiBiomoléculas Inorgánicas. Estados de La Materiaopuebla344eÎncă nu există evaluări
- Temario Quimica de Alimentos PDFDocument96 paginiTemario Quimica de Alimentos PDFMAGALY VICTORIAÎncă nu există evaluări
- Agua Parte DosDocument5 paginiAgua Parte DosEstefany PamelaÎncă nu există evaluări
- Anomalía Del AguaDocument14 paginiAnomalía Del AguaLoreto Castro Rojas100% (1)
- El Agua BioquimicaDocument19 paginiEl Agua BioquimicaGeraldine GarciaÎncă nu există evaluări
- Propiedades Físicas y Químicas Del AguaDocument4 paginiPropiedades Físicas y Químicas Del AguaAlex BautistaÎncă nu există evaluări
- El AguaDocument8 paginiEl AguaJosé Arriaza GonzálezÎncă nu există evaluări
- La Dilatación Anómala Del AguaDocument1 paginăLa Dilatación Anómala Del AguaDiana NavarreteÎncă nu există evaluări
- El AguaDocument123 paginiEl AguaDaniiela TiriaÎncă nu există evaluări
- Agua Salada!!Document4 paginiAgua Salada!!Bryam Espinoza OsorioÎncă nu există evaluări
- El AguaDocument29 paginiEl AguaalejandraÎncă nu există evaluări
- AguaDocument48 paginiAguaIC Mel100% (2)
- Lo Que Pasa Cuando Bebes Coca ColaDocument1 paginăLo Que Pasa Cuando Bebes Coca ColaFlorentino Rodriguez ChaviraÎncă nu există evaluări
- Montaje Equipo RefrigeracionDocument40 paginiMontaje Equipo Refrigeracionmartin scheinerÎncă nu există evaluări
- Nikola TeslaDocument3 paginiNikola TeslaFlorentino Rodriguez ChaviraÎncă nu există evaluări
- Qué Pasa Con Mi Dinero Del SAR 92Document2 paginiQué Pasa Con Mi Dinero Del SAR 92Florentino Rodriguez ChaviraÎncă nu există evaluări
- Electric Id Ad (Bueno y CompletitoDocument72 paginiElectric Id Ad (Bueno y Completitoapi-3804733100% (3)
- Semiconductores, Diodos Y TransistoresDocument48 paginiSemiconductores, Diodos Y Transistoresapi-374400360% (5)
- La Diabetes en La IRCDocument28 paginiLa Diabetes en La IRCAnonymous NtJg6VÎncă nu există evaluări
- Recuperar SAR 92Document1 paginăRecuperar SAR 92Florentino Rodriguez ChaviraÎncă nu există evaluări
- La Diabetes en La IRCDocument28 paginiLa Diabetes en La IRCAnonymous NtJg6VÎncă nu există evaluări
- Los Ojos Ofrecen Claves para Detectar EnfermedadesDocument2 paginiLos Ojos Ofrecen Claves para Detectar EnfermedadesFlorentino Rodriguez ChaviraÎncă nu există evaluări
- Guias de Hipertension ArterialDocument25 paginiGuias de Hipertension ArterialFlorentino Rodriguez ChaviraÎncă nu există evaluări
- Guias de Hipertension ArterialDocument25 paginiGuias de Hipertension ArterialFlorentino Rodriguez ChaviraÎncă nu există evaluări
- Proceso de Copíadoras y Sus PartesDocument5 paginiProceso de Copíadoras y Sus PartesFlorentino Rodriguez Chavira0% (1)
- Mitos alimentariosDocument24 paginiMitos alimentariosPsi Claudio Cesar Orias HuayllaÎncă nu există evaluări
- Electricidad - Libro de Instalaciones ElectricasDocument299 paginiElectricidad - Libro de Instalaciones ElectricasFlorentino Rodriguez ChaviraÎncă nu există evaluări
- 6th Central Pay Commission Salary CalculatorDocument15 pagini6th Central Pay Commission Salary Calculatorrakhonde100% (436)
- Alimentos y Grupos Sanguíneos PDFDocument81 paginiAlimentos y Grupos Sanguíneos PDFregescÎncă nu există evaluări
- Tipo de Usuario FBDocument5 paginiTipo de Usuario FBFlorentino Rodriguez ChaviraÎncă nu există evaluări
- Como Prevenir La Obesidad InfantilDocument1 paginăComo Prevenir La Obesidad InfantilFlorentino Rodriguez ChaviraÎncă nu există evaluări
- Automovil - Sistemas de Inyeccion Electronic ADocument40 paginiAutomovil - Sistemas de Inyeccion Electronic AAndresessÎncă nu există evaluări
- El Milagro Del Aceite de OlivaDocument2 paginiEl Milagro Del Aceite de OlivaClaudia AgramonteÎncă nu există evaluări
- Consejos para Ahorro de GasolinaDocument3 paginiConsejos para Ahorro de GasolinaFlorentino Rodriguez ChaviraÎncă nu există evaluări
- Principios Basicos de LubricantesDocument63 paginiPrincipios Basicos de LubricantesFlorentino Rodriguez ChaviraÎncă nu există evaluări
- Aloe Vera Planta MilagrosaDocument5 paginiAloe Vera Planta MilagrosaFlorentino Rodriguez ChaviraÎncă nu există evaluări
- Aloe Vera Planta MilagrosaDocument5 paginiAloe Vera Planta MilagrosaFlorentino Rodriguez ChaviraÎncă nu există evaluări
- In Stephen Hawking Words en Palabras de Stephen HawkingDocument3 paginiIn Stephen Hawking Words en Palabras de Stephen HawkingFlorentino Rodriguez ChaviraÎncă nu există evaluări
- Las Locas LeyesDocument5 paginiLas Locas LeyesFlorentino Rodriguez ChaviraÎncă nu există evaluări
- Leccion Pulsador de Picos (1) Maquina Limpia InyectoresDocument8 paginiLeccion Pulsador de Picos (1) Maquina Limpia InyectoresAnton Nicolas Kryzanowskyj RodriguezÎncă nu există evaluări
- Aprendiendo A Pensar en Grande PDFDocument48 paginiAprendiendo A Pensar en Grande PDFpabloÎncă nu există evaluări
- Laboratorio 3matDocument10 paginiLaboratorio 3matelvisÎncă nu există evaluări
- Manual de Diseño de Mezcla de Laboratorio para Los Sellos de Lechada Asfáltica (Slurry Seals) en Costa Rica PDFDocument44 paginiManual de Diseño de Mezcla de Laboratorio para Los Sellos de Lechada Asfáltica (Slurry Seals) en Costa Rica PDFCarmen CenzanoÎncă nu există evaluări
- Corrosion HebertDocument22 paginiCorrosion HebertHebert ChavezÎncă nu există evaluări
- Simultaneidad - RelatividadDocument6 paginiSimultaneidad - RelatividadafreynaÎncă nu există evaluări
- Eddy CurrentDocument9 paginiEddy CurrentLuis Criollo0% (1)
- QU-181 Compuesto inorgánicoDocument28 paginiQU-181 Compuesto inorgánicoFranks EspinozaÎncă nu există evaluări
- Plantas de ElectroobtencionDocument27 paginiPlantas de ElectroobtencionMaycol Alexander H. CHÎncă nu există evaluări
- Sales de DiazonioDocument3 paginiSales de Diazoniohalleffect09Încă nu există evaluări
- MeteorizacionDocument28 paginiMeteorizacionDagoberto VergaraÎncă nu există evaluări
- Elaboración Mapa MorfometricoDocument9 paginiElaboración Mapa MorfometricoSéptimo CicloÎncă nu există evaluări
- Gráfica Velociad 1Document4 paginiGráfica Velociad 1DSMA98Încă nu există evaluări
- QU0200 - 2018-2S - Semana 13a - Cap 19 y 20Document28 paginiQU0200 - 2018-2S - Semana 13a - Cap 19 y 20Jose Enrique Conejo CambroneroÎncă nu există evaluări
- Informe Congreso JEQCDocument29 paginiInforme Congreso JEQCLUIS MIGUEL GARCIA VENTURAÎncă nu există evaluări
- Ciclo Del AguaDocument6 paginiCiclo Del AguaSaul LaraÎncă nu există evaluări
- Acid FoamDocument6 paginiAcid FoamLolita Jiménez AlvaradoÎncă nu există evaluări
- Plan para Clase Sobre PolímerosDocument4 paginiPlan para Clase Sobre PolímerosMagda ReynaÎncă nu există evaluări
- Gravimetría - Parte 1Document32 paginiGravimetría - Parte 1Marcelo VallejosÎncă nu există evaluări
- Determinaciones estequiométricas de sustancias en ingeniería ambientalDocument3 paginiDeterminaciones estequiométricas de sustancias en ingeniería ambientalBruno Carrasco0% (1)
- Química agrícola: Formación y constituyentes del sueloDocument5 paginiQuímica agrícola: Formación y constituyentes del sueloJona FG100% (1)
- Sobrevilla AnDocument159 paginiSobrevilla AnTiezma OamaÎncă nu există evaluări
- Clase 1 y Tarea 1 Fisica 9 2021Document20 paginiClase 1 y Tarea 1 Fisica 9 2021alexandraÎncă nu există evaluări
- Practico de Cromatografia PDFDocument5 paginiPractico de Cromatografia PDFVanesa Vaca MontesÎncă nu există evaluări
- 100 Problemas Fisica 1Document53 pagini100 Problemas Fisica 1Elmer Santiago LeonÎncă nu există evaluări
- Sísmica de Reflexión - Principios y métodos de trabajoDocument15 paginiSísmica de Reflexión - Principios y métodos de trabajoErick Enrique Mallqui SantosÎncă nu există evaluări
- Informe Previo 7Document5 paginiInforme Previo 7AngsusParrizÎncă nu există evaluări
- Reforzamiento de QuimicaDocument3 paginiReforzamiento de QuimicaAlberto Rodriguez AlemanÎncă nu există evaluări
- Los Planetas de Nuestro Sistema SolarDocument2 paginiLos Planetas de Nuestro Sistema SolarLuisaDiazLeon100% (1)
- Determinación de Minerales en Alimentos.Document36 paginiDeterminación de Minerales en Alimentos.Lucia G. Carballo Fabián100% (2)
- Fuerzas Diversas. P8Document2 paginiFuerzas Diversas. P8Harold DanielÎncă nu există evaluări
- Determinación de La Viscosidad de Un Fluido Por El Método Del Viscosimetro Rotacional de BrookfieldDocument28 paginiDeterminación de La Viscosidad de Un Fluido Por El Método Del Viscosimetro Rotacional de Brookfieldfrancis beto100% (1)