Documente Academic
Documente Profesional
Documente Cultură
Informe#1. Corrosión de Metales A Elevadas Temperaturas
Încărcat de
Anny FigueroaTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Informe#1. Corrosión de Metales A Elevadas Temperaturas
Încărcat de
Anny FigueroaDrepturi de autor:
Formate disponibile
Universidad Nacional Experimental Politcnica Antonio Jos de Sucre Vice-Rectorado Puerto Ordaz Corrosin
Profesora: Linda Gil
Elaborado por: Mara Salazar CI: 17.526.926 Keilis gonzalez CI: 18.665.664
Ciudad Guayana, Junio de 2010
Corrosin de metales a elevadas Temperaturas
INTRODUCCIN
La corrosin se define como la destruccin o deterioro de un material debido a la interaccin de la naturaleza qumica o electroqumica con su medio ambiente. Es un problema industrial importante, ya que puede causar accidentes y, adems, representa un costo importante, ya que se calcula que cada pocos segundos se disuelven 5 toneladas de acero en el mundo, procedentes de unos cuantos nanmetros o picmetros, pero que multiplicados por la cantidad de acero que existe en el mundo, constituyen una cantidad importante. En funcin de la naturaleza de la interaccin con el medio, es importante distinguir dos tipos de corrosin: la corrosin qumica y la corrosin electroqumica. En este caso, slo se har mencin especial de la corrosin qumica, la cual representa la base fundamental sobre la que se desarrolla la presente prctica. La corrosin qumica de los metales se define como la interaccin espontnea del metal con el medio ambiente corrosivo con el que est en contacto. Este tipo de corrosin se observa cuando sobre el metal actan gases secos y lquidos no electrolticos, y es una reaccin qumica del medio lquido o gaseoso (o sus componentes oxidantes) con el metal. Cuando un metal es expuesto a un gas oxidante a temperaturas elevadas, la corrosin puede ocurrir por la reaccin directa con el gas sin la presencia de un lquido. Este tipo de corrosin es conocida como Empaamiento, Escamamiento o Corrosin por Altas Temperaturas. Generalmente esta clase de corrosin depende directamente de la temperatura y acta de la siguiente manera: al estar expuesto el metal al gas oxidante, se forma una pequea capa sobre el metal, producto de la combinacin entre el metal y el gas en esas condiciones de temperatura. Esta capa o empaamiento acta como un electrolito slido, que permite que se produzca la corrosin de la pieza metlica mediante el movimiento inico en la superficie. Uno de los tipos de corrosin qumica que ms ha sido estudiado es el debido a la accin de gases calientes sobre los diferentes metales y materiales metlicos. La oxidacin qumica de los metales, segn el modelo simplificado Me(s)+O2(g)MeO(s), ha permitido determinar las leyes bsicas de la corrosin qumica, que generalmente se expresan como la dependencia del aumento de masa de los productos de corrosin en funcin del tiempo, o el aumento del espesor de la capa de xidos o productos de corrosin con el tiempo . Estas leyes bsicas son la ley lineal, la ley parablica o la ley logartmica.
Corrosin de metales a elevadas Temperaturas
Con la finalidad de comprender los mecanismos que controlan los procesos de corrosin de un metal a elevadas temperaturas y as poder determinar el comportamiento de un metal a la oxidacin a elevadas temperaturas, se desarrolla en la presente prctica un procedimiento para determinar la ley cintica que rige el proceso. Para ello, se grafica Log (g/A) Vs. Log (t), si el resultado es una lnea recta, la pendiente de la grfica permitir determinar si la ley es lineal (en cuyo caso corresponder a una capa de xido muy poco protectora o no protectora) o de tendencia parablica (que se genera de productos de corrosin protectores). De lo contrario, es necesario graficar (g/A) Vs. Log (t), lo que indicara que la ley cintica es logartmica y la capa de oxido formada es extremadamente protectora. Antes de entrar al anlisis y descripcin detallada de la experiencia desarrollada en la presente prctica, es importante mencionar algunos factores que deben considerarse como medidas de prevencin para este tipo de corrosin: Alta estabilidad termodinmica, para generar en lo posible otros productos para reacciones distintas. 2. Baja Presin de Vapor, de forma tal que los productos generados sean slidos y no gases que se mezclen con el ambiente.
1.
Corrosin de metales a elevadas Temperaturas
OBJETIVOS
Objetivo General:
Estudiar el comportamiento de un metal a la oxidacin a altas temperaturas.
Objetivos Especficos:
Establecer la influencia de la temperatura en la velocidad de corrosin de un metal
en aire.
Calcular la ley que rige el crecimiento de la capa de xido del metal estudiado.
Calcular la energa de activacin.
Corrosin de metales a elevadas Temperaturas
MATERIALES Y REACTIVOS
Crisoles de porcelana Pinzas para crisoles Muestras de acero al carbono Desecador Etanol (Desengrasante) Guantes Lijas
EQUIPOS UTILIZADOS
Vernier Balanza analtica Horno elctrico
Corrosin de metales a elevadas Temperaturas
METODOLOGA EXPERIMENTAL
Se enciende el horno y se regula la temperatura a 600C, que es la temperatura de trabajo.
Posteriormente se procede a colocar cada probeta en un crisol, haciendo uso de las pinzas para luego pesarlos.
Se introducen en la estufa 8 crisoles limpios y se mantienen durante 15 minutos a una temperatura de 150C. Al cabo de este tiempo, se sacan y se introducen en el desecador.
Seguidamente se colocan los crisoles en el horno por orden de extraccin para no tener confusiones.
Una vez limpios los crisoles y puestos en el desecador durante 15 minutos, se pesan y se introducen nuevamente en el desecador.
8 8
Las muestras se mantienen en el horno durante 15, 30, 60 y 90 minutos, sacando dos crisoles para cada tiempo
Se toman 8 muestras de acero al carbono, y se procede a tomar sus respectivas dimensiones con el vernier.
Al retirar los crisoles del horno, estos son colocados en el desecador destapado durante 5 minutos, luego se dejan en el desecador tapado hasta que se enfren completamente.
Luego se procede a la preparacin de las muestras lijndolas, lavndolas con agua destilada, limpindolas con desengrasante y secndolas finalmente.
1 0
Finalmente, se pesan las muestras junto con el crisol.
Corrosin de metales a elevadas Temperaturas
DATOS EXPERIMENTALES
Tabla 1. Dimensiones de las lminas de acero
Temperatur a (C) Nro. Muestra 1 2 3 4 5 6 7 8 1 2 3 4 5 6 7 8 1 2 3 4 5 6 7 8 Largo (mm) 29,8 29,8 29,8 28,7 29,5 28,7 29,5 28,5 30,04 30,35 29,18 29,19 29,37 29,08 30,04 28,27 29 28,7 29,4 28,6 30,5 29,5 29,9 30,9 Ancho (mm) 9,3 9,4 9,4 9,4 9,5 9,4 9,4 9,4 9,35 9,3 9,35 9,35 9,25 9,35 9,25 9,4 9,5 9,5 9,5 9,5 9,5 9,5 9,9 9,5 Espesor (mm) 1,5 1,5 1,5 1,5 1,5 1,5 1,5 1,5 1,3 1,3 1,3 1,3 1,25 1,3 1,25 1,25 1,5 1,5 1,5 1,5 1,5 1,5 1,5 1,5
600C
700C
850C
Tabla 2. Peso de los crisoles antes y despus del ensayo experimental
Corrosin de metales a elevadas Temperaturas
Temperat ura (C) Nro. Muestra 1 2 3 4 5 6 7 8 1 2 3 4 5 6 7 8 1 2 3 4 5 6 7 8 Tiempo (min) Peso del crisol Vaco (g) 18,34 23,04 21,1 19,1 22,87 19,8 21,17 20,21 18,34 23,04 21,1 19,1 22,87 19,8 21,17 20,21 18,34 23,04 21,1 19,1 22,87 19,8 21,17 20,21 Peso del crisol con muestra antes (g) 21,47 26,17 24,1 22,27 25,84 22,88 24,36 23,43 24,1893 24,3101 23,2626 25,9967 22,2613 21,4898 26,2394 22,9924 23,6215 24,0624 25,4124 23,284 24,3004 23,9843 25,7709 25,3007 Peso del crisol a la salida del horno (g) 21,47 26,18 24,1 22,28 25,85 22,89 24,37 23,45 24,2045 24,3249 23,2806 26,0169 22,2876 21,4964 26,2697 23,0258 23,6311 24,0721 25,4777 23,3375 24,3735 24,0286 25,8234 25,4053
600C
700C
850C
15 15 30 30 60 60 90 90 15 15 30 30 60 60 90 90 15 15 30 30 60 60 90 90
CLCULOS Y RESULTADOS
Para determinar la ley cintica que rige la velocidad de corrosin de las lminas de acero, y as poder establecer la influencia de la temperatura en la velocidad de corrosin de las mismas, se realiz el ensayo para diferentes temperaturas: 600, 700 y 850C,
Corrosin de metales a elevadas Temperaturas obtenindose para cada temperatura los datos respectivos. A continuacin se presentan los clculos para la temperatura de trabajo de 600C, asumindose el mismo procedimiento para temperaturas posteriores:
Temperatura de trabajo: 600C
Determinacin del rea (A)
El rea de la lmina que se debe calcular, corresponde a la expuesta al medio corrosivo (parte externa de la lmina); para ello, se tomaron las dimensiones necesarias para el clculo de la misma (Largo, ancho y espesor). Las dimensiones de las lminas para esta temperatura se muestran en la Tabla 1.1. Figura 1. Dimensiones de la Lmina de acero y reas expuestas al medio corrosivo
Anch o
A
(rea 2 superior)
A
(rea 1 frontal)
Largo
Espeso r
A
(rea 3 Lateral)
Tabla 1.1: Dimensiones de las lminas de acero a la temperatura de trabajo de 600C
Temperat ura (C) Nro. Muestra 1 2 3 4 5 6 7 8 Largo (mm) 29,8 29,8 29,8 28,7 29,5 28,7 29,5 28,5 Ancho (mm) 9,3 9,4 9,4 9,4 9,5 9,4 9,4 9,4 Espesor (mm) 1,5 1,5 1,5 1,5 1,5 1,5 1,5 1,5
600C
Ecuacin (i)
Para la muestra 1:
Corrosin de metales a elevadas Temperaturas
Sustituyendo en la ecuacin (i), se tiene el rea de la lmina de la muestra A.1
Se procede de la misma manera para calcular el rea de las dems lminas. Los resultados obtenidos se muestran en la Tabla 1.2
Tabla 1.2: rea de las lminas de acero a la temperatura de trabajo de 600C Muestra 1 2 3 4 5 6 7 8 rea (mm) 671,58 677,84 677,84 653,86 677,5 653,86 671,3 649,5 rea (cm2) 6,7158 6,7784 6,7784 6,5386 6,775 6,5386 6,713 6,495
Determinacin de la ganancia de peso (g) La diferencia entre el peso de la muestra (lmina) de acero antes de entrar al horno, con respecto al peso de la misma despus de su salida del horno, nos permite conocer la ganancia de peso de la muestra con respecto al tiempo. Los resultados obtenidos de los pesos de los crisoles antes de entrar y despus de salir del horno en los diferentes tiempos de control (15, 30, 60 y 90s) para la temperatura de 600C, se muestran en la tabla 1.3.
Tabla 1.3: Peso de los crisoles antes de entrar y despus de salir del horno a la temperatura de trabajo de 600C. Peso del crisol Vaco (g) 18,34 Peso del crisol con muestra antes (g) 21,47 Peso del crisol con muestra despus (g) 21,47
Muestra 1
Corrosin de metales a elevadas Temperaturas
2 3 4 5 6 7 8 23,04 21,1 19,1 22,87 19,8 21,17 20,21 26,17 24,1 22,27 25,84 22,88 24,36 23,43 26,18 24,1 22,28 25,85 22,89 24,37 23,45
Peso inicial de la muestra (g)= Peso del crisol con muestra antes (g) Peso del crisol vaco (g) Peso final de la muestra (g)= Peso del crisol con muestra despus (g) Peso del crisol vaco (g)
g (g) = Peso final de la muestra (g) Peso inicial de la muestra (g) Para la muestra 1: Peso inicial de la muestra 1= 21,47 g 18,34 g= 3,13 g Peso final de la muestra 1= 21,47 g 21,47 g = 0 g g (g) = 3,13 g 0 g = 3,13 g
Tabla 1.4. Ganancia de peso de las muestras de acero para los diferentes tiempos de control a la temperatura de trabajo de 600C Muestra 1 2 3 4 5 6 7 8 Tiempo (min) 15 15 30 30 60 60 90 90 Peso Inicial Peso Final (g) (g) 3,13 3,13 3,13 3,14 3 3 3,17 3,18 2,97 2,98 3,08 3,09 3,19 3,2 3,22 3,24 g (g) 0 0,01 0 0,01 0,01 0,01 0,01 0,02
Determinacin de Expresin de la ley cintica Para deducir la ecuacin de la ley cintica que rige el comportamiento de la velocidad de corrosin, es necesario determinar los valores de la ganancia de peso por unidad de rea (g/A)(g/cm2), logaritmizarlos y graficar dichos valores en funcin del tiempo(min). A continuacin se muestran dichos valores en la tabla 1.5, y su grfica correspondiente (grfica 1). Tabla 1.5 Valores de Ganancia de peso por unidad de rea en funcin del tiempo, para la temperatura de trabajo de 600C
Muestra P/A (g/Cm2) prom P/A (g/Cm2) t (min) Log (P/A) Log t (min)
Corrosin de metales a elevadas Temperaturas
(g/Cm2) -3,13216 -3,11651 -2,82313 -2,64121
1 2 3 4 5 6 7 8
0,00000 0,00148 0,00000 0,00153 0,00148 0,00153 0,00149 0,00308
0,00074 0,00076 0,00150 0,00228
15 30 60 90
1,17609 1,47712 1,77815 1,95424
Grfica 1. Curva representativa de Log (g/A) Versus Log(t) para la temperatura de trabajo de 600C
Con la finalidad de determinar la ecuacin de dicha ley cintica a la temperatura de trabajo de 600C, se parte de la siguiente expresin:
Logaritmizando se tiene:
Corrosin de metales a elevadas Temperaturas
Esta ltima expresin tiene la forma de una recta: tenemos que:
. Al hacer la similitud,
mx
Y haciendo la similitud para la ecuacin de la recta obtenida al graficar Log(g/A) Vs. Log(t) para la temperatura de trabajo de 600C, se tiene que: y = 0,653x - 3,971 y= mx + b
[Ley Lineal (predominantemente)]
Corrosin de metales a elevadas Temperaturas
Finalmente, sustituyendo en la expresin (ii), se encuentra que la ley cintica que rige el comportamiento de la velocidad de corrosin a una temperatura de 600C es la siguiente:
Es importante resaltar que debido a que se realizan los mismos clculos para las temperaturas de trabajo de 700 y 850C, solamente se mostrarn los resultados obtenidos para tales temperaturas.
Temperatura de trabajo: 700C
Determinacin del rea (A) Tabla 2.1. Dimensiones y rea de las lminas de acero a la temperatura de trabajo de 700C
Temperat ura (C) Nro. Muestra 1 2 3 4 5 6 7 8 Largo (mm) 30,04 30,35 29,18 29,19 29,37 29,08 30,04 28,27 Ancho (mm) 9,35 9,3 9,35 9,35 9,25 9,35 9,25 9,4 Espesor (mm) 1,3 1,3 1,3 1,3 1,25 1,3 1,25 1,25
700C
Determinacin de la ganancia de peso (g) Tabla 2.2. Ganancia de peso de las muestras de acero para los diferentes tiempos de control a
la temperatura de trabajo de 700C Muestra 1 2 3 4 5 6 7 8 Tiempo (min) 15 15 30 30 60 60 90 90 Peso Inicial Peso Final (g) (g) 5,8493 5,8645 1,2701 1,2849 2,1626 2,1806 6,8967 6,9169 -0,6087 -0,5824 1,6898 1,6964 5,0694 5,0997 2,7824 2,8158 g (g) 0,0152 0,0148 0,018 0,0202 0,0263 0,0066 0,0303 0,0334
Corrosin de metales a elevadas Temperaturas
Determinacin de Expresin de la ley cintica Tabla 2.3. Valores de Ganancia de peso por unidad de rea en funcin del tiempo, para la temperatura de trabajo de 700C
Muestra 1 2 3 4 5 6 7 8 g/A (g/Cm2) 0,00229 0,00222 0,00279 0,00313 0,00411 0,00103 0,00463 0,00534 prom g/A (g/Cm2) 0,00225 0,00296 0,00257 0,00499 t (min) 15 30 60 90 Log (g/A) (g/Cm2) -2,64729 -2,52917 -2,59046 -2,30226 Log t (min) 1,17609 1,47712 1,77815 1,95424
Grfica 2. Curva representativa de Log (g/A) Versus Log(t) para una temperatura de trabajo de 700C
y = 0,340x 3,060 y= mx + b
Corrosin de metales a elevadas Temperaturas
Finalmente, sustituyendo en la expresin (ii), se encuentra que la ley cintica que rige el comportamiento de la velocidad de corrosin a una temperatura de 700C es la siguiente:
Temperatura de trabajo: 850C
Determinacin del rea (A)
Tabla 3.1. Dimensiones y rea de las lminas de acero a la temperatura de trabajo de 850C
Nro. Muestra 1 2 3 4 5 6 7 8 Largo (mm) 29 28,7 29,4 28,6 30,5 29,5 29,9 30,9 Ancho (mm) 9,5 9,5 9,5 9,5 9,5 9,5 9,9 9,5 Espesor (mm) 1,5 1,5 1,5 1,5 1,5 1,5 1,5 1,5
Determinacin de la ganancia de peso (g)
Tabla 3.2. Ganancia de peso de las muestras de acero para los diferentes tiempos de
control a la temperatura de trabajo de 850C Muestra 1 2 3 4 5 6 7 Tiempo (min) 15 15 30 30 60 60 90 Peso Inicial Peso Final (g) (g) 5,2815 5,2911 1,0224 1,0321 4,3124 4,3777 4,184 4,2375 1,4304 1,5035 4,1843 4,2286 4,6009 4,6534 g (g) 0,0096 0,0097 0,0653 0,0535 0,0731 0,0443 0,0525
Corrosin de metales a elevadas Temperaturas
8 90 5,0907 5,1953 0,1046
Determinacin de Expresin de la ley cintica
Tabla 3.3. Valores de Ganancia de peso por unidad de rea en funcin del tiempo, para la temperatura de trabajo de 850C
g/A (g/Cm2) 0,00144 0,00147 0,00967 0,00813 0,01045 0,00654 0,00738 0,01477 prom g/A (g/Cm2) 0,00146 0,00890 0,00849 0,01107 Log (g/A) (g/Cm2) -2,83710 -2,05051 -2,07086 -1,95571 Log t (min) 1,17609 1,47712 1,77815 1,95424
Muestra 1 2 3 4 5 6 7 8
t (min) 15 30 60 90
Grfica 3. Curva representativa de Log (g/A) Versus Log(t) para una temperatura de trabajo de 850C
y = 1,025x 3,865 y= mx + b
Corrosin de metales a elevadas Temperaturas
Finalmente, sustituyendo en la expresin (ii), se encuentra que la ley cintica que rige el comportamiento de la velocidad de corrosin a una temperatura de 850C es la siguiente:
Tabla 4. Cuadro resumen que muestra expresin cintica que rige la velocidad de corrosin de las lminas de acero para las temperaturas de 600C, 700C y 850C Temperatura (C) 600 700 850 n 1,53 2,94 0,98 K 8,40x10-7 1,01x10-9 1,63x10-4 Expresin cintica
Grfica 4. Representacin de Log(g/A) Vs. t para las temperaturas de trabajo de 600C, 700C y 850C.
Corrosin de metales a elevadas Temperaturas Grfica 5. Representacin de la velocidad de corrosin en funcin del tiempo a las temperaturas de 600, 700 y 850C.
Determinacin de la Energa de Activacin (Q)
Una vez deducida la ley cintica para las lminas de acero expuestas a las diferentes temperaturas (600, 700 y 850 C), se calcula la energa den activacin (Q); a travs de la expresin (iii).
Siendo; : Constante de Velocidad : Energa de Activacin : Constante universal de los Gases : Temperatura en grados kelvin Aplicando logaritmo a ambos lados de la expresin (iii), nos queda lo siguiente:
Corrosin de metales a elevadas Temperaturas
Al hacer la similitud con la ecuacin de una recta, tenemos que:
Donde,
Una vez establecida la ecuacin para determinar la energa de activacin, se grafica log(k) Vs (1/T), para lo cual se hace uso de los valores mostrados en la tabla 5. Tabla 5. Valores de Log(K) vs. (1/T) para temperaturas de 600, 700 y 850C.
T(C) 600 700 973 850 1123 0,00103 0,00089 1,01E-09 1,63E-04 T (k) 873 1/T 0,00115 K 8,40E-07 log(k) 0,00115 6,0757207 1 0,00103 8,9956786 3 0,00089 3,7878124 (1/T)
Grfica 4. Curva de Log(K) Vs. (1/T) para las temperaturas de 600, 700 y 850C Log (K) Vs. (1/T)
Corrosin de metales a elevadas Temperaturas Despejando Q, tenemos que: Q= - (- 9767 * (2,303 * 8,314 J/mol) ) Q= 187.010,14 J/mol
DISCUSIN DE RESULTADOS
Al realizar los clculos correspondientes para la determinacin de la ley cintica a las temperaturas de trabajo de 600C, 700C y 850C, se obtuvieron valores correspondientes al orden de reaccin de n= 1,53 para la temperatura de 600C; n=2,94 para la temperatura de trabajo de 700C y de n=0,98 para la temperatura de trabajo de 850C.
Corrosin de metales a elevadas Temperaturas De acuerdo a los resultados obtenidos a la temperatura de trabajo de 600C, se observa que la ley cintica que rige el proceso de corrosin a dicha temperatura, es de tipo lineal predominantemente, lo cual indica que las capas de xido formadas son porosas y poco protectoras, siendo el paso controlante, una reaccin qumica que ocurre rpidamente sin freno alguno a travs de la capa porosa de xidos. Para la temperatura de trabajo de 700C, se observa que la ley cintica no pudo ser determinada de manera satisfactoria, pues los resultados obtenidos para tal temperatura no concuerdan con lo registrado en la teora. Esto puede atribuirse principalmente a cambios en el gradiente trmico ocurridos en el interior del horno. Por otra parte, se observa que para la temperatura de trabajo de 850C, la ley cintica que rige el proceso de corrosin es de tipo lineal, siendo el paso controlante (como ya se mencion para la temperatura de 600C) una reaccin que ocurre con gran velocidad a travs de la porosa capa de xidos. Al observar la grfica 5, la cual involucra una representacin de (g/A) Vs. t, para las diferentes temperaturas de trabajo, se puede notar que a medida que se incrementa la temperatura de trabajo, se produce un aumento de la ganancia de peso por unidad de rea, lo cual significa que a mayor temperatura se favorecen las reacciones qumicas que ocurren a travs de la capa porosa de xidos, las cuales representan el mecanismo controlante para una ley de tipo lineal (esto exceptuando la temperatura de trabajo de 700C, que como se mencion anteriormente, no se pudo determinar satisfactoriamente). Esto a su vez nos indica que a mayor temperatura de trabajo, mayor es la velocidad de corrosin del material. Al analizar ahora la grfica 5 detalladamente y por separado para cada una de las temperaturas de trabajo, se observa adems, que para la temperatura de trabajo de 600C, a medida que se incrementa el tiempo de oxidacin, aumenta ganancia de peso por unidad de rea, y lo mismo ocurre para las temperaturas de trabajo de 700 y 850C. Todo esto nos indica, que a medida que se incrementa el tiempo de permanencia de la muestra en el horno, se incrementa la velocidad de las reacciones de oxidacin.
Siguiendo un anlisis cuidadoso de los resultados obtenidos en esta experiencia, se observa que para el caso del proceso de corrosin estudiado, la energa de activacin obtenida, definida como la cantidad de energa necesaria para que ocurra una transformacin, fue de 187.010,14 J/mol, y a pesar de que es necesario el alcance de dicho valor para que ocurra corrosin, se observa que para todas las temperaturas de trabajo dicho valor fue alcanzado, ms sin embargo, para temperaturas mayores la velocidad a la que ocurre dicha transformacin se ve favorecida.
Corrosin de metales a elevadas Temperaturas De manera general se puede decir que el proceso de corrosin de las lminas de acero al carbono empleado para la realizacin de la presente prctica, se rige por una ley de tipo lineal, exceptuando la temperatura de trabajo de 700C, para la cual se obtuvieron resultados no satisfactorios. Entre las posibles fuentes de error a las cuales pudiera atribuirse la obtencin de resultados no satisfactorios para la temperatura de trabajo de 700C, pueden mencionarse las siguientes: 1. Cada de temperatura en el horno a la hora de abrirlo y sacar las muestras.
2. Sobrecalentamiento de las muestras dentro del horno debido cambios en el gradiente trmico.
3. Prdida de peso de las muestras por la fractura de la capa de xido, ocasionada
por el choque trmico en el material al sacarlo del horno. Un cambio bruzco de temperatura podra causar un agrietamiento de la capa de corrosin y posteriormente una prdida de la capa de productos de corrosin que se ha formado sobre el metal. Al realizar los pesajes de las probetas, los valores de masa de productos de corrosin sern menores a los que se deberan ser obtenidos, causando as ciertas discrepancias en los valores. 4. Errores de medicin del rea expuesta a la corrosin. 5. Errores en la medicin del peso de las muestras debido a que cualquier objeto que se coloca cerca de las balanzas durante la medicin, las descalibra fcilmente.
6. Mala limpieza de las probetas. Un mal lijado de la superficie de las lminas de
metal, dara lugar a una posible disminucin del rea de adherencia de la capa de productos de corrosin sobre la probeta.
7. Posibles capas de grasa adheridas a la superficie de la muestra, debido al contacto
directo entre la mano del medidor y la superficie de la misma. Esto da lugar a una disminucin del rea de adherencia de la capa de corrosin. CONCLUSIONES
La ley cintica que rige la corrosin del acero al carbono estudiado, a altas
temperaturas es del tipo lineal, con una expresin general: y=k.t
Corrosin de metales a elevadas Temperaturas
El mecanismo controlante del proceso de corrosin es la velocidad de las reacciones qumicas que ocurren sobre la capa porosa de xidos. El incremento de la temperatura no produce efecto sobre la ley cintica que rige el proceso de corrosin, pero si favorece dicho proceso. A mayor temperatura, mayor es la velocidad de corrosin y mayor es la ganancia de peso por productos de corrosin en el metal estudiado. A mayor temperatura, menor es la energa necesaria para que el proceso de corrosin inicie (energa de activacin).
La energa de activacin del proceso de corrosin fue de 187.010,14 J/mol
RECOMENDACIONES
Corrosin de metales a elevadas Temperaturas
Limpiar bien la superficie de las muestras a ensayar y evitar el contacto con las
manos luego de la etapa de lavado y desengrasado del metal, ya que la grasa adherida a stas, disminuye el rea efectiva expuesta a la corrosin e introduce errores en los resultados.
Al introducir las probetas en el horno, llevar un control estricto del tiempo con el
fin de evitar una mayor ganancia de peso a causa de tiempos prolongados en el interior del horno, pues sto conllevara a posibles errores en los clculos. Monitorear constantemente la temperatura del horno, para evitar el sobrecalentamiento de las muestras que posteriormente pueda ocasionar errores durante los respectivos clculos.
Al momento de sacar las muestras del horno, intente hacerlo lo ms rpido posible
para evitar cadas en la temperatura dentro del horno as como disminuir riesgos de daos en el recubrimiento refractario de ste.
Realizar un esquema claro que identifique cada uno de los crisoles para evitar
confusiones a la hora de sacarlos del horno.
Corrosin de metales a elevadas Temperaturas
REFERENCIAS BIBLIOGRFICAS
Gil, Linda. Fundamentos de Corrosin y Proteccin de los metales. Trabajo
de Ascenso de la UNEXPO. (1993).
http://es.wikipedia.org/wiki/Corrosi%C3%B3n
S-ar putea să vă placă și
- Informe de Lab de Tratamientos Termicos.Document5 paginiInforme de Lab de Tratamientos Termicos.Emelys MorenoÎncă nu există evaluări
- Practica 3 Comportamiento Mecánico Ensayo de CompresiónDocument10 paginiPractica 3 Comportamiento Mecánico Ensayo de CompresiónJose Antonio MartinezÎncă nu există evaluări
- Fatiga y Fluencia (Creep)Document31 paginiFatiga y Fluencia (Creep)AliÎncă nu există evaluări
- Potencial de CorrosionDocument3 paginiPotencial de CorrosionAnabella Marycarmen Cuba Villanueva100% (1)
- Practica 4 Comportamiento MecánicoDocument5 paginiPractica 4 Comportamiento MecánicoJose Antonio MartinezÎncă nu există evaluări
- Corrosion Bajo TensionDocument9 paginiCorrosion Bajo TensionEliamnyÎncă nu există evaluări
- P1. Lixiviación.Document9 paginiP1. Lixiviación.Ivan ReynaÎncă nu există evaluări
- TAFELDocument13 paginiTAFELGustavo CabreraÎncă nu există evaluări
- 4 Ataque QuimicoDocument13 pagini4 Ataque QuimicoPABLO DIAZ ENRIQUEZÎncă nu există evaluări
- Fenomenos de Pasivacion Del MetalDocument1 paginăFenomenos de Pasivacion Del MetalJean Carlos Quispe SÎncă nu există evaluări
- Subenfriamiento ConstitucionalDocument5 paginiSubenfriamiento ConstitucionalIsaac ZTÎncă nu există evaluări
- Fundamentos de La Corrosión Asistida Por Esfuerzo para ExpoDocument4 paginiFundamentos de La Corrosión Asistida Por Esfuerzo para ExpoAndres Carmona0% (1)
- Normalizado, Recocido y Relevado de EsfuerzosDocument30 paginiNormalizado, Recocido y Relevado de EsfuerzosMIGUEL ANGEL SAMANO MORENOÎncă nu există evaluări
- Criterio de Desplazamiento Del Potencial 300 MVDocument8 paginiCriterio de Desplazamiento Del Potencial 300 MVAndres CarmonaÎncă nu există evaluări
- Plataforma Alexander KiellandDocument7 paginiPlataforma Alexander KiellandErikson Omar Pérez OrrilloÎncă nu există evaluări
- Mat Resistentes-CorrosiónDocument77 paginiMat Resistentes-CorrosiónpaolaÎncă nu există evaluări
- Mecanismos de Daño en HornosDocument94 paginiMecanismos de Daño en HornosMisAÎncă nu există evaluări
- Reporte 1 Deformacion PlasticaDocument4 paginiReporte 1 Deformacion Plasticamayin007mixÎncă nu există evaluări
- Reporte PIRODocument18 paginiReporte PIROJAVIER NICOLAS CERON ROMEROÎncă nu există evaluări
- Examen Ceramicos 2Document2 paginiExamen Ceramicos 2Cordova RaphaelÎncă nu există evaluări
- Serie 2.1 2018-2Document3 paginiSerie 2.1 2018-2ChpÎncă nu există evaluări
- P 3 - DiAGRAMAS DE ELLINGHAMDocument10 paginiP 3 - DiAGRAMAS DE ELLINGHAMAntony Quispe RoqueÎncă nu există evaluări
- Al P2 H Crisol Sem 22-1Document18 paginiAl P2 H Crisol Sem 22-1Jose Antonio MartinezÎncă nu există evaluări
- Electrometalurgia Practica 1Document5 paginiElectrometalurgia Practica 1DiegoÎncă nu există evaluări
- Práctica 2 ElectrometalurgiaDocument3 paginiPráctica 2 ElectrometalurgiaJonathan BautistaÎncă nu există evaluări
- Fabricacion de Polvos MetalurgicosDocument72 paginiFabricacion de Polvos MetalurgicosJjmc JjmcÎncă nu există evaluări
- Curvas de PolarizaciónDocument47 paginiCurvas de PolarizaciónChristian0% (1)
- Solucionario Metalurgia Mecanica DieterDocument19 paginiSolucionario Metalurgia Mecanica DieterMoisés Morera AlfaroÎncă nu există evaluări
- Materiales RefractariosDocument6 paginiMateriales RefractariosAleks Meraz GtnÎncă nu există evaluări
- VARDocument14 paginiVARcarolina rodriguezÎncă nu există evaluări
- Previo de Poder CubrienteDocument2 paginiPrevio de Poder CubrienteItzelitaiqmÎncă nu există evaluări
- Jitorres - La Transformación Bainitica en Aceros, GuiaDocument11 paginiJitorres - La Transformación Bainitica en Aceros, Guiajuanpablo bohorquez ricoÎncă nu există evaluări
- Articulo CorrosiónDocument2 paginiArticulo CorrosiónlolaÎncă nu există evaluări
- Consideraciones Del Tratamiento Térmico Según La Norma Astm A600Document3 paginiConsideraciones Del Tratamiento Térmico Según La Norma Astm A600Calis ThenicsÎncă nu există evaluări
- Corrosión Bajo TensiónDocument13 paginiCorrosión Bajo TensiónPablo Xavier Martz Monts100% (1)
- Atmósferas en Los Tratamientos TérmicosDocument8 paginiAtmósferas en Los Tratamientos TérmicosJoshua ThomasÎncă nu există evaluări
- Informe de Recocido y NormalizadoDocument17 paginiInforme de Recocido y NormalizadoPablo Salinas ValeroÎncă nu există evaluări
- Solidificacion LingotesDocument6 paginiSolidificacion LingotesenriqueÎncă nu există evaluări
- Lección VDiagramas de Pourbaix 2018Document78 paginiLección VDiagramas de Pourbaix 2018Benjamín VitónÎncă nu există evaluări
- Ensayo JominyDocument20 paginiEnsayo JominyvhenriquezmÎncă nu există evaluări
- Introduccion Al GalvanizadoDocument103 paginiIntroduccion Al GalvanizadoGerman Agudelo CorreaÎncă nu există evaluări
- Laboratorio #1 Recocido y NormalizadoDocument19 paginiLaboratorio #1 Recocido y NormalizadoMiguel ArguzÎncă nu există evaluări
- Primer Examen de Hidrometalurgia02Document1 paginăPrimer Examen de Hidrometalurgia02Ivan Carpio VilchisÎncă nu există evaluări
- Prob. Corrosion 02Document13 paginiProb. Corrosion 02Manuel AguilarÎncă nu există evaluări
- Fundición Tarea 1 (2023-2)Document4 paginiFundición Tarea 1 (2023-2)Ariadna VeraÎncă nu există evaluări
- Tarea 12 - ResueltaDocument5 paginiTarea 12 - ResueltaZyanya HernándezMÎncă nu există evaluări
- Practica 2 Comportamiento MecánicoDocument7 paginiPractica 2 Comportamiento MecánicoJose Antonio MartinezÎncă nu există evaluări
- Electrobeneficio de CobrepaolaDocument21 paginiElectrobeneficio de CobrepaolaLibros Argón100% (1)
- Villafranca Martinez Fundicion Tarea 1 (2022-1)Document3 paginiVillafranca Martinez Fundicion Tarea 1 (2022-1)Jose Antonio MartinezÎncă nu există evaluări
- Corrosión GravimetríaDocument5 paginiCorrosión GravimetríaLina MedinaÎncă nu există evaluări
- Silabo Corrosión 2019Document7 paginiSilabo Corrosión 2019José CorreaÎncă nu există evaluări
- Corrosion Clase 2Document19 paginiCorrosion Clase 2Maite ZuritaÎncă nu există evaluări
- Materias Primas No Plásticas PDFDocument5 paginiMaterias Primas No Plásticas PDFAnonymous mvcs2YÎncă nu există evaluări
- Obtencion de Icorr y Unidades de Velocidad de CorrosionDocument4 paginiObtencion de Icorr y Unidades de Velocidad de CorrosionIván HTÎncă nu există evaluări
- Tarea RPL JuanValenciaDocument13 paginiTarea RPL JuanValenciajuan valencia100% (1)
- Astm A514 GR BDocument6 paginiAstm A514 GR BelweldÎncă nu există evaluări
- Recristalización de AcerosDocument10 paginiRecristalización de AcerosJuan Mendoza100% (1)
- Articulo CTODDocument8 paginiArticulo CTODlduran_63Încă nu există evaluări
- Ingeniería de procesos siderúrgicos: La experiencia de AHMSADe la EverandIngeniería de procesos siderúrgicos: La experiencia de AHMSAÎncă nu există evaluări
- El Informe TécnicoDocument42 paginiEl Informe TécnicoMarcelo DelgadoÎncă nu există evaluări
- Analisis Por Elementos Finitos de Solid WorksDocument61 paginiAnalisis Por Elementos Finitos de Solid WorksDavid Rios CruzÎncă nu există evaluări
- Curso SAP2000 J.lavado&JJ - Granados v2012Document173 paginiCurso SAP2000 J.lavado&JJ - Granados v2012simonrierallordellaÎncă nu există evaluări
- Motion Sim Student WB 2011 ESPDocument23 paginiMotion Sim Student WB 2011 ESPAlcides Luis Fabián BráñezÎncă nu există evaluări
- Expo de IndustrialDocument27 paginiExpo de IndustrialAnny FigueroaÎncă nu există evaluări
- Tablas Perfiles MetalicosDocument44 paginiTablas Perfiles MetalicosOmar ST100% (1)
- PDF Manual Lineas de Aire PDFDocument16 paginiPDF Manual Lineas de Aire PDFMAXI ZAPATAÎncă nu există evaluări
- Ajustando Distribución (Datos Censurados)Document17 paginiAjustando Distribución (Datos Censurados)justorfcÎncă nu există evaluări
- Dinamica de GrupoDocument5 paginiDinamica de GrupoAnny FigueroaÎncă nu există evaluări
- Análisis de ParetoDocument6 paginiAnálisis de ParetojustorfcÎncă nu există evaluări
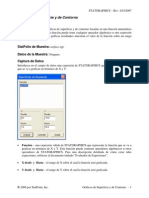
- Gráficos de Superficie y ContornoDocument7 paginiGráficos de Superficie y ContornoAnny FigueroaÎncă nu există evaluări
- OrganigramaDocument1 paginăOrganigramaAnny FigueroaÎncă nu există evaluări
- Inp TrabequiDocument15 paginiInp TrabequiJulio Cesar PonceÎncă nu există evaluări
- Análisis Componentes de La VarianzaDocument9 paginiAnálisis Componentes de La VarianzajustorfcÎncă nu există evaluări
- Presentación 1Document1 paginăPresentación 1Anny FigueroaÎncă nu există evaluări
- Villasenor Ruiz Oscar Gerardo 44548Document75 paginiVillasenor Ruiz Oscar Gerardo 44548Lisa ScottÎncă nu există evaluări
- Pastel de Zanahoria (Baja en Calorías)Document1 paginăPastel de Zanahoria (Baja en Calorías)Anny FigueroaÎncă nu există evaluări
- Capitulo I AnnyDocument30 paginiCapitulo I AnnyAnny FigueroaÎncă nu există evaluări
- Los SindicatosDocument4 paginiLos SindicatosAnny FigueroaÎncă nu există evaluări
- Obtención Del Coque y Carbón de HumoDocument3 paginiObtención Del Coque y Carbón de HumoAnny FigueroaÎncă nu există evaluări
- Estudio de OptimizacionDocument14 paginiEstudio de OptimizacionAnny FigueroaÎncă nu există evaluări
- JvelazDocument10 paginiJvelazAnny FigueroaÎncă nu există evaluări
- Coste SiderurgicoDocument12 paginiCoste SiderurgicoAnny FigueroaÎncă nu există evaluări
- Tipos de Antena Que Se Utiliza en Las MicroondasDocument39 paginiTipos de Antena Que Se Utiliza en Las MicroondasGlenmar Valladares SalasÎncă nu există evaluări
- Análisis Del Comportamiento Sísmico de Entibaciones en Suelos Finos Del SectorDocument203 paginiAnálisis Del Comportamiento Sísmico de Entibaciones en Suelos Finos Del Sectordavidfer2Încă nu există evaluări
- Taller 1 Mecanica de MaterialesDocument15 paginiTaller 1 Mecanica de MaterialesALEX DANIEL MENESES ANDRADEÎncă nu există evaluări
- Taller 3 LipidosDocument3 paginiTaller 3 LipidosSergio Rozo PerdomoÎncă nu există evaluări
- Thionyl Chloride MSDS SPDocument4 paginiThionyl Chloride MSDS SPBrayan GallosoÎncă nu există evaluări
- Ensayo de Corte DirectoDocument38 paginiEnsayo de Corte DirectoDaniel GarciaÎncă nu există evaluări
- Laboratorio de Topografia I y IIDocument13 paginiLaboratorio de Topografia I y IIAide marily Charca CoilaÎncă nu există evaluări
- Actividad 1Document3 paginiActividad 1Yehidi CarrascoÎncă nu există evaluări
- Tarea 5-Realizar Síntesis Método Muestreo Enfoque Cualitativo Investigación CientíficaDocument5 paginiTarea 5-Realizar Síntesis Método Muestreo Enfoque Cualitativo Investigación CientíficaWalter AguirreÎncă nu există evaluări
- Trabajo Practico N 2 de Algebra Lineal 2Document11 paginiTrabajo Practico N 2 de Algebra Lineal 2Francisco PolzoniÎncă nu există evaluări
- Geologia Estructural. 2015-1Document347 paginiGeologia Estructural. 2015-1Rosy GuzmanÎncă nu există evaluări
- Exda-2 Conocemos Actividades para Mejorar La Convivencia en FamiliaDocument7 paginiExda-2 Conocemos Actividades para Mejorar La Convivencia en FamiliaJeniffer Julisa Zela HuaytaÎncă nu există evaluări
- Inhaloterapia y NebulizacionesDocument47 paginiInhaloterapia y NebulizacionesAna Claudia Bullon Cuadra60% (5)
- La Holonimia y La MeronimiaDocument13 paginiLa Holonimia y La MeronimiaCALIDAD SUPREMA Y LOS QUE ELLOS QUIERANÎncă nu există evaluări
- Punteros en C++Document13 paginiPunteros en C++Gabriel AguirreÎncă nu există evaluări
- Puente HidraulicoDocument6 paginiPuente HidraulicoJosue Zenteno ortizÎncă nu există evaluări
- Estudio Ecologico MGDocument36 paginiEstudio Ecologico MGRaul Cerron GarciaÎncă nu există evaluări
- Comparación Ecofisiológica de Tres Especies Del Género Lantana L. (VerbenaCeae)Document12 paginiComparación Ecofisiológica de Tres Especies Del Género Lantana L. (VerbenaCeae)Diego FlosiÎncă nu există evaluări
- BGH Folleto Multisplits 2016Document7 paginiBGH Folleto Multisplits 2016Romina GalachoÎncă nu există evaluări
- Formulario de Refrigeración y Aire AcondicionadoDocument4 paginiFormulario de Refrigeración y Aire Acondicionadoauca56640123100% (2)
- Sismica TAREA 3Document5 paginiSismica TAREA 3Elio MuñozÎncă nu există evaluări
- 1 Distensibilidad Vascular y Funciones de Los Sistemas Arterial y VenosoDocument2 pagini1 Distensibilidad Vascular y Funciones de Los Sistemas Arterial y Venosoclases FCSÎncă nu există evaluări
- Tarjetas Kardex Productos TerminadosDocument28 paginiTarjetas Kardex Productos Terminadosjuly coyÎncă nu există evaluări
- Visualidad - Algoritmo-InteracciónDocument180 paginiVisualidad - Algoritmo-InteracciónPabloÎncă nu există evaluări
- Clase 9. Biología de Los EcosistemasDocument17 paginiClase 9. Biología de Los EcosistemasCesar Britos AquinoÎncă nu există evaluări
- Probabilístico, Mapa Mental!Document2 paginiProbabilístico, Mapa Mental!Wendy ChiÎncă nu există evaluări
- 02 - Etapas de Salida de SensoresDocument16 pagini02 - Etapas de Salida de SensoresCarlos HerreraÎncă nu există evaluări
- Devenir e InmutabilidadDocument19 paginiDevenir e Inmutabilidadapi-3819692Încă nu există evaluări
- Jaime Segarra El Excitante Camino Al Exito Segunda Edicion GratuitoDocument7 paginiJaime Segarra El Excitante Camino Al Exito Segunda Edicion Gratuitoerick_abreuvÎncă nu există evaluări
- Examen FinalDocument4 paginiExamen FinalJorge Alatrista RojasÎncă nu există evaluări