Documente Academic
Documente Profesional
Documente Cultură
Cancer de Mama
Încărcat de
Karla Lorena0 evaluări0% au considerat acest document util (0 voturi)
22 vizualizări81 paginicancer de mama diplomado ecografia
Titlu original
CANCER DE MAMA
Drepturi de autor
© © All Rights Reserved
Formate disponibile
PPTX, PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentcancer de mama diplomado ecografia
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PPTX, PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
22 vizualizări81 paginiCancer de Mama
Încărcat de
Karla Lorenacancer de mama diplomado ecografia
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PPTX, PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 81
El Cancer
MsC Dr. Gustavo Yanes.
Cancer. ¿De dónde sale?
• La diferenciación celular es el proceso por el
cual las células de un linaje celular concreto
(el linaje celular se determina en el momento
de la formación del embrión) sufren
modificaciones en su expresión génica, para
adquirir la morfología y las funciones de un
tipo celular específico y diferente al resto de
tipos celulares del organismo.
Diferenciacion celular
Celula madre pluripotencial
Diferenciación
• Todas las células del organismo proceden de un
cigoto, de la fecundación de un óvulo por
un espermatozoide, se desarrollan a un tejido
integral gracias a la diferenciación celular.
• En los organismos pluricelulares todas las células
no son idénticas. Por ejemplo, las células que
forman la piel son diferentes se organizan por
estratos que van remplazandose entre si, sin
embargo todos derivan de una sola célula inicial.
Capacidad de diferenciación.
• Las celulas con capacidad de diferenciación se
denominan célula madre. Se clasifican según su
capacidad de diferenciación
en totipotentes, pluripotentes, multipotentes y u
nipotentes.
• No todos los tejidos tienen la misma capacidad de
diferenciacion.
• En los mamíferos, solo el cigoto y las células
embrionarias jóvenes son totipotentes, mientras
que en las plantas y hongos, muchas células son
totipotentes.
Mecanismos para la diferenciacion
• La diferenciación es un mecanismo mediante el cual una célula no
especializada sufre modificaciones citológicas, dando lugar a los
numerosos tipos celulares que forman el cuerpo
• Durante la diferenciación, ciertos genes son expresados mientras
que otros son reprimidos.
• Este proceso es intrínsecamente regulado gracias a distintos
mecanismos de regulación de la expresión genética de las células
para que la célula diferenciada adquiera determinadas funciones.
• Todos estos aspectos pueden ser modificados durante la
diferenciación.
• En citopatología, el nivel de diferenciación celular es utilizado
como una medida de la progresión de un cáncer.
Mecanismos generales de control de la
diferenciación celular
• Como cualquier proceso celular, la diferenciación
celular se debe a reacciones bioquímicas que tienen
lugar en el interior de la célula, y está promovida por
complejas cascadas de señalización.
• Morfógenos: Sustancias, normalmente proteínas que
aparecen en un gradiente de concentración en la
célula o en el medio que la rodea coadyuga en el
destino durante la diferenciación, son clave en la
señalización que lleve a la expresión de unos u otros
genes.
• Regulación génica como control genómico, control
transcripcional, control posttranscripcional, control
traduccional y control posttraduccional.
Reprogramación de células
animales diferenciadas a
células indiferenciadas
• La clonación de la oveja Dolly demostró que en los ovocitos de
mamíferos se encontraban presentes ciertos factores de
transcripción capaces de reprogramar el núcleo, no sólo
manteniendo su estado de indiferenciación, sino induciendo
en núcleos de células diferenciadas una vuelta hacia el estado
indiferenciado.
• Mediante estudios por técnicas de microarrays se
encontraron algunos de estos factores como Oct4, Sox 2,
Nanog, Tdgf1, Utf1, Lin28, etc.
• El hecho de que estos factores pueden no sólo mantener la
célula indiferenciada si no reprogramar su núcleo una vez
diferenciada, fue demostrado por el grupo de Yamanaka
(Nobel 2012) . También se ha conseguido reprogramar
fibroblastos humanos con estos factores.
Metaplasia
• Se llama metaplasia a la transformación citológica de un
epitelio maduro en otro que puede tener un parentesco
próximo o remoto, la gran mayoría de las veces responde
a cambios adaptativos, agentes físicos, químicos o
biológicos
• Los fenómenos de metaplasia son completamente
normales y reversibles como mecanismos adaptativos.
• La metaplasia implica una regresión en la especialización o
maduración de las células hacia formas más primitivas
para más tarde madurar hacia otra clase de células.
• La metaplasia puede presentarse como una respuesta
adaptativa fisiológica frente al estrés celular y es
reversible una vez cesa el estímulo agresor.
• No se considera una lesión neoplásica o premaligna.
• La metaplasia más común es la de epitelio columnar a
epitelio escamoso.
Metaplasia
• La zona de transición entre el tejido normal y el
metaplásico por ser una zona muy activa mitóticamente
puede ser el asiento para la generación de células
displásicas con el consiguiente potencial de malignidad.
• Existe una controversia en considerar la metaplasia
intestinal del esófago como lesión premaligna, pero en
líneas generales se considera como un mecanismo
adaptativo que revierte con el cese del estímulo.
• Si el estímulo agresor persiste puede inducir la
transformación neoplásica a partir de mutaciones en el
genoma de la célula existiendo diversos marcadores de
mutación como inactivación del gen P16 y p53.
Displasia.
• Displasia (Dificultad para hacer) refiere a una anormalidad en el
aspecto de las células debido a alteraciones en el proceso de
maduración de las mismas.
• Lesión celular caracterizada por una modificación irreversible
del ADN que causa la alteración de la morfología y/o de la
función celular.
• La displasia también puede acabar provocando una neoplasia.
• Presentan alteraciones atípicas que afectan a su tamaño, forma
y organización.
• El nivel de cambio respecto a su orientación esperada es
indicativo de la fase de evolución hacia la transformación en
neoplasia. Por lo tanto la displasia es un cambio preneoplásico
o precanceroso.
• Si se produce un incremento en el número de células se
convierte en una hiperplasia.
Displasia
• Este crecimiento anormal se restringe a la capa
epitelial, no invadiendo el tejido más profundo.
• Aunque la displasia puede desaparecer
espontáneamente, es posible extirparla mediante
cirugía, métodos quimicos, calor quemante, láser,
o aplicación de frío (crioterapia).
• Estos cambios pueden ser reversibles, y al
desaparecer la causa inductora, el epitelio puede
volver a la normalidad.
• Los cambios displásicos de los tejidos están
considerados como precursores del cáncer.
• También se utiliza el término displasia para
expresar la anomalía en el desarrollo de un
órgano.
• Dependiendo del órgano afectado puede
hablarse de displasia dental, displasia
congénita de cadera, displasia facial, displasia
renal, etc.
• Estas anomalías no tienen relación alguna con
el cáncer ni son alteraciones premalignas.
Cáncer
• Cáncer: Es el nombre común que recibe un conjunto de enfermedades
relacionadas en las que se observa un proceso descontrolado en la
división de las células del cuerpo.
• El cáncer se menciona en documentos históricos muy antiguos, entre
ellos papiros egipcios del año 1600 a. C. Se cree que el
médico Hipócrates fue el primero en utilizar el término carcinos.
• Puede conducir a la muerte del paciente si o recibe tratamiento
adecuado.
• Se conocen más de 200 tipos diferentes de cáncer. Los más comunes
son: de piel, pulmón, mama y colorrectal.
• Es el resultado de dos procesos sucesivos: la proliferación de un grupo
de células, denominado tumor o neoplasia, y la capacidad invasiva que
les permite colonizar y proliferar en otros tejidos u órganos, proceso
conocido como metástasis.
Malignidad
• La malignidad del cáncer es variable, según la
agresividad de sus células y demás características
biológicas de cada tipo tumoral.
• El comportamiento de las células cancerosas se
caracteriza por carecer del control reproductivo que
requiere su función original, perdiendo sus
características primitivas y adquiriendo otras que no les
corresponden, como la capacidad de invadir de forma
progresiva y por distintas vías a órganos próximos
(metástasis), con crecimiento y división más allá de los
límites normales del órgano, diseminándose por el
organismo fundamentalmente a través del sistema
linfático o el sistema circulatorio, y ocasionando el
crecimiento de nuevos tumores en otras partes del
cuerpo alejadas de la localización original.
Benignidad vs malignidad
• Las diferencias entre tumores benignos y malignos consisten en
que los benignos son de crecimiento lento, no se propagan a otros
tejidos y rara vez recidivan tras ser extirpados muchas veces son
encapsulados.
• Los malignos son de crecimiento rápido, se propagan a otros
tejidos, recidivan y provocan la muerte en un periodo variable de
tiempo.
• Los tumores malignos tienen repercusiones graves, puesto que
estas células consumen los nutrientes que necesitan otros
órganos. Mientras crece un tumor, este crea vasos sanguíneos
(angiogénesis) para alimentarse, ya no pocas veces su crecimiento
supera la capacidad de neoformación de vasos produciendo areas
de necrosis en el mismo tumor.
• Las células normales al entrar en contacto con las células vecinas
inhiben su multiplicación, pero las células malignas no tienen este
freno de ahí su capacidad de invadir órganos vecinos.
• La mayoría de los cánceres forman tumores sólidos, pero algunos
no, por ejemplo la leucemia.
Benigno Maligno
Benigno Maligno
Benigno Maligno
• El cáncer puede afectar a personas de todas las
edades, incluso a fetos, pero el riesgo de sufrir los
más comunes se incrementa con la edad.
• El cáncer causa cerca del 13 al 24 % de todas las
muertes.
• La carcinogénesis se debe a alteraciones en el
material genético de las células motivadas por
distintos agentes carcinógenos como la radiación
ionizante, ultravioleta, productos químicos
procedentes de la industria, del humo
del tabaco y de la contaminación en general, o de
agentes infecciosos como el virus del papiloma
humano o el virus de la hepatitis B.
• Anormalidades genéticas cancerígenas son
adquiridas durante la replicación normal del ADN,
heredadas o bien al no corregirse los errores que
se producen durante dicho proceso.
• Otras aspectos de la genética del cáncer, como
la metilación del ADN y los microARNs y
elementos oxidativos están siendo estudiados
como importantes factores a tener en cuenta por
su implicación.
Composicion
• Todos los tumores, benignos y malignos, tienen
dos componentes básicos en su estructura:
• Las células proliferantes que forman el tumor
propiamente dicho y constituyen el parénquima.
• El estroma de sostén, constituido por tejido
conectivo y vasos sanguíneos.
• Los vasos sanguíneos que lo componen no es
tejido tumoral, su formación ha sido inducida por
el propio tumor.
• La nomenclatura oncológica se basa en el
componente parenquimatoso.
Clasificación del cancer
• El cáncer se clasifica según el tejido a partir del cual las
células cancerosas se originan y su carácter benigno o
maligno.
• Para su determinación se tienen en cuenta aspectos clínicos
e imagenológicos pero la clasificación histológica tras
la biopsia de la lesión, es quien determina.
• En los últimos años se ha producido un significativo
progreso en el desarrollo de medicamentos que actúan
específicamente en anormalidades moleculares de ciertos
tumores y minimizan el daño a las células normales.
• A pesar de las mejoras continuas de las tasas de curación,
algunas formas de cáncer continúan presentando mal
pronóstico.
Clasificacion
• El 90 % de los tumores son generados por
células epiteliales, denominándose
carcinomas.
• Los sarcomas derivados de células del tejido
conectivo o muscular.
• Las leucemias, linfomas, y mielomas se
originan de las células de la sangre.
• Los neuroblastomas y gliomas derivan de
células del sistema nervioso.
Nomenenclatura de los tumores
benignos
• Tumores benignos: Su nombre acaba en el
sufijo oma. Dependiendo del tejido del que
procedan, pueden ser: fibroma (tejido conjuntivo
fibroso), mixoma (tejido conjuntivo
laxo), lipoma (tejidoadiposo), condroma (tejido
cartilaginoso), etc.
• Algunos de los tumores benignos derivados de
tejido epitelial terminan con el sufijo "adenoma"
porque el tejido epitelial de origen forma
glándulas.
Nomenclatura de los tumores malignos
o cáncer
• Tumores malignos o cáncer: su nombre suele
acabar en el sufijo sarcoma o carcinoma.
• Muchos de ellos como el melanoma el
seminoma y el linfoma son de carácter
maligno a pesar de que su nombre termine
en el (sufijo oma) similar a la de los tumores
benignos.
Carcinomas, sarcomas, gliomas
Leucemias y linfomas.
• Neoplasias malignas de origen epitelial, son el 80 % del los
tumores malignos; por ejemplo: carcinoma epidermoide o
escamoso, adenocarcinoma, cistoadenocarcinoma, coriocarcinom
a, carcinoma de mama.
• Sarcomas. Los cánceres que derivan de los tejidos
mensenquimatosos o mesodermo se denominan sarcomas (del
griego sarcos, "carnoso");
liposarcoma, condrosarcoma, osteosarcoma.
• Gliomas. Los tumores que proceden del tejido nervioso son los
gliomas, realmente no se trata de un tumor derivado de células
nerviosas, sino de uno de los tipos celulares encargados de su
sostén, las células gliales. Algunas de las variedades de gliomas
son el glioblastoma, oligodendroglioma y ependimoma.
• Leucemias y linfomas. Son cánceres hematológicos derivados del
tejido linfoide y el mieloide respectivamente.
Mecanismos supresores de tumores
• Sistema Inmunologico celulas K
• La regulación de la transducción de señales.
• La apoptosis. La muerte celular programada o
apoptosis
• La reparación del ADN. Es un conjunto de
procesos mediante los cuales una célula
identifica y corrige los daños producidos en el
ADN.
Factores asociados al cancer
• Autoinmunidad e inflamación.
• Hormonas.
• Algunas hormonas juegan un papel en el desarrollo del cáncer, mediante
la promoción de la proliferación celular. Los factores de crecimiento
insulínico desempeñan un papel clave en la proliferación de células
cancerosas, la diferenciación celular y la apoptosis, lo que sugiere la
posible participación en la carcinogénesis. Las hormonas tambien son
agentes importantes en los cánceres relacionados con el sexo, como
el cáncer de mama, de endometrio de próstata, de ovario y de testículo, y
también en el cáncer de tiroides y el cáncer de hueso.
• Agentes físicos y químicos.
• Genética
• Radiación
• Infección Los virus que pueden causar cáncer se denominan oncovirus.
• Productos químicos
Gradación y estadificación
• La gradación es un sistema que emplea para clasificar
las células cancerosas en cuanto a su diferencia de las
células normales observadas al microscopio.
• El grado histológico, también llamado diferenciación,
se refiere a la semejanza que tengan las células del
tumor con las células normales del mismo tipo de
tejido.
• Las células bien diferenciadas o de grado 1 se parecen
a las células normales, por ello tienden a multiplicarse
lentamente y el cáncer es menos agresivo, por contra
las células indiferenciadas
• El grado 4, tienden a multiplicarse y extenderse con
más rapidez, por lo que se encuentran en cánceres
que se comportan con más agresividad.
• Grado:
• GX No es posible asignar un grado (Grado indeterminado).
• G1 Bien diferenciado (Grado bajo).
• G2 Moderadamente diferenciado (Grado intermedio).
• G3 Mal diferenciado (Grado alto).
• G4 Indiferenciado (Grado alto).
• La estadificación se utiliza para describir la gravedad del
cáncer basándose en la extensión del tumor original y si el
cáncer se ha diseminado en el cuerpo. El sistema más
empleado es el TNM (Tumor, Node (nódulo, ganglio) y
Metástasis) que valora la enfermedad local (tamaño
tumoral), regional (número de ganglios afectados) y
diseminación a distancia (presencia de metástasis).83
Tamaño del tumor
• TX El tumor primario no puede ser evaluado.
• T0 No hay evidencia de tumor primario.
• Tis Carcinoma in situ (cáncer inicial que no se
ha diseminado a tejidos vecinos)
• T1, T2, T3, T4 Tamaño y/o extensión del
tumor primario.
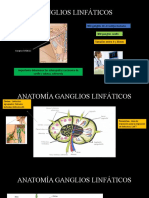
Ganglios linfáticos
• Ganglios linfáticos regionales
• NX No es posible evaluar los ganglios linfáticos
regionales
• N0 No existe complicación de ganglios
linfáticos regionales (no se encontró cáncer en
los ganglios linfáticos).
• N1, N2, N3 Complicación de ganglios linfáticos
regionales (número y/o extensión de
diseminación).
Metástasis
• MX No es posible evaluar una metástasis
distante.
• M0 No existe metástasis distante (el cáncer no
se ha diseminado a otras partes del cuerpo).
• M1 Metástasis distante (el cáncer se ha
diseminado a partes distantes del cuerpo).
Elementos comunes de los sistemas de
estadificación:
• Sitio del tumor primario.
• Tamaño y número de tumores.
• Complicación de ganglios linfáticos
(diseminación del cáncer a los ganglios
linfáticos).
• Tipo de célula y grado del tumor (qué tanto se
parecen las células cancerosas al tejido
normal).
• Presencia o ausencia de metástasis.
Tratamiento
El tratamiento del cáncer se fundamenta en tres
pilares: cirugía, quimioterapia y radioterapia. Otras
posibilidades de tratamiento incluyen
la hormonoterapia, o supresores hormonales,
la inmunoterapia, nuevas dianas terapéuticas no
citotóxicas y el trasplante de médula. El tratamiento
puede ser multidisciplinar, por exigir la cooperación
entre distintos profesionales: médico de cabecera,
cirujano, oncólogo, dermatólogo, neumólogo,
ginecólogo, etc
Pronóstico
• Las posibilidades de supervivencia una vez realizado el
diagnóstico, dependen primordialmente de lo
temprano que se haya descubierto la enfermedad y
del tipo de cáncer, pues algunos son más agresivos
que otros. Las estadísticas de supervivencia se realizan
generalmente en porcentaje de pacientes vivos 5 años
después del momento del diagnóstico. Excluyendo los
carcinomas de piel que se curan casi en el 100 % de los
casos, con las técnicas terapéuticas actuales, el cáncer
es curable en aproximadamente el 50 % de los
pacientes. Los principales factores que influyen en el
pronóstico son
Cancer de mama
realización de la US
mamaria según las guías del Colegio
Americano de Radiología
• 1. Evaluación inicial de anomalías palpables en
mujeres
• menores de 30 años.
• 2. Caracterización de las lesiones quísticas.
• 3. Identificación y caracterización de anomalías
mamográ-ficas palpables y no palpables en mujeres
mayores.
• 4. Como guía para procedimientos intervencionistas.
• 5. Evaluación de problemas asociados con implantes
• mamarios.
• 6. Evaluación del seno de las mujeres embarazadas
• Del total de los carcinomas de mama, menos del 1 % ocurren en varones
El cáncer de mama
Es una proliferación maligna de las células
epiteliales que revisten los conductos o lobulillos
mamarios. Es una enfermedad clonal; donde una
célula individual producto de una serie de
mutaciones somáticas o de línea germinal adquiere
la capacidad de dividirse sin control ni orden,
haciendo que se reproduzca hasta formar un tumor.
El tumor resultante, que comienza como anomalía
leve, pasa a ser grave, invade tejidos vecinos y,
finalmente, se propaga a otras partes del cuerpo.
Dos tipos principales de cáncer de
mama.
- El carcinoma ductal infiltrante, que comienza en los
conductos que llevan leche desde la mama hasta
el pezón, es por mucho el más frecuente
(aproximadamente el 80 % de los casos).
- El segundo lugar lo ocupa el carcinoma lobulillar
infiltrante (10 a 12 % de los casos), que comienza en
partes de las mamas llamadas lobulillos, que producen
la leche materna. (adenocarcinomas, ya que derivan de células de
estirpe glandular)
Los restantes tipos de cáncer de mama no superan en
conjunto el 10 % de los casos.
Existen tumores malignos de mama que no son de estirpe glandular ni epitelial. Estos tumores, poco frecuentes, reciben otros
nombres genéricos diferentes. Los sarcomas son producto de la transformación maligna de células del tejido conectivo de la
mama. Los linfomas derivan de los linfocitos, un tipo de glóbulos blancos que procede de los ganglios linfáticos. En general, los
linfomas no son tumores raros, pero es raro que un linfoma tenga su lugar de origen en una mama y no en otras regiones del
cuerpo.
Estadificacion del cancer de mama
• Estadio 0: es una enfermedad pre-maligna o con marcadores
positivos (a veces llamada CDIS: carcinoma ductal in situ). Sería el
momento en que la célula se ha transformado recientemente en
cancerígena, pero todavía no ha roto la membrana basal.
• Estadio 1: las células cancerígenas ya han superado la membrana
basal, pero el tumor no supera los 2 cm de tamaño.
• Estadio 2: semejante al estadio 1 pero el tumor ya es mayor de
2 cm, pero no más de 5 cm ya que no se ha diseminado todavía a
los ganglios linfáticos.
• Estadio 3: dentro de este estadio se tienen distintos clasificaciones
en función del tamaño de la masa tumoral y de si los nódulos
linfáticos están afectados o no.
• El estadio 4 se define como cáncer en etapa 'avanzada' y/o cáncer
metastásico porque el cáncer se diseminó hasta otros órganos del
cuerpo. Este tipo de cáncer metastatiza con mayor frecuencia en
los huesos, los pulmones, el hígado o el cerebro y tiene un mal
pronóstico.
Factores de riesgo
• Edad avanzada.
• Primera menstruación a temprana edad.
• Edad avanzada en el momento del primer parto o
nunca haber dado a luz.
• Antecedentes familiares de cáncer de mama.
• Hormonas como estrógeno y progesterona.
• Alcohol y tabaco
• Raza blanca.
• Entre 5 a 10 % de los casos, el cáncer de mama es
causado por mutaciones genéticas heredadas.
Desde hace varias décadas, el cáncer de mama se ha incrementado en
grado notable alrededor del mundo, sobre todo en países occidentales
Detección de el cáncer de mama.
• Mamografía
• Ultrasonido mamario con transductores de alta resolución
(ecografía).
• Prueba de receptores de estrógeno y progesterona o
imágenes por resonancia magnética.
• Biopsia mamaria (PAAF o BAAF).
• Hay técnicas que, mediante ultrasonido, pueden sugerir
malignidad, como la Ecografía Doppler, 3D multicortes o
elastografía, pero todas deben ser evaluadas y solo se
tendrá un diagnóstico definitivo mediante una biopsia.
• Obviamente, por todos los métodos de imagen, se tienen
caracterizaciones de lo que puede ser un cáncer o no, para
lo cual, se usa el método BI-RADS, con el fin de decidir la
conducta según esa clasificación.
Sensibilidad a receptores.
Marcadores biológicos
En el cáncer de mama hay tres receptores que son
usados como marcadores tumorales:
Receptor de estrógeno (ER) (+ en el 70%).
Receptor de progesterona (PR)
HER2/neu (+ en el 30% oncogen).
Aquellas células que no sobre-expresen ninguno de
estos receptores se denominan basales o triple
negativos. Todos de estos receptores son
identificados por inmuno-histoquimica y genética
molecular.
• Ya desde el año 1992 el American College of
Radiology desarrolló el Breast Imaging
Reporting and Data System (BI- RADS®), como
un método para clasificar los hallazgos
mamográficos. Los objetivos del BI-RADS son:
• Sistema de categorización
• BI-RADS 0: Evaluación adicional
• BI-RADS 1: Negativa
• BI-RADS 2: Benigna
• BI-RADS 3: Probablemente benigna
• BI-RADS 4: Anormalidad sospechosa
• BI-RADS 5: Altamente sugestiva de malignidad
• BI-RADS 6: Malignidad conocida
Quistes.
• Los quistes simples son las masas encontradas
con mayor frecuencia y constituyen un 25%
de las masas palpables. El uso de la US
mamaria ayudó a reducir en un 35% el
número de biopsias, pues la mamografía no
permite determinar su naturaleza quística o
sólida.
Quistes. Hallazgo benigno, BI-RADS 2 y
riesgo de malignidad 0%
• La precisión de la US para la caracterización
de los quistes alcanza un 100%, siempre y
cuando se cumplan los siguientes parámetros:
• 1. Forma redondeada o ligeramente ovalada
• 2. Márgenes bien circunscritos
• 3. Refuerzo acústico posterior
• 4. Compresibilidad
Tratamiento
• Si el quiste es sintomático se puede realizar
vaciamiento por aspiración, si el líquido obtenido
es de color verdoso u oscuro se puede descartar
malignidad, si el líquido es sanguinolento puede
ser llevado a examen citológico. Del 18% al 20%
de ellos residivan sin otra consecuencia.
• Polmet et all en un trabajo de casi 7.000
aspiraciones de quistes, no se encontró células
malignas.
• Cuando el estudio reporta papiloma intraductal es
necesario tener precaución puesto que pueden
existir zonas focales de malignidad dentro del
papiloma, el cual puede no ser detectado con el
método de biopsia por aguja trucut.
• El manejo de los papilomas deber ser con la
escisión quirúrgica, pues algunos reportes indican
que cuando las lesiones papilares muestran
atipias se encuentra hasta un 30% de malignidad.
Bi-RADS 4B
Quistes atípicos BI-RADS 3 o 4a
Son aquellos que básicamente no cumplen con
todos los criterios de los quistes simples.
Usualmente tienen ecos internos, paredes un poco
gruesas en forma sectorial o difusa, que pueden ser
irregulares, septos internos y/o masas intramurales
En general, los quistes atípicos se pueden clasificar
en complicados o complejos, dependiendo de
ciertas características ultrasonográficas.
Actualmente no hay un consenso claro con el
manejo de los quistes atípicos.
Microquistes agrupados:
(patrón quístico)
• Indica la presencia de múltiples pequeños
quistes agrupados con septos delgados (0,5
mm) y generalmente son debido a metaplasia
apocrina y cambios fibroquísticos.
• Se deben considerar como lesiones
probablemente benignas BI-RADS 3.
• Se han realizado varios estudios con relación a
los microquistes agrupados si que existan
diferencias notables con los quistes aislados.
Quistes complicados
• Aproximadamente entre el 7 y el 10% de los
quistes se complican, cambian su apariencia
tradicional a ecos internos y niveles, los cuales
pueden corresponder a contenido proteináceo,
células epiteliales y células apocrinas, entre otras.
Los ecos internos pueden movilizarse y estos
quistes deben presentar refuerzo acústico
posterior. También pueden presentar septos, los
que deben ser delgados (0,5 mm). La evolucion
hacia el abseso es otra complicacion.
Lesiones de aspecto mixto o complejo:
• Son aquellos que presentan paredes y septos
gruesos (>0.5 mm), masa intraquística o
componentes sólidos y quísticos. Es importante
mencionar que los septos gruesos pueden ser
secundarios a una infección (absceso).
• Estos abscesos deben ser drenados, realizar
tratamiento antibiótico y control ultrasonográfico
en 4 a 6 semanas.
• Si no hay antecedente de infección o trauma no
se debe esperar y se sigue con las indicaciones
para todos los quistes complejos
Subdivisiones de la Categoría 4
• 4a- lesiones con bajas probabilidades de
malignidad a las que se les recomienda biopsia. –
Quistes complicados – Abscesos – Fibroadenomas
• • 4b Pacientes post-bx con dx de benignidad
como fibroadenomas o necrosis grasa, papiloma •
4c Lesiones con características moderadas de
malignidad pero no “clásicas” – masa sólida
irregular – Calcificaciones pleomórficas
Subdivisiones de la Categoría 4
Masas sólidas.
• Uno de los avances más significativos en la US
mamaria, además de establecer la diferencia
entre lesiones quísticas y sólidas, es poder
sugerir aspectos de benignidad o malignidad.
• Las características de benignidad fueron
establecidas:
• Iso o hiperecogenicidad
• Homogenicidad
• Lobulaciones (3 o menos)
• Forma elipsoide.
• Presencia de cápsula delgada.
Lesiones indeterminadas 4b y C
sensibilidad del 98,4%, especificidad del 67,8%.
• Fueron clasificadas si no cumplían
exactamente con los criterios de benignidad.
Calcificaciones
• • Las calcificaciones tienden a ocupar un
espacio y adquirir su forma
• • Si se encuentran en el acino serán
redondeadas
• • Dentro de un ducto pequeño serán lineales.
Si el ducto es de mayor calibre, entonces
serán gruesas y cilíndricas
• • Si se encuentran en el estroma mamario,
serán amorfas o distróficas
• Evaluación de las Calcificaciones • Forma:
Redondas, lineales, gruesas o finas? Mono
morfas o polimorfas? • Tamaño: Si están
agrupadas, el tamaño es similar? • Densidad:
Alta o baja? Si están agrupadas, la densidad es
similar? • Distribución: Lineales, uni o
bilaterales? es uno ó varios focos?,
distribución regional o segmentaria?
Subdivisiones de la Categoría 4
Aspectos ecográficos en lesiones solidas:
• 1. Forma: Ovalada, redondeada o irregular
• 2. Orientación: Paralela o antiparalela
• 3. Márgenes: Circunscritos o no circunscritos (mal
definido, angular, microlobulado o espiculado)
• 4. Periferia de la lesión: Interfase abrupta, halo
ecogénico e. Ecogenicidad: Anecoico, hiperecoico,
hipoecoico o isoecoico
• 5. Características ultrasonográficas posteriores: Sin
características ultrasonográficas posteriores, refuerzo
acústico posterior, sombra acústica posterior, patrón
acústico mixto
• 6. Tejido adyacente: Cambio en los ductos, cambio en
los ligamentos de Cooper, edema, distorsión de la
arquitectura mamaria, engrosamiento y/o retracción
de la piel y/o irregularidad.
Calcificaciones:
• Las calcificaciones son caracterizadas
pobremente mediante ecografía, sin embargo
pueden ser descubiertas particularmente
dentro de una masa.
• 1. Macrocalcificaciones (mayor de0,5 mm).
• 2. Microcalcificaciones dentro de una masa
(menor de 0,5 mm)
• 3. Microcalcificaciones por fuera de la masa.
Vascularización
• 1 No presente/No evaluada.
• 2. Presente dentro de la lesión.
• 3. Presente inmediatamente o adyacente a la
lesión (hasta 5 cm).
• 4. Aumento de la vascularización de forma
difusa en tejido circundante.
Dureza
• Con patron elastico.
• Con patron parcialemnte duro.
• Lesion dura.
Ganglios
• La lesión no se encuentra dentro de la mama.
El comité del CAR del BIRADS está en proceso
de otorgar la clasificación.
• • Paciente conocida con Artritis Reumatoide o
Sarcoidosis, etc. Se cataloga BIRADS 4
• • Si se requiere biopsia del ganglio debe darse
la categoría 4
• • En caso de un linfoma o leucemia debe
darse categoría 6
• Aunque se han realizado estudios con el fin de
demostrar la eficacia de la ecografía mamaria
como método adjunto a la mamografía, esto
no ha sido comprobado científicamente, así
como tampoco la validez de las características
ultrasonográficas del cáncer
S-ar putea să vă placă și
- Manual de Quimioterapia Del CáncerDocument994 paginiManual de Quimioterapia Del CáncerEduard RomeroÎncă nu există evaluări
- Informe Sonografico AbdomenDocument3 paginiInforme Sonografico Abdomenramon77% (13)
- Preguntas de Ginecologia y ObstetriciaDocument21 paginiPreguntas de Ginecologia y ObstetriciaFrancisco Martínez100% (6)
- Absceso Anorrectal: Síntoma Inflamación SupuraciónDocument2 paginiAbsceso Anorrectal: Síntoma Inflamación SupuraciónKarla LorenaÎncă nu există evaluări
- 2Document9 pagini2Karla LorenaÎncă nu există evaluări
- NACs UNIDAD 1 Traum Envenenamientos UrgenciasDocument92 paginiNACs UNIDAD 1 Traum Envenenamientos UrgenciasRosa Maria Gonzales PerezÎncă nu există evaluări
- Educacion Sexual Integral PDFDocument50 paginiEducacion Sexual Integral PDFKarla LorenaÎncă nu există evaluări
- Diapostivias 23Document20 paginiDiapostivias 23Karla LorenaÎncă nu există evaluări
- Cartilla 5Document2 paginiCartilla 5Karla LorenaÎncă nu există evaluări
- Articulo 2Document56 paginiArticulo 2Ahi MarielaÎncă nu există evaluări
- 2 Abordaje Del Nodulo Tiroideo y Cancer de TiroidesDocument31 pagini2 Abordaje Del Nodulo Tiroideo y Cancer de TiroidesKarla LorenaÎncă nu există evaluări
- Guia 2 Adulto Mayor PDFDocument32 paginiGuia 2 Adulto Mayor PDFcoterfieldÎncă nu există evaluări
- Cartilla 1Document32 paginiCartilla 1Karla LorenaÎncă nu există evaluări
- RotuloDocument1 paginăRotuloKarla LorenaÎncă nu există evaluări
- Historia ClinicaDocument1 paginăHistoria ClinicaKarla LorenaÎncă nu există evaluări
- Unidad 1Document8 paginiUnidad 1Karla LorenaÎncă nu există evaluări
- Wila AjayuDocument1 paginăWila AjayuKarla LorenaÎncă nu există evaluări
- Deli RumDocument34 paginiDeli RumKarla LorenaÎncă nu există evaluări
- PaludismoDocument31 paginiPaludismoKarla LorenaÎncă nu există evaluări
- Todo Comenzó Con El Nuevo Niño Que Llego Al Colegio en 3ro de SecundariaDocument1 paginăTodo Comenzó Con El Nuevo Niño Que Llego Al Colegio en 3ro de SecundariaKarla LorenaÎncă nu există evaluări
- Antibiotic OsDocument47 paginiAntibiotic OsKarla LorenaÎncă nu există evaluări
- Croquis DomicialiarioDocument1 paginăCroquis DomicialiarioKarla LorenaÎncă nu există evaluări
- GinecologiaDocument12 paginiGinecologiaKarla LorenaÎncă nu există evaluări
- Tumores conjuntivales: desde benignos a malignosDocument21 paginiTumores conjuntivales: desde benignos a malignosJoel Ramirez PadillaÎncă nu există evaluări
- AcalasiaDocument25 paginiAcalasiaCindycita Rojas100% (1)
- Tumores OseosDocument10 paginiTumores OseosJhon DeyvilopÎncă nu există evaluări
- Efectos y Beneficios Del Entrenamiento de Fuerza en Pacientes Con Cáncer: Revisión Sistemática de La LiteraturaDocument15 paginiEfectos y Beneficios Del Entrenamiento de Fuerza en Pacientes Con Cáncer: Revisión Sistemática de La LiteraturaLaura S RodriguezÎncă nu există evaluări
- Celulas CancerosasDocument12 paginiCelulas CancerosasMery Huanca CarcaustoÎncă nu există evaluări
- Cancer Higado y Via BiliarDocument9 paginiCancer Higado y Via BiliarmacgyvermdÎncă nu există evaluări
- Ecografía y Tumores de OvarioDocument11 paginiEcografía y Tumores de OvarioCQ AndyÎncă nu există evaluări
- Cáncer de Esófago y Estómago.Document18 paginiCáncer de Esófago y Estómago.aliaÎncă nu există evaluări
- Condrosarcoma, CodroblastomaDocument15 paginiCondrosarcoma, CodroblastomaTatiana TorresÎncă nu există evaluări
- Tesis Final de Nayireth Rincón 2018Document48 paginiTesis Final de Nayireth Rincón 2018Delitzabeth SanchezÎncă nu există evaluări
- Tumores de GlandulasDocument6 paginiTumores de GlandulasPARASITOLOGÍA 2020Încă nu există evaluări
- Cancer de PulmonDocument51 paginiCancer de PulmonJames Russell JR Mollocondo MurilloÎncă nu există evaluări
- Patología de La Pared Torácica Con Énfasis en La Utilización de La Tomografía ComputadaDocument21 paginiPatología de La Pared Torácica Con Énfasis en La Utilización de La Tomografía ComputadaFelipe RoncerosÎncă nu există evaluări
- Preguntas Cáncer de ColonDocument2 paginiPreguntas Cáncer de Colonerica corral corralÎncă nu există evaluări
- AGO 53 - 3 WebDocument68 paginiAGO 53 - 3 WebStephanie Zuñiga MuñozÎncă nu există evaluări
- CA de VaginaDocument28 paginiCA de VaginaLeomar Nathaly BlascoÎncă nu există evaluări
- Fenómeno TumoralDocument31 paginiFenómeno TumoralEmilio Rey TorrijosÎncă nu există evaluări
- Guia 1 Material Genetico y Reproduccionuuuuuuuuuuuuuuuuuu CelularDocument31 paginiGuia 1 Material Genetico y Reproduccionuuuuuuuuuuuuuuuuuu CelularstaresperandoteÎncă nu există evaluări
- Medicina Fisica en OncologiaDocument36 paginiMedicina Fisica en OncologiaGaia8888Încă nu există evaluări
- CARCINOMA ADENOIDEO QUÍSTICO: REVISTA MÉDICA DE COSTA RICADocument5 paginiCARCINOMA ADENOIDEO QUÍSTICO: REVISTA MÉDICA DE COSTA RICARaul CastillejaÎncă nu există evaluări
- Descripción General de La Biopsia de Ganglio Linfático Centinela en Cáncer de Mama - UpToDate PDFDocument36 paginiDescripción General de La Biopsia de Ganglio Linfático Centinela en Cáncer de Mama - UpToDate PDFJosé Abraham Amaya DuarteÎncă nu există evaluări
- Cancer WikipediaDocument13 paginiCancer WikipediaJaviz CervantesÎncă nu există evaluări
- HamerDocument90 paginiHamerNataliaCuellarÎncă nu există evaluări
- Ganglios y GlandulasDocument62 paginiGanglios y GlandulasSamanta OchoaÎncă nu există evaluări
- Farmacología Molecular PDFDocument1 paginăFarmacología Molecular PDFCrick GalesÎncă nu există evaluări
- Daños Que Causa El Cloro Diluido en Agua, en Los Perros (Tesis)Document69 paginiDaños Que Causa El Cloro Diluido en Agua, en Los Perros (Tesis)AlejandroBello33% (3)
- Sexto LinfaticoDocument9 paginiSexto LinfaticoVerenice Garcia GarciaÎncă nu există evaluări
- Ca MamaDocument278 paginiCa MamaSaraÎncă nu există evaluări