Documente Academic
Documente Profesional
Documente Cultură
5.alegerea Lungimii Optime de Analiza in Absorbtia Moleculara
Încărcat de
VladJucanTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
5.alegerea Lungimii Optime de Analiza in Absorbtia Moleculara
Încărcat de
VladJucanDrepturi de autor:
Formate disponibile
Alegerea lungimii optime de analiza in absorbtia moleculara
PRIBCIPIUL METODEI spectrofotometrice:
Spectrofotometria de absorţie moleculară în UV – VIs se bazează pe absorbţia
radiaţiilor de regulă între 180 – 800 nm de către speciile moleculare din probe lichide,
solide sau gazoase.
Proba lichidă se pune într-o cuvă şi asupra ei se trimite un fascicul primar emis de o
sursă externă de spectru continuu. Fotonii întâlnesc în calea lor speciile absorbante
moleculare, care absorb o parte din radiaţia incidentă. Puterea radiantă transmisă prin
cuvă este măsurată cu ajutorul unui detector optic sensibil în domeniul UV – Vis.
Spectrometrie moleculara: Au loc interacţiuni între radiaţia UV VIS cu moleculele din probă
la nivel de electroni de legătură. (Schema curs 4 slide 8)
Se utilizaeză în absorbţia moleculară: surse primare de radiatie de spectru continuu.
Dispozitivele de selectare a benzii spectrale: izoleaza benzi spectrale de trecere înguste
pe care se consideră că radiaţia este monocromatică(radiatie cu o singura lungume de
unda). Cu alte cuvinte au rolul de a selecta radiaţii cu anumite lungimi de undă din
spectrul policromatic. Selectează odată o singură lungime de undă (o singură bandă
spectrală de trecere) din spectru, cele de tip monocromator. Selectează simultan mai
multe lungimi de undă (mai multe benzi spectrale de trecere) din spectru cele de tip
policromator.
Determinarea lungimii optime de analizat: Se aleg lungimile optime corespunzătoare
maximelor, deoarece la aceste lungimi de undă dreptele de etalonare au panta maximă,
respectiv abaterile de la liniaritate sunt neglijabile. Implict metoda are sensibilitate şi
precizie foarte bune.
Se lucrează pe maximul de absorbţie din următoarele considerente:
1. Metoda are sensibilitatea maximă (panta dreptei de etalonare este maximă)
2. Dreapta de etalonare are cea mai bună liniritate (nu prezintă abateri
semnificative de la legea lui Lambert – Beer.
3. Se pot determina precis concentraţii mai mici de analit.
(Desen curs 6 slide 32)
Punctul Izobestic:
Există situaţii în analizele chimice de absorbţie moleculară pentru care nu se poate
lucra pe maximul de absorbţie. O situaţie specială în acest sens este atunci când
compusul de determinat se află sub 2 forme în echilibru cu spectre de absorbţie diferite.
Me n mL MeLm
( nm)
pL
MeLm p ( nm p )
Complex I ( ) Complex II ( )
1 2
Dacă se doreşte determinarea cationul metalic nu se poate lucra la maximele de
absorbţie a celor doi complecşi (1 şi 2), deoarece se determină din amestec doar unul
din cei complecşi.
In acest caz se lucrează la altă lungime de undă () la care absorbanţa soluţiei să nu
depindă de concentraţia relativă a celor doi complecşi, sau de poziţia echilibrului, ci să
depindă numai de concentraţia totală a complecşilor.
(Desen curs 6 slide 34):
Absorbanţa probei depinde numai de concentraţia totală a compleşilor.
:lungimea de undă izosbestică. La punctul izosbetic absorbtivitatea molară
molară a speciilor aflate în echilibru 1 : 1 este aceeaşi.
Pentru un echilibru de forma: X Y
Absorbanţa amestecului este: At b( X c X Y cY )
Deoarece concentraţia analitică este: c cX cY
şi absorbtivităţile sunt egale, rezultă: X Y At b c
Absorbanţa totală a probei At la lungimea de undă izosbestică nu depinde de
concentraţia relativă a complecşilor aflaţi în echilibru.
Concluzie: Dacă în soluţie există doi compleci în echgilibru 1 : 1 lungimea optimă de
analiză este cea izosbestică.
Exemplu det. Cu (2+) sub forma de complex cu biuret:
2+
Ionii de Cu formează complecşi cu tartratul şi biuretul în mediu puternic bazic (pH >
12).
La adaosul de biuret în sistemul Cu – tartrat se foemează complexul Cu – biuret mai
stabil. Deoarece ionii de cupru se află în soluţie sub forma a doi complecşi în echilibru
1 : 1, lungimea optimă de analiză este cea izosbestică pentru acest amestec, unde
ambii complecşi au aceeaşi absorbtivitate molară.
CuT2 2 2B2 CuB2 2 2T 2
Albastru Violet
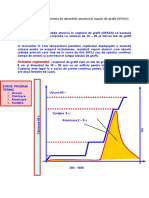
Influenta dechiderii fantei si a lungimii de unda selectate asupra dreptei de etalonare a
spectrofotometrului:
Dreapta de etalonare în absorbţia moleculară este reprezentarea grafică a absorbanţei
faţă de concnetraţia etaloanelor. Dreapta de etalonare se trasează la lungimea optimă
de analiză.
(Desen curs 6 slide 18)
1. Situaţia A. Dacă se lucrează pe maximul peakului (la m) şi fanta este
infinitezimală se obţine liniaritate prefectă a curbei de etalonare
2. Situaţia B. Se lucrează pe maximul absorbţiei şi ef este 1/10 din semilărgimea
benzii de absorbţie, abaterile de la liniaritate sunt neglijabile
3. Situaţia C. Se lucrează pe maximul absorbţiei dar fanta este largă apar abateri
negative în soluţii concentrate.
4. Situaţia D. Se lucrează la alată lungime decât maximul de absorbţie. Panta
dreptei scade semnificativ şi abaterile de la liniaritate sunt cele mai mari.
S-ar putea să vă placă și
- Spectrometria de Absorbtie Atomica in Cuptor de GrafitDocument3 paginiSpectrometria de Absorbtie Atomica in Cuptor de GrafitVladJucanÎncă nu există evaluări
- Analiza Prin Difractia de Raze XDocument3 paginiAnaliza Prin Difractia de Raze XVladJucanÎncă nu există evaluări
- 1.interactiunea Radiatiei Electromagnetice Su SubstantaDocument1 pagină1.interactiunea Radiatiei Electromagnetice Su SubstantaVladJucanÎncă nu există evaluări
- Analiza Prin Spectrometria Ir Cu Transformare FourierDocument4 paginiAnaliza Prin Spectrometria Ir Cu Transformare FourierVladJucanÎncă nu există evaluări