Documente Academic
Documente Profesional
Documente Cultură
C7 DezvoltareaMedicNoi PDF
Încărcat de
miravoinea0 evaluări0% au considerat acest document util (0 voturi)
9 vizualizări11 paginiTitlu original
C7.DezvoltareaMedicNoi.pdf
Drepturi de autor
© © All Rights Reserved
Formate disponibile
PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
9 vizualizări11 paginiC7 DezvoltareaMedicNoi PDF
Încărcat de
miravoineaDrepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 11
C7.
DEZVOLTAREA DE MEDICAMENTE
NOI
AUTORIZAREA MEDICAMENTELOR
Conf. Dr. Olah Neli - Kinga
Medicamentul parcurge un drum lung de la concepere
pn ajunge s fie administrat pacienilor. Costurile legate
de cercetarea i dezvoltarea unui medicament nou
presupune resurse financiare imense i un timp foarte
lung, 10-12 ani de cercetare n laboratoare i dezvoltarea
industrial.
Etapele conceperii i produciei industriale a unui
medicament sunt:
cercetarea i dezvoltarea
realizare n faz pilot
producia industrial
Descoperirea, evaluarea i dezvoltarea unei noi
molecule presupune o platform tehnic complex. Pn
ce o molecul ajunge s fie medicament sunt testate sute
de compui izomeri, nrudii, derivai de la o anumit
entitate chimic.
Azi exist i posibilitatea de modelare a unor compui cu
potenial efect terapeutic folosind soft-uri de simulare.
Dezvoltarea unui medicament nou are dou etape:
dezvoltarea preclinic
dezvoltarea clinic
Dezvoltarea preclinic presupune:
analiza substanei pentru o caracterizare fizico-chimic
complet, evaluarea posibilelor impuriti, produi de
degradare, etc.
determinarea biodisponibilitii substanei i a formei
farmaceutice
calcule de cost
producia la nivel micro
evaluarea d.p.d.v. legislativ a viitorului medicament
evaluri de marketing
evaluarea eficacitii
evaluarea stabilitii caracteristicilor analitice i cinetice
evaluri toxicologice
Preformularea
se definitiveaz, pe baza proprietilor fizico-chimice,
forma i compoziia medicamentului final.
Formularea i optimizarea
presupune alegerea compoziiei, formei farmaceutice i
a cii de administrare respectiv optimizarea modului de
formulare astfel nct s corespund cerinelor
prevzute de standarde, dar i a celor ale pacientului
sau medicului.
se contureaz tehnologia de producere a
medicamentului.
Dezvoltarea preclinic este reunit ca i documentaie n
modulele 3 i 4 ale dosarului de autorizare.
Dup ce s-a stabilit prin studiile din cadrul dezvoltrii
preclinice nivelul de siguran i eficacitate se poate trece
la studii clinice:
faza I: studii de farmacocinetic pe voluntari sntoi
faza II: studii pe voluntari bolnavi i pentru a
demonstra eficacitatea posologiei propuse
faza III: studii de eficacitate i acceptare la un numr
mare de bolnavi (evaluarea efectelor secundare)
faza IV: studii comparative pe numr mare de bolnavi
Rezultatele acestor studii vor intra n modulul 5 al
documentaiei de autorizare.
Dezvoltarea unor medicamente noi pe baz de plante
urmeaz aceeai etape.
studiile preliminare urmresc separarea i identificarea
diferitelor componente din diferitele pri de plant,
obinerea diferitelor tipuri de extracte i verificarea aciunii
lor terapeutice.
Azi se ncearc evidenierea compusului sau compuilor
responsabili de efectul terapeutic i eventual sinteza lor.
substanele sintetizate, dei au structur chimic identic, ar
putea avea efect terapeutic diferit, mai ales ca intensitate.
multe pete albe care urmeaz s fie studiate, majoritatea
plantelor ateptnd nc s li se deslueasc efectele
terapeutice i compusul sau compuii responsabili de
acestea precum i mecanismul de aciune.
Autorizarea de punere pe pia a medicamentelor este eliberat de
Agenia Naional a Medicamentului pe baza unei documentaii
detaliate. Documentaia const din 5 module:
modulul 1 conine
parte administrativ,
rezumatul caracteristicilor produsului
machete de etichete, cutii ambalaje secundare
prospectul i studiul de lizibilitate a prospectului
partea de impact asupra mediului
partea de farmacovigilen
modulul 2 conine raportul experilor la partea chimico-farmaceutic,
preclinic i clinic
modulul 3 reprezint partea de documentaie chimico-farmaceutic i
biologic conine
date referitoare la materii prime (compoziie, mod de obinere, specificaii,
buletine de analiz)
date referitoare la ambalajele primare
date referitoare la produsul finit (compoziie, procesul de obinere,
specificaie, buletine de analiz, excipieni i studii de stabilitate)
modulul 4 se refer la studiile farmacotoxicologice i
farmacologice conine
studii de toxicitatea acut i cronic, toxicitate asupra
aparatului genital, mutagenitate, carcinogenitate, etc.
studiile farmacologice se refer la studii farmacocinetice -
biodisponibilitate i farmacodinamice
modulul 5 se refer la studiile clinice
aceste studii trebuie aprobate ca i protocoale mai nti i
vizate de comisia de etic
n cazul medicamentelor generice trebuie efectuate i studii de
bioechivalen cu produsul princeps, adic trebuie demonstrat
dac au eficiena i sigurana asemntoare cu a primului
produs care a coninut molecula de medicament sau formula
respectiv.
n cazul medicamentelor pe baz de plante
metod simplificat dac planta are o aplicaie
tradiional.
studiile farmacotoxicologice, farmacologice i clinice
se pot baza exclusiv pe date de literatur.
n cazul medicamentelor homeopatice care nu au indicaii
metod de autorizare simplificat,
modulul 4 este nlocuit de date din literatur,
modulul 5 nu mai trebuie ntocmit, dac se
demonstreaz caracterul homeopat al suelor.
Ghiduri la nivel de EMEA care ajut productorii s
ntocmeasc documentaiile de autorizare.
Medicamentele care au fost autorizate i n alte ri ale
UE se autorizeaz prin metoda recunoaterii mutuale ntre
statele membre.
Unele medicamente se pot depune n aceeai timp n mai
multe ri prin procedura centralizat.
Medicamentele homeopate nu se autorizeaz prin
procedurile de recunoatere mutual sau centralizat.
S-ar putea să vă placă și
- C1 Introducere PDFDocument29 paginiC1 Introducere PDFmiravoineaÎncă nu există evaluări
- Marketing Curs 1 Si 2Document35 paginiMarketing Curs 1 Si 2miravoineaÎncă nu există evaluări
- SupozitoareDocument15 paginiSupozitoaremiravoineaÎncă nu există evaluări
- Medicatia Citostatic1Document4 paginiMedicatia Citostatic1miravoineaÎncă nu există evaluări
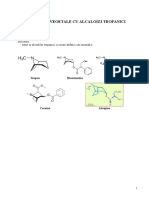
- Produse Vegetale Cu Alcaloizi TropaniciDocument11 paginiProduse Vegetale Cu Alcaloizi TropanicimiravoineaÎncă nu există evaluări
- PRODUSE VEGETALE CU ALCALOIZI pp8Document21 paginiPRODUSE VEGETALE CU ALCALOIZI pp8miravoinea100% (1)
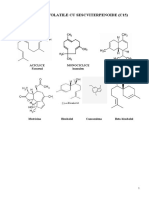
- Uleiuri Volatile Cu Sescviterpenoide (C15) : Chamomillae Flos - Musetel, Romani - FamDocument10 paginiUleiuri Volatile Cu Sescviterpenoide (C15) : Chamomillae Flos - Musetel, Romani - FammiravoineaÎncă nu există evaluări
- Medicatia AntitromboticaDocument7 paginiMedicatia AntitromboticamiravoineaÎncă nu există evaluări
- Uleiuri Volatile Cu SescviterpenoideDocument10 paginiUleiuri Volatile Cu SescviterpenoidemiravoineaÎncă nu există evaluări
- Uleiuri Volatile Cu Monoterpene Monociclice (C10)Document12 paginiUleiuri Volatile Cu Monoterpene Monociclice (C10)miravoineaÎncă nu există evaluări