Documente Academic
Documente Profesional
Documente Cultură
Testicul 2020 PDF
Încărcat de
Irina Serpi0 evaluări0% au considerat acest document util (0 voturi)
0 vizualizări131 paginiTitlu original
10. Testicul 2020 PDF
Drepturi de autor
© © All Rights Reserved
Formate disponibile
PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
0 vizualizări131 paginiTesticul 2020 PDF
Încărcat de
Irina SerpiDrepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 131
Cei doi testiculi sunt în mod normal coborâți într-un pliu cutanat situat în
exteriorul abdomenului și sub regiunea inghinală, cunoscut ca fiind punga
scrotală. Temperatura scrotală este în consecință inferioară temperaturii
intraabdominale, fapt ce favorizează spermatogeneza. Testiculii sunt
capitonați de trei straturi – tunica vaginalis internă, tunica intermediară de
colagen (albugineea) și tunica vasculosa, acestea formând capsula
testiculară. Testiculii adultului au dimensiunea comparabilă cu a unei nuci.
(aproximativ 5x2x3 cm). Testiculii au un pachet bogat vasculonervos de
care sunt suspendați. Fiecare testicul este înconsjurat în partea lor
posterioară de o structură palpabilă numită epididim. Epididimul se
continuă cu canalul deferent.
Fiecare testicul este divizat de lame ale albugineei în 250-300 lobi
piramidali, fiecare conținând tubi seminiferi (mai mult de 400 metri pentru
fiecare testicul, formând circa 50% din volumul testicular). Între tubii
seminiferi se găsesc 350 milioane de celule Leydig, care produc
testosteron, cât și vase de sânge, limfatice și fibroblaste. Tubii seminiferi
formează o rețea tubulară cunoscută sub numele de rete testis, care se
varsă prin ducte eferente într-un canal unic – canalul deferent. Canalul
deferent este contorsionat în interiorul epididimului, ieșind în final din
acesta pentru a se continua până la nivelul uretrei, unde se varsă.
Tubii seminiferi conțin celule germinale care se diferențiază în
spermatozoizi. Spermatozoizii sunt transportați până în epididim timp de 12
zile, unde sunt depozitați într-un lichid de secreție. Fiecare ejaculare
adaugă spermei produșii de secreție ai veziculelor seminale (60% din
ejaculat, conținând fructoză, fosforilcolină, ergotioneină, acid ascorbic,
flavine și prostaglandine) și ai prostatei (20% din ejaculat, conținând
spermină, acid citric, colesterol, fosfolipide, fibrinolizină, fibrinogen, zinc,
fosfatază acidă, PSA).Sperma se acumulează într-o ampulă a canalului
deferent până la relaxarea unui sfincter care îi permite intrarea în uretră. La
sperma intrată în uretră se adaugă secreția glandelor bulbouretrale. Toți
acești produși de secreție favorizează nutriția spermatozoizilor, cât și o
motilitate optimă. Contracția uretrei finalizează ejacularea și sperma este
astfel expulzată în interiorul vaginului.
Erecția penisului, necesară pentru intromisie, este determinată de
relaxarea pereților musculari ai structurilor erectile – corpul spongios (care
conține uretra și se termină cu glandul penian) și cei doi corpi cavernoși
(vezi mai departe în același curs).
Organele genitale externe ale bărbatului sunt acoperite de piele. Pliul
cutanat care acoperă glandul și poate fi decalotat este numit prepuț. Un
strat de piele dublu plicaturat formează punga scrotală.
Tubii seminiferi conțin două tipuri majore de celule: celulele germinale, care
sunt precursori ai spermatozoizilor prin procesul de spermatogeneză și
celulele Sertoli – celule mari cu margini întrepătrunse cu joncțiuni strânse,
care formează o barieră împotriva sistemului imunitar. Celulele Sertoli au
un rol de protecție și nutriție pentru celulele germinale. Ele secretă totodată
proteine importante, precum proteina de legare a testosteronului
(testosterone binding protein) și inhibina de tip 1. Între tubii seminiferi se
găsesc celulele Leydig care secretă testosteron.
Imaginea unui tub seminifer la microscopie electronică. În centru se
observă cozile spermatozoizilor.
Spermatogeneza durează 64 zile. În perioada fetală, celulele stem
(simpatogoniile) se multiplică prin diviziune mitotică. Spermatocitele
primare se divizează apoi mitotic rezultând spermatocitele secundare.
Acestea se vor diviza meiotic, pierzând astfel jumătate din cromozomi,
rezultând spermatidele care se vor matura în spermatozoizi printr-un
proces cunoscut ca spermiogeneză. Spermatozoizii au 23 cromozomi.
Spermatozoizii care conțin cromozomul X vor produce un gamet de sex
feminin prin fecundarea ovulului, în timp ce spermatozoizii care conțin
cromozomul Y vor produce un gamet de sex masculin.
Aspectul și structura unui spermatozoid normal.
Celulele Leydig sunt bogate în mitocondrii.
Sinteza testosteronului pornește de la colesterol, precursorul său.
Colesterolul intră din rezervele celulare (1) în inteiorul mitocondriilor prin
transport activ mediat de un transportor specific, Steroidogenic acute
regulatory protein (StAR) (2). Odată intrat în mitocondrie, colesterolul
suferă o clivare a catenei laterale sub acțiunea 20,22 desmolazei (enzimă
dependentă de citocromul p450), rezultând o moleculă precursor,
pregnenolonul (3). Pregnenolonul iese din mitocondrie și intră în compexul
Golgi (4),unde e supus unor activări enzimatice succesive, rezultând
testosteronul.
Lanțul de activare enzimatică include traiectul 20,22 desmolază – 3 beta
hidroxisteroid dehidrogenază – 17 alfa hidroxilază – 17,20 desmolază – 17
beta hidroxisteroid dehidrogenază, rezultând testosteronul.Există totodată
și căi alternative de sinteză, mai puțin utilizate în testicul.
Androgenii sunt precursorii estrogenilor și pot să se transforme în estrogeni
printr-o reacție chimică denumită aromatizare, sub efectul unor enzime
denumite aromataze. Testosteronul poate fi totodată redus în
dihidrotestosteron (DHT) sub acțiunea unei enzime numită 5 alfa
reductază. DHT este mai eficace decât testosteronul în procesul de
stimulare a receptorului androgenic.
Androgenii plasmatici pot circula liberi sau legați de proteine de transport
specifice (sex hormone binding globulin sau SeBG) sau non- specifice
(albumina). Fracția liberă a testosteronului este singura care poate intra în
interiorul celulelor țintă pentru a-și exercita efectele. Dozarea fracției libere
nu reflectă integral efectele periferice ale testosteronului, din moment ce
testosteronul se poate desprinde de proteinele de transport și în
proximitatea țesuturilor țintă. Totodată diverse afecțiuni precum
acromegalia, hipotiroidia și obezitatea, determină un nivel scăzut de SeBG,
așadar testosteronul total ar putea fi diminuat în aceste afecțiuni.
Receptorul androgenic face parte din superfamilia receptorilor nucleari.
Gena pentru receptorul androgenic e amplasată pe cromozomul X.
Receptorul androgenic are un fragment carboxiterminal care recunoaște
specific ligandul și un fragment aminoterminal cu două degete de zinc (câte
un atom de zinc legat non-covalent de 4 molecule de cisteină) care
recunoaște regiunea promotor a genelor a căror transcripție este modulată
de androgeni. Receptorii androgenici se găsesc în citoplasmă, legați de
proteine inactivatoare (heat shock proteins sau HSP). Legarea
androgenilor de receptor îl separă de HSP, favorizând dimerizarea a doi
receptori androgenici și pătrunderea acestui complex în interiorul nucleului
pentru a-și exercita efectele.
Androgenii au efecte multiple. Testosteronul este secretat în decursul vieții
intrauterine doar de feții de sex masculin. Androgenii favorizează
diferențierea și coborârea testiculilor, precum și diferențierea organelor
genitale externe înspre sexul masculin. DHT joacă un rol important în acest
proces de diferențiere. Amprenta sexuală asupra maturării creierului
masculin este realizată în timpul vieții intrauterine, atunci când
testosteronul fătului masculin pătrunde în sistemul nervos central, unde
este aromatizat în estrogeni. Androgenii determină apariția semnelor de
pubertate (dezvoltarea masculină a scheletului, cu umeri largi, șolduri
înguste și densitate osoasă crescută, precum și a sistemului muscular,
apariția pilozității androgen dependente și secreția glandelor sebacee și
sudoripare, dezvoltarea laringelui cu îngroșarea timbrului vocal, creșterea
în dimensiuni a organelor genitale externe), precum și comportamentul
masculin, mai agresiv, spermatogeneza și alte procese de diferențiere
precum hematopoieza.
Majoritatea testosteronului circulant provine din secreția testiculară, în timp
ce alți androgeni mai slabi precum androstenedionul,
dehidroepiandrosteronul (DHEA) și metabolitul său DHEA-S sunt secretați
mai ales de corticosuprarenală. Testosteronul poate fi redus în DHT în
testiculi, astfel încât 20% din DHT circulant provine direct din sinteza
testiculară. Alte țesuturi sensibile la acțiunea androgenilor, precum mușchii,
OGE sau pielea posedă 5 alfa reductază și pot activa testosteronul în
metabolitul mai activ, DHT. Deficitul de 5 alfa reductază poate determina
intersexualitate, demonstrând astfel importanța DHT în diferențierea
sexuală. 80% din DHT circulant provine din reducerea testosteronului în
alte țesuturi decât testiculii.
Aromatizarea androgenilor este esențială în procesul de sinteză a estrogenilor la
femeie, androgenii reprezentând precursorii estrogenilor. Aromatizarea are loc și la
bărbați. 20% din estradiolul circulant al bărbaților provine din aromatizarea
testosteronului la nivel testicular. Aromatizarea testiculară este mai intensă în perioada
pubertară, când funcția testiculară este încă imatură, iar surplusul estrogenic din
această perioadă reprezintă substratul apariției ginecomastiei peripubertare de grade
variate de severitate în 10-15% din adolescenți. Lte țesuturi, precum țesutul adipos,
creierul sau osul au capacitatea de aromatizare a androgenilor în estrogeni. În perioada
intrauterină, testiculii fetusului masculin secretă testosteron care intră în sistemul nervos
central unde este aromatizat în estradiol, cu rol important în diferențierea de tip
masculin a creierului și comportamentului ulterior. Androgenii sunt aromatizați în
estrogeni și la nivel osos, iar estrogenii sintetizați local sunt importanți pentru închiderea
cartilagiilor de creștere și achiziția de masă osoasă la bărbați. Deficitul aromatazei
osoase determină o talie foarte înaltă și osteoporoză la rarii bărbați care posedă
această afecțiune. Aromatizarea androgenică din țesutul adipos al obezilor reprezintă o
resursă suplimentară de estrogeni care favorizează apariția ginecomastiei.
Secreția pulsatilă de GnRH la pubertate (vezi cursul dedicat) stimulează
secreția hipofizară de LH (hormon luteinizant) și FSH (hormon
foliculostimulator). LH stimulează celulele Leydig care secretă testosteron.
FSH stimulează celulele Sertoli care secretă Androgen Binding Protein
(ABP), proteină care leagă testosteronul testicular, prelungind prezența
acestuia în țesutul testicular, precum și inhibina 1. Testosteronul secretat
local, împreună cu FSH, stimulează spermatogeneza din celulele
germinale. Testosteronul inhibă prin feedback negativ secreția
gonadotropilor hipofizari și a GnRH hipotalamic. Inhibina 1 inhibă selectiv
secreția de FSH.
Testiculii au capacitatea de a sintetiza temporar testosteron în perioada
intrauterină, până la mijlocul sarcinii, când testiculii încep să devină
insensibili la acțiunea gonadotropilor iar testosteronul scade până la
valorile prepubere. Această secreție tranzitorie este importantă pentru că
reprezintă o resursă de DHT, important pentru coborârea testiculilor în
scrot și diferențierea organelor genitale externe înspre sexul masculin, dar
și o resursă de estrogeni prin aromatizare, pentru maturarea de tip
masculin a sistemului nervos central. Nivelul testosteronului rămâne scăzut
de la naștere până la pubertate când, laolaltă cu dezvoltarea testiculilor,
crește determinând dezvoltarea caracterelor sexuale secundare și
spermatogeneza. Nivelul testosteronului și mai ales al testosteronului liber
scad ușor cu vârsta (așa-zisa andropauză, prin analogie cu menopauza, de
fapt un deficit androgenic instalat insidios, iar nu brusc și brutal).
Deficitul secreției testosteronului în perioada intrauterină conduce la o stare
de intersexualitate a băieților la naștere.
Deficitul de testosteron la vârste la care ar trebui să se instaleze pubertatea
întârzie declanșarea pubertății, dând pacienților un aspect eunucoid (umeri
înguști, șolduri late, membre lungi, cușcă toracică scurtă, absența pilozității
androgen dependente, voce subțire, organe genitale externe mici).
Deficitul de testosteron instalat în timpul vieții adulte determină o regresie a
caracterelor sexuale secundare (diminuarea pilozității androgen
dependente, subțierea vocii, atrofia organelor genitale externe), precum și
instalarea de impotență și infertilitate.
Penisul și testiculii trebuie examinați și măsurați. Penisul adult în stare
flască are o lungime care variază în populația caucaziană adultă între 12
și16 cm. Deschiderea uretrei poate fi uneori anormală – inferioară
(hipospadias) sau superioară (epispadias). Penisul poate avea deformări
cauzate de prezența de țesut fibros – deformarea glandului (cordee) sau a
corpului penian (maladie Peyronie, frecvent asociată retracției Dupuytren a
tendoanelor mâinii).
Testiculii pot fi măsurați cu orchidometrul Prader. Volumul testicular al
adultului trebuie să fie mai mare de 15 ml. Palparea testiculară poate
depista prezența unei tumori testiculare. Consistența testiculară, de obicei
elastică, poate deveni moale la pacienții cu hipogonadism central sau la
persoanele în vârstă, sau dură în cazul sindromului Klinefelter.
Volumul testicular poate fi evaluat echografic, măsurând trei diametre în
două secțiuni diferite și apoi multiplicând produsul acestora cu π/6.
Pacienții, mai ales cei cu probleme de infertilitate, trebuie verificați cu
privire la prezența varicocelului (varicozități scrotale). Crearea unei presiuni
pozitive abdominale suflând pe fața dorsală a mâinii (manevra Valsalva)
determină creșterea volumului varicocelului prin creșterea presiunii
venoase, iar atunci acesta poate fi sesizat mai ușor la examenul clinic.
Evaluarea spermogramei dă informații importante cu privire la fertilitatea
pacientului.
Spermatozoizii pot fi absenți sau în număr prea mic, pot să aibă probleme
de mobilitate sau pot avea malformații.
Spermatozoizi normali (stânga) și anormali (dreapta).
Spermograma poate fi cuantificată prin programe speciale.
Nivelul testosteronului total variază în timpul zilei. Pentru a avea o imagine
mai clară a secreției de testosteron se pot preleva trei probe de sânge, în
momente diferite și amestecate pentru măsurarea testosteronului o singură
dată.
Valorile normale ale diverșilor hormoni la bărbatul adult.
Nivelul scăzut de testosteron confirmă prezența hipogonadismului. Dacă
testoteronul scăzut e însoțit de valori crescute de LH și/sau FSH, atunci
leziunea este localizată la nivel testicular (1, hipogonadism primar). Dacă
valorile de LH și FSH sunt, dimpotrivă, scăzute sau anormal de normale
pentru nivelul prea scăzut de testosteron, atunci leziunea este localizată la
nivel hipotalamo-hipofizar (2, hipogonadism central). În acest caz este
necesară și dozarea prolactinei.
Câteva teste dinamice pot fi utile pentru evaluarea axei gonadotrope a
bărbatului: (1) testul la hCG (analog de LH) care stimulează direct secreția
de testosteron, testând prezența și/sau severitatea depleției rezervei
celulelor Leydig testiculare, (2) testul la comifen citrat, care evaluează
integritatea secreției GnRH hipotalamic și gonadotropilor hipofizari și (3)
testul la GnRH, care evaluează direct capacitatea hipofizară de a secreta
LH și FSH.
Le testul la hCG: administrarea de hCG 4000 UI/zi timp de 4 zile
consecutive, urmată de evaluarea testosteronului. Intrarea testosteronului
în limitele normalului sau dublarea nivelului inițial sugerează o secreție
normală de testosteron și pune problema existenței unei leziuni centrale,
hipotalamo-hipofizare.
Testul la clomifen citrat. Clomifenul citrat este un modulator selectiv de
receptor estrogenic care antagonizează estradiolul la nivel hipotalamic,
creind un vârf de secreție al GnRH, urmat de creșterea secreției de LH și
FSH. Aministrarea de clomifen citrat 100 mgx2/zi, timp de 10 zile
stimulează secreția de LH, FSH și testosteron ca în figuraă și poate de
exemplu să confirme prezența unei pubertăți întârziate, încă nedeclanșată.
Testul la GnRH. Administrarea de GnRH (100 μg iv) stimulează modest
secreția de LH ți FSH la persoane normale. Un hipogonadism primar este
însoțit de un răspuns exploziv al hormonilor hipofizari (1), confirmând
leziunea primară testiculară. Un răspuns exagerat exclusiv al FSH confirmă
distrucția izolată a tubilor seminiferi în contextul unor celule Leydig normale
și a unei secreții normale de testosteron (2).
Biopsia testiculară este indicată doar în contextul azoospermiei care
însoțește testiculi de talie normală, pentru a diferenția insuficiența
spermatogenă de obstrucția ductală.
Aspecte ale biopsiei testiculaire.
Eunucii – bărbați castrați (de exemplu servitori, gardieni ai reginei,
delincvenți sexuali, etc.)
Schemă de evaluare a hipogonadismului masculin, pornind de la
spermogramă și măsurarea testosteronului, a LH și FSH.
Etiologia hipogonadismului masculin: central (hipotalamo-hipofizar),
periferic (testicular), defecte de biosinteză și defecte ale receptorului
androgenic.
Etiologia centrală a fost detaliată în cursurile dedicate hipofizei, defectele
de biosinteză și ale receptorului androgenic determină situații de
intersexualitate care vor fi discutate în cursul dedicat, în timp ce în acest
curs vom detalia deficitele periferice, primare (testiculare).
Sindromul Klinefelter este un sindrom genetic caracterizat printr-un cariotip
particular, cu un cromozom X suplimentar la bărbați (47XXY).
Incidența sindromului Klinefelter este mare, existând și alte variante
genetice cu un fenotip asemănător.
Ovocitul primar este supus la două diviziuni meiotice, rezultând ovulul și doi
globuli polari care degenerează. Ovulul, odată fecundat, are din nou 46
chromozomi. Dacă spermatozoidul are un cromozom Y, atunci cariotipul
va fi 46XY (masculin).
Non-disjuncția ovulului poate avea loc în decursul primei (la mijloc) sau
celei de a doua meioze (la dreapta) rezultând ovule cu 2 cromozomi X.
Dacă aceste ovule sunt fecundate, produsul de concepție va avea un
cariotip 47 XXY (sindrom Klinefelter). Mult mai rar, spermatozoidul ar putea
fi agentul non-disjuncției (variantă nereprezentată în figură).
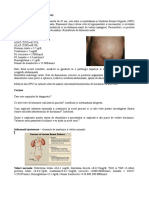
Aspectul clinic al unui pacient cu sindrom Klinefelter. Acest aspect este
variabil – hipogonadismul nu e întotdeauna prezent. Chiar dacă acești
pacienți au picioare lungi, lungimea mâinilor este de obicei normală.
Sindromul este mai atenuat în caz de mozaicisme, care pot fi foarte rar și
fertili.
În sindromul Klinefelter, tubii seminiferi sunt hialinizați și atrofiați. Datorită
atrofiei tubilor seminiferi, celulele Leydig dau impresia că sunt mai mari. De
fapt, celulele Leydig au ades și ele probleme de sinteză a testosteronului,
uneori pacienții cu sindrom Klinefelter putând avea și hipogonadism sever.
Volumul testicular este foarte mic la pacienții cu sindrom Klinefelter,
datorită atrofiei tubilor seminiferi care formeaă mai mult de 50% din volumul
testiculului normal. Hialinizarea tubilor seminiferi este însoțită de testiculi
mici și duri la palpare.
Histologia testiculilor unui pacient cu sindrom Klinefelter.
Pacient cu sindrom Klinefelter și hipogonadism sever.
Ginecomastia este frecventă în sindromul Klinefelter, chiar la pacienții cu
secreție normală de testosteron, datorită aromatizării androgenilor în
testiculii displazici în estrogeni, în paralel cu un deficit de testosteron mai
mult sau mai puțin important. Dacă ginecomastia este foarte neplăcută,
pacienții pot beneficia de mamoplastie. Riscul de cancer mamar, chiar
dacă mult mai mic decât la femei, rămâne de 20 ori mai crescut decât a
bărbații cu cariotip normal.
Alte probleme de sănătate ale pacienților cu sindrom Klinefelter.
Cromatina sexuală este o dovadă a prezenței celui de al doilea cromozom
X. Cromatina sexuală poate certifica prezența unuia, a doi sau trei
cromozomi X suplimentari.
Mai mulți cromozomi X (ex. - 48XXXY) diminuă particularitățile fizice ale
sindromului Klinefelter, dar sunt mai frecvent însoțiți de un deficit intelectual
sever.
O variantă genetică a cromozomilor sexuali multipli este sindromul Jacobs
(47XYY).
Diagnosticul pozitiv de sindrom Klinefelter.
Tratamentul sindromului Klinefelter.
Coborârea testiculilor în scrot în perioada embrionară este dependentă de
prezența DHT. Toate cauzele de deficit de DHT determină probleme de
coborâre a testiculilor în scrot.
Toate cauzele de deficit de DHT provoacă tulburări de coborâre a
testiculilor.
Tipuri de criptorhidie (criptorhidism).
Absența coborârii testicullilor în scrot determină disfuncții ale
spermatogenezei, determinând atrofia tubilor seminiferi. Chiar dacă unul
din testiculi este coborât, acesta poate avea la rându-i probleme de
spermatogeneză, sugerând că absența coborârii unuia dintre testiculi poate
influența și testiculul controlateral coborât.
Criptorhidia este frecvent asimptomatică. Uneori lipsa de coborâre
testiculară se poate însoți de o hernie inghinală. Testiculul necoborât poate
suferi o torsiune cu inflamație sau degenerare malignă (mai frecvent
întâlnită la testiculii necoborâți). Riscul de infertilitate este de asemeni
mărit.
Testicul necoborât torsionat.
Diagnosticul diferențial între criptorhidia bilaterală și anorhidie.
Echografia în criptorhidie.
RMN în criptorhidie.
Tratamentul în criptorhidie. Stimularea testiculilor cu hCG sau GnRH ar
putea crește nivelul de DHT, contribuind astfel la coborârea testiculară.
Testiculii găsiți deja pe traiectul de coborâre pot fi coborâți în scrot prin
orhidopexie. Testiculii compromiși trebuie extirpați datorită riscului lor
crescut de malignizare.
Există copii cu anorhie (lipsa testiculului) uni- sau bilaterală.
Dacă testiculii suferă în viața intrauterină, copilul se poate naște fără
testiculi. Această anorhie bilaterală e cunoscută sub denumirea de
« vanishing testes » (testiculi dispăruți). Foarte probabil, testiculii au fost
prezenți cel puțin până în săptămânile 14-16 de gestație, pentru că acești
copii sunt fenotipic băieți, fără intersexualitate. Dacă leziunea testiculară ar
fi apărut înainte de 14 săptămâni, atunci nou născutul ar fi avut
pseudohermafroditism masculin, datorită lipsei de diferențiere către sexul
feminin prin absența DHT.
Diagnosticul de « vanishing testes ». Testosteronul nu e stimulat de testul
la hCG dacă testiculii nu sunt prezenți.
Impactul terapiei cu testosteron asupra dimensiunilor penisului.
Mutațiile inactivatoare ale receptorului pentru LH produce o atrofie a
celulelor Leydig, care nu vor mai secreta testosteron.
Histologia testiculară arată hipoplazia/aplazia celulelor Leydig și o
spermatogeneză compromisă. Celulele Sertoli sunt totuși prezente și
secretă hormon antimullerian (antimullerian hormone, AMH) care inițiază
regresia ductelor feminine (canalelor mulleriene, conducând la absența
uterului și trompelor uterine).
Pacientul are de la naștere grade variate de intersexualitate până la
pseudohermafroditism masculin, deoarece a avut un deficit de DHT
începând cu primele săptămâni de gestație. În viața adultă, pacienții
netratați au ades un fenotip feminin, dar fără 2/3 vaginale superioare și fără
uter. Caracterele sexuale secundare ale fenotipului feminin sunt slab
dezvoltate deoarece pacienții sunt hipogonadici.
Diagnosticul diferențial trebuie făcut cu « vanishing testes » care are un
fenotip masculin și cu alte condiții de intersexualitate.
Strategia terapeutică depinde de vârsta la diagnostic și de orientarea
sexuală a pacientului.
Sindromul Noonan este caracterizat de talie mică, malformații multiple și un
aspect fizic asemănător sindromului Turner, dar cu un cariotip normal.
Pacienții cu sindrom Noonan pot fi în egală măsură băieți și fete și sunt
subfertili.
Sindromul Noonan masculin.
Distonia miotonică amiotrofică Steinert este o afecțiune neuromusculară
genetică însoțită de perturbări ale spermatogenezei.
Aspecte clinice ale bărbaților cu distrofie miotonică. Se remarcă atrofia
mușchilor faciali, mai ales a mușchilor temporali, ptoză palpebrală și
calviție.
Diverse afecțiuni pot leza tubii seminiferi în viața adultă prin mecanisme
infecțioase, modificări ale temperaturii optime, cauze iatrogene, toxice,
ischemice, genetice sau chiar fără cauze precise.
Diverse afecțiuni pot leza tubii seminiferi în viața adultă prin mecanisme
infecțioase, modificări ale temperaturii optime, cauze iatrogene, toxice,
ischemice, genetice sau chiar fără cauze precise.
Terapia medicamentoasă este dezamăgitoare. Terapia chirurgicală este
rezervată doar cazurilor particulare.
Vârsta avansată duce la o scădere ușoară, dar statistic semnificativă a
nivelului de testosteron (andropauza, cunoscută și ca « Partial Androgen
Deficiency of the Aging Male » - PADAM). Datorită unei importante
aromatizări din țesutul adipos, nivelul estrogenic al bărbaților în vârstă
poate fi crescut, explicând creșterea sintezei hepatice de SeBG, substratul
unei scăderi suplimentare de testosteron liber.
Scăderea testosteronului la bărbații de vârsta a treia determină o creștere a
nivelului de LH și FSH, dovedind astfel că problema de secreție hormonală
la acești bărbați este la nivel testicular.
Un cuplu este suspectat de infertilitate atunci când după minimum 6 luni –
un an de contacte sexuale neprotejate nu poate procrea.
Pentru a fi fertil, bărbatul are nevoie de o spermatogeneză normală precum
și de o bună calitate a lichidului seminal, cât și de o bună deplasare a
spermatozoizilor până la nivelul trompelor uterine și de o bună penetrare a
ovulului.
Cauzele de infertilitate masculină.
Funcție de tipul de infertilitate, pacientul poate avea semne clinice specifice
sau poate fi complet asimptomatic.
Investigarea unui bărbat cu infertilitate de cuplu.
Terapia diverselor forme de infertilitate masculină.
Terapia diverselor forme de infertilitate masculină.
Terapia diverselor forme de infertilitate masculină.
Penisul este format din structuri erectile – corpul spongios care conține
uretra și se termină cu glandul și cei doi corpi cavernoși situați pe fața
dorsală a penisului.
Erecția este esențială pentru penetrare. În timpul erecției, pereții de
musculatură netedă a structurilor erectile încep să se relaxeze, astfel încât
presiunea din interiorul acestor structuri scade sub nivelul tensiunii arteriale
din circulați generală și sângele începe să intre în penis ca într-un burete,
atingându-se un nivel maxim de erecție limitat de albuginee (teacă
inextensibilă care înconjură penisul). În timpul erecției, venele de retur sunt
colabate prin presarea lor de pereții albugineei, sângele devenind astfel
prizonier în interiorul penisului. Așadar, erecția are ca substrat fiziologic
miorelaxarea.
O bună erecție are nevoie de o bună impregnare hormonală care crește
libidoul și facilitează mecanismele de apariție a miorelaxării, precum și de o
inervație și vascularizație intacte.
Definirea disfuncției erectile este dificilă. Limitele normale ale activității
sexuale variază larg în populația sănătoasă, de la șapte contacte pe zi la
un contact la șapte săptămâni.
Miorelaxarea este influențată direct de acumularea intracelulară de cGMP.
Durata de acțiune a cGMP este însă limitată de inactivarea sa de către
fosfodiesteraza 5 (PDE5). Drogurile care inhibă selectiv PDE5, precum
Sildenafil Citrat, facilitează erecția prin prelungirea duratei de acțiune a
cGMP, care se acumulează în celulele musculaturii netede ale structurilor
erectile peniene.
Inhibitorii selectivi de PDE5 au efecte neglijabile asupra altor
fosfodiesteraze, dar ar putea fi totuși însoțite de efecte secundare precum
vasomotricitate facială, modificarea acuității vizuale și a percepției culorilor
și nu pot fi asociate cu coronarodilatatoare pentru că pot determina în
această asociație scăderi severe ale tensiunii arteriale până la colaps.
Inhibitorii de PDE5.
Etiologia disfuncției erectile poate fi comparată cu un iceberg inversat.
Majoritatea disfuncțiilor erectile au un substrat predominant psihogen, în
timp ce o minoritate sunt produse de modificări organice. În ambele situații
utilizarea unui inhibitor de PDE5 poate fi eficace, dar eficacitatea poate fi
redusă sau chiar absentă în disfuncțiile organice.
Diferențele clinice dintre disfuncțiile erectile psihogene și organice.
Cauzele organice de disfuncție erectilă.
Schemă de investigare a disfuncțiilor erectile.
Tratamentul disfuncțiilor erectile de la modificarea stilului de viață până la
protezarea peniană.
Ginecomastia reprezintă creșterea dimensiunilor glandei mamare la bărbat.
Maturarea glandei mamare este stimuată de estrogeni și inhibată de
androgeni. O glandă mamară în prealabil preparată estrogenic devine
sensibilă la acțiunea prolactinei care stimulează lactația. Lactația nu este
abundentă sau este chiar absentă în timpul sarcinii deoarece nivelul foarte
crescut de estrogeni și progesteron inhibă acțiunea prolactinei, chiar dacă
aceasta este crescută. La naștere, odată cu eliminarea placentei și a
secreției hormonale aferente, glanda mamară devine sensibilă la acțiunea
prolactinei și se declanșează lactația, întreținută de reflexul suptului. În
concluzie, impregnarea estrogenică a glandei mamare și secreția
prolactinei sunt esențiale pentru declanșarea alăptării, în timp ce suptul
este important pentru menținerea acesteia prin stimularea prolactinei prin
arc reflex.
Echilibrul dintre androgeni și estrogeni are o influență importantă asupra
dezvoltării glandei mamare la bărbat. Un exces androgenic însoțit de un
deficit relativ estrogenic (varianta normală la bărbat) inhibă dezvoltarea
glandei mamare a bărbatului.
Dacă un bărbat are o scădere a nivelului androgenic și/sau o creștere a
nivelului estrogenic, acest dezechilibru va duce la instalarea ginecomastiei.
Cauze de ginecomastie.
Cauze de ginecomastie.
Investigarea unei ginecomastii care ar putea fi un semn al unor afecțiuni
mai generale.
Tratamentul ginecomastiei.
Epidemiologia tumorilor testiculare.
Factorii predispozanți ai tumorilor testiculare și cauzele unei ginecomastii
asociate.
Tipuri de tumori testiculare.
Tipuri de tumori testiculare.
Semne clinice care ar putea însoți unele tumori testiculare.
Modificări de laborator în unele tumori testiculare.
Tumori testiculare – aspecte echografice.
Terapia tumorilor testiculare.
S-ar putea să vă placă și
- Fisa de Identificare A Factorilor de Risc ProfesionalDocument2 paginiFisa de Identificare A Factorilor de Risc ProfesionalBadoiu Liviu100% (2)
- PapuleDocument6 paginiPapuleIrina SerpiÎncă nu există evaluări
- 6 7 BiiDocument161 pagini6 7 BiiIrina SerpiÎncă nu există evaluări
- Criteriii Referat ColocviuDocument1 paginăCriteriii Referat ColocviueduardÎncă nu există evaluări
- 9.11 - Leucemiile Acute Ale Copilului UltimateDocument87 pagini9.11 - Leucemiile Acute Ale Copilului UltimateIrina SerpiÎncă nu există evaluări
- Caz Clinic 2Document1 paginăCaz Clinic 2Irina SerpiÎncă nu există evaluări
- Caz Clinic 2Document1 paginăCaz Clinic 2Irina SerpiÎncă nu există evaluări
- Caz Clinic 3Document1 paginăCaz Clinic 3Dan DamaschinÎncă nu există evaluări
- Caz ClinicDocument2 paginiCaz ClinicIrina SerpiÎncă nu există evaluări
- Infectiile OsoaseDocument50 paginiInfectiile OsoaseAdelinaArghire100% (1)
- Diformitatile OsoaseDocument72 paginiDiformitatile OsoaseAdelinaArghireÎncă nu există evaluări