Documente Academic
Documente Profesional
Documente Cultură
Ep 1
Ep 1
Încărcat de
VIerme VRm ZOrTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Ep 1
Ep 1
Încărcat de
VIerme VRm ZOrDrepturi de autor:
Formate disponibile
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
EXERCIII I PROBLEME
*****************************************************************************
1.1.
Care este prima substan organic obinut prin sintez? Scrie formula molecular a
acestei substane i calculeaz-i compoziia procentual. (Masele atomice: C 12, H 1,
N 14, O -16).
Rezolvare:
(NH2)2C=O ureea;
Muree = 2(14+2)+12+16 = 60 g /mol;
60 g uree ..12 g C..4 g H .2*14 g N..16 g O
100 g uree.%C%H..%N%O
_______________________________________________
%C = 100*12/60 = 20 %;
%H = 100*4/60 = 6,66 %;
%N = 100*28/60 = 46,66 %;
%O = 100*16/60 = 26,66 %.
*****************************************************************************
1.2.
Scrie simbolurile chimice pentru patru elemente organogene. Modeleaz formarea
legturilor chimice dintre elementele organogene enumerate i hidrogen.
Rezolvare: C, H, O, N.
CH4 ; H2 ; H2O ; NH3.
*******************************************************************
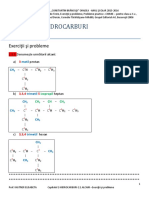
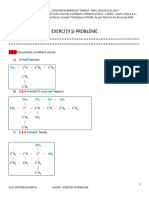
1.3.
Scrie catena care se formeaz prin legarea a 5 atomi de carbon, liniar, numai prin
legturi . Completeaz valenele libere ale atomului de carbon cu atomi de hidrogen i
scrie formula molecular a substanei organice obinute.
Rezolvare:
CCCCC
caten liniar saturat
1
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
H3C CH2 CH2 CH2 CH3
Formula molecular: C5H12
n-pentan
*******************************************************************
1.4.
a) Modeleaz formarea legturilor chimice multiple posibile ntre carbon i azot.
b) Definete electronii neparticipani i precizeaz numrul de perechi de electroni
neparticipani n urmtorul compus organic:
H3C CH2 H
(O are 2 perechi de electroni neparticipani sus i jos)
Rezolvare:
a) H2C = NH i H C N
b) Electronii neparticipani sunt electroni care se gsesc n startul de valen, dar
care nu particip la formarea legturii chimice. Sunt dou perechi de electroni
neparticipani.
*****************************************************************************
1.5.
Completeaz cu atomi de hidrogen urmtoarea caten de atomi de carbon:
C
I
- CI
C
C C C - C
astfel nct, pentru toi atomii de carbon, cele patru covalene s fie satisfcute.
Precizeaz natura fiecrui atom de carbon din caten.
Rezolvare:
(CH3)3C - CH2 - CH2 - CH2 - CH3
- conine 4 atomi de carbon primari; 3 atomi de carbon secundari; 1 atom de carbon
cuaternar.
*****************************************************************************
1.6.
a) Scrie o caten ciclic format din 6 atomi de carbon care s conin cel puin
un atom de carbon teriar.
2
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
b) Scrie o caten aciclic nesaturat, format din 7 atomi de carbon.
Rezolvare:
*****************************************************************************
1.7.
Precizeaz tipul fiecrui atom de carbon din urmtoarele catene hidrocarbonate:
a) H3C - CH2- (CH3)CH - CH2 - CH3
- conine 3 atomi de carbon primari; 1 atom de carbon teriar; 2 atomi de carbon
secundari.
b) HC C (CH3)CH HC = CH2
- conine 1 atom de carbon primar; 3 atomi de carbon teriari; 1 atom de carbon
secundar, 1 atom de carbon cuaternar.
c)
H2C = C = CH CH3
- conine 1 atom de carbon primar; 1 atom de carbon teriar; 1 atom de carbon
secundar, 1 atom de carbon cuaternar.
*****************************************************************************
1.8.
Explic folosind cuvintele tale noiunile:
a)
analiz elementar calitativ;
3
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
b)
analiz elementar cantitativ;
c)
formul brut;
d)
formul molecular.
Rezolvare:
*****************************************************************************
1.9. n urma combustiei a 3.52 g substan organic s-au obinut 7.04 g CO2 i 2.88 g H2O.
Determin formulele procentual, brut i molecular, tiind c substana organic are masa
molar 88 g /mol. (Masele atomice: C 12, H 1, O 16).
Rezolvare:
3,52 g
CxHyOz
7,04 g
tO2
88 g
xCO2
x*44 g
2,88 g
y/2H2O
(y/2)*18
M CxHyOz = 88 g /mol;
MCO2 = 12 + 2*16 = 44 g /mol;
MH2O = 2 + 16 = 18 g /mol.
x = (88*7,04)/(3,52*44) = 4;
4
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
y = (88*2,88)/(3,52*9) = 8;
M CxHyOz = x*12 + y*1 + z*16 = 88 g /mol;
4*12 + 8*1 + z*16 = 88;
z*16 = 32;
z = 2.
Formula molecular este:
C4H8O2
Formula brut este: (C2H4O)n
unde n = 2;
Calculm formula procentual:
88 g C4H8O2 4*12 g C..8*1 g H2*16 g O
100 g C4H8O2 % C . % H % O
------------------------------------------------------------------------------% C = 100*4*12/88 = 54,54 %
% H = 100*8/88 = 9,09 %
% O = 100*2*16/88 = 36,36 %.
*****************************************************************************
1.10. S-a supus analizei elementare o hidrocarbur cu masa molar 84 g /mol. S-au analizat
1,68 g hidrocarbur i s-au obinut 120 mmoli CO2. Determin formula molecular a
hidrocarburii i scrie o formul de structur posibil tiind c are n molecul o legtur .
(Masele atomice: C 12, H 1).
Rezolvare:
5
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
1,68 g
CxHy
0,12 moli
tO2
84 g
xCO2
y/2H2O
x moli
M CxHy = 84 g /mol;
120 mmoli CO2 = 0,120 moli CO2
x = (84*0,12)/1,68 = 6
M CxHy = x*12 + y*1 = 84 g /mol;
6*12 + y = 84
Y = 12
Formula molecular este:
C6H12
H2C = CH CH2 CH2- CH2 CH3
1 hexen
*****************************************************************************
1.11. n molecula unei substane organice care conine 2 atomi de brom, numrul atomilor de
hidrogen este de dou ori mai mare dect numrul atomilor de carbon. n urma analizei a 2,16
g din aceeai substan organic s-au obinut 3,76 g precipitat , alb-glbui de AgBr. Determin
formula molecular a substanei organice i calculeaz-i compoziia procentual. (Masele
atomice: C -12, H -1, Br -80, Ag 108).
Rezolvare:
Formula molecular este:
CxH2xBr2
M CxH2xBr2 = x*12 + 2x*1 + 2*80 = (26x + 160) g /mol.
6
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
2,16 g
3,76 g
CxH2xBr2
2AgBr pp alb-glbui
(14x + 160) g
2*188 g
M AgBr = 108 + 80 = 188 g /mol
(14x +160) = (2,16*2*188)/3,76
(14x + 160) = 216
14x = 56
x=4
Formula molecular este:
C4H8Br2
Calculm compoziia procentual:
M C4H8Br2 = 4*12 + 8*1 + 2*80 = 216 g /mol.
216 g C4H8Br2 4*12 g C..8*1 g H2*80 g Br
100 g C4H8Br2 % C . % H % Br
------------------------------------------------------------------------------% C = 100*4*12/216 = 22,22 %
% H = 100*8/216 = 3,70 %
% O = 100*2*80/216 = 74,07 %.
*****************************************************************************
1.12. O substan organic necunoscut formeaz la analiza (descompunerea termic ?- nu permite
legea conservrii masei) a 1,86 g substan, 448 ml CO (c.n.), 1,76 g CO2 i 1,62 g H2O. tiind c
molecula substanei organice conine 2 atomi de carbon, determin formula ei molecular.
(Masele atomice: C 12, H 1, O -16).
7
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
Rezolvare:
1,86 g
Cx+yHzOt
0,448 l
vO2
(24 + z + 16t) g
xCO
x*22,4 l
1,76 g
yCO2
y*44 g
1,62 g
z/2H2O
(z/2)*18
MC2HzOt = 2*12 + z*1 + t*16 = (24 + z + 16t) g /mol;
Substana organic conine 2 atomi de carbon, deci x + y = 2 iar dintr-un mol de substan la
descompunere termic vor rezulta x moli de CO i y moli de CO2.
MCO2 = 12 + 2*16 = 44 g /mol;
448 ml CO = 0,448 l CO;
0.448*y*44 = x*22.4*1.76
2y = 4x
y = 2x
x + 2x =2
3x = 2
x = 2/3
y = 4/3
l calculm pe z din reacie:
z =[ (4/3)*44*1,62]/(1.76*9) = 6
MC2H6Ot = (1,86*22,4*2/3)/0,448 = 62 g /mol;
24 +6 +16t = 62
16t = 32
8
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
t =2.
Formula molecular este: C2H6O2
Bilanul oxigenului:
t +2v = x +2y +0,5z
2 + 2v = 2/3+8/3+0,5*6
2v = 10/3 +3 -2
2v = 10/3 + 3/3
2v = 13/3
v =13/6
***********************************************************************************
1.13. Densitatea n raport cu aerul a unei hidrocarburi care conine 20 % H este de 1,038. Care
este formula molecular a hidrocarburii. (Masele atomice: C 12, H 1 iar Maer = 28,9 g /mol).
Rezolvare:
MCxHy = x*12 + y*1
daer = MCxHy / Maer = 1.038
MCxHy = 1.038*28.9 = 30 g /mol;
12x + y = 30
30 g CxHy .12x g C.y g H
100 g CxHy 80 %C..20 %H
-----------------------------------------------------------9
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
x = (30*80)/(100*12) = 2
12*2 + y = 30
y=6
Formula molecular este C2H6
************************************************************
1.14. S-au supus analizei elementare 0,2 moli dintr-o substan organic, A i s-au obinut
2,24 l N2. Dioxidul de carbon obinut a fost barbotat n 400 ml soluie de Ca(OH)2 de
concentraie 0,1 M obinndu-se 60 g de precipitat de CaCO3. Apa obinut, introdus n 200 g
soluie de H2SO4 de concentraie 30 % i scade concentraia la 28,22 %. tiind c n molecula
substanei A se gsesc, pe lng ali atomi i 2 atomi de O determin formula molecular a
substanei A. (Masele atomice: C 12, H 1, N 14, O 16, S 32, Ca 40)
Rezolvare:
Determinm masa de N din N2 rezultat:
MN2 = 14*2 = 28 g /mol;
1 mol N2 22,4 l N2.28 g N2
x moli N2 2,24 l N2..mN
mN = 2,24*28/22,4 = 2,8 g N
Determinm masa de C din CO2 rezultat i transformat n CaCO3:
MCaCO3 = 40 + 12 +3*16 = 100 g /mol;
100 g CaCO3 ..12 g C
60 g CaCO3 ..mC
10
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
mC = 60*12/100 = 0,72 g C
Determinm masa de H din x g de H2O rezultat :
Vom calcula masa de ap care introdus n 200 g soluie de H2SO4 de concentraie 30 % i
scade concentraia la 28,22 %.
Soluia 1: ms1 = 200 g soluie H2SO4 de concentraie 30 %;
md1 = ?
cp1 = 30 %
---------------------------------------------------------------------------------------------------------------------------Soluia 2: ms2 = (200+x) g soluie H2SO4 de concentraie 28,22 %;
md2 = md1
cp2 = 28,22 %
unde x reprezint masa de ap introdus.
100 g soluie..
cp1
ms1 md1
Formula:
Calculm
md1
md1 = 200*30/100 = 60 g H2SO4
md2 = md1 = 60 g H2SO4
(200 + x) g sol..60 g H2SO4
100 g sol 28,22 g H2SO4
11
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
(200 + x) = 100*60/28,22
200 + x = 212,61
x = 12,61 g H2O
MH2O = 2 + 16 = 18 g /mol
18 g ap2 g H
12,61 g apmH
mH = 12,61*2/18 = 1,4 g H
Calculm masele de C, H, N dintr-un mol de substan A cu formula CxHyNzO2
0,2 moli AmC.mHmN
1 mol A .12xy..14z
0,2 moli A0,72 g C1,4 g H2,8 g N
1 mol A 12xy..14z
x = 0,72/(0,2*12) = 3
y = 1,4/0,2 = 7
z = 2,8/(0,2*14) = 1
Substana A conine 2 atomi de O deci:
Formula molecular este: C3H7NO2
*****************************************************************************
3
1.15. n condiii normale 532 cm dintr-o hidrocarbur gazoas cntresc 1,33 g i formeaz,
prin arderea a 2,1 g hidrocarbur, 6,6 g CO2. Determin formula molecular a hidrocarburii.
Rezolvare:
12
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
MCxHy = x*12 + y*1
532 cm3 hidrocarbur= 0,532 l hidrocarbur
Calculm masa molar a hidrocarburii CxHy
(12x + y) g CxHy 22,4 l CxHy
1,33 g CxHy ...0,532 l CxHy
(12x +y) = (1,33*22,4)/0,532 = 56 g CxHy
MCO2 = 12 + 2*16 = 44 g /mol;
56 g CxHy x*44 g CO2
2,1 g CxHy ..6,6 g CO2
x = (56*6,6)/(2,1*44) = 4
12x + y = 56
12*4 + y = 56
y=8
Formula molecular este C4H8
*****************************************************************************
1.16. Determin formulele brute ale substanelor care au rapoartele de mas:
a) C : H : O = 3 : 1 : 4;
b) C : H : N = 6 : 2 : 7;
c) C : H : N : O = 9 : 2 : 7: 8.
Masele atomice: C 12, H 1, O -16, N 14.
Rezolvare:
13
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
a) C : H : O = 3 : 1 : 4;
Amplificm raportul de mas pn la multipli ai maselor atomice. Se amplific cu 4:
C : H : O = 12 : 4 : 16;
12 g C reprezint 1 atom de C, 4 g H reprezint 4 atomi de H i 16 g O reprezint 1 atom de O
deci formula brut va fi
CH4O
----------------------------------------------------------------------------------------------------------------------------b) C : H : N = 6 : 2 : 7;
Amplificm raportul de mas pn la multipli ai maselor atomice. Se amplific cu 2:
C : H : N = 12 : 4 : 14;
12 g C reprezint 1 atom de C, 4 g H reprezint 4 atomi de H i 14 g N reprezint 1 atom de N
deci formula brut va fi
CH4N
----------------------------------------------------------------------------------------------------------------------------c) C : H : N : O = 9 : 2 : 7: 8.
Amplificm raportul de mas pn la multipli ai maselor atomice. Se amplific cu 4:
C : H : N : O = 36 : 8 : 28 : 32;
36 g C reprezint 3 atomi de C, 8 g H reprezint 8 atomi de H, 28 g N reprezint 2 atomi de N i
32 g O reprezint 2 atomi de O deci formula brut va fi
C3H8N2O2
*****************************************************************************
1.17. O substan organic B, are formula molecular C4H10O2 . Se cere:
a) calculeaz formula procentual a substanei B;
b) Determin formula brut a substanei B;
c) Scrie o formula de structur pentru substana B, tiind c are n molecula numai
legturi i are o structur aciclic.
14
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
Masele atomice: C 12, H 1, O 16.
Rezolvare:
MC4H10O2 = 4*12 + 10*1 + 2*16 = 90 g /mol;
90 g C4H10O2 48 g C10 g H..32 g O
100 g C4H10O2 % C% H..% O
% C = (100*48)/90 = 53,33 %
% H = (100*10)/90 = 11,11 %
% O = (100*32)/90 = 35,55 %
Formula procentual a substanei B este 53,33 % C; 11,11 % H; 35,55 % O.
Formula brut este C2H5O.
Formula molecular este: C4H10O2
HO C1H2 C2H2 C3H2 C4H2 OH
1,4 butandiol
*****************************************************************************
1.18. n urma analizei a 6,32 g substan organic a crei molecul este format din carbon,
hidrogen, oxigen i un atom de sulf s-au obinut 5,376 l CO2, 2,16 g H2O i 9,56 g PbS.
Determin formula molecular a substanei. (Masele atomice: C -12, H 1, O 16, S 32, Pb
207).
Calculm masa de C din CO2 rezultat:
22,4 l CO2.12 g C
5,376 l CO2.mC
15
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
mC = (5,376*12)/22,4 = 2,88 g C
Calculm masa de H din H2O rezultat:
MH2O = 2*1 + 16 = 18 g H2O
18 g H2O2 g H
2,16 g H2O mH
mH = (2,16*2)/18 = 0,24 g H
Calculm masa de S din PbS rezultat:
MPbS = 207 + 32 = 239 g PbS
239 g PbS.32 g S
9,56 g PbSmS
mS = (9,56*32)/239 = 1,28 g S
Formula molecular a substanei B este: CxHyOzS
6,32 g B....mCmH mO ....mS
MB....12x..y...16z32 g S
Facem nlocuirile:
6,32 g B....2,88 g C0,24 g H
mO ...1,28 g S
MB..12x.y....16z32 g S
Calculm masa de O notat cu mO :
6,32 = 2,88 + 0,24 + mO + 1,28
16
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
COLEGIUL TEHNIC CONSTANTIN BRNCUI ORADEA -ANUL COLAR 2012-2013
Probleme rezolvate din Culegerea de Teste, Exerciii i probleme, Probleme practice CHIMIE pentru clasa a X-a ,
Luminia Vldescu, Luminia Irinel Doicin, Corneliu Trrbanu-Mihil, Grupul Editorial Art, Bucureti 2006
mO = 6,32- (2,88 +0,24 + 1,28)
mO = 1,92 g O
Calculm masa molar a lui B notat cu MB :
MB = (6,32*32)/1,28 = 158 g / mol.
Calculm pe x, y i z:
x = (158*2,88)/(6,32*12) = 6
y = (158*0,24)/(6,32*1) = 6
z = (158*1,92)/(6,32*16) = 3
Formula molecular a substanei B este: C6H6SO3
*****************************************************************************
17
Prof. KASTNER ELISABETA
INTRODUCERE N STUDIUL CHIMIEI ORGANICE EXERCIII I PROBLEME
S-ar putea să vă placă și
- Metode de Rezolvare A Problemelor de Chimie OrganicaDocument16 paginiMetode de Rezolvare A Problemelor de Chimie OrganicaDaniel Oancea95% (20)
- Probleme Chimie Clasa X RezolvateDocument6 paginiProbleme Chimie Clasa X RezolvateFayerah100% (3)
- Chimie OrganicaDocument111 paginiChimie Organicactinralu9289% (27)
- Subiecte Rezolvate Chimie OrganicaDocument0 paginiSubiecte Rezolvate Chimie OrganicaIoana Georgiana82% (11)
- Sinteze Chimie OrganicăDocument10 paginiSinteze Chimie OrganicăMarinela Burtescu100% (4)
- Chimie UMFCV 2021Document164 paginiChimie UMFCV 2021Ioana Petrescu100% (1)
- Chimie Organică - AlcaniiDocument41 paginiChimie Organică - AlcaniiBianca Voisa90% (39)
- Probleme Rezolvate Chimie OrganicaDocument30 paginiProbleme Rezolvate Chimie OrganicaBurtan Diana82% (11)
- 100varinate Chimie OrganicaDocument300 pagini100varinate Chimie Organicaalinutza9775% (4)
- Test2 5 1Document10 paginiTest2 5 1Cristina Ștefania100% (1)
- Chimie X Examen Corigenta12Document4 paginiChimie X Examen Corigenta12rariustinÎncă nu există evaluări
- Fizica fenomenologică: Compendiu - Volumul 1De la EverandFizica fenomenologică: Compendiu - Volumul 1Evaluare: 4.5 din 5 stele4.5/5 (2)
- Chimie OrganicăDocument57 paginiChimie OrganicăAntonio Spița100% (5)
- Alcani - Exercitii RezolvateDocument34 paginiAlcani - Exercitii RezolvateStefan Serb87% (15)
- Alcani Exercitii Si ProbDocument34 paginiAlcani Exercitii Si ProbSorina Bob100% (1)
- Teste Chimie OrganicaDocument7 paginiTeste Chimie Organicacs_83298973Încă nu există evaluări
- Alchine-Exercitii Si Probleme PDFDocument36 paginiAlchine-Exercitii Si Probleme PDFVlad IonutÎncă nu există evaluări
- Test AreneDocument14 paginiTest AreneAndrea100% (2)
- Test ChimieDocument13 paginiTest ChimieMihaiÎncă nu există evaluări
- Probleme ChimieDocument15 paginiProbleme ChimieSuditu SimonaÎncă nu există evaluări
- Subiecte Chimie OrganicăDocument2 paginiSubiecte Chimie OrganicăMaria ȚagaÎncă nu există evaluări
- Metode Rezolvare Probleme-Chimie AnorganicaDocument93 paginiMetode Rezolvare Probleme-Chimie Anorganicanycole1107100% (1)
- Capitolul 2 - HIDROCARBURI 2.4.ALCADIENEDocument14 paginiCapitolul 2 - HIDROCARBURI 2.4.ALCADIENERadu SlatinaÎncă nu există evaluări
- Compuşi Organici MonofuncţionaliDocument14 paginiCompuşi Organici Monofuncţionalighost2011Încă nu există evaluări
- Test Alcani 2Document6 paginiTest Alcani 2Nicoleta CosteaÎncă nu există evaluări
- T 2 ADocument5 paginiT 2 AVIerme VRm ZOr0% (1)
- Probleme RezolvateDocument34 paginiProbleme RezolvateAnonymous TNyPmi7sÎncă nu există evaluări
- Ep2 5Document37 paginiEp2 5Ela ElaÎncă nu există evaluări
- AlcaniDocument23 paginiAlcaniNicoleta CosteaÎncă nu există evaluări
- Test3 2 3Document10 paginiTest3 2 3CostinÎncă nu există evaluări
- Test Alcani 1Document7 paginiTest Alcani 1Nicoleta CosteaÎncă nu există evaluări
- Test2 5 4 PDFDocument12 paginiTest2 5 4 PDFAna-Maria MisiciÎncă nu există evaluări
- UuDocument8 paginiUuScoala GârbăuÎncă nu există evaluări
- 9 CH Probl Alcani RezolvateDocument4 pagini9 CH Probl Alcani Rezolvategcimpan100% (1)
- Test AlcadieneDocument7 paginiTest AlcadieneAndreaÎncă nu există evaluări
- SUBIECT Simulare Bac2011 Chimie Organica IasiDocument3 paginiSUBIECT Simulare Bac2011 Chimie Organica IasidpÎncă nu există evaluări
- Suport de Curs Chimie CL X - 2019 - Gheorghe IlcosDocument20 paginiSuport de Curs Chimie CL X - 2019 - Gheorghe IlcosNicoleta DraguleasaÎncă nu există evaluări
- D222fe6fDocument4 paginiD222fe6fAlin CiubotaruÎncă nu există evaluări
- Chemistry2005 PDFDocument48 paginiChemistry2005 PDFMarcela Ivona ȘimonÎncă nu există evaluări
- Proiect Didactic MarinaDocument5 paginiProiect Didactic MarinaMarina CebotariÎncă nu există evaluări
- Edeleanu X Uman Locala 2020-Varianta1Document6 paginiEdeleanu X Uman Locala 2020-Varianta1Vlad CheaburuÎncă nu există evaluări
- C. Simionescu Teoretic 2022Document23 paginiC. Simionescu Teoretic 2022draguleasaÎncă nu există evaluări
- Curs Compusi CarboxiliciDocument26 paginiCurs Compusi CarboxiliciIoana ManoleÎncă nu există evaluări
- Edeleanu X Uman Judeteana 2019-FinalDocument4 paginiEdeleanu X Uman Judeteana 2019-FinalAna-Maria100% (2)
- Test - Introducere În Chimia OrganicăDocument5 paginiTest - Introducere În Chimia OrganicăAlexandru NutuÎncă nu există evaluări
- ccs2022 s1Document23 paginiccs2022 s1TudorÎncă nu există evaluări
- Test2 2 1Document9 paginiTest2 2 1Scoala GârbăuÎncă nu există evaluări
- Subiect Bac Chimie OrganicaDocument3 paginiSubiect Bac Chimie OrganicaCristina Guță100% (1)
- Test Initial Chimie Clasa XiDocument4 paginiTest Initial Chimie Clasa Xiedi ediÎncă nu există evaluări
- Chimia OrganicaDocument20 paginiChimia OrganicaEmanuel BaltaretuÎncă nu există evaluări
- Test3 2 4Document12 paginiTest3 2 4Nicoleta Draguleasa JitianuÎncă nu există evaluări
- 0 Introducere in Chimia OrganicaDocument20 pagini0 Introducere in Chimia OrganicaCarmen MatiasÎncă nu există evaluări
- Exercitii Si ProblemeDocument34 paginiExercitii Si ProblemeLorena IlincaÎncă nu există evaluări
- Subiecte Si Bareme Chimie Clasa A X-A 2022Document7 paginiSubiecte Si Bareme Chimie Clasa A X-A 2022Ionel BudÎncă nu există evaluări
- Sorin Roșca - Clasa10 - Subiect - Varianta 2Document7 paginiSorin Roșca - Clasa10 - Subiect - Varianta 2Johnny FreshÎncă nu există evaluări
- Teza 10 SN 2012Document4 paginiTeza 10 SN 2012teiubesciubireÎncă nu există evaluări