Documente Academic
Documente Profesional
Documente Cultură
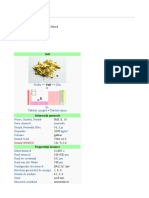
Mercur (HG)
Încărcat de
mihaifarcas10Titlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Mercur (HG)
Încărcat de
mihaifarcas10Drepturi de autor:
Formate disponibile
Proprietati fizice chimice si tehnologice la mercur
FIZICE:
Mercurul este singurul metal care este întâlnit în starea de agregare lichidă în
condiții standard de temperatură și presiune este un metal non-combustibil,
greu, de culoare argintie, care se va contracta sau își va mări volumul odată cu
creșterea temperaturii, făcându-l un material ideal pentru termometre.
Este ușor volatil, eliberând vapori toxici dacă este încălzit, iar vaporii acestuia
(deși incolori) pot fi recunoscuți după culoarea lor albastru-violacee în momentul
când electricitatea este prezentă. Prezintă un punct unic de topire, -38,83 °C, un punct de
fierbere de 356,73 °C, și are o densitate de 13.5336 g/cm3. La încălzire, metalul se dilată în
mod uniform, fierbând la temperatura de 357,01 °C și vaporizându-se la 360 °C. Mercurul
prezintă solubilitate mare.
Sublimatul coroziv de mercur este o sare neutră, formată prin uniunea acidului unei sări
comune și mercur și care conține o cantitate de acid destul de abundentă pentru a putea
dizolva noua cantitate de mercur, din moment ce patru părți din sublimat pot dizolva mai
mult de trei părți de mercur proaspăt. Dacă este privat de acidul conținut, mai este
cunoscut și sub numele de mercur dulce (mercure doux), și se prezintă într-o stare perfectă
de sare neutră; prezintă mai puțin acid decât s-ar putea să conțină, în timp ce sublimatul
coroziv de mercur reprezintă excesul de acid al sării comune).
CHIMICE:
Mercurul dizolvă aurul, zincul și multe alte metale formând aliaje cu acestea
denumite amalgame. Deoarece fierul este o excepție de la această regulă,
recipientele de fier au fost folosite în comerțul cu mercur. Încălzirea mercurului în
aer conduce la formarea oxidului de mercur.
Poziția sa în seria reactivității metalelor face mercurul un metal care nu
reacționează cu acizii obișnuiți precum acid sulfuric diluat, deși acizii oxigenați
concentrați ca acidul sulfuric sau acidul azotic sau apa regală (acid clorhidric + acid
azotic) pot să dizolve mercurul în scopul obținerii sulfaților, azotaților și
clorurilor. La fel ca și argintul, poate reacționa cu acidul sulfhidric
atmosferic. Mercurul reacționează cu sulful, neutralizând astfel vaporii rezultați în
cazul unor scurgeri accidentale de mercur.
Mercurul în stare elementară este relativ inert în aerul uscat, oxigen, oxid
nitros, dioxid de carbon, amoniac; în atmosferă umedă este acoperit de o peliculă
de oxid mercuros, iar încălzirea în aer sau oxigen la 350 °C îl transforma în oxidul
mercuric de culoare roșie: 2Hg(s) + O2(g) → 2HgO(s). Mercurul metalic
reacționează cu halogenurile, formând săruri; astfel rezultând:
S-ar putea să vă placă și
- AurulDocument7 paginiAurulGreg34t100% (1)
- Sodiu ReferatDocument2 paginiSodiu ReferatAlexandruyeah100% (1)
- SodiulDocument3 paginiSodiulFlorian Lucian60% (5)
- ARGINTULDocument10 paginiARGINTULMihaela PașcanÎncă nu există evaluări
- TerbiulDocument17 paginiTerbiulMihaela RoscaÎncă nu există evaluări
- Metale AlcalineDocument13 paginiMetale AlcalineIuliu Pîslaru100% (4)
- MERCURDocument23 paginiMERCURHorhe Geo Proiect ParalaxaÎncă nu există evaluări
- Referat ClorDocument3 paginiReferat ClorNidelea Rareș100% (2)
- MercurulDocument2 paginiMercurulAlexandru Marian CronţÎncă nu există evaluări
- Curs 5 Sem II 2021 Chimie AnorganicaDocument63 paginiCurs 5 Sem II 2021 Chimie AnorganicaAndreeaÎncă nu există evaluări
- Sodiul Si Compusii LuiDocument3 paginiSodiul Si Compusii LuisimsimoniÎncă nu există evaluări
- SODIUDocument2 paginiSODIUIonica PorumbÎncă nu există evaluări
- AurulDocument19 paginiAurulNataliaGhiletchiÎncă nu există evaluări
- Prezentarea SulfuluiDocument7 paginiPrezentarea SulfuluiStanislav PislariÎncă nu există evaluări
- Metale PrețioaseDocument25 paginiMetale PrețioaseAlexandra Dîrțu100% (1)
- SulfulDocument20 paginiSulfulOana Lavinia Achim100% (1)
- SulfulDocument12 paginiSulfulCirneala Anca80% (5)
- Substantele Chimice Clasificare v1Document15 paginiSubstantele Chimice Clasificare v1Gabriela HorvathÎncă nu există evaluări
- PlumbulDocument8 paginiPlumbulTanya WhiteÎncă nu există evaluări
- Prezentare SodiuDocument8 paginiPrezentare SodiuAndreea CarmenÎncă nu există evaluări
- Metalele AlcalineDocument14 paginiMetalele AlcalineVeronica Plamadeala100% (1)
- Oxizi Chimie....Document18 paginiOxizi Chimie....chirila sabinaÎncă nu există evaluări
- AURULDocument16 paginiAURULgiulyaÎncă nu există evaluări
- Proiect ChimieDocument9 paginiProiect ChimieALEXIA CIUMĂRNEANÎncă nu există evaluări
- SULFDocument20 paginiSULFGeorgeta Marioara100% (1)
- Elemente ChimiceDocument11 paginiElemente ChimiceLaura StoicaÎncă nu există evaluări
- ArgintulDocument22 paginiArgintulEmőke VargaÎncă nu există evaluări
- MercurulDocument19 paginiMercurulcsekearianaÎncă nu există evaluări
- Referat Chimie-MercurulDocument10 paginiReferat Chimie-MercurulMadalina Dinescu100% (2)
- MERCURDocument7 paginiMERCURStanciuValentin100% (1)
- De La Wikipedia, Enciclopedia Liberă: Număr EINECSDocument14 paginiDe La Wikipedia, Enciclopedia Liberă: Număr EINECSMai IncearcaÎncă nu există evaluări
- Curs 4 - Grupa16, Sulfuri, Se Si TeDocument22 paginiCurs 4 - Grupa16, Sulfuri, Se Si TeBianca OlteanuÎncă nu există evaluări
- MercurDocument12 paginiMercurIbanescu StefanÎncă nu există evaluări
- Compusii HidrogenatiDocument3 paginiCompusii Hidrogenatisergiu1994Încă nu există evaluări
- Biomateriale ArgintulDocument14 paginiBiomateriale ArgintulAnca NegruÎncă nu există evaluări
- Totul Despre Mercur-Gilca Andra, AF, Anul I, GR 2Document20 paginiTotul Despre Mercur-Gilca Andra, AF, Anul I, GR 2AndraCatalinaÎncă nu există evaluări
- Oxizi Metalici BaziciDocument18 paginiOxizi Metalici BaziciVasilache DamianÎncă nu există evaluări
- Clorura de SodiuDocument35 paginiClorura de SodiuAndreea Bocirnea100% (1)
- OXIZII - Importanta Si Utilizari - Cazan Bianca ElenaDocument7 paginiOXIZII - Importanta Si Utilizari - Cazan Bianca ElenaClaudia ElenaÎncă nu există evaluări
- CuprulDocument4 paginiCuprulAmdregaz2Încă nu există evaluări
- Hidrogenul Sulfurat Si SulfurileDocument10 paginiHidrogenul Sulfurat Si Sulfurileadrian cernatescuÎncă nu există evaluări
- MercurulDocument2 paginiMercurulmaxmichael218Încă nu există evaluări
- Acidul AceticDocument12 paginiAcidul AceticAdam Blair50% (4)
- Referat Chimie - Clorul - Tanase Iuliana Cls IX A BDocument4 paginiReferat Chimie - Clorul - Tanase Iuliana Cls IX A BIuliana DumitruÎncă nu există evaluări
- Plmbul Si Compusii AcestuiaDocument6 paginiPlmbul Si Compusii AcestuiaZoican RaduÎncă nu există evaluări
- Tehnologia de Obtinere A LitiuluiDocument22 paginiTehnologia de Obtinere A LitiuluiŞarîngă George Alexandru100% (1)
- Hidrurile Metalelor RareDocument37 paginiHidrurile Metalelor RareSilvia BijuteriiHandmadeÎncă nu există evaluări
- OXIZII - Importanta Si UtilizariDocument7 paginiOXIZII - Importanta Si UtilizariClaudia ElenaÎncă nu există evaluări
- Acid SulfuricDocument2 paginiAcid SulfuricCristina-Andreea TudorÎncă nu există evaluări
- Proprietati Fizice Si ChimiceDocument2 paginiProprietati Fizice Si ChimiceannaÎncă nu există evaluări
- IodDocument8 paginiIodAdy BrudariuÎncă nu există evaluări
- SulfulDocument20 paginiSulfulVio BanÎncă nu există evaluări
- Silviu SulfulDocument3 paginiSilviu Sulfulraportaru93Încă nu există evaluări
- Substantele AnorganiceDocument16 paginiSubstantele AnorganiceAndrei AvdeevÎncă nu există evaluări
- Clorul Si Compusii LuiDocument15 paginiClorul Si Compusii LuiEmanuell04Încă nu există evaluări