Documente Academic
Documente Profesional
Documente Cultură
Legile Gazului Ideal
Încărcat de
EcaterinaDrepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Legile Gazului Ideal
Încărcat de
EcaterinaDrepturi de autor:
Formate disponibile
34 Termotehnica
3 TRANSFORM!RI SIMPLE DE STARE A GAZELOR
n termodinamic! se consider! c! procesele pe care le sufer! agen"ii
termici n interiorul instala"iilor termice sunt compuse dintr-un ansamblu de
transform!ri termodinamice simple. Transform!rile simple reprezint! procese
termodinamice n cursul c!rora varia"ia parametrilor de stare se face dup! o
aceea#i lege, neschimbat!, din starea ini"ial! pn! n cea final! .
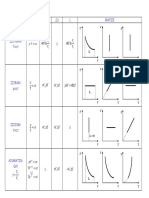
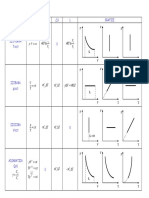
Transform!rile simple de stare sunt: izocora, izobara, izoterma, adiabata #i
politropa. Gazul este considerat gaz perfect.
Procesele care se desf!#oar! n sensul de cre#tere a volumului se numesc
destinderi, iar cele care au loc n sensul diminu!rii volumului se numesc
compresiuni. n prezentarea de mai jos, diagramele sunt construite pentru un gaz
cu masa de o unitate, deci m!rimile care intervin sunt m!rimi specifice.
3.".Transformarea izocor# (legea lui Charles)
Transformarea izocor! se desf!#oar! la volum constant:
v=ct , deci dv=0.
Se scrie ecua"ia de stare ($.4 a) pentru starea ini"ial! $#i pentru cea final! 2
ale unui gaz perfect, ntr-o transformare la volum constant. Rezult!:
2 1 2
1 1 1
RT v p
RT v p
2
2
1
1
T
p
T
p
Ecua"ia transform!rii izocore:
(3.1) ct
T
p
a) b)
Fig. 3.$ Reprezentarea transform!rii izocore
a)Diagrama mecanic!; b)Diagrama caloric!
Reprezentarea transform!rii izocore n diagrama p-v este un segment de
dreapt! perpendicular pe axa volumelor (fig.3.$a).
Lucrul mecanic schimbat cu mediul exterior este nul, deoarece volumul
r!mne constant:
v
1
p
1
p
2
v
p
v
1
=v
2
=ct
v=ct
s
2
s
1
T
1
T
2
s
T
Termotehnica 35
(3.2) 0 pdv l
2
1
12
Schimbul de c!ldur! ntre sistem #i mediul exterior n timpul transform!rii
izocore:
(3.3) ( )
1 2 v 12 1 2 12
T T c l u u q + ; [J/kg]
Dac!
12
q >0, ceea ce implic!
2
T >
1
T nseamn! c! gazul prime#te c!ldur!
n timpul transform!rii, de la mediul exterior . C!ldura
12
q este propor"ional! cu
aria cuprins! ntre curba transform!rii, axa absciselor #i cele dou! drepte verticale
corespunz!toare st!rii ini"iale #i finale reprezentate n diagrama caloric!.
3.2. Transformarea izobar# (legea Guy-Lussac)
Transformarea izobar! se desf!#oar! la presiune constant!:
p=ct , deci dp=0.
Se scrie ecua"ia de stare pentru starea ini"ial! $ #i pentru cea final! 2 ale
unui gaz perfect, ntr-o transformare la presiune constant!. Rezult! :
2 2 1
1 1 1
RT v p
RT v p
2
1
2
1
T
T
v
v
Ecua"ia transform!rii izobare rezult!:
(3.4) ct
T
v
Izobara se reprezint! n diagrama p-v printr-un segment de dreapt!
perpendicular pe axa presiunilor (fig.3.2a). Lucrul mecanic schimbat de sistem cu
mediul exterior n timpul transform!rii:
(3.5) ( ) ( )
1 2 1 2
2
1
12
T T R v v p pdv l
[J/kg].
Lucrul mecanic este egal, n valoare absolut!, cu aria dreptunghiului
m!rginit de axa absciselor, izobar! #i perpendicularele coborte din capetele
izobarei pe axa absciselor .
C!ldura schimbat! cu mediul exterior:
(3.6) ( )
1 2 p 1 2 12
T T c h h q [J/kg] .
a) b)
Fig. 3.2 Reprezentarea transform!rii izobare
a)Diagrama mecanic!; b)Diagrama caloric!
v
2
p
1
=p
2
=ct
v
1
p
1
v
p
p=ct
s
2
s
1
T
1
T
2
s
T
36 Termotehnica
3.3.Transformarea izoterm# (legea Boyle-Mariotte)
Transformarea izoterm! se desf!#oar! la temperatur! constant!:
T=ct , deci dT=0.
a) b)
Fig 3.3 Reprezentarea transform!rii izoterme
a)Diagrama mecanic!; b)Diagrama caloric!
Se scrie ecua"ia de stare pentru starea ini"ial! 1 #i pentru cea final! 2 ale
unui gaz perfect, ntr-o transformare la temperatur! constant!. Rezult! :
RT v p
RT v p
2 2
1 1
2 2 1 1
v p v p .
Ecua"ia caracteristic! a transform!rii izoterme rezult!:
(3.7) ct pv
Fig.3.4 Reprezentarea a trei transform!ri izoterme oarecare
n diagrama p-v , transformarea izoterm! se reprezint! printr-un arc de
hiperbol! echilateral! (fig.3.3a). Coeficientul unghiular al tangentei la curb! este:
T
=ct
T
=ct
T=ct
p
v
T<T
<T
v
1
s
2
s
1
v
v
2
s
T=ct
T
T p
i
2
1
T=ct
p
1
p
2
Termotehnica 37
(3.8)
v
p
dv
dp
tg
i
.
Lucrul mecanic specific, schimbat cu exteriorul n timpul unei transform!ri
izoterme, exprimat n [J/kg]:
(3.9)
1
2
1
2
2
1
1 1
1
2
1 1
2
1
1
2
1
1 12
p
p
ln RT
v
v
ln RT
p
p
ln v p
v
v
ln v p
v
dv
v p pdv l
n diagrama p-v, lucrul mecanic specific este propor"ional cu aria
suprafe"ei determinat! de axa absciselor, curba izotermic! #i ordonatele extreme.
Schimbul de c!ldur! se deduce din expresia primului principiu :
pdv q du
#i din ecua"ia caloric! pentru gaze perfecte :
dT c du
v
.
Pentru transformarea izoterm!, dT=0, rezult!:
; pdv q deci
(3.10)
12 12
l q [J/kg]
n cazul transform!rii izotermice a unui gaz perfect, cantitatea de c!ldur!
schimbat! cu mediul exterior (absorbit! sau evacuat!) se transform! integral n
lucru mecanic.
Teoretic, viteza de desf!#urare a unui proces izoterm este infinit!. n
practic!, nu exist! procese izoterme, deoarece viteza de desf!#urare a proceselor
este finit!. Se pot considera izoterme acele transform!ri care se desf!#oar! cu
vitez! foarte mic!, astfel nct gazul s! aib! suficient timp pentru a evacua
/absorbi c!ldur! #i a-#i men"ine temperatura constant!. Apropierea proceselor
reale de caracteristicile izotermei se face, practic, prin r!cirea instala"iilor n care
se produc compresiuni.
3.4.Transformarea adiabat#
ntr-o transformare adiabat!, agentul termic nu schimb! c!ldur! cu
exteriorul:
( ) 0 q ; 0 q
12
.
Din ecua"ia primului principiu al termodinamicii:
pdv du q +
n care se nlocuiesc ecua"iile calorice ale gazelor perfecte :
dT c dh
dT c du
p
v
#i #tiind c! entalpia elementar! este:
vdp pdv du dh + + conform rela"iei de defini"ie (2.13b), rezult!:
0 vdp dT c q
0 pdv dT c q
p
v
+
Egalnd rela"iile de mai sus:
(3.11)
dv p
dp v
c
c
k
v
p
Rezult!:
38 Termotehnica
ct p ln v ln k 0
p
dp
v
dv
k
0 vdp kpdv
+ +
+
Se ob"ine ecua"ia caracteristic! a adiabatei:
(3.12) ct pv
k
Din ecua"ia de stare ($.4a) se ob"ine, prin derivare logaritmic!:
(3.13)
T
dT
v
dv
p
dp
+ .
Se deriveaz! logaritmic #i ecua"ia caracteristic! a adiabatei (3.$2)#i
rezult!:
(3.14) 0
v
dv
k
p
dp
+
Se nlocuie#te
v
dv
T
dT
p
dp
n ecua"ia (3.$4) #i rezult!
( ) ct Tv 0
v
dv
1 k
T
dT
1 k
+
Rela"ia:
(3.15) ct Tv
1 k
reprezint! o alt! form! a ecua"iei de stare a adiabatei.
Eliminnd volumul ntre ecua"iile (3.$2) #i (3.$5) se ob"ine
(3.16) ct
p
T
k
1 k
o a treia form! a ecua"iei caracteristice a adiabatei.
a) b)
Fig. 3.5 Reprezentarea transform!rii adiabate
a)Diagrama mecanic!; b)Diagrama caloric!
a
s
1
T
2
T
1
s
T
s
1
=s
2
=ct
v
2 v
1 v
p
p
1
p
2
s=ct
Termotehnica 39
n diagrama p-v , adiabata se reprezint! (fig.3.5a) printr-un arc de
hiperbol!, care are o pant! mai mare dect izoterma (rela"ia 3.8). Panta
adiabatei este dat! de rela"ia:
(3.17)
v
p
k
dv
dp
tg
a
Lucrul mecanic schimbat de sistem cu mediul exterior, n timpul
transform!rii adiabate este :
2
1
12
pdv l
Din expresia principiului nti:
pdv q du rezult!:
(3.18) du l
#i , deci:
(3.19) ( )
2 1 v 12
T T c l [J/kg].
n concluzie, ntr-o destindere adiabat!, lucrul mecanic se efectueaz! pe
seama reducerii energiei interne a gazului. ntr-o compresiune adiabat!, lucrul
mecanic primit din exterior se transform! integral n energie intern!. Expresia
lucrului mecanic se mai poate deduce :
2
1
12
pdv l unde ct v p v p pv
k
2
2
k
1
1
k
(3.20)
1
1
1
]
1
,
_
k
1 k
1
2 1 1 2 1
2 2 1 1
k 1
1
k 1
2 k
1 1
2
1
k
k
1
1 12
p
p
1
1 k
v p
1 k
RT RT
1 k
v p v p
k 1
v v
v p
v
dv
v p l
n practic!, transform!rile care pot fi considerate adiabatice sunt acele
transform!ri care se desf!#oar! cu viteze mari, astfel nct gazul s! nu aib! timp
s! schimbe c!ldur! cu mediul.
3.5 Transformarea politropic#
Transformarea politropic! reprezint! o transformare de stare general!, care
define#te procesele termodinamice n cursul c!rora agentul termic schimb!
energie sub form! de c!ldur! #i lucru mecanic cu mediul exterior #i n care se
modific! to"i parametrii de stare p,v,T.
n practic!, destinderea sau comprimarea gazelor nu se poate realiza n
mod riguros adiabatic #i nici izotermic. n procesele reale, schimbul de c!ldur!
dintre agentul termic #i mediu nu poate fi mpiedicat complet, pentru o izolare
adiabatic!, dup! cum nu poate fi nici intensificat att de mult nct temperatura
agentului s! se men"in! constant! n timpul procesului termodinamic. Procesele
reale de comprimare sau destindere din instala"iile termice pot fi considerate
transform!ri politropice.
Transformarea politropic! poate fi definit! printr-o lege de varia"ie a
presiunii #i volumului de forma:
40 Termotehnica
(3.21) ct pv
n
, n care [ ] + , n reprezint! exponentul politropic.
Formulele de calcul stabilite pentru transformarea adiabatic!, se pot folosi
pentru transformarea politropic! nlocuind exponentul adiabatic, k, prin
exponentul politropic, n :
(3.22) ct Tv
1 n
(3.23) ct
p
T
n
1 n
Forma curbei politropice n digrama p-v este de hiperbol! . n
termodinamic!, prezint! interes transform!rile politropice care au exponentul
cuprins n domeniul 1<n<k.
Lucrul mecanic al transform!rii politropice va fi:
(3.24)
( )
1
1
1
]
1
,
_
n
1 n
1
2 1 1 2 1 2 2 1 1
12
p
p
1
1 n
v p
1 n
T T R
1 n
v p v p
l
exprimat n [J/kg]
C!ldura unitar! schimbat! ntre sistem #i mediu:
(3.25) dT c q
n
sau, prin integrare:
(3.26) ( )
1 2 n 12
T T c q [J/kg]
unde c
n
-reprezint! c!ldura specific! politropic!,
( )1
]
1
kgK
J
.
C!ldura specific! politropic! se deduce pornind de la expresia primului
principiu al termodinamicii, scris! pentru un sistem nchis:
l q pdv q du
n care se nlocuiesc ecua"iile calorice de stare precum #i rela"ia lucrului mecanic
elementar dedus! din forma (3.22) a ecua"iei caracteristice a politropei:
( ) 1 n
RdT
T 1 n
dT pv
dv p l
dT c q
dT c du
n
v
unde
v p
c c R ,
( )1
]
1
kgK
J
Se ob"ine:
(3.27)
1 n
c nc
c
p v
n
,
( )1
]
1
kgK
J
C!ldura schimbat! se mai poate, deci, calcula cu rela"ia:
(3.28) ( )
1 2 v 12
T T c
1 n
k n
q
,
1
]
1
kg
J
Transformarea politropic! reprezint! un proces termodinamic general.
Particulariznd valorile exponentului n n ecua"ia (3.2$), se pot ob"ine celelalte
transform!ri termodinamice simple ale gazelor perfecte
p n
c c ; ct p ; 0 n -izobar!
n
c ; ct pv ; 1 n -izoterm!
Termotehnica 41
0 c ; ct pv ; k n
n
k
-adiabat!
v n
c c ; ct v ; n -izocor!
n fig.3.6 s-a reprezentat transformarea politropic! pentru diferite valori
particulre ale exponentului politropic n. Se observ! c!, pe acelea#i axe de
coordonate au fost trasate curbele caracteristice pentru izobar!, izoterm!, adiabat!
#i izocor!, al!turi de dou! politrope, k n > #i k n 1 < < .
Fig.3.6 Reprezentarea politropei n diagram! mecanic!
ntreb!ri test
$.Izocora este transformarea de stare care se reprezint! n coordonate p-v prin:
a) o perpendicular! pe axa volumului specific, v;..................................................
b) o paralel! la axa volumului specific, v; a) b) c)
c) o perpendicular! la axa presiunilor, p.
2.Care dintre rela"iile urm!toare reprezint! legea unei transform!ri simple de stare:.........
a) ct v p
n
; b) ct T p ; c) ct v p a) b) c)
3.Intr-o destindere adiabatic! a unui gaz, lucrul mecanic se efectueaz! pe seama:
a)reducerii energiei interne a gazului;......................................................................
b)cre#terii energiei interne a gazului; a) b) c)
c)reducerii entropiei gazului.
4.ntr-o transformare izoterm! a unui gaz perfect, lucrul mecanic primit de sistem:
a)are valoare negativ!;........................................................................................
b)se reg!se#te n varia"ia energiei interne; a) b) c)
c)se transform! integral n c!ldur!.
5.Lucrul mecanic efectuat de un sistem termodinamic n timpul unui proces de destindere, din
starea $ n starea 2, este propor"ional cu aria ha#urat! n figura:......................................
a) b) c)
a) b) c)
v
p
1
2
v
p
1
2
v
p
2
1
n=1
n>k
1<n<k
n
n=k
n=0
v
p
42 Termotehnica
6 n practic!, transform!rile care pot fi considerate izoterme sunt cele care se desf!#oar! cu viteze:
a)mari, astfel nct c!ldura s! poat! fi schimbat! cu exteriorul;..............................
b)mici, astfel nct c!ldura s! poat! fi schimbat! cu exteriorul; a) b) c)
c)oarecare, iar sistemul este r!cit n mod adecvat.
7.Intr-o destindere izoterma a unui gaz, lucrul mecanic se efectueaz! pe seama:
a)reducerii energiei interne a gazului;................................................................
b)caldurii introduse din exterior; a) b) c)
c)caldurii evacuate n exterior.
8 n practic!, transform!rile care pot fi considerate adiabatice sunt cele care se desf!#oar! cu
viteze:
a)mici, astfel nct c!ldura s! poat! fi schimbat! cu exteriorul;........................
b)mari, astfel nct c!ldura s! poat! fi schimbat! cu exteriorul; a) b) c)
c)mari, astfel nct sistemul s! nu aib! timp s! schimbe c!ldur! cu exteriorul.
Problema 3.1
3.1.Un kilogram dintr-un gaz perfect, cu constanta
K kg
J
300 R
, se destinde
de la starea $, caracterizat! prin parametrii bar 6 p
1
#i
kg
m
25 , 0 v
3
1
, pn! la
starea 2, la care volumul specific este de 2,5 ori mai mare. Procesul de destindere
este politropic, cu exponentul 5 , 1 n . S! se calculeze:
a)lucrul mecanic schimbat de sistem cu exteriorul, n procesul politropic 1-2;
b)c!ldura schimbat! de sistem cu mediul, n acest proces, dac! se cunosc
exponentul adiabatic 41 , 1 k #i c!ldura specific! sub volum constant
k kg
kJ
7 , 0 c
v
.
Rezolvare
Masa gazului fiind unitar!, volumul total coincide cu cel specific v V .
Transformarea politropic! are legea ct v p
n
. nseamn! c!, pentru st!rile
ini"ial! #i final! se poate scrie egalitatea:
n
2 2
n
1 1
v p v p
Presiunea dup! destindere rezult!:
n
2
1
1 2
v
v
p p
,
_
Dar
1 2
v 5 , 2 v , deci presiunea p
2
va fi:
bar 518 , 1
5 , 2
1
10 6 p
5 , 1
5
2
,
_
la volumul specific
kg
m
625 , 0 25 , 0 5 , 2 v
3
2
Fig. 3.$.Destindere politropic!, n=$,5
0,625
0,25
v,
[m
3
/kg]
p,
[bar]
6
1,518
Termotehnica 43
Lucrul mecanic:
( )
( )
kg
J
10 102 , 1 25 , 0 625 , 0
1 5 , 1
1
25 , 0 10 6
v v
1 n
1
v p dv v v p
v
dv
v p l L
5 1 5 , 1 1 5 , 1 5 , 1 5
1 n
1
1 n
2 1 1
2
1
2
1
n n
1 1
n
n
1 1 12 12
+
+
+ +
+ +
are valoare pozitiv!, deci este efectuat de c!tre sistem n exterior.
b)C!ldura schimbat! cu mediul exterior este:
( )
1 2 n 12 12
T T c q Q
unde c!ldura specific! politropic!, c
n
, se calculeaz! cu rela"ia:
K kg
J
126
1 5 , 1
41 , 1 5 , 1
700
1 n
k n
c c
v n
iar temperaturile se afl! din ecua"ia termic! de stare:
K 500
300
25 , 0 10 6
R
v p
T
5
1 1
1
K 25 , 316
300
625 , 0 10 518 , 1
R
v p
T
5
2 2
2
Rezult!
( )
kg
J
5 , 23152 500 25 , 316 126 q
12
Observa"ie. Valoarea ob"inut! este negativ!, deci sistemul a cedat c!ldur!
mediului, n timpul destinderii.
Probleme propuse
3.2.Aerul din interiorul unui cilindru cu piston sufer! o expansiune de la volumul
specific
kg
m
8 , 0 v
3
1
, pn! la volumul specific
kg
m
8 , 1 v
3
2
la presiunea
constant! bar 1 p . Cunoscnd constanta aerului
K kg
kJ
287 , 0 R
, precum #i
c!ldura specific! izobar!,
K kg
kJ
01 , 1 c
p
, s! se determine:
a)lucrul mecanic specific schimbat de sistem cu mediul exterior,
b)c!ldura unitar! schimbat! de sistem cu mediul exterior,n timpul
evolu"iei din starea $ n starea 2.
3.3.Considernd aceea#i evolu"ie a aerului ca n problema 3.2., s! se determine
varia"ia energiei interne specifice #i varia"ia entalpiei specifice ntre st!rile $ #i 2.
3.4.O butelie metalic! nchis!, cu capacitatea de 40 de litri este plin! cu oxigen.
Oxigenul se consider! gaz perfect, cu constanta
. K kg
J
84 , 259 R
Presiunea
din butelie este de 150 bar, la temperatura de 288 K. Butelia este mutat! ntr-un
mediu ambiant cu temperatura de 25
o
C. S! se afle prin ce proces termodinamic
simplu trece oxigenul din butelie, pn! n momentul n care temperatura din
butelie este egal! cu cea a mediului ambiant. S! se determine schimbul de lucru
44 Termotehnica
mecanic #i de c!ldur! cu exteriorul. Se cunoa#te c!ldura specific! la presiune
constant!, pentru oxigen,
K kg
J
4 , 908 c
p
.
3.5.ntr-un cilindru cu piston, se afl! aer la presiunea bar 2 , 1 p
1
#i volumul
specific
kg
dm
1250 v
3
1
. Constanta aerului este
. K kg
J
13 , 287 R
Pistonul se
deplaseaz! n sensul comprim!rii aerului, pn! cnd presiunea atinge valoarea
bar 5 p
2
. Mi#carea se desf!#oar! att de ncet, nct transformarea se poate
considera izoterm!. Se cere s! se afle:
a)temperatura la care se desf!#oar! procesul;
b)lucrul mecanic specific schimbat de sistem cu exteriorul;
c)c!ldura unitar! schimbat! de sistem cu exteriorul;
d)varia"ia entalpiei sistemului, ntre cele dou! st!ri de echilibru.
R!SPUNSURI $I REZOLV!RI
ntreb!ri test
1.a; 2.a,c; 3.a; 4.a,c; 5.c; 6.b,c; 7.b; 8.c.
Probleme
3.2. Rezolvare
Procesul izobar este reprezentat grafic n figura 3.1.
Fig.3.2.Expansiune izobar!
a)Lucrul mecanic specific se calculeaz! cu rela"ia:
( ) ( )
kg
J
10 8 , 0 8 , 1 10 1 v v p dv p dv p l
5 5
1 2
2
1
2
1
12
Lucrul mecanic a rezultat pozitiv, deci, conform conven"iei pentru semne, el
este efectuat de c!tre sistem n exterior.
b)C!ldura unitar! se calculeaz! cu ajutorul ecua"iei calorice, care pentru un
proces izobar devine:
( )
1 2 p 12
T T c q
2 1
v
2
p
1
=p
2
=ct
v
1
p
1
v
p
Termotehnica 45
Temperaturile T
1
#iT
2
se pot afla aplicnd ecua"ia de stare pentru starea $,
respectiv starea2:
K 6 , 278
13 , 287
8 , 0 10 1
R
v p
T
5
1 1
1
K 89 , 626
13 , 287
8 , 1 10 1
R
v p
T
5
2 2
2
( )
kg
kJ
783 , 351
kg
J
351783 6 , 278 89 , 626 10 01 , 1 q
3
12
C!ldura are valoare pozitiv!, deci, conform conven"iei semnelor, c!ldura aceasta
este primit! de sistem din mediul exterior.
3.3. Rezolvare
Expresia primului principiu al termodinamicii, scris! pentru mas! unitar! a
agentului termic (aerul, n acest caz):
12 1 2 12
l u u q +
ne d! posibilitatea s! calcul!m varia"ia energiei interne.
kg
J
251783 100000 351783 l q u u u
12 12 1 2
Rela"ia dintre varia"ia entalpiei #i varia"ia energiei interne (vezi problema 2.2)
este: u k h
Coeficientul adiabatic k se ob"ine din rela"ia:
41 , 1
13 , 287 1010
1010
R c
c
c
c
k
p
p
v
p
n care s-a utilizat rela"ia lui Mayer:
v p
c R c +
Varia"ia entalpiei rezult!:
kg
J
2 , 352496 251783 41 , 1 h
3.4. Rezolvare
Butelia fiind un sistem nchis, rigid, procesul suferit de oxigenul din interior se
desf!#oar! la volum constant (transformare izocor!). Se observ! imediat c! lucrul
mecanic este nul, deoarece volumul nu variaz!.
C!ldura schimbat! cu exteriorul este dat! de rela"ia:
( )
1 2 v v 12
T T c m T c m Q
Masa oxigenului se poate calcula din ecua"ia de stare scris! pentru starea
ini"ial! a sistemului, pentru care se cunosc parametrii:
1 1 1
T R m V p rezult! kg 017 , 8
288 84 , 259
10 40 10 150
RT
V p
m
3 5
1
1 1
C!ldura specific! sub volum constant se deduce din rela"ia lui Mayer:
p v
c R c + rezult!
K kg
J
56 , 648 84 , 259 4 , 908 R c c
p v
Temperatura final! este cea a mediului ambiant:
K 15 , 288 25 15 , 273 T
2
+
C!ldura schimbat! cu mediul va fi:
46 Termotehnica
( ) kJ 215 , 51 15 , 288 298 56 , 648 017 , 8 Q
12
Observa"ie. C!ldura este primit! de c!tre sistem, deoarece valoarea sa este
pozitiv!. Conform principiului I al termodinamicii, n cazul unei transform!ri
izocore, c!ldura primit! de sistem se transform! integral n energie intern!,
deoarece lucrul mecanic este nul.
3.5. Rezolvare
a)Ecua"ia de stare scris! pentru starea ini"ial! permite calculul temperaturii la care
se desf!#oar! procesul:
K 4 , 522
13 , 287
25 , 1 10 2 , 1
R
v p
T
5
1 1
Fig.3.5 Reprezentarea unui proces izoterm: curba este o hiperbol! echilater!
b)Legea transform!rii izoterme conduce la egalitatea:
2 2 1 1
v p v p din care rezult!
kg
m
3 , 0
10 5
25 , 1 10 2 , 1
v
3
5
5
2
Lucrul mecanic specific va fi:
( )
1
2
1 1 1 2 1 1
2
1
2
1
1 1 12
v
v
ln v p v ln v ln v p
v
dv
v p dv p l
(unde presiunea s-a exprimat ca func"ie de volum, folosind legea izotermei scris!
pentru starea ini"ial! #i pentru o stare intermediar! oarecare:
v
1
v p p
1 1
)
Rezult!
kg
J
5 , 214067
25 , 1
3 , 0
ln 25 , 1 10 2 , 1 l
5
12
Lucrul mecanic specific este negativ, ceea ce nseamn! c! sistemul a primit acest
lucru mecanic din exterior.
c)n rela"ia primului principiu al termodinamicii, scris! pentru sisteme nchise:
12 12
l u q +
varia"ia energiei interne se anuleaz! deoarece temperatura sistemului a r!mas
aceea#i n timpul transform!rii. Deci,
p, [bar]
v, [m
3
/kg]
1,25
p
v
v
2
1
2
5
1,2
Termotehnica 47
kg
J
5 , 214067 l q
12 12
d)Varia"ia entalpiei, ca #i a energiei interne este nul!:
0 u k h
Observa"ie ntr-o transformare izoterm!, att energia intern!, ct #i entalpia
r!mn constante.
S-ar putea să vă placă și
- Termodinamica Pentru BacalaureatDocument12 paginiTermodinamica Pentru Bacalaureationcazacu100% (4)
- Motoare TermiceDocument16 paginiMotoare Termicevadim100% (2)
- Barem Bac Mate-Info Simulare Bucuresti 1 Februarie 2013 PDFDocument2 paginiBarem Bac Mate-Info Simulare Bucuresti 1 Februarie 2013 PDFAnonymous j9sTxpVRÎncă nu există evaluări
- Marimi Legate de StructuraDocument2 paginiMarimi Legate de StructuraIrene Ungureanu100% (1)
- Istoria MotoarelorDocument9 paginiIstoria MotoarelorBuzoianu StefanÎncă nu există evaluări
- Combinatii ComplexeDocument4 paginiCombinatii ComplexeSergiu JecÎncă nu există evaluări
- Poluarea LuminoasaDocument6 paginiPoluarea Luminoasaanghelmariana17Încă nu există evaluări
- Test Electricitate XDocument3 paginiTest Electricitate XEva AntoniaÎncă nu există evaluări
- Relatia R.MayerDocument2 paginiRelatia R.MayerAnonymous ByZYdUU39RÎncă nu există evaluări
- Circuite de Curent Alternativ - Lista de Texte PDFDocument8 paginiCircuite de Curent Alternativ - Lista de Texte PDFHuzumÎncă nu există evaluări
- Tabel Formule TermoDocument2 paginiTabel Formule TermoAndreea LilianaÎncă nu există evaluări
- Raspunsuri IntrebariDocument18 paginiRaspunsuri IntrebariElla Elly100% (1)
- Amestecuri de GazeDocument5 paginiAmestecuri de GazeDiaconuAlexandru100% (1)
- Motorul OttoDocument5 paginiMotorul Ottoadinaa23100% (1)
- Principiul Zero Al TermodinamiciiDocument2 paginiPrincipiul Zero Al TermodinamiciiAndreea Luiza ScripcaruÎncă nu există evaluări
- Rezolvari Variante Curent Continuu 1-100Document100 paginiRezolvari Variante Curent Continuu 1-100Tanase Mihai100% (7)
- Mecanica 2009 S2 PDFDocument100 paginiMecanica 2009 S2 PDFmihaiÎncă nu există evaluări
- Principiul I Al TermodinamiciiDocument3 paginiPrincipiul I Al TermodinamiciiBernad AmandaÎncă nu există evaluări
- Termotehnica Si Masini Termice PDFDocument369 paginiTermotehnica Si Masini Termice PDFOvy Nita100% (7)
- Circuit Serie Cu Rezistor, Bobină Și Condensator În Curent Alternativ. (Circuit RLC Serie În C.a)Document2 paginiCircuit Serie Cu Rezistor, Bobină Și Condensator În Curent Alternativ. (Circuit RLC Serie În C.a)Davide MuresanÎncă nu există evaluări
- Bateriile GalvaniceDocument5 paginiBateriile GalvaniceIftimie Dan IonutÎncă nu există evaluări
- Pile ElectriceDocument11 paginiPile ElectriceStanciu Ionuţ100% (1)
- ProblemeDocument9 paginiProblemeLoredana Vasilciuc0% (1)
- Randamentul DieselDocument1 paginăRandamentul DieselIonuțSava100% (2)
- Calorimetrie PDFDocument7 paginiCalorimetrie PDFvancearadu100% (1)
- Compozitia Chimica A PetroluluiDocument6 paginiCompozitia Chimica A PetroluluiIrina Tudorache100% (1)
- Amortizarea OscilaţiilorDocument2 paginiAmortizarea OscilaţiilorAndreea Cristina100% (1)
- Pendulul GravitationalDocument3 paginiPendulul GravitationalMocanita Steluta100% (1)
- Chimie ReferatDocument9 paginiChimie ReferatMoldovanu Ionut100% (1)
- Transformări TermodinamiceDocument4 paginiTransformări TermodinamiceDumbravă Sergiu100% (1)
- Continuitatea Functiilor Cu ExempleDocument28 paginiContinuitatea Functiilor Cu ExempleRadulescu ClaudiaÎncă nu există evaluări
- Echilibrul Punctului MaterialDocument6 paginiEchilibrul Punctului MaterialGherman Adrian100% (1)
- Circuite Basculante AstabileDocument18 paginiCircuite Basculante AstabileCristian Ionut DicaÎncă nu există evaluări
- Lucrari de Laborator TermodinamicaDocument8 paginiLucrari de Laborator TermodinamicaBianca GulerÎncă nu există evaluări
- LP8-Determinarea Caldurii Latente de Topire A GhetiiDocument2 paginiLP8-Determinarea Caldurii Latente de Topire A GhetiiDanalache Maria100% (1)
- Test TermodinamicaDocument2 paginiTest TermodinamicaEmilianAlexe0% (1)
- Test I AlchineDocument2 paginiTest I AlchineTase DaratÎncă nu există evaluări
- Legea Lui OhmDocument9 paginiLegea Lui OhmEugen Vlad100% (1)
- Raspunsuri 100 Variante Termodinamica 2007 PDFDocument100 paginiRaspunsuri 100 Variante Termodinamica 2007 PDFDany DanielÎncă nu există evaluări
- 15.sisturile BituminoaseDocument1 pagină15.sisturile BituminoaseRobert MihailescuÎncă nu există evaluări
- Termodinamica Formule GraficeDocument2 paginiTermodinamica Formule GraficeJohn Grosu100% (2)
- Formule Fizica Clasa IX-aDocument1 paginăFormule Fizica Clasa IX-aZuZuÎncă nu există evaluări
- Inelele Lui NewtonDocument6 paginiInelele Lui NewtonGeta GutanuÎncă nu există evaluări
- 50 - 56 - Probleme de Termodinamica. CicluriDocument7 pagini50 - 56 - Probleme de Termodinamica. CicluriTraian Anghel100% (3)
- Masina Frigorifica Si Pompa de CalduraDocument3 paginiMasina Frigorifica Si Pompa de CalduraSabina Nistor100% (1)
- Grile Fizica AdmitereDocument121 paginiGrile Fizica AdmitereLiliana BalanÎncă nu există evaluări
- Termodinamica Formule GraficeDocument2 paginiTermodinamica Formule GraficeJohn GrosuÎncă nu există evaluări
- 7.2. Procese Ciclice PDFDocument2 pagini7.2. Procese Ciclice PDFMariana CalinÎncă nu există evaluări
- Obtinerea AluminiuluiDocument7 paginiObtinerea AluminiuluiOlei AdrianÎncă nu există evaluări
- Compusi HalogenatiDocument4 paginiCompusi HalogenatiSilviu PopÎncă nu există evaluări
- Subiecte Bac Fizica - Electricitate/curentDocument100 paginiSubiecte Bac Fizica - Electricitate/curentmada_t9460% (5)
- Transformari de Stare Ale Gazului PerfectDocument8 paginiTransformari de Stare Ale Gazului PerfectZavturCorneliuÎncă nu există evaluări
- Curs Termo 5-6Document8 paginiCurs Termo 5-6Niculinho NicushorÎncă nu există evaluări
- Curs 4 Termo 21-22-4Document9 paginiCurs 4 Termo 21-22-4Lorena ionelaÎncă nu există evaluări
- Probleme FizicaDocument10 paginiProbleme FizicaVoicu RaduÎncă nu există evaluări
- Termodinamica p1 Adnotari FinalDocument21 paginiTermodinamica p1 Adnotari FinalIonuț CarpÎncă nu există evaluări
- Curs 4 TermodinamicaDocument6 paginiCurs 4 TermodinamicaPara CataÎncă nu există evaluări
- Principiul II Al TermodinamiciiDocument12 paginiPrincipiul II Al Termodinamiciicos2inÎncă nu există evaluări
- Consideratii Privind Marirea Preciziei de Calcul Pentru Transformarile Care Stau La Baza Aprecierii Performantelor La Cazanelor Si Turbinelor Cu AburDocument6 paginiConsideratii Privind Marirea Preciziei de Calcul Pentru Transformarile Care Stau La Baza Aprecierii Performantelor La Cazanelor Si Turbinelor Cu AburConstantin CHIPERÎncă nu există evaluări
- Cursuri Lucrare 1Document54 paginiCursuri Lucrare 1Opris AlexandruÎncă nu există evaluări
- Mihai Eminescu - De-Or Trece Anii...Document1 paginăMihai Eminescu - De-Or Trece Anii...Opris AlexandruÎncă nu există evaluări
- Mihai Eminescu - DespartireDocument2 paginiMihai Eminescu - DespartirenenapsxÎncă nu există evaluări
- Mihai Eminescu - de Ce Nu-Mi Vii....Document2 paginiMihai Eminescu - de Ce Nu-Mi Vii....Opris AlexandruÎncă nu există evaluări
- Mihai Eminescu - Ce Te Legeni Codrule ....Document1 paginăMihai Eminescu - Ce Te Legeni Codrule ....Opris Alexandru100% (1)
- Mihai Eminescu - De-Or Trece Anii...Document1 paginăMihai Eminescu - De-Or Trece Anii...Opris AlexandruÎncă nu există evaluări
- Mihai Eminescu - de Cate Ori Iubito....Document1 paginăMihai Eminescu - de Cate Ori Iubito....Opris AlexandruÎncă nu există evaluări
- Mihai Eminescu - Craiasa Din PovestiDocument1 paginăMihai Eminescu - Craiasa Din PovestiOpris AlexandruÎncă nu există evaluări
- Povestea Lui Harap Alb - RezumatDocument1 paginăPovestea Lui Harap Alb - RezumatOpris AlexandruÎncă nu există evaluări
- La Argeş - Mateiu Ion CaragialeDocument1 paginăLa Argeş - Mateiu Ion CaragialeOpris AlexandruÎncă nu există evaluări
- Vasile Alecsandri - StelutaDocument2 paginiVasile Alecsandri - Stelutageraldine mouseÎncă nu există evaluări
- Mihai Eminescu - Atat de FragedaDocument2 paginiMihai Eminescu - Atat de FragedaOpris AlexandruÎncă nu există evaluări
- Arghezi Flori de MucigaiDocument1 paginăArghezi Flori de Mucigaimalone6x6Încă nu există evaluări
- Grădinele Amăgirii - Mateiu Ion CaragialeDocument1 paginăGrădinele Amăgirii - Mateiu Ion CaragialeOpris AlexandruÎncă nu există evaluări
- Luceafarul de M. EminescuDocument2 paginiLuceafarul de M. EminescuAlex PascariuÎncă nu există evaluări
- Aplicatii Bazele TermodinamiciiDocument7 paginiAplicatii Bazele TermodinamiciiAlin WhiskeyÎncă nu există evaluări
- George Cosbuc - Noi Vrem PamantDocument2 paginiGeorge Cosbuc - Noi Vrem PamantOpris AlexandruÎncă nu există evaluări
- Arghezi Flori de MucigaiDocument1 paginăArghezi Flori de Mucigaimalone6x6Încă nu există evaluări
- Mihai Eminescu - Ce Te Legeni CodruleDocument1 paginăMihai Eminescu - Ce Te Legeni CodruleOpris AlexandruÎncă nu există evaluări
- Carte Catia v5 Exemple PracticeDocument72 paginiCarte Catia v5 Exemple PracticeClaudiu Class75% (4)
- FA1Document38 paginiFA1Andreea Diana UngureanuÎncă nu există evaluări
- Transformari de Stare, Diagrame PV, Ts - TermotehnicaDocument14 paginiTransformari de Stare, Diagrame PV, Ts - TermotehnicaOpris AlexandruÎncă nu există evaluări
- MAE Transformatorul2014Document60 paginiMAE Transformatorul2014George SorinÎncă nu există evaluări
- Fa3 PDFDocument20 paginiFa3 PDFOpris AlexandruÎncă nu există evaluări
- Fa5 PDFDocument16 paginiFa5 PDFOpris AlexandruÎncă nu există evaluări
- FA2Document16 paginiFA2OnelIulianÎncă nu există evaluări
- Fa4 PDFDocument12 paginiFa4 PDFOpris AlexandruÎncă nu există evaluări
- Fa6 PDFDocument8 paginiFa6 PDFOpris AlexandruÎncă nu există evaluări
- Fisa de InscriereDocument1 paginăFisa de InscriereOpris AlexandruÎncă nu există evaluări