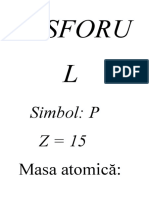Documente Academic
Documente Profesional
Documente Cultură
Fosforul Final
Încărcat de
petreionutz87Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Fosforul Final
Încărcat de
petreionutz87Drepturi de autor:
Formate disponibile
FOSFORUL
Structura fosforului : Simbolul fosforului este : P ; Z=15 ; Masa atomica : 30,974 Pe baza interpretarii mechanic-cautice a datelor microscopice, atomul neutru de fosfor are urmatoarea configuratie electronica : 1s22s22p63s23p3. Se cunosc dou forme alotropice extreme ale fosforului: fosforul alb i fosforul negru i, ntre acestea, formele intermediare fosforul violet, fosforul rou i fosforul rou deschis. Forma cea mai srac n energie, deci cea mai stabil, este fosforul negru. ntre diferitele forme alotropice ale fosforului nu exist puncte de transformare reversibil (ca la sulf) ; raportul dintre ele este deci cel al monotropiei.
Stare natural Fosforul se gsete in natura numai sub forma de ioni de fosfat, PO4,cea mai stabil combinaie a acestui element. Principalul mineral coninnd fosfor, format la solidificarea scoarei pmntului, este apatita, care poate fi considerat ca o soluie solid de fosfat de calciu, dar este n realitate un compus cristalizat, format din ioni de Ca2+, PO43- i F-, corespunznd formulei brute: Ca5[(PO4)3F].
Prin aciunea lent a agenilor atmosferici (CO 2 i H2O) apatita se transform n fosforite. Acestea sunt mult mai rspndite, n concentraii mici, n solul cultivabil al pdurilor i au o mare importan pentru viaa plantelor. Se gsesc n puine locuri pe glob i zcminte mari, exploatabile, de fosforite. Fosforitele (considerate nainte, n mod eronat, ca fosfat tricalcic) sunt n realitate amestecuri neomogene de hidroxil-apatit, Ca5[(PO4)3OH] i carbonat-apatit, Ca10[(PO4)6CO3](H2O). Partea anorganic a oaselor vertebratelor este un amestec de mult hidroxil-apatit cu puin carbonat-apatit.
Stare naturala : Fosforul nu exista liber in natura datorita afinitatii sale pentru oxigen dar exista un numar mare de fosfati. Fosforul considerat inainte ca un difosfat tricalcic, Ca3(PO4)2 este un amestec de hidrohil-apatita Ca3(PO4)2 * Ca(PO)2 si carbonato-apatita. Are culoarea cenusie, galbuie sau uneori neagra care indica prezenta substantelor bituminoase. Cel mai important mineral fiind apatita. Exista un numar foarte mare de zacaminte fosfatice calcaroase in Suedia , Norvegia , Australia , Ungaria , Belgia , Franta , Spania, U.R.S.S , S.U.A , Peru , Algeria , Tunisia, Maroc si Oceania. Fosfatii naturali se clasifica in 3 categorii : fosforiti adica fosfati impuri de origine minerala, de compozitie apropiata de a apatitei, guoanoul, care provine din putrefactiile dejectiilor si a cadavrelor pasarilor marine care contin fosfat de calciu , de magneziu si acid oxalic si caprolitele de origine animala provenite din excrementele unor reptile. Recoltele successive saracacesc solul. Din pacate fosforul trece la animale si la om. Acidul fosforic se gaseste in roci in cantitate mica. In cuptoarele inalte fosforul pus in libertate modifica proprietatile produselor.
Prepararea fosforului : Fosforul se obtine numai industrial din oasele animalelor sau din fosfati minerali. Procesul K.W. Scheele sau a lui J.Pelletier : prin acest process al chimistilor francezi se poate distinge oseina avand oasele la rosu viu. Cenusa amestecata cu apa se trateaza cu acid sulfuric. Lichidul care se evaporeaza la consistenta siropoasa este amestecata cu carabine si calciu moderat pentru a transforma difosfatul tetrahidracalcic in dimentafosfat de calciu care este redus la rosu. Distilarea fosforului incepe la 7500 si se termina la 12000C iar vaporii care se obtin se condenseaza in apa. Proprietati fizice : Fosforul in stare solida este incolor , transparent, acid si moale. Prin sublimare din solutii de sulfura de carbon fosforul se depune in stare cristalina. Fosforul este aproape insolubil in apa si alcool si putin solubil in glicerina, acid acetic, mai solubil in eter si foarte solubil in disulfura de carbon. Cu razele X s-a confirmat faptul ca la temperatura obisnuita el cristalizeaza in sistemul cubic. Fosforul alb se topeste intre44 si 44,20C iar densitatea lichidului fiind de 1,745 la 440 si 1,4850 la temperatura de fierbere. La temperatura camerei , presiunea de vapori este mare, motiv pentru care poate fi usor distilat la 1000C cu vapori de apa.
Proprietati chimice : Reactia fosforului cu metalele si nemetalele conduce la patru tipuri de compusi: 1. Fosfine volatile. Acestea sunt compusi de tip molecular. 2. Fosfine ionice. Acest tip de fosfine se formeaza cu metalele alkaline, alcalino-pamantoase. 3. Fosfine covalente. 4. Fosfine de tip metallic. Acesta prezinta duritate, luciu metalic, insolubil in apa, conductibilitate electrica. Fosforul alb reactoneaza cu aproape toate nemetalele. Deoarece se oxideaza foarte usor, fosforul se taie la apa. Fosforul arde in oxygen lent sau aprinzanduse la circa 450C. In exces de fosfor se formeaza pentaoxide de difosfor. Fosforul alb se combina lent cu sulful la temperatura ordinara, violent de cald si explozibil la temperatura mai inalta. Fosforul alb se combina cu majoritatea metalelor. Incalzit pe o placa de platina o strapunge din cauza formarii unor fosfuri solubile. Aurul si argintul absorb vaporii de fosfor sub punctul lor de topire si ii cedeazala racier producand fenomenul rosaj la solidificare. O bagheta de fosfor alb introdusa intr-o solutie de sulfat de cupru , acopera rapid cu un strat rosu de cupru metalic. Fosforul reduce o solutie de azotat de argint. Cu acidul clorhidric la 2000C formeaza , in tub uscat hidrogenul fosforat de azotat de argint. Cu acidul clorhidric la 2000C formeaza, in tub uscat hidrogenul fosforat iar cu acizii bronhidrici si iodhidrici, saruri de fosfoniu. Utilizari :
S-ar putea să vă placă și
- FosfOr (76543464567)Document9 paginiFosfOr (76543464567)Dumitru BuzduganÎncă nu există evaluări
- FosforDocument15 paginiFosforAlexandra CismasÎncă nu există evaluări
- FOSFORULDocument6 paginiFOSFORULvioletabadanÎncă nu există evaluări
- FosforulDocument6 paginiFosforultobi92100% (3)
- Acidul FosforicDocument9 paginiAcidul Fosforicdiana fenichiuÎncă nu există evaluări
- Fosforul PDocument19 paginiFosforul PEne Violeta Alina100% (1)
- FosforulDocument7 paginiFosforulRoxana Axinte100% (1)
- Pentaoxid de FosforDocument7 paginiPentaoxid de FosforAna-Maria TurcuÎncă nu există evaluări
- Fosforul PDocument12 paginiFosforul Pnicucazacu0% (1)
- FosforulDocument2 paginiFosforulNicholas Owens67% (3)
- Oxizii Şi Oxiacizii FosforuluiDocument6 paginiOxizii Şi Oxiacizii FosforuluiIoanaToader100% (1)
- FosforulDocument1 paginăFosforulEleonoreKtrÎncă nu există evaluări
- Forme de Fosfor in Sol Si Accesibilitatea AgrochimieDocument2 paginiForme de Fosfor in Sol Si Accesibilitatea AgrochimieMonica DamocÎncă nu există evaluări
- Referat FosforulDocument4 paginiReferat FosforulAnaMariaÎncă nu există evaluări
- Chimie Grupa 5Document11 paginiChimie Grupa 5just meÎncă nu există evaluări
- AGROCHIMIE 11 Ing Chim Cu FosforDocument2 paginiAGROCHIMIE 11 Ing Chim Cu FosforoanaÎncă nu există evaluări
- Note 2Document2 paginiNote 2Daniel MogildeaÎncă nu există evaluări
- Chimie 4Document3 paginiChimie 4Adam SmithÎncă nu există evaluări
- FluorulDocument5 paginiFluorulSorina M. TeiusanuÎncă nu există evaluări
- ChibritulDocument8 paginiChibritulCatalinaÎncă nu există evaluări
- FosforulDocument3 paginiFosforulAlex GramaÎncă nu există evaluări
- C6-Chimie Anorganica - GR 15Document38 paginiC6-Chimie Anorganica - GR 15dia_didu_14Încă nu există evaluări
- ChibritulDocument8 paginiChibritulCatalinaÎncă nu există evaluări
- Ingrasaminte Cu Fosfor Usor Solubile in Apa.Document5 paginiIngrasaminte Cu Fosfor Usor Solubile in Apa.No BodyÎncă nu există evaluări
- FOSFORDocument4 paginiFOSFORdianaionelav23Încă nu există evaluări
- Fosforul ReferatDocument20 paginiFosforul ReferatArdelean LiudmilaÎncă nu există evaluări
- FluorulDocument12 paginiFluorulAndreea DemianÎncă nu există evaluări
- Radicali AnorganiciDocument23 paginiRadicali AnorganiciAndreiu Vlad ValentinaÎncă nu există evaluări
- Acid FosforicDocument4 paginiAcid FosforicLorry Ank100% (2)
- FosforDocument11 paginiFosforCris QualityÎncă nu există evaluări
- Fosfor ChimieDocument11 paginiFosfor ChimieGabriel RusuÎncă nu există evaluări
- HALOGENURIDocument6 paginiHALOGENURIScott HowellÎncă nu există evaluări
- Determinarea Fosforului Din ApaDocument1 paginăDeterminarea Fosforului Din ApaDan DascalitaÎncă nu există evaluări
- HalogeniiDocument10 paginiHalogeniiAnca-Alina BujenitaÎncă nu există evaluări
- Circuitul Fosforului in NaturaDocument6 paginiCircuitul Fosforului in NaturaAnca Elena100% (1)
- FenoliDocument32 paginiFenoliadinaprsÎncă nu există evaluări
- FluorulDocument4 paginiFluorulcatikakiÎncă nu există evaluări
- Iodul: DescoperireDocument7 paginiIodul: DescoperireDan Mihai SlăvoiuÎncă nu există evaluări
- Ciornei ElenaDocument16 paginiCiornei ElenaAdriana TicsaÎncă nu există evaluări
- Obtinerea Oxidului Mixt de Fier 1Document4 paginiObtinerea Oxidului Mixt de Fier 1Indira MustafaÎncă nu există evaluări
- Ciclul Azotului Si SulfuluiDocument7 paginiCiclul Azotului Si SulfuluiCosti PaunescuÎncă nu există evaluări
- PotasiulDocument4 paginiPotasiulAndreea CatalinaÎncă nu există evaluări
- Sinteza Orange IIDocument16 paginiSinteza Orange IIElena DiculescuÎncă nu există evaluări
- Fisă de Lucru FosforulDocument1 paginăFisă de Lucru FosforulAlina BugaÎncă nu există evaluări
- FerulDocument20 paginiFerulMarianaCiocîrlanÎncă nu există evaluări
- Chimie Organica CursDocument35 paginiChimie Organica CursRoxana AlinaÎncă nu există evaluări
- StronţiuDocument3 paginiStronţiuAlina MalaiÎncă nu există evaluări
- Compusi Cu SulfDocument11 paginiCompusi Cu SulfRogue AndreeaÎncă nu există evaluări
- Indicatori Fizico-ChimiciDocument5 paginiIndicatori Fizico-ChimiciMarcel Daniel PopaÎncă nu există evaluări
- Curs 9-10.doc - 0.odtDocument5 paginiCurs 9-10.doc - 0.odtmariaÎncă nu există evaluări
- Curs 9 P As SB BiDocument14 paginiCurs 9 P As SB BiMadalina RusuÎncă nu există evaluări
- Proiect ArsenicDocument9 paginiProiect ArsenicFlorentin AlexÎncă nu există evaluări
- IDENTIFICAREA IONULUI Fe3+Document14 paginiIDENTIFICAREA IONULUI Fe3+RobertLărgeanuÎncă nu există evaluări
- SULFDocument20 paginiSULFGeorgeta Marioara100% (1)
- HalogeniiDocument4 paginiHalogeniiAdy Brudariu100% (1)
- IodDocument8 paginiIodAdy BrudariuÎncă nu există evaluări
- Sablon Deviz Lucrare Regie ProprieDocument1 paginăSablon Deviz Lucrare Regie Propriepetreionutz8725% (4)
- Planul CalendaristicDocument5 paginiPlanul Calendaristicpetreionutz87Încă nu există evaluări
- Planul Calendaristic I-IIDocument8 paginiPlanul Calendaristic I-IIpetreionutz87Încă nu există evaluări
- Delirium TremensDocument5 paginiDelirium TremensIonut PetreÎncă nu există evaluări