Documente Academic
Documente Profesional
Documente Cultură
MARIA-PARASCHIVA FELDEREAN - FISA - VARIATIA CARACTERULUI METALIC - Exp
Încărcat de
CristyGMTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
MARIA-PARASCHIVA FELDEREAN - FISA - VARIATIA CARACTERULUI METALIC - Exp
Încărcat de
CristyGMDrepturi de autor:
Formate disponibile
VARIAŢIA CARACTERULUI METALIC ÎN PERIOADĂ
1. Completați spațiile punctate din coloana cu Observații. (Ștergeți punctele pentru a avea loc să scrieți.)
2. Ștergeți cuvintele scrise cu culoare roșie și font italic (înclinat) din coloana cu Observații, conform observațiilor din experimente.
Ecuaţiile reacţiilor chimice
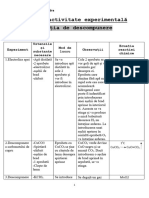
Experimentul Reactivi şi ustensile Modul de lucru Concluzii
Observaţii
Lăsat în aer, Na,
Atenţie! Priviţi de la distanţă! Particulele 2Na +O2 Na2O2 reacţionează uşor / nu
Na peroxid de Na reacţionează cu O2.
incandescente de Na produc arsuri.
A. Reacţia dintre sticlă de ceas
Tăiaţi o bucată mică de Na, o curăţaţi de stratul de
Na şi O2 hârtie de filtru oxid, o ştergeţi de petrol şi o aşezaţi pe hârtie. Na se păstrează sub petrol
lingură de ars Luciul metalic dispare
Observați aspectul sodiului în tăietură proaspătă. ……………………….. pentru a nu veni în contact cu
oxigenul.
Prindeţi o bucată de magneziu într-un cleşte de metal 2 Mg + O2 2 MgO
B. Reacţia dintre Mg şi încălziţi-o în flacăra unui bec de gaz. După Mg reacţionează cu O2 la
Mg şi O2 cleşte de fier aprindere, o scoateţi din flacără şi urmăriţi cum arde. Mg arde cu o flacără ................. încălzire / la rece.
Observaţi substanţa rezultată. Rezultă un praf .............. de MgO
C. Reacţia dintre pulbere de În flacăra albastră a unui bec de gaz, presăraţi cu 4 Al + 3 O2 2 Al2O3
Al reacţionează cu O2 numai fin
Al şi O2 Al ajutorul unei spatule pulbere de aluminiu. Observaţi
divizat / în bucată mare.
spatulă fenomenul. Pulberea de Al se ………………
Concluzie: reactivitatea față de O2.creşte în ordinea:…………………………………………………..
2 Na + 2 H2O 2 NaOH + H2
Na Atenţie! Se priveşte de la distanţă. Na se
Bobiţa de Na Na reacţionează greu /
soluţie poate aprinde.
energic cu apa.
alcoolică de Tăiaţi o bucată mică de Na, o curăţaţi de stratul de ………………………. pe
D. Reacţia dintre
fenolftaleină oxid şi o ştergeţi de petrol pe o hârtie de filtru.
Na şi H2O suprafaţa apei.
cristalizor Introduceţi bucata de Na într-un cristalizor cu apă,
NaOH este o bază slabă /
pâlnie de în care aţi pus câteva picături de soluţie de Se degajă un gaz ……………
tare.
sticlă fenolftaleină. Soluţia se colorează în …....... ,
datorită formării de NaOH.
Mg + H2O Mg(OH)2 + H2
Mg Mg reacţionează cu apa, la
· soluţie Într-o eprubetă, puneţi puţină apă, câteva picături La fierbere, de pe suprafaţa rece / la încălzire.
E. Reacţia dintre alcoolică de de soluţie de fenolftaleină şi panglică de Mg. Mg, se degajă bule de ..........
Mg şi H2O fenolftaleină Încălziţi până la fierbere. Observaţi fenomenul. Soluţia se colorează Mg(OH)2 este o bază slabă /
eprubetă în……………..datorită tare
formării ............................
Al nu reacționează
Într-un pahar puneți bucăți sau folie de Al și /reacționează cu apa. Al este
F. Reacţia dintre câteva picături de fenolftaleină. Puneți paharul pe Soluția rămâne ……….. protejat de stratul de Al2O3,
Al şi H2O
o sită de azbest și încălziți până la fierbere. insolubil în apă. În vase de Al
se poate fierbe apă.
Concluzie: : reactivitatea față de H2O creşte în ordinea:…………………………………………………..
VARIAȚIA CARACTERULUI CHIMIC ÎN TABELUL PERIODIC
3. Aranjați în ordinea descrescătoare a caracterului metalic (electropozitiv) elementele din seria: Al, Mg, Na.
4. Aranjați în ordinea crescătoare a caracterului metalic (electropozitiv) elementele din seria: Na, Li, Cs, K.
5. Aranjați în ordinea crescătoare a caracterului nemetalic (electronegativ) elementele din seria: Cl, F, I, Br.
6. Aranjați în ordinea descrescătoare a caracterului nemetalic (electronegativ) elementele din seria: S, Cl, P.
3.
4.
5.
6.
S-ar putea să vă placă și
- Cls 9 Lucrare 1Document3 paginiCls 9 Lucrare 1radus_3Încă nu există evaluări
- Caracterul Metalic Activitate ExperimentalaDocument1 paginăCaracterul Metalic Activitate Experimentalaender8421Încă nu există evaluări
- Cls 9 Lucrare 1Document3 paginiCls 9 Lucrare 1Naomi Mihai0% (1)
- Activitate Experimentala Caracter MetalicDocument2 paginiActivitate Experimentala Caracter MetalicDaniel CrapellaÎncă nu există evaluări
- Fisa Lucru Caracter MetalicDocument2 paginiFisa Lucru Caracter MetalicCatalina StefanovÎncă nu există evaluări
- Fisa ExperimentalaDocument2 paginiFisa ExperimentalaAlina CotleţÎncă nu există evaluări
- Experimente ChimieDocument6 paginiExperimente ChimieEddy HolidayÎncă nu există evaluări
- Acidul AzoticDocument5 paginiAcidul AzoticKingGeorgeVIIÎncă nu există evaluări
- Subiecte + Bareme Concursul National de Chimie C. D. Nenitescu, Proba Practica de Chimie AnorganicaDocument4 paginiSubiecte + Bareme Concursul National de Chimie C. D. Nenitescu, Proba Practica de Chimie AnorganicaChemmonÎncă nu există evaluări
- Proprietatile Acidului Acetic Si ObtinereaDocument3 paginiProprietatile Acidului Acetic Si ObtinereaRotariSergiuÎncă nu există evaluări
- 14 Compuşi Organici Cu AzotDocument20 pagini14 Compuşi Organici Cu AzotOvy NitaÎncă nu există evaluări
- Hidrogenul. Proprietăţi. Metode de Preparare 1. Stare NaturalăDocument15 paginiHidrogenul. Proprietăţi. Metode de Preparare 1. Stare NaturalăIoana PauceanÎncă nu există evaluări
- Fisa de Activitate Experimentalaelectrolizametoda de Obtinere A Metalelor Si NemetalelorDocument1 paginăFisa de Activitate Experimentalaelectrolizametoda de Obtinere A Metalelor Si NemetalelorCornelia BeliciuÎncă nu există evaluări
- Proiect SodiuDocument5 paginiProiect Sodiualex7.soareÎncă nu există evaluări
- Reactivi: Ustensile:: Cuso, CusoDocument2 paginiReactivi: Ustensile:: Cuso, CusoOlga RabeiÎncă nu există evaluări
- Reacția de ÎnlocuireDocument2 paginiReacția de ÎnlocuireMinaila OanaÎncă nu există evaluări
- Proprietatile Chimice Ale SodiuluiDocument2 paginiProprietatile Chimice Ale SodiuluiEliza TodorÎncă nu există evaluări
- Lucrare Practica Chimie Cazacu DragosDocument9 paginiLucrare Practica Chimie Cazacu DragosDragos CazacuÎncă nu există evaluări
- !reactii de Identificare A CationilorDocument19 pagini!reactii de Identificare A CationilorMilianno0% (4)
- Calcule Pe Baza Formulelor ChimiceDocument3 paginiCalcule Pe Baza Formulelor ChimiceNitulescu AndreeaÎncă nu există evaluări
- Cation IDocument17 paginiCation IDorina BuimistruÎncă nu există evaluări
- Fisa Activitati - D-1Document5 paginiFisa Activitati - D-1Alexandra MariaÎncă nu există evaluări
- Apa Oxigenată - LaboratorDocument2 paginiApa Oxigenată - LaboratorDediu AnişoaraÎncă nu există evaluări
- Lucrare PracticăDocument4 paginiLucrare PracticăLaurentia Grati100% (1)
- Reacția de CombinareDocument2 paginiReacția de CombinareMinaila OanaÎncă nu există evaluări
- OL22 Chimi Barem Soluții 10 RoDocument6 paginiOL22 Chimi Barem Soluții 10 Rovaleria duschinÎncă nu există evaluări
- Reactia de DescompunereDocument2 paginiReactia de DescompunereMinaila OanaÎncă nu există evaluări
- II. Azot Fosfor Arsen Carbon Siliciu BorDocument43 paginiII. Azot Fosfor Arsen Carbon Siliciu BorIsabela Gavrilei0% (1)
- AzotDocument3 paginiAzotUngurianu AndiÎncă nu există evaluări
- Lucrare de Laborator Azot - Compusii AzotuluiDocument3 paginiLucrare de Laborator Azot - Compusii AzotuluiGheorghe GutuÎncă nu există evaluări
- CL 9 Lucrare de Laborator NR 1Document4 paginiCL 9 Lucrare de Laborator NR 1Dragos CazacuÎncă nu există evaluări
- LP 7 Anul IV StudentiDocument33 paginiLP 7 Anul IV StudentiMihai CalinÎncă nu există evaluări
- Chimie FarmaceuticaDocument10 paginiChimie Farmaceuticaili_eÎncă nu există evaluări
- Obținerea EteneiDocument3 paginiObținerea EteneiRotariSergiuÎncă nu există evaluări
- Lucrarea 1 Ag + PBDocument3 paginiLucrarea 1 Ag + PBFlorina GeorgianaÎncă nu există evaluări
- Chim. Anorg. Laborator CaietDocument36 paginiChim. Anorg. Laborator Caietnicoleta turcanuÎncă nu există evaluări
- ChinalfinalDocument5 paginiChinalfinalMariana RoşcaÎncă nu există evaluări
- Chimia Analitică Studiul 3Document6 paginiChimia Analitică Studiul 3Mihaela DidencuÎncă nu există evaluări
- Proiectdelec Ie Acizi CozmaDocument7 paginiProiectdelec Ie Acizi Cozmamirela borcauÎncă nu există evaluări
- Wa0013.Document14 paginiWa0013.galcarolina722202Încă nu există evaluări
- EP6.0 02 81.enDocument3 paginiEP6.0 02 81.enAlexandra CociuÎncă nu există evaluări
- Caiet HalogenDocument11 paginiCaiet HalogenAna CecansciucÎncă nu există evaluări
- Apa OxigenatăDocument6 paginiApa OxigenatădanstfÎncă nu există evaluări
- Combinatiile Metalelor AlcalineDocument5 paginiCombinatiile Metalelor AlcalineTudor VataÎncă nu există evaluări
- OxigenulDocument10 paginiOxigenulMaria TodircanÎncă nu există evaluări
- Chimie Farmaceutica An III Sem 2 - LP 8Document26 paginiChimie Farmaceutica An III Sem 2 - LP 8Cristina ElenaÎncă nu există evaluări
- Chimia AnorganicaDocument21 paginiChimia AnorganicaNatashka100% (1)
- Identificarea CationilorDocument27 paginiIdentificarea CationilorBanica Marian Valentin67% (3)
- Proprietățile Chimice Generale Ale AcizilorDocument2 paginiProprietățile Chimice Generale Ale AcizilorRotariSergiuÎncă nu există evaluări
- 02 HidrogenulDocument5 pagini02 HidrogenulAlin CamarăÎncă nu există evaluări
- Chimie AlimentaraDocument5 paginiChimie AlimentaraAlex FilÎncă nu există evaluări
- HidroxiziDocument10 paginiHidroxizidana zbrancaÎncă nu există evaluări
- Baze FinalDocument10 paginiBaze FinalCornelia DingaÎncă nu există evaluări
- Chimia Nemetalelor L1 Hidrogenul 2021Document9 paginiChimia Nemetalelor L1 Hidrogenul 2021Lidia GogaÎncă nu există evaluări
- Laborator 5 OrganicaDocument6 paginiLaborator 5 OrganicaElena GheorghițăÎncă nu există evaluări
- IODOMETRIADocument4 paginiIODOMETRIAAdelina SimonÎncă nu există evaluări
- Harta ValorilorDocument7 paginiHarta ValorilorCristyGM100% (1)
- Aplicatie Practica in WordDocument2 paginiAplicatie Practica in WordCristyGMÎncă nu există evaluări
- De Ce Sunt Importante TezeleDocument3 paginiDe Ce Sunt Importante TezeleCristyGMÎncă nu există evaluări
- ProcesorulDocument6 paginiProcesorulCristyGMÎncă nu există evaluări
- Monarhia EgipteanaDocument2 paginiMonarhia EgipteanaCristyGMÎncă nu există evaluări