Documente Academic
Documente Profesional
Documente Cultură
Cancerul Esofagian
Încărcat de
valcovemiTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Cancerul Esofagian
Încărcat de
valcovemiDrepturi de autor:
Formate disponibile
Tabel I.
Factori de risc pentru cancerul esofagian (9 factori)
Factor Comentarii
Vârsta Riscul creşte cu vârsta.
Rasa Adenocarcinomul este mai frecvent la rasa albă.
Sexul Adenocarcinomul şi carcinomul scuamos esofagian sunt mai frecvente la sexul masculin.
Consumul de alcool/fumatul Reprezintă principalii factori de risc pentru carcinomul scuamos.
Dieta Incriminate:
- deficitele vitaminice (A, C, E, B2, B12, acid folic);
- dieta bogată în carbohidraţi, grăsimi, colesterol şi săracă în legume şi fructe proaspete;
- aportul crescut de nitraţi/nitrozamine.
Obezitatea (IMC > 30) Se asociază cu adenocarcinomul esofagian.
Genetica Afecţiuni asociate cu carcinomul scuamos: tilosis, sindromul Plummer-Vinson.
Afecţiuni dobândite Acalazia netratată, stenozele post-caustice se asociază cu un risc crescut de
dezvoltare a carcinomului scuamos.
Sindromul Barrett Asociat cu incidenţa crescută a adenocarcinomului esofagian.
3. Diagnostic și stadializare
Diagnosticul cancerului esofagian este fundamentat pe urmă toarele
metode: 1) anamneză şi examen clinic, 2) examen radiologic (clasic şi tomografie
computerizată) şi 3) endoscopie digestivă cu prelevare de biopsii/examen citologic
şi ecoendoscopie. Diagnosticul de certitudine al carcinomului esofagian se
stabileşte prin endoscopie digestivă şi examen histopatologic. În raport cu invazia
parietală şi prezenţa metastazelor ganglionare regionale, cancerul esofagian se
subclasifică în precoce şi local avansat; cele 2 forme diferă din punct de vedere
terapeutic şi prognostic. Cancerul esofagian precoce este definit histologic ca
fiind limitat la mucoasă (cel mult T1a), fă ră metastaze ganglionare. Cancerul
esofagian local avansat este cancerul care, indiferent de stadiul T, are metastaze
ganglionare, dar nu prezintă metastaze la distanță .
3. Diagnostic și stadializare (mov)
Diagnosticul cancerului esofagian este fundamentat pe urmă toarele
metode: 1) anamneză şi examen clinic, 2) examen radiologic (clasic şi tomografie
computerizată) şi 3) endoscopie digestivă cu prelevare de biopsii/examen citologic
şi ecoendoscopie. Diagnosticul de certitudine al carcinomului esofagian se
stabileşte prin endoscopie digestivă şi examen histopatologic. În raport cu invazia
parietală şi prezenţa metastazelor ganglionare regionale, cancerul esofagian se
subclasifică în precoce şi local avansat; cele 2 forme diferă din punct de vedere
terapeutic şi prognostic. Cancerul esofagian precoce este definit histologic ca
fiind limitat la mucoasă (cel mult T1a), fă ră metastaze ganglionare. Cancerul
esofagian local avansat este cancerul care, indiferent de stadiul T, are metastaze
ganglionare, dar nu prezintă metastaze la distanță .
3.1. Anamneză şi examen clinic
Cancerul esofagian precoce este, în general, asimptomatic, iar diagnosticul
acestuia în afara programelor de screening şi supraveghere este rar. Rareori,
leziunile ulcerate pot determina hemoragie digestivă . Disfagia este întâ lnită la
peste 90% din pacienţii simptomatici şi denotă , de regulă , prezenţa cancerului
esofagian avansat. Disfagia asociată cancerului esofagian are caracter progresiv,
fiind semnalată iniţial la alimente solide, ulterior la semisolide şi lichide. Odinofagia
(deglutiţia dureroasă ) este întâ lnită la aproximativ 50% dintre pacienţi, iar
anorexia şi scă derea ponderală sunt prezente în aproximativ 75% din cazuri. O
serie de simptome se asociază cu invazia tumorală extraesofagiană sau cu prezenţa
metastazelor la distanţă : durerea retrosternală sau iradierea dorsală a
acesteia sugerează invazia mediastinală ; tusea indică apariţia unei fistule esotraheo-
bronşice sau a pneumoniei de aspiraţie; disfonia se asociază cu afectarea
nervului laringian recurent, iar durerile osoase cu prezenţa metastazelor osoase.
Examenul fizic poate evidenţia adenopatii latero-cervicale sau supraclaviculare,
hepatomegalie, caşexie.
3.2. Examen radiologic
Examenul radiologic baritat reprezintă metoda iniţială de evaluare a
orică rui pacient cu disfagie. El poate releva anomalii de contur şi motilitate
esofagiană datorate stenozelor sau acalasiei, precum şi prezenţa fistulelor esotraheale/
eso-bronşice. Cancerul esofagian precoce se caracterizează din punct de
vedere radiologic printr-un aspect granular al mucoasei, prezenţa de ulceraţii
unice sau multiple asociate cu mici defecte de umplere. Cancerul esofagian local
avansat poate avea aspect polipoid, infiltrativ sau ulcerat sau se poate prezenta
printr-un aspect radiologic combinat al acestor tipuri de leziuni (Figura 3). În
diagnosticul cancerului esofagian, examenul radiologic standard tinde a fi înlocuit
de endoscopia digestivă superioară , el ră mâ nâ nd însă destinat pentru cazuri selecţionate
(stenoze maligne care nu pot fi depă şite endoscopic, fistule eso-bronşice
sau eso-traheale). Tomografia computerizată (CT) toracică și abdominală este
indicată pentru detecţia metastazelor și pentru extensia periesofagiană , mai ales
în localiză rile medio-esofagiene. Pentru detecția metastazelor, poate fi indicat și PET-CT.
3.3. Endoscopia cu prelevare de biopsii/citologie.
Ecoendoscopia. Bronhoscopia
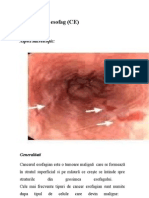
Endoscopia este metoda preferată de diagnostic a cancerului esofagian precoce sau avansat.
Examenul endoscopic poate evidenţia leziuni polipoid-vegetante, ulcerate, infiltrativ-stenozante
sau combinaţii ale acestora . Metoda permite prelevarea de biopsii ţintite din leziunile detectate
endoscopic.
Se recomandă prelevarea de 6-8 biopsii pentru diagnostic histologic, inclusiv
imunohistochimie și diagnostic molecular.
În prezenţa stenozelor care nu pot fi traversate endoscopic, diagnosticul
este posibil prin examen citologic efectuat cu ajutorul periuţei de citologie.
Pentru diagnosticul cancerului esofagian precoce poate fi utilizată coloraţia
intravitală cu soluţie Lugol ce colorează mucoasa esofagiană normală în brun,
facilitâ nd prelevarea ţintită a biopsiilor din ariile de mucoasă anormal colorată
(galben-roşiatic) (Figura 11). Ecoendoscopia (EUS) este considerată cea mai bună
metodă pentru stadializarea invaziei tumorale (T din clasificarea TNM) şi este
mai puţin fidelă pentru stadializarea afectă rii ganglionare (N din clasificarea
TNM). Acurateţea globală pentru stadiul T este de 90%, iar pentru stadiul N
de 85%. Acurateţea cea mai bună se înregistrează în cazul stadiilor T3 şi T4
(Figura 12) şi mai redusă în cazul stadiului T1-T2. Biopsia cu ac fin ghidată EUS
în adenopatiile cu caracteristici maligne creşte acurateţea stadializă rii N. Bronhoscopia
este indicată în unele cancere de esofag superior sau mijlociu pentru a
exclude invazia traheobronșică .
4. Diagnostic diferențial (mov)
Diagnosticul diferențial se poate face cu alte tumori epiteliale benigne sau
maline (papilomul scuamos, melanomul, tumori neuroendocrine) sau tumori nonepiteliale
benigne (leiomiomul, tumoră cu celule granulare, polip fibrovascular,
hemangiom, limfangiom, lipom, fibrom) sau maligne (sarcom, limfom, carcinom
metastatic). În general, endoscopia cu biopsie stabilește diagnosticul.
6. Screening şi supraveghere în cancerul esofagian (rosu)
Screeningul în masă al cancerului scuamos esofagian este justificat numai
în regiunile cu incidenţă crescută din nordul Chinei şi Iranului, India (peste 100
de cazuri la 100.000 loc.) şi se efectuează prin examen citologic. În celelalte arii
geografice, este indicată numai supravegherea endoscopică individuală a subiecţilor
cu risc crescut. Principalele condiţii cu risc crescut pentru carcinomul scuamos
esofagian sunt: fumatul a peste 25 de ţigă ri pe zi, asocierea dintre consumul
de alcool şi fumat, acalazia cu evoluţie îndelungată (peste 2 decade), tilosis,
cancere ale regiunii capului şi gâ tului, stenozele post-caustice după 4 decade de la
ingestia de substanţă caustică . Nu există o metodologie standardizată de supraveghere
cost-eficientă a acestor pacienţi pentru riscul apariţiei cancerului scuamos
esofagian, strategia recomandată constâ nd în examinarea endoscopică periodică
pe criterii individuale. Pacienţii cu esofag Barrett necesită supraveghere endoscopică
şi endobioptică la intervale adecvate, în raport cu prezenţa şi gradul displaziei.
Supravegherea esofagului Barrett este justificată de caracterul premalign al
afecţiunii pentru adenocarcinomul esofagian. Adenocarcinomul esofagian se dezvoltă
prin intermediul secvenţei metaplazie intestinală-displazie-adenocarcinom.
Obiectivul supravegherii endoscopic-endobioptice a esofagului Barrett constă în
detecţia displaziei ca leziune premalignă sau a adenocarcinomului esofagian în
stadii precoce. Deoarece displazia este o modificare focală , se recomandă prelearea
de biopsii multiple circumferenţial din 4 cadrane la fiecare 2 cm, pe toată
lungimea esofagului Barrett, precum şi din ariile ulcerate, nodulare sau stenozate.
Intervalele la care se recomandă efectuarea endoscopiei cu endobiopsii variază în
raport cu gradul displaziei (Tabel III).
Tabel III. Supravegherea esofagului Barrett în raport cu gradul displaziei
Barrett cu metaplazie intestinală, dar fără displazie = Endoscopie-endobiopsii (4 fragmente la interval 2 cm) la
interval 3-5 ani
Displazie blandă confirmată de doi anatomopatologi, dintre care unul specializat în patologie de tub digestiv =
Terapie endoscopică sau endoscopie-endobiopsie anual
Displazie severă confirmată de doi anatomopatologi, dintre care unul specializat în patologie de tub digestiv =
Terapie endoscopică sau/și chirurgicală
8.5. Terapia endoscopică
Terapia endoscopică în scop curativ este rezervată tumorilor esofagiene
superficiale. Acestea sunt tumori plane, limitate la mucoasă , fă ră invazia
submucoasei. Ecoendoscopia este utilă pentru stadializarea tumorii cu scopul
excluderii invaziei în submucoasă şi/sau prezenţei ganglionilor periesofagieni
tumorali. Este indicat ca terapia endoscopică să fie terapie de primă intenţie în
cancerul esofagian stadiul I. Carcinomul in situ reprezintă condiţia optimă de
rezecţie endoscopică . Dacă pe piesa de rezecţie endoscopică există o invazie
masivă submucoasă care nu a fost diagnosticată în prealabil sau dacă apare
recidiva, este indicat tratamentul chirurgical. Tehnicile endoscopice folosite în
scop curativ și indicate de ghidurile experților sunt rezecția endoscopică mucosală
(REM) și disecția endoscopică mucosală (DEM). Prin REM, tumora este rezecată
direct cu ajutorul unei anse de polipectomie sau iniţial este aspirată într-un dispozitiv
special de platic sau ligaturată şi apoi rezecată cu ansa de polipectomie. În
toate cazurile, rezecţia se efectuează după injectarea în prealabil în submucoasă a
unei mixturi de ser fiziologic cu adrenalină cu ridicarea leziunii în scopul unei
mai bune rezecţii şi evită rii perforaţiei. REM se poate efectua într-un singur fragment
dacă dimensiunea tumorii nu depă șește 15-20 mm în diametru. Mucosectomia
fragmentată se efectuează la tumori mai mari de 20 mm în diametru. DEM
este o tehnică prin care, după elevarea tumorii prin injecţie de ser fiziologic cu
adrenalină în submucoasă , se efecuează o tă iere circumferenţială a tumorii cu
anumite accesorii speciale şi apoi o disecţie treptată în submucoasă dintr-un capă t
într-altul, pâ nă la excizia completă într-un singur fragment. DEM este o rezecție
endoscopică mai profundă , oferind o piesă completă anatomopatologului în
scopul evaluă rii histologice și stadializă rii. Tehnica ablativă prin radiofrecvenţă
permite tratarea unor arii largi de mucoasă patologică ; este asociată terapiei de
rezecţie endoscopică a esofagului Barrett cu displazie.
Terapia endoscopică în scop paliativ
Montare endoscopică de gastrostomă : aplicarea pe cale endoscopică a
unei sonde la nivelul stomacului în scopul introducerii alimentelor semisolide
direct în stomac, cu scurt-circuitarea esofagului care este obstruat tumoral. Montarea
de proteze esofagiene: în caz de disfagie completă , se indică proteze esofagiene
expandabile la cei la care prognosticul de supravieţuire depă şeşte 6 luni. De
asemenea, proteza esofagiană metalică şi/sau traheobronşică este indicată în prezenţa
fistulei eso-bronşice.
S-ar putea să vă placă și
- C15 8. Adenocarcinom de JEGDocument46 paginiC15 8. Adenocarcinom de JEGNico Ionaşcu100% (1)
- Cancerul GastricDocument3 paginiCancerul GastricvalcovemiÎncă nu există evaluări
- Terapia Oncologica-Optiuni Bazate Pe Evidente-Cancerele DigDocument91 paginiTerapia Oncologica-Optiuni Bazate Pe Evidente-Cancerele DigAndra Birladeanu SurugiuÎncă nu există evaluări
- 7 Cancer Gastric 2018Document47 pagini7 Cancer Gastric 2018Hasan Diab100% (3)
- 4 Cancerul GastricDocument29 pagini4 Cancerul Gastricirynka19Încă nu există evaluări
- 035 Covalcic MDocument5 pagini035 Covalcic MIoana Cristina IonescuÎncă nu există evaluări
- Cancerul Gastric Carol DavilaDocument30 paginiCancerul Gastric Carol DavilaDenise DnsÎncă nu există evaluări
- Curs Cancer GastricDocument35 paginiCurs Cancer GastricSabina Marcu100% (3)
- Tumorile EsofaguluiDocument48 paginiTumorile EsofaguluiflamboyantyÎncă nu există evaluări
- Cancer GastricDocument38 paginiCancer GastricIrina PopoviciÎncă nu există evaluări
- Cancerul ColorectalDocument11 paginiCancerul ColorectalAriana SabăuÎncă nu există evaluări
- Tumori EsofagDocument47 paginiTumori EsofagDumitrita PetrasescuÎncă nu există evaluări
- Cancerul GastricDocument14 paginiCancerul GastricAna AlexandraÎncă nu există evaluări
- Cancerul GastricDocument6 paginiCancerul GastricHappy Friend100% (1)
- Cancerul Colo-Rectal Violeta VacariuDocument6 paginiCancerul Colo-Rectal Violeta VacariuSbarcea RaduÎncă nu există evaluări
- Tumori EsofagDocument47 paginiTumori EsofagAdÎncă nu există evaluări
- OncologieDocument96 paginiOncologielacramioraÎncă nu există evaluări
- OncologieDocument63 paginiOncologieVoicu DanielaÎncă nu există evaluări
- Colon - Referat 2Document33 paginiColon - Referat 2Ramona OanăÎncă nu există evaluări
- Cancerul EsofagianDocument29 paginiCancerul EsofagianMateas Szabi50% (2)
- 209 729 1 PB PDFDocument8 pagini209 729 1 PB PDFMarina CiobanuÎncă nu există evaluări
- Cancerul GastDocument6 paginiCancerul GastHorga LucianÎncă nu există evaluări
- Cancerul Esofagului - Docx ELEDocument17 paginiCancerul Esofagului - Docx ELESerban ElenaÎncă nu există evaluări
- Cancerul Gastric 2014Document31 paginiCancerul Gastric 2014Cosmina GheorgheÎncă nu există evaluări
- 2.cancer ColonDocument22 pagini2.cancer ColonEva FancyÎncă nu există evaluări
- Curs 8 Oncologie - GASTRICDocument34 paginiCurs 8 Oncologie - GASTRICIoana Monica Marinescu100% (1)
- Cancer GastricDocument5 paginiCancer GastricUngureanu OanaÎncă nu există evaluări
- Cancerul Gastric Medicina GeneralaDocument163 paginiCancerul Gastric Medicina GeneralabailescuiuliaÎncă nu există evaluări
- Cancerul EsofagianDocument25 paginiCancerul EsofagianFlorida Elena MitroiÎncă nu există evaluări
- Cancerul EsofagianDocument37 paginiCancerul EsofagianElena EllenaÎncă nu există evaluări
- 1 Cancer ColorectalDocument40 pagini1 Cancer ColorectalzukantalusÎncă nu există evaluări
- Cancerul ColorectalDocument9 paginiCancerul ColorectalElena JercanÎncă nu există evaluări
- Cancer GastricDocument18 paginiCancer GastricAmalia Elena BulanceaÎncă nu există evaluări
- Prezentarea Generală A Neoplasmului GastricDocument7 paginiPrezentarea Generală A Neoplasmului GastricCelina BeldimanÎncă nu există evaluări
- Cancer GastricDocument19 paginiCancer GastricBianca StoicaÎncă nu există evaluări
- Gastroenterologie Curs 8 AMG II Sem II (DR Popa Pavel)Document21 paginiGastroenterologie Curs 8 AMG II Sem II (DR Popa Pavel)Sbarcea RaduÎncă nu există evaluări
- 46 - Cancerul StomaculuiDocument8 pagini46 - Cancerul StomaculuiAdrian PetrosÎncă nu există evaluări
- Curs 3 UMFDocument35 paginiCurs 3 UMFIrina PopoviciÎncă nu există evaluări
- Cancerul Gastric - Panait VladDocument50 paginiCancerul Gastric - Panait VladgiorgianaÎncă nu există evaluări
- Cancerul GastricDocument3 paginiCancerul Gastricbratu.eugen710Încă nu există evaluări
- Cancer GastricDocument18 paginiCancer Gastric1alexandra12Încă nu există evaluări
- Cancer PancreasDocument24 paginiCancer PancreasAdriana VladutuÎncă nu există evaluări
- Ghid Neoplasm ColonDocument31 paginiGhid Neoplasm ColonJuncut BiancaÎncă nu există evaluări
- Neoplasmul GastricDocument36 paginiNeoplasmul GastricCosmin FlorinÎncă nu există evaluări
- Neoplasm GastricDocument9 paginiNeoplasm GastricobrejaÎncă nu există evaluări
- Cancerul Esofagian: PrevalenţăDocument7 paginiCancerul Esofagian: PrevalenţăVadim CovaciÎncă nu există evaluări
- Cr. Esofagian Prelegere Rezidenti 2016 Martalog4197414466857721808456694503Document19 paginiCr. Esofagian Prelegere Rezidenti 2016 Martalog4197414466857721808456694503Tatiana ManoilaÎncă nu există evaluări
- Tumorile Cailor Urinare Superioare.Document7 paginiTumorile Cailor Urinare Superioare.Berindean AlexÎncă nu există evaluări
- Cancerul GastricDocument51 paginiCancerul GastriccristinaelenasperiatÎncă nu există evaluări
- Metastazele Hepatice Când Și Unde Apar, Cum Le Tratăm - NewsMedDocument1 paginăMetastazele Hepatice Când Și Unde Apar, Cum Le Tratăm - NewsMedAlexandra ParaschivÎncă nu există evaluări
- Prevenirea cancerului. 10 reguli obligatorii pentru sănătate și viață lungăDe la EverandPrevenirea cancerului. 10 reguli obligatorii pentru sănătate și viață lungăÎncă nu există evaluări
- Strategii naturiste împotriva canceruluiDe la EverandStrategii naturiste împotriva canceruluiEvaluare: 5 din 5 stele5/5 (2)