Documente Academic
Documente Profesional
Documente Cultură
Terapia Oncologica-Optiuni Bazate Pe Evidente-Cancerele Dig
Încărcat de
Andra Birladeanu SurugiuTitlu original
Drepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Terapia Oncologica-Optiuni Bazate Pe Evidente-Cancerele Dig
Încărcat de
Andra Birladeanu SurugiuDrepturi de autor:
Formate disponibile
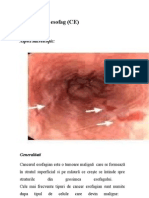
Cancerul esofagian
VI. CANCERELE DIGESTIVE
Lucian Miron, Mihai Marinca
Cancerele tubului digestiv reprezint circa 20% dintre toate cancerele viscerale i
determin 25% dintre decesele prin cancer, fiind n cretere constant ca frecven de
mai multe decenii, n special n rile cu nivel socio-economic crescut. Totui, n cadrul
acestui grup heterogen de neoplazii, unele prezint istorii naturale diferite: scderea
incidenei cancerelor gastrice i de colon, de exemplu.
Dei exist modificri preneoplazice caracteristice, precum i factori de risc bine
cunoscui, diagnosticul precoce al cancerelor digestive rmne puin performant, marea
majoritate a acestora fiind descoperite tardiv.
Tratamentul chirurgical rmne mijlocul terapeutic principal n oncologia digestiv.
Totui, innd cont de rezultatele mediocre, este adesea necesar recursul la alte
tratamente asociate, n special cele radio-chimioterapice.
Chimioterapia singur nu este curativ la pacienii cu boal clinic metastatic. Recent,
noile citostatice (camptotecin, oxaliplatin) i noile molecule intite i-au demonstrat
eficacitatea, lrgind sfera de aciune terapeutic n cancerele digestive considerate iniial
chimiorezistente.
Cancerul esofagian
EPIDEMIOLOGIE
Cancerul esofagian (CE) reprezint circa 1% dintre toate cancerele i 6% dintre toate
cancerele gastrointestinale; mortalitatea nalt rivalizeaz cu cea prin cancer pancreatic
i este de circa 4 ori mai crescut fa de a cancerelor rectale. Incidena brut (6,6/
100.000 locuitori/an) i mortalitatea (6,1/100.000 locuitori/an) sunt n cretere n
Uniunea European; vrsta medie de apariie este de 67 ani (rar sub 25 ani) [1].
n ntreaga lume sunt consemnate n prezent circa 500.000 cazuri de CE, dar exist o
marcat variaie geografic; regiunile cu inciden crescut includ China (Linxian), Iran,
Frana i Africa de Sud [2].
Factori de risc
Fumatul pe termen lung i consumul de alcool sunt factorii cei mai importani de risc
pentru carcinoamele scuamocelulare, iar esofagul Barett, obezitatea, refluxul gastro-
esofagian sunt incriminate pentru adenocarcinoamele esofagiene.
Factori predispozani
sindrom Howel-Evans sau tilosis (hiperkeratoz palmo-plantar, achalazia cardiei)
(30% din cazuri);
sindrom Plummer-Vincent (anemie feripriv, disfagie, fald esofagian) (10%);
esofag scurt (5%);
esofagit peptic (1%);
boal celiac, achalazie, infecii cu Human Papilloma Virus (HPV), cancere de sfer
ORL etc. [3].
169
CANCERELE DIGESTIVE
HISTOLOGIE
Sediul cel mai frecvent al CE este 1/3 inferioar a esofagului (toracic inferior, 43%),
urmat de 1/3 medie (toracic superior, 37%) i cea superioar (cervical, 20%).
Carcinoamele epidermoide sunt cele mai frecvente (95%) i se localizeaz n 1/3
superioar; adenocarcinoamele (5%) se localizeaz aproape exclusiv n 1/3 inferioar.
n numeroase ri vestice, incidena adenocarcinoamelor esofagiene (esofag distal i
jonciune gastroesofagian tipic la nivelul esofagului Barett) este n cretere rapid,
incidena carcinoamelor scuamocelulare fiind n scdere.
Clasificarea Siewert submparte tumorile jonciunii gastroesofagiene n 3 tipuri: tip I (tumori ale
esofagului distal), tip II (tumori ale cardiei) i tip III (tumori gastrice subcardiale) [4].
Printre tumorile maligne neepiteliale, leiomiosarcomul este cel mai frecvent, mai rare
fiind rabdomiosarcoamele, coriocarcinoamele i mioblastoamele.
Tumorile gastrointestinale stromale (TGIS) pot surveni la nivel esofagian, dar de obicei
sunt benigne.
DIAGNOSTIC
Examen clinic
semne precoce: disfagie progresiv, pierdere ponderal rapid, senzaie de presiune
retrosternal, durere iradiat interscapular n timpul deglutiiei;
semne tardive: paralizie a corzii vocale drepte/ diafragmatic, regurgitaie, tuse;
examenul fizic: adenopatii cervico-supraclaviculare, caexie sau hepatomegalie.
Investigaii paraclinice
esofago-gastro-fibroscopie cu biopsie;
tranzit esofagian baritat: stenoz neregulat, lacun sau imagine de adiie;
radiografie toracic;
ecografie abdominal;
examen CT toraco-abdominal:
extensie peri-esofagian aortic, traheo-bronic i/sau n ganglionii paraesofagieni i
mediastinali;
metastaze hepatice (35%), pulmonare (20%), osoase (9%) i suprarenaliene;
scintigrafie osoas i/sau examen CT cerebral doar n cazul apariiei de simptome
osoase, respectiv neurologice;
examen prin IRM rezultate similare cu examenul CT;
fibroscopie traheo-bronic: extensie bronic de vecintate (necesar n tumorile cu
dimensiuni > 25 mm pentru a exclude invazia traheei sau fistula traheoesofagian);
endoscopie cu ultrasunete (EUS) poate completa informaiile obinute prin
examenul CT:
profunzimea invaziei;
metastazele n ganglionii periesofagieni (50%);
depistarea precoce a tumorii recidivate [5,6];
tomografie cu emisie de pozitroni (PET) - util atunci cnd examenul CT este negativ
pentru boala metastatic, iar diagnosticul ar putea schimba tratamentul (20-25%
dintre pacieni) [7];
mediastinoscopie, laparotomie - rar utilizate.
170
Cancerul esofagian
STADIALIZARE
n Europa este utilizat clasificarea TNM a tumorilor esofagiene a UICC, n timp ce n
S.U.A. este utilizat cea elaborat de AJCC; aceste dou stadializri sunt foarte
apropiate.
Ediia a 6-a a stadializrii TNM UICC/AJCC (2002) nu aduce modificri clasificrilor
precedente [8].
Din punct de vedere practic, este important mprirea esofagului n segment cervical
(18 cm de la arcada dentar), toracic superior (21 cm) i toracic inferior (32 cm).
TABEL 6-1. Stadializarea TNM UICC/AJCC 2002 a cancerelor esofagiene
T (tumora primar)
To fr semne de tumor esofagian primitiv
Tis carcinom in situ
T1 tumor ce invadeaz lamina proprie sau submucoasa
T2 tumor ce invadeaz musculatura proprie
T3 tumor ce invadeaz adventicea
T4 tumor ce invadeaz structurile adiacente
N (adenopatiile loco-regionale)
No fr metastaze n ganglionii regionali
N1 metastaze n ganglionii regionali
M (metastazele la distan)
Mo fr prezena metastazelor la distan
M1 cu prezena metastazelor la distan
Pentru tumorile esofagului toracic inferior - M1a metastaze n ganglioni celiaci
- M1b alte metastaze la distan
Pentru tumorile esofagului toracic superior - M1a nu se aplic
- M1b alte metastaze la distan/ n ganglionii non-regionali
pTNM Clasificarea patologic
Categoriile pT, pN i pM corespund categoriilor T, N, M clinice.
pNo - Examenul histologic al piesei de limfadenectomie mediastinal va include 6 ganglioni
profunzi.
Gruparea pe stadii
Stadiul 0 Tis No Mo
Stadiul I T1 No Mo
Stadiul IIA T2-3 No Mo
Stadiul IIB T1-2 N1 Mo
Stadiul III T3 N1 Mo
T4 Orice N Mo
Stadiul IV Orice T Orice N M1
Stadiul IVA Orice T Orice N M1a
Stadiul IVB Orice T Orice N M1b
Diagnostic diferenial
tumori esofagiene benigne;
stenoza esofagian post caustic;
achalazia cardiei;
cancerul gastric al fornixului [9].
171
CANCERELE DIGESTIVE
EVOLUIE
CE se extinde pe cale limfatic, prin contiguitate sau pe cale hematogen.
Diseminarea limfatic poate fi submucoas sau intramural, pe o distan de 5-10 cm de
tumora primar i la ganglionii regionali. Cnd tumora se localizeaz n poriunea medie
a esofagului sunt interesai (2/3 cazuri) i ganglionii subdiafragmatici. Dac tumora
primar se localizeaz n poriunea terminal a esofagului, ganglionii pericardiali i
coronarieni sunt afectai n peste 80% cazuri.
n fazele avansate de evoluie, complicaiile mai frecvente sunt reprezentate de: fistule
de perete posterior al traheei/ bronhiei stngi, mediastinite, hemoragii grave (prin
interesarea sau perforarea marilor vase mediastinale) [10].
PRINCIPII DE TRATAMENT
Tratamentul loco-regional: Chirurgia
Chirurgia este mijlocul cel mai important n tratamentul CE cu extensie local sau
loco-regional i reprezint cea mai bun ans pentru vindecare, paliaia disfagiei
i/sau controlul local.
Chirurgia cu scop curativ
Procedurile chirurgicale includ o varietate de rezecii radicale largi (Ro, margini de
rezecie > 5 cm n esut sntos) ale tumorii primare, cu limfadenectomie regional
(esofagectomie transtoracic/ transhiatal/ toracic total, laringo-esofagectomie [CE
cervical], esofagectomie radical n bloc, rezecie endoesofagian endotoracic).
Exist o relaie demonstrat ntre volumul rezeciei tumorale i rezultatele obinute,
rezecia incomplet prezentnd doar un beneficiu minim sau nici un avantaj.
Intervenia de elecie n CE const n excizia "n bloc" a tractusului esofagian, cu 10 cm de esut
sntos n amonte i aval de neoplazie. Concomitent se extirp ntreg esutul mediastinal posterior
care nconjoar esofagul. n funcie de experiena chirurgical, se va practica limfadenectomia
lrgit prin extensia de la plexul celiac (inferior) pn la vasele pulmonare (superior). n general,
pacienii cu CE cervicale nu sunt considerai candidai pentru rezecia local [3,4].
Vrsta singur nu mai reprezint o contraindicaie a chirurgiei.
Controverse:
tipul de intervenie preferabil: transtoracic, transhiatal, altele;
extensia rezeciei (axial, radial, limfatic);
metodele de reconstrucie;
validitatea conceptului de esofagectomie de salvare [1].
Mortalitatea operatorie este de 5-10%, iar supravieuirea pe termen lung nu depete
25% dac sunt invadai ganglionii regionali. La pacienii la care rezecia complet este
posibil (25-30%), supravieuirea la 5 ani este de 15-30%. Supravieuirea general la 5
ani la pacienii cu CE operai variaz ntre 5 i 20% [10].
Chirurgia paliativ
Laserterapia endoscopic pentru combaterea obstruciei i/sau hemoragiei
(mortalitate <1%) necesit dilataie mecanic prealabil, n edine repetate.
Fotosensibilizarea tumorilor esofagiene cu un derivat de porfirin crete energia
laser absorbit de tumor, dar se asociaz cu riscul de fotosensibilizare generalizat
(dureaz 4-6 sptmni).
172
Cancerul esofagian
Dilatarea esofagian poate fi eficace n combaterea disfagiei la peste 90% din
pacieni. Efectul su este ns temporar (durat medie 4 sptmni).
Protezarea endoesofagian este necesar la circa 15% dintre pacienii cu CE
obstructiv. Sunt disponibile 17 tipuri de proteze expandabile, relativ uor de inserat
sub ghidaj endoscopic sau fluoroscopic, cu o rat de succes tehnic de 85-95%.
Eficacitatea este de 80-100%, dar cu o durat a rspunsului de 5-6 luni. Rata de
complicaii precoce i tardive este de 10-20%.
Avantaje: crete capacitatea de nghiire a salivei, permite alimentaia oral, reduce
riscul de aspiraie prin fistul esotraheal.
Dezavantaje: perforaie, dislocare, necroz, simptome de reflux, sngerare, senzaie de
corp strin, pre de cost foarte crescut.
Contraindicaii: localizare tumoral la mai puin de 2 cm de sfincter, speran de via <
6 sptmni, pacient necooperant.
Dieta const n eliminarea alimentelor care blocheaz esofagul sau ader la locul de
fixare a protezei.
Stent-urile pot fi utilizate cu succes nainte sau dup chimio-radioterapie, pentru
combaterea edemului indus de tratament, care agraveaz iniial disfagia [1,3,4].
Sondele de gastrostom sunt necesare pentru nutriia enteral numai cu indicaii
precise (a se vedea capitolul Nutriia la pacientul oncologic) [11,12].
Tratamentul loco-regional: Radioterapia
Radioterapia extern
Carcinomul epidermoid al esofagului este radiosensibil.
Radioterapia definitiv
Radioterapia extern (RTE) poate fi utilizat n tumorile inoperabile cu extensie
inferioar, cu intenie curativ la 5-10% din cazurile fr metastaze sau fistule
traheo-bronice (DT 50-60 Gy, fracionare convenional).
RTE cu intenie curativ este recomandat i n cazurile cu tumori limitate dar cu
contraindicaii medicale, sau cu o localizare anatomic care face dificil abordul
chirurgical.
Persistena sau recidiva tumorii primare dup RTE se ntlnesc n 56-85% din cazuri.
Pacienii care rspund la RTE pot fi propui pentru rezecia chirurgical.
Supravieuirea pacienilor tratai cu RTE singur nu s-a modificat substanial n ultimele
dou decade: ratele de supravieuire la 1, 2 i 5 ani sunt de 33%, 8% i respectiv, 7%, iar
supravieuirea median este de circa 12 luni.
Radioterapia singur este considerat paliativ, i se recomand la pacienii incapabili s
tolereze chimio-radioterapia concomitent [1].
Radioterapia preoperatorie
Studiile randomizate nu au demonstrat c RTE preoperatorie singur ar aduce un
beneficiu la pacienii cu CE; aceasta nu determin o cretere semnificativ a procentelor
de rezecabilitate i nici a supravieuirii globale.
Tratamentul radioterapic preoperator nu se recomand n afara studiilor clinice i
nu-i gsete indicaii n practica curent actual [13].
173
CANCERELE DIGESTIVE
Radioterapia postoperatorie
RTE ca singur modalitate terapeutic postoperatorie nu a confirmat beneficii n CE.
Este indicat, dac rezecia chirurgical este incomplet, sau marginile de rezecie
sunt pozitive; scade semnificativ riscul de recidiv (de la 35% la 10%) la pacienii cu
ganglioni negativi dup rezecia curativ, fr efect aparent pe supravieuire [10,14].
Brahiterapia
Brahiterapia de paliaie poate fi utilizat numai n anumite cazuri bine selecionate ca
tratament simptomatic i poate fi preconizat n completarea RTE sau ca alternativ
terapeutic la pacienii prealabil tratai cu RTE.
Paliaia este obinut n 50-90% din cazuri.
Tratamentul sistemic: Chimioterapia
Carcinoamele scuamocelulare par a fi mai sensibile la chimioterapie, dar nu exist nici
o diferen n rezultatele pe termen lung ntre acestea i adenocarcinoame.
Chimioterapia paliativ
Chimioterapia (CHT) reprezint frecvent o modalitate de tratament paliativ eficace; va
fi asociat cu chirurgia, RT sau protezarea esofagian n scopul combaterii disfagiei.
Agenii chimioterapici utilizai n monoterapie determin rate de rspuns (RR) de 15-25%
(rspunsuri pariale, de scurt durat 2-5 luni), fr impact asupra supravieuirii.
Polichimioterapia cu cisplatin, 5-fluorouracil (5-FU), taxani crete RR (pn la 45-80%), durata
rspunsului (7 luni), dar i toxicitatea secundar, fr a ameliora ns supravieuirea; rezultatele
rmn nesatisfctoare [12].
Asocierea cisplatin cu 5-FU este regimul actual cel mai frecvent utilizat (eventual
concomitent cu RTE), att n boala localizat ct i pentru paliaia bolii metastatice.
n prezent, datele care s clarifice rolul CHT n formele metastatice de CE lipsesc.
Terapia simptomatic, intensiv, rmne o alternativ de preferat la vrstnici sau la
pacienii cu stare general alterat [21].
TABEL 6-2. Protocoale de CHT utilizate n cancerul esofagian
PF
Cisplatin 75-100 mg/m I.V. ziua 1
5-Fluorouracil 1000 mg/m/zi I.V. (perfuzie continu) zilele1-4(5)
Se repet la fiecare 4 sptmni.
PFC
Cisplatin 75-100 mg/m I.V. ziua 1
5-Fluorouracil 1000 mg/m/zi I.V. (perfuzie continu) zilele1-4(5)
Paclitaxel 175 mg/m I.V. (perfuzie 3h) ziua 1
Se repet la fiecare 4 sptmni.
RR 37.7%
IP
Irinotecan 65 mg/m) I.V. ziua 1
Cisplatin 30 mg/m I.V. zilele 1,8,15,22
Se repet la fiecare 6 sptmni.
RR 57%
174
Cancerul esofagian
Chimioterapia adjuvant
Esofagectomia este asociat cu morbiditate perioperatorie considerabil, comparativ cu
cancerul mamar, de exemplu, care limiteaz uneori opiunile terapeutice ulterioare.
Chimioterapia adjuvant a fost evaluat n dou studii care au inclus numai pacieni cu
carcinoame epidermoide. Nu au fost observate diferene n termenii supravieuirii.
Chimioterapia postoperatorie nu este recomandat ca practic de rutin (I,A) [20].
Chimioterapia neoadjuvant (preoperatorie)
Tratamentul chimioterapic preoperator poate determina o cretere a rezecabilitii, fr
creterea mortalitii i morbiditii operatorii; rata recidivelor la distan a fost
considerabil redus cu CHT neoadjuvant, dar recidiva local a rmas nemodificat.
Se poate utiliza asocierea cisplatin/5-FU, 2-3 cicluri nainte de intervenia chirurgical
(i 2 cicluri postoperator, dac pacientul prezint rspuns histologic sau boal
staionar). Oxaliplatin ar putea deveni candidat la utilizarea n CHT preoperatorie [19].
Ratele de rspuns la polichimioterapia neoadjuvant pot depi 40-50%, dintre care
peste 25% dintre pacieni pot obine rspuns histologic complet; totui, supravieuirea
nu este ameliorat n CE epidermoide comparativ cu chirurgia singur (studiu pe 440 de
pacieni). n ciuda beneficiilor teoretice poteniale, sunt necesare alte studii care s
demonstreze avantajul CHT preoperatorii n supravieuirea pacienilor cu CE rezecabil.
n adenocarcinoamele esofagiene, CHT preoperatorie a devenit un standard n Marea
Britanie i unele ri de Europa, n timp ce n S.U.A. acesta este chirurgia singur sau
chimio-radioterapia definitiv (fr chirurgie).
n cancerele epidermoide esofagiene n stadii potenial rezecabile (I-III), CHT
neoadjuvant singur nu este un tratament standard.
Terapiile asociate: Chimio-radioterapia
Fiecare pacient cu CE trebuie evaluat individual. La persoanele fr comorbiditi, cu
status bun de performan, stadiu avansat i dorin de a fi tratat n manier agresiv,
chimio- i/sau radioterapia preoperatorie poate fi propus dup o discuie cu pacientul.
Pacienii vrstnici, sau medical compromii, care sunt incapabili s tolereze efectele
secundare severe ale chimio-radioterapiei, vor fi tratai chirurgical [10].
Chimio-radioterapia concomitent este considerat actual standard de tratament
pentru pacienii cu CE nerezecabil, sau o alternativ la chirurgie n CE rezecabil.
Chimio-radioterapia preoperatorie
Rezultatele nesatisfctoare dup chirurgia imediat, datorate n mare parte tehnicilor
chirurgicale neadecvate, au concentrat atenia asupra tratamentelor asociate (chimio-
radioterapia) preoperator, mai ales n stadiile II-III de CE. Aceast modalitate rmne
controversat, datorit att dificultii de a dispune preoperator de o stadializare corect,
ct i rezultatelor contradictorii din studiile clinice randomizate.
Rezultatele chimio-radioterapiei (CHT-RT) fr chirurgie sunt comparabile cu cele
obinute prin chirurgia singur [12].
Cnd se preconizeaz un tratament preoperator, este necesar o stadializare mai
agresiv, prin examen endoscopic (eventual cu ultrasunete), CT, laparoscopie; frecvent
este necesar montarea unei sonde de gastrostom pentru nutriie.
Rezultatele studiilor randomizate au demonstrat obinerea de rspunsuri complete (RC)
la mai mult de 25% dintre pacieni, ca i o cretere a supravieuirii [15].
175
CANCERELE DIGESTIVE
Asocierea concomitent a chimio-radioterapiei determin efecte secundare importante
cu impact profund asupra strii de nutriie a pacientului.
CHT-RT concomitent este o cauz major a sindromului anorexie-caexie la pacienii
cu CE. Din acest motiv, instituirea precoce a terapiei nutriionale este un principiu de
tratament n CE avansat [16,17,18].
Chimio-radioterapia adjuvant
Chimio-radioterapia adjuvant rmne n curs de studiu [10,20].
CHT-RT adjuvant a fost testat ntr-un studiu randomizat (US Intergroup INT0116,
556 pacieni) ce demonstreaz ameliorarea supravieuirii fr boal i a supravieuirii la
3 ani numai la pacienii cu limfadenectomie extensiv (D2) i CHT-RT. Totui, se
remarc toxicitatea hematologic sever (grad 3/4 la 54% dintre pacieni) i toxicitatea
digestiv (grad 3/4 la 33% dintre pacieni).
Recomandri NCCN 2006: Pacienii cu adenocarcinoamele jonciunii eso-gastrice tratai
chirurgical trebuie s primeasc CHT-RT postoperatorie dac stadiul iniial este IB sau
mai mare, mai ales dac tumora invadeaz ganglionii limfatici regionali. [22].
Chimio-radioterapia definitiv
Chimio-radioterapia definitiv trebuie utilizat la pacienii cu contraindicaii medicale
sau la cei cu tumori nerezecabile din punct de vedere tehnic (mai ales la cei cu carcinom
epidermoid), n cazul lipsei de experien a chirurgului toracic n practicarea
esofagectomiei sau al preferinei pacientului/ medicului ctre un tratament
nechirurgical.
Rezultatele mai multor studii au evideniat o cretere a procentelor de rspuns cu o
supravieuire mai lung dup asocierea CHT cu cisplatin i 5-FU la RT (studiul RTOG
85-01: rate de supravieuire la 5 ani de 27% vs. 0% dup RT singur, supravieuire
median 14.1 vs. 9.3 luni) [12].
TABEL 6-3. Chimio-radioterapia concomitent n CE
5-Fluorouracil 1000 mg/m I.V. (perfuzie continu 24h) zilele 1-4,29-32,50-53,71-74
Cisplatin 75mg/m I.V. zilele 1,29,50,71
Radioterapie 2.0 Gy/zi 5 zile/sptmn sptmnile 1-5 (DT 50 Gy)
Pacienii ce primesc tratament concomitent chimio-radioterapic prezint un rspuns
local crescut i scderea frecvenei recidivelor, ns cu preul unei toxiciti secundare
crescute (esofagit, neuropatii, leucopenii).
Efectele secundare ale CHT-RT concomitente sunt severe n 44% din cazuri i cu risc
vital n 20% din cazuri, fa de 25%, i respectiv 3%, la pacienii tratai cu RT singur.
Esofagita este universal i face necesar susinerea nutriional, prin plasarea unei
sonde de enterostomie pentru alimentare (alimentarea parenteral este dificil datorit
administrrilor cvasicontinue de CHT n protocoalele de mai sus).
Din aceste motive, administrarea concomitent a CHT-RT poate fi propus numai
pacienilor cu vrste tinere, cu status de performan bun, cu stare de nutriie acceptabil
i care i asum o toxicitate secundar ntotdeauna sever [21].
176
Cancerul esofagian
Noile terapii
Trei noi clase de terapii biologice sunt n curs de studiu n cancerele esofagiene i
gastrice: anticorpii monoclonali i inhibitorii tirozinkinazici (TKI) ai receptorului
factorului de cretere epidermal (EGFR, prezent n 70% dintre CE epidermoide) i ai
factorului vascular endotelial de cretere (VEGF, prezent n 50% dintre CE) i reglatorii
ciclului celular.
Studiile actuale evalueaz rolul TKI de EGFR cu administrare oral (gefitinib,
Iressa
; erlotinib, Tarceva
), i respectiv cel al anticorpilor monoclonali anti-VEGF
(bevacizumab, Avastin
) n CE, ca o component a tratamentului preoperator.
Kinazele ciclin-dependente (cdk) sunt reglatori ai ciclului celular care pot fi intii
direct prin molecule mici (mai active cnd se asociaz cu CHT sau/i RT). Dintre
inhibitorii de cdk, flavopiridol este cel mai avansat n studiile clinice; un studiu actual
de faz II testeaz asocierea docetaxel sptmnal cu flavopiridol vs. docetaxel
singur la pacienii cu cancere eso-gastrice avansate.
Survivin este un membru al familiei de proteine inhibitorii a apoptozei (IAP) care
regleaz ciclul celular i este supraexprimat n cancerele digestive. Comparativ cu
celulele epiteliale nemaligne, celulele de cancer eso-gastric exprim nivele de
survivin crescute de 10 ori. Un studiu actual ce utilizeaz rebamipide (inhibitor al
expresiei de survivin) a demonstrat activitate pozitiv i toleran bun la aceti
pacieni.
Studiile epidemiologice au sugerat c utilizarea medicaiei AINS ar putea reduce
incidena CE, posibil prin inhibarea ciclooxigenazei 2 (COX2), o enzim indus de
citokine, factori de cretere i oncogene care contribuie la sinteza prostaglandinelor
n esuturile neoplazice inflamate. Sunt planificate studii care s investigheze
eficacitatea AINS sau a altor inhibitori de COX2 la pacienii cu esofag Barett.
Terapia de susinere
Prevalena tulburrilor nutriionale, valoarea lor predictiv privind incidena i
severitatea complicaiilor n timpul tratamentului este bine stabilit la pacienii cu CE.
Terapia de susinere (paliativ) ocup un loc important n tratamentul CE, cele mai
frecvente simptome care necesit paliaie fiind disfagia i durerea, cu mpiedicarea
aportului alimentar. Incidena tulburrilor nutriionale este de 78,9%, acestea fiind
datorate obstruciei mecanice, anorexiei dar i alterrilor metabolice (sindromul de
anorexie-caexie). Terapia oncologic activ contribuie la deteriorarea statusului
nutriional (radioterapia poate induce esofagit, ulterior fibroz i strictur;
chimioterapia induce greuri, vrsturi, anorexie; interveniile chirurgicale interfereaz
cu anatomia normal, ceea ce conduce invariabil la deteriorarea statusului nutriional).
Un numr redus de studii au abordat tratamentul nutriional la pacientul cu cancer
esofagian. Dei acestea raporteaz ameliorarea variabilelor biologice (greutate, balan
azotat, albumin seric), nu au demonstrat ameliorarea supravieuirii sau scderea
mortalitii asociate suplimentrii nutriionale.
Evaluarea nutriional reprezint primul pas n identificarea i tratamentul tulburrilor
nutriionale, i include: anamneza nutriional, examinarea fizic, curba ponderal, i
parametrii biofizici. n majoritatea cazurilor, nutriia enteral este preferat datorit
conservrii integritii intestinale, scderii riscului de complicaii post-terapeutice i a
preului de cost.
177
CANCERELE DIGESTIVE
Restabilirea aportului alimentar se poate obine prin:
Intervenii chirurgicale (by-pass, gastro-/ jejunostomie).
Radioterapie extern (DT 40-45 Gy), fie singur, fie n asociere cu chimioterapia,
(ofer paliaia disfagiei la 80% dintre pacieni, iar 50% o menin pn la deces).
Laserterapie, dilatare (balon, bujii) sau protezare (stent) dac pacienii necesit
paliaie rapid.
Brahiterapie endocavitar dac radioterapia extern nu este posibil.
Nutriie parenteral utilitate neclar la pacienii tratai chimio-radioterapic (nu se
recomand ca tratament de rutin).
Decizia de a aplica nutriia enteral sau parenteral la pacienii cu boal avansat,
incurabil necesit reconsiderarea atent a scopului i indicaiei interveniei nutriionale.
Terapia de susinere nutriional nu trebuie administrat la pacienii la care nu este
posibil un tratament antitumoral (cel puin paliativ) eficace; acetia vor fi mai bine
tratai cu analgezice i ngrijiri paliative ambulatorii.
Terapia nutriional precoce i abordul pluridisciplinar pot conduce la ameliorarea
toleranei la tratament a pacienilor cu CE tratai chimio-radioterapic [23].
STRATEGIE TERAPEUTIC
Stadiul I
Chirurgia radical reprezint tratamentul standard (supravieuirea la 3 ani este de
75% n cazul unei rezecii complete, dar nu depete 25% dac sunt invadai
ganglionii regionali).
Pacienii care din motive medicale nu pot suferi intervenia chirurgical vor fi supui
chimio-radioterapiei, cu rezultate superioare RT singure (I,A).
Stadiul IIA
n cazul adenocarcinoamelor, chirurgia este tratamentul de rutin.
Chirurgia singur nu este alegerea optim, dac rezecia complet a tumorii nu este
posibil (30% dintre tumorile T3, i 50% dintre tumorile T4). n aceste situaii, se
recomand RT postoperatorie pentru a crete controlul local. Supravieuirea pe
termen lung rareori depete 15% chiar n cazul rezeciei complete.
Se poate interveni chirurgical dup chimio-radioterapie, dar beneficiile acestei
modaliti nu au fost probate de studiile multicentrice de faz III.
Stadiul IIB
Se poate propune rezecia chirurgical iniial, dar rezultatele sunt nesatisfctoare
la pacienii cu afectare ganglionar.
Se poate interveni chirurgical dup chimio-radioterapie, dar beneficiile acestei
modaliti nu au fost probate de studiile multicentrice de faz III.
Chimioterapia primar concomitent cu radioterapia s-a dovedit benefic (studiul
RTOG 85-01 sau studiul European)
Stadiul III
Rezecii chirurgicale paliative pot fi luate n considerare pentru toate leziunile T3.
178
Cancerul esofagian
Recomandri ESMO 2005:
Pacienii cu boal local-avansat ar putea beneficia de chimioterapie preoperatorie, i n
special de chimio-radioterapie preoperatorie, prin creterea ratelor de rezecie complet
tumoral, creterea controlului local i ameliorarea supravieuirii (I,B). Totui, chimio-
radioterapia preoperatorie poate crete mortalitatea postoperatorie. Pacienii cu rspuns
tumoral iniial la chimio-radioterapie ar putea s nu beneficieze de chirurgie, motiv
pentru care ar trebui tratai numai prin chimio-radioterapie definitiv (II,B).
Protocolul cisplatin cu 5-FU asociat cu RT, urmat de chirurgie, poate fi considerat cea
mai bun opiune terapeutic (II,B). n prezent, nu este clar dac RT crete supravieuirea
comparativ cu chimioterapia singur, i care pacieni nu ar beneficia de chirurgie [20].
Stadiul IV
La momentul diagnosticului, circa 50% din pacienii cu CE vor prezenta metastaze i
sunt candidai la terapia paliativ. Pacienii cu boala metastatic prezint o supravieuire
medie de 6 luni.
Opiunile terapeutice standard sunt:
Montarea unui stent esofagian
Laserterapia endoluminal (distrucie tumoral prin electrocoagulare).
Radioterapia cu sau fr intubare intraluminal i dilatare (DT 30 Gy, 2 Gy/fracie,
zilele 1-5, sptmnile 1-3).
Brahiterapia intraluminal.
Chimioterapia rspunsuri pariale la pacienii diagnosticai cu adenocarcinoame
esofagiene distale metastatice:
Pn n prezent, nu sunt disponibile date care s clarifice rolul chimioterapiei n formele
metastatice de cancer esofagian.
Se administreaz regimuri de CHT similare cu cele utilizate n carcinoamele gastrice, sau n
carcinoamele epidermoide de sfer ORL, dar cu rspunsuri obiective mai modeste. CHT nu
a fost asociat cu o prelungire a supravieuirii.
Terapia simptomatic (alternativ recomandabil la vrstnici sau la pacienii cu stare
general alterat).
Recomandri ESMO 2005:
Tratamentul n stadiul IV este paliativ. Chimioterapia poate fi administrat numai la
anumii pacieni (III,B).
Protezarea (stent) esofagian poate fi cost-eficient pentru restaurarea nutriiei orale
(III,B). Disfagia este rapid combtut dup montarea stent-ului, dar o ameliorare pe
termen lung a disfagiei se poate obine cu RT paliativ n doz unic de 12 Gy sau prin
brahiterapie intracavitar (II,B) [20].
Boala recidivat
Recidivele esofagiene prezint probleme dificile de paliaie.
Opiunile terapeutice n aceste situaii se bazeaz pe tratamentele de susinere i cele
simptomatice.
Excepional, pot fi utilizate RT sau CHT.
179
CANCERELE DIGESTIVE
PROGNOSTIC
Cei mai buni factori predictivi pentru prognostic sunt:
prezena invaziei ganglionare (n special celiac M1a, depistat prin EUS)
prezena metastazelor la distan [4]
Cancerul esofagian rmne o neoplazie cu prognostic foarte grav. Supravieuirea medie
nu depete 12 luni, iar la 5 ani mai sunt n via mai puin de 10% dintre pacieni.
Atunci cnd tumora este diagnosticat n stadiile iniiale i cnd posibilitatea de rezecie
complet este crescut, supravieuirea la 5 ani crete la 20-25% (experiena rilor
orientale, Japonia i China).
CE poate fi vindecat atunci cnd este diagnosticat n stadiul I; invazia ganglionilor
regionali reduce procentele de supravieuire de la 30 la 10%.
Cele mai bune rezultate dup chirurgie se concretizeaz n supravieuiri la 5 ani ntre
10-20%; radioterapia poate determina supravieuiri la 5 ani de 20% [1].
URMRIRE
Nu exist un standard de supraveghere la pacienii cu CE avansat loco-regional. Se
practic examenul clinic cu anamneza simptomelor recente, hemoleucograma, ureea,
electroliii, testele hepatice la fiecare 4 luni n primul an, ulterior la 6 luni timp de 2 ani
i apoi anual.
Radiografia toracic, examenul CT abdominal/ toracic i endoscopia digestiv
superioar se vor solicita cnd aspectul clinic este sugestiv pentru recidive sau
metastazare.
Recomandare ESMO 2005:
Nu exist dovezi c urmrirea regulat dup tratamentul iniial influeneaz
rezultatele. Vizitele de urmrire trebuie concentrate pe simptomele, problemele de
nutriie i psiho-sociale ale pacientului [20].
Bibliografie
1. Leonard DG, Kelsen DP, Allegra CJ. Esophageal cancer. In: Abraham J, Allegra CJ, Gulley J, eds.
Bethesda Handbook of clinical oncology. 2nd ed. Philadelphia: Lippincott Williams&Wilkins 2005:61-71
2. Alberts R.S, Goldberg RM. Gastrointestinal tract cancers. In: Casciato DA, ed. Manual of clinical
oncology. 5th ed. Philadelphia: Lippincott, Williams & Wilkins, 2004: 185-195.
3. Chau I, Cunningham D. Cancer of the oesophagus. n: Williams C, ed. Evidence-based oncology. Londra:
BMJ Books 2003:223-242.
4. Posner MC, Forastiere AA, Minsky BD. Cancer of the esophagus. In: DeVita VT Jr., Hellman S,
Rosenberg SA, eds. Cancer: principles & practice of oncology. Philadelphia: Lippincott, Williams &
Wilkins, 2005:861-908.
5. Miron L. Cancerul esofagian. In: Bild E, Miron L, eds. Terapia cancerului - ghid terapeutic. Iai: Editura
Tehnopress, 2003:105-113.
6. Heitmiller FR, Forastiere AV. Esophagus. In: Abeloff MD, Armitage JO, Lichter AS, eds. Clinical
oncology. 2nd ed. New York: Churchill Livingstone, 2000:1517-1545.
7. Kleinberg LR, Forastiere AA, Heitmiller R. Esophagus. In: Abeloff MD, ed. Clinical oncology. 3rd ed.
New York: Elsevier Churchill Livingstone, 2004:1787-1818.
8. American Joint Committee on Cancer. Esophagus. n: AJCC Cancer Staging Manual. 6th ed. New York:
Springer, 2002:91-98.
9. Robustelli della Cuna G, Bonadonna G. Carcinoma dell esofago. In: Bonadonna G, ed. Medicina
oncologica. 7ma ed. Milano: Mason, 2003:847-954.
10. Urshel JD. Esophageal cancer. In: Chang AE, Ganz PA, Hayes DF, eds. Oncology - an evidence based
approach. New York: Springer, 2006:664- 679.
180
Cancerul esofagian
11. Boyce HW. Esophageal malignancies and premalignant conditions. In: Kirsner J, ed. The growth of
gastroenterologic knowledge during the twentieth century. Malvern: Lea & Febiger, 1994:11-34.
12. Cooper JS, Guo MD, Herskovic A, et al. Chemoradiotherapy of locally advanced esophageal cancer:
long-term follow-up of a prospective randomized trial (RTOG 85-01). Radiation Therapy Oncology
Group. JAMA 1999;281(17):1623-167.
13. Smith TJ, Ryan LM, Douglass HO Jr, et al. Combined chemoradiotherapy vs. radiotherapy alone for early
stage squamous cell carcinoma of the esophagus: a study of the Eastern Cooperative Oncology Group. Int
J Radiat Oncol Biol Phys 1998; 42 (2): 269-276.
14. Minsky BD, Pajak TF, Ginsberg RJ, et al. INT 0123 (Radiation Therapy Oncology Group 94-05) phase
III trial of combined-modality therapy for esophageal cancer: high-dose versus standard-dose radiation
therapy. J Clin Oncol 2002; 20(5):1167-1174.
15. Bosset JF, Gignoux M, Triboulet JP, et al. Chemoradiotherapy followed by surgery compared with
surgery alone in squamous-cell cancer of the esophagus. N Engl J Med 1997; 337(3):161-167.
16. Bates BA, Detterbeck FC, Bernard SA, et al. Concurrent radiation therapy and chemotherapy followed by
esophagectomy for localized esophageal carcinoma. J Clin Oncol 1996;14(1):156-163.
17. Kelsen DP, Bains M, Burt M. Neoadjuvant chemotherapy and surgery of cancer of the esophagus. Semin
Surg Oncol 1990;6(5):268-273.
18. Benson Al-B III. Carcinomas of the gastro-intestinal tract. In: Skeel RT, ed. Handbook of cancer
chemotherapy. Philadelphia: Lippincott, Williams & Wilkins, 2007: 257-263.
19. Chong G, Cunninham D. Oesophagian cancer: preoperative chemotherapy. Ann Oncol 2004;
15(suppl.4):iv87-iv91.
20. Stahl M, Kataja VV, Oliveira J. ESMO Minimum clinical recommendations for diagnosis, treatemnt and
follow up of esophageal cancer. Ann Oncol 2005;16(suppl.1):i26-i28.
21. Scheithauer W. Esophageal cancer: chemotherapy. Ann Oncol 2004;15(suppl.4):iv83-iv86.
22. Urba S. Esophageal cancer: preperative or definitive chemoradiation. Ann Oncol 2004;15(suppl.4): iv983-
iv96.
23. Riccardi D, Allen K. Nutritional management of patients with esophageal and esogastric junction cancer.
Moffitt Center Cancer Control Journal 1999;6(1):12-15.
24. Paz BI, Hwang JJ, Iyer R. Esophageal cancer. In: Pazdur R, Coia LR, Hoskins WJ, eds. Cancer
management: a multidisciplinary approach. 10th ed. New York: CMP Medica Oncology 2007:251-271.
25. Stahl M. Esophageal cancer: ESMO Clinical recommendations for diagnosis, treatment and follow-up.
Ann Oncol 2007;18(suppl.2):ii15-ii16.
181
CANCERELE DIGESTIVE
Cancerul gastric
EPIDEMIOLOGIE
Cancerul gastric (CG) reprezint a doua cauz de deces prin cancer n lume (12,1% din
totalitatea deceselor prin cancer) i a doua sau a treia neoplazie ca frecven. Prevalena
i mortalitatea CG (particular a localizrilor distale) a sczut semnificativ n toate
regiunile geografice, i la toate vrstele, cu 2% pn la 7% pe an.
Incidena CG n Uniunea European este actual de 18.9 cazuri/ 100.000 locuitori/ an, cu
rate de 1,5 ori mai crescute la sexul masculin i cu vrful de inciden n decada a
aptea; mortalitatea este de 14,7 cazuri/ 100.000 locuitori/ an. n Japonia, Europa de Est
i America de Sud (n special Chile i Costa Rica), incidena CG este epidemic. n
Japonia, incidena CG este maxim (100 cazuri/100.000 locuitori/an) i reprezint prima
cauz de deces prin cancer. La nivel modial, CG reprezint aproximativ 930.000 de
cazuri noi i determin mai mult de 700.000 de decese [1,2].
ETIOLOGIE
Principalii factori asociai cu risc crescut de CG sunt:
nutriionali:
consumul sczut de grsimi i proteine;
consumul de carne sau pete srat;
consumul crescut de nitrai;
dieta srac n vitaminele A i C.
de mediu:
preparare insuficient a mncrii;
lipsa refrigerrii;
diet hidric srac;
profesie: industria cauciucului, mine de crbuni;
fumatul.
! alcoolul nu a demonstrat o relaie cauzal cu apariia CG
sociali:
condiie socio-economic precar.
iatrogeni:
intervenii chirurgicale anterioare pe stomac, n special pentru ulcer gastric.
! tipul interveniei nu influeneaz riscul relativ.
infecioi:
Helicobacter pylori este detectat n 90% dintre neoplaziile gastrice de tip intestinal, n 32%
din leziunile de tip difuz i n limfomul gastric.
genetici:
anomalii ale genei p53, observate n > 60% din CG;
alterarea genei APC n >50% dintre adenocarcinoamele bine difereniate;
amplificarea oncogenei c-met n CG avansat [2].
leziuni premaligne:
gastrita cronic atrofic sau hipertrofic (boala Mntrier);
anemia pernicioas;
indivizi cu grup sangvin AII (CG predominant de tip infiltrativ, mai rar exofitic);
metaplazia intestinal (80% din piesele de rezecie n Japonia).
182
Cancerul gastric
HISTOLOGIE
Recomandare ESMO 2005: Diagnosticul de cancer gastric trebuie bazat pe biopsia
gastroscopic / chirurgical, iar histologia se va formula n acord cu clasificarea OMS.
Circa 90-95% din CG sunt adenocarcinoame (difuz, papilar, tubular, mucinos, de tip
intestinal etc.), restul de 5% fiind leiomiosarcoame, limfoame, tumori carcinoide,
carcinoame (scuamocelulare, nedifereniate, cu celule n inel cu pecete); tumorile
gastro-intestinale stromale (TGIS) reprezint 2-3% din toate tumorile gastrice, i sunt
cel mai frecvent localizate la nivel gastric [4,5].
Localizarea cancerelor la nivelul stomacului este distal n 40% din cazuri, proximal n
35% din cazuri i la nivelul corpului gastric n 25% din cazuri.
Clasificarea histologic (Lauren):
tip difuz (leziuni unice sau depozite reduse de celule mici n submucoas);
tip intestinal (celule mari columnare, cu infiltrate inflamatorii, localizate n arii de gastrit
atrofic sau metaplazie intestinal);
tipuri mixte.
Clasificarea anatomic macroscopic:
tipul cu diseminare superficial, focal (polipoid, aspect fungic sau ulcerativ);
tipul infiltrativ (linita plastic).
Clasificarea Societii Japoneze de Endoscopie (JES):
tip I (polipoid sau pseudotumoral);
tip II (plat, minim supradenivelat/subdenivelat);
tip III (cancer asociat cu ulcer adevrat).
DIAGNOSTIC
Examen clinic
astenie;
dureri minime (jen, disconfort) epigastrice i/sau abdominale;
disfagie (CG cardial);
pierdere ponderal, anorexie/saietate precoce (linita plastic);
eructaii,vrsturi (CG antral);
hematemez (10-15%), melen/hemoragii oculte n materiile fecale;
mas tumoral palpabil n epigastru;
adenopatie metastatic supraclavicular stng (semnul Virchow-Troisier) sau axilar
stng (semnul Irish);
noduli subcutanai periombilicali (semnul Sister Mary Joseph);
hepatomegalie, icter, ascit (stadiu foarte avansat, incurabil);
sindroame paraneoplazice:
achantosis nigricans (55%);
polimiozita, dermatomiozita;
eritem circinat, pemfigoid;
demena, ataxia cerebeloas;
tromboza venoas idiopatic;
sindrom Cushing ectopic sau sindrom carcinoid (rar);
semnul Lesser-Trlat.
183
CANCERELE DIGESTIVE
Investigaii paraclinice:
anemie hipocrom hiposideremic;
anemie Biermer;
markerii tumorali:
antigenul carcino-embrionar (ACE) este crescut n 40-50% din cazuri (util n urmrirea
pacienilor, nu ns i n screening);
alfa-fetoproteina (AFP) i CA19.9 sunt crescute la 30% dintre pacienii cu CG.
radiografia abdominal cu substan de contrast (BaSO
4
) nu faciliteaz biopsia (n
75% din cazuri), dar prezint avantajul non-invazivitii; permite diagnosticul pozitiv
al unor leziuni de 5-10 mm:
pierderea mobilitii peretelui gastric;
defecte de umplere (imagini lacunare);
alterri ale mucoasei cu imagine de ulceraie i/sau zon extins de rigiditate a peretelui
gastric (linita plastic).
tomografia computerizat (torace, abdomen, pelvis) permite aprecierea:
extensiei tumorii primare;
implicrii ganglionilor limfatici regionali;
metastazelor la distan.
ecografia endoscopic (sonde de 7.5-12 MHz) este o modalitate de stadializare
complementar examenului CT, excelent pentru evaluarea:
extensiei n profunzime;
statusului ganglionilor regionali, perigastrici.
scintigrafia osoas se efectueaz n scopul detectrii metastazelor osoase, la pacieni:
simptomatici, cu dureri osoase sugestive;
asimptomatici, dar cu valori crescute ale fosfatazei alcaline.
gastrofibroscopia:
prezena tumorii de diferite aspecte (vegetant, ulcerat, linita plastic);
tumorile submucoase infiltrative sau extensia extramural la nivelul nervilor vagi pot fi
detectate prin alterri funcionale (peristaltism anormal, scderea distensibilitii pereilor
gastrici, tulburarea funciei pilorice) [6,7,8].
Ulcerele peptice persistente refractare la tratament trebuie prompt evaluate radiologic
(examen baritat) sau endoscopic !
laparoscopia (asociat sau nu cu ecografia laparoscopic):
detecteaz metastazele oculte hepatice sau peritoneale;
permite o stadializare cu o acuratee mai mare (este complementar evalurii CT);
laparotomia exploratorie determin extensia bolii cu mult mai mare exactitate dect
examinarea CT.
STADIALIZARE
Actualul sistem de stadializare TNM utilizat n CG nu ia n considerare:
localizarea tumoral la nivelul stomacului;
tipul histologic;
tipul creterii tumorale (linita plastic);
rezecabilitatea bolii [9].
184
Cancerul gastric
TABEL 6-4. Clasificarea stadial TNM AJCC/UICC 2002 (ediia a 6-a) a CG
T (tumora primar)
Tx tumora primar nu poate fi evideniat
To fr evidenierea tumorii primare
Tis carcinom in situ (tumor intraepitelial, fr invazia laminei propria)
T1 tumora invadeaz lamina propria sau submucoasa
T2 tumora invadeaz stratul muscular sau subseros*
* penetrarea stratului muscular, cu extensie la nivelul ligamentelor gastrocolic sau gastrohepatic sau al marelui,
respectiv al micului epiploon, fr perforarea seroasei peritoneale viscerale ce acoper aceste structuri, se
clasific drept T2; dac peritoneul visceral, ce acoper ligamentele gastrice sau epiploanele este perforat, atunci
tumora este clasificat drept T3.
T2a tumora invadeaz muscularis propria
T2b tumora invadeaz subseroasa
T3 tumora invadeaz seroasa visceral peritoneal
T4 tumora invadeaz structurile adiacente (splina, colonul transvers, ficatul, diafragmul,
pancreasul, peretele abdominal, glanda suprarenal, rinichiul, ansele intestinului subire,
retroperitoneul)**
** extensia intramural la nivelul duodenului sau esofagului este clasificat dup cel mai profund nivel de invazie,
pe oricare localizare, inclusiv stomacul.
N (adenopatiile loco-regionale)
Nx ganglionii regionali nu pot fi evideniai
No fr metastaze n ganglionii regionali
N1 metastaze n 1-6 ganglioni limfatici regionali
N2 metastaze n 7-15 ganglioni limfatici regionali
N3 metastaze n mai mult de 15 ganglioni regionali
** ganglionii regionali sunt cei situai de-a lungul marii i micii curburi, arterei gastrice stngi, hepatice comune,
splenice, celiace, i ganglionii hepatoduodenali. Alte adenopatii intra-abdominale (retropancreatice, mezenterice,
paraaortice) sunt clasificate drept metastaze la distan.
M (metastazele la distan)
Mx nu se evideniaz metastaze la distan
Mo fr metastaze la distan
M1 metastaze la distan prezente
pTNM Clasificarea patologic
Categoriile pT, pN i pM corespund categoriilor T, N i M clinice.
pNo Examinarea histologic va include obinuit 15 sau mai muli ganglioni.
Gruparea pe stadii
Stadiul 0 Tis No Mo
Stadiul IA T1 No Mo
Stadiul IB T1 N1 Mo
T2a/b No Mo
Stadiul II T1 N2 Mo
T2 N1 Mo
T3 No Mo
Stadiul IIIA T2a/b N2 Mo
T3 N1 Mo
T4 No Mo
Stadiul IIIB T3 N2 Mo
Stadiul IV T4 N1-3 Mo
T1-3 N3 Mo
Orice T Orice N M1
185
CANCERELE DIGESTIVE
PROGNOSTIC
Supravieuirea la 5 ani n CG local avansate este redus la 5-15%, n ciuda eforturilor
constante de ameliorare diagnostic i terapeutic. Circa 20% dintre pacieni se prezint
cu boal rezecabil. Riscul de recidiv loco-regional sau la distan este mai mare de
80%, chiar dup gastrectomia curativ [3].
Cel mai important element cu importan prognostic rmne diagnosticul precoce al
bolii. Este n continuare intens discutat importana limfadenectomiei regionale i a
extensiei acesteia.
Factorii asociai cu prognostic nefavorabil sunt:
vrsta avansat;
localizarea proximal;
pierderea ponderal >10%;
aspectul de linnitus plastica;
grad histologic sczut (G3-4);
invadarea a >4 ganglioni limfatici;
tumori aneuploide (flowcitometrie).
Analiza multifactorial a studiilor publicate relev ca factori prognostici semnificativi:
infiltrarea peretelui gastric (invazia sau nu a seroasei);
prezena metastazelor ganglionare [10].
PRINCIPII DE TRATAMENT
Tratamentul loco-regional: Chirurgia
Tratamentul chirurgical este unica soluie cu intenie curativ. Problema rmne aceea
de a stabili care sunt pacienii candidai la rezecie. n rile europene, circa 18% din
pacienii cu cancer gastric sunt inoperabili, 19% sunt supui unei intervenii paliative i
numai 37% sunt susceptibili de intervenie curativ.
Rezecia chirurgical rmne tratamentul definitiv n stadiile precoce de CG (T1-2), cu
supravieuiri la 5 ani de la 70% la 95%. Totui, formele de CG care, dei localizate, sunt
asociate cu extensie tumoral dincolo de submucoas, prezint supravieuiri la 5 ani de
doar 20-30% din cazuri [12].
Tratamentul chirurgical cu intenie curativ
Obiectivele tratamentului chirurgical n CG potenial curabile sunt: confirmarea
rezecabilitii, rezecia extins, stadializarea patologic ct mai corect, refacerea
continuitii tubului digestiv i a funciei gastro-intestinale.
Aprecierea posibilitilor de rezecie
Laparoscopia s-a dovedit o excelent modalitate pentru evaluarea extensiei i a
rezecabilitii bolii (naintea efecturii laparotomiei), fiind complementar explorrilor
imagistice prin acurateea diagnosticului nsmnrilor peritoneale sau al metastazelor
hepatice mici, nedecelabile prin alte metode; n cazul tumorilor nerezecabile,
laparoscopia reduce morbiditatea, timpul de spitalizare i costurile de diagnostic.
n plus, ecografia laparoscopic reuete s identifice leziunile cu risc crescut de
recidiv (T3-4), care necesit tratament chimioterapic neoadjuvant.
186
Cancerul gastric
Extensia rezeciei (aprecierea gradului de rezecie)
Rezecia gastric depinde de localizarea i de extensia tumorii primare. Gastrectomia
subtotal este preferat celei totale, care nu aduce nici un beneficiu pentru
supravieuire i este grevat de o morbiditate ridicat.
Singurele excepii n care poate fi aplicat gastrectomia total sunt: (a) cancerul treimii
superioare (proximale) a stomacului (caracterizat printr-o inciden crescut a penetrrii
seroasei, tumori mari ulcero-infiltrative, metastaze ganglionare); (b) infiltrarea tumoral
difuz sau tumora de corp gastric cu extensie pn la 6 cm spre cardia sau pilor.
Intervenia va include n aceste cazuri rezecia esofagului inferior (se asociaz frecvent
cu infiltrarea vaselor limfatice submucoase esofagiene), a duodenului proximal i
omentectomia. n tumorile cu localizare median sau distal este suficient o margine
de siguran de 5 cm la periferia tumorii macroscopice [14,15].
Extensia limfadenectomiei
Trebuie excizai cel puin 15 ganglioni limfatici pentru o stadializare N valabil.
Limitele rezeciei ganglionare n timpul gastrectomiei sunt nc un subiect de
controvers. De regul, limfadenectomia include lanurile limfatice situate de-a lungul
arterelor celiace, gastric stng, splenic i hepatic (nivel D2), ceea ce permite o
stadializare pTNM mai corect dect n cazul rezeciei ganglionare D1 (numai
adenopatiile paracardiale i perigastrice).
Limfadenectomia extins (D2 sau mai mult) a fost corelat cu o stadializare mai
precis, o mbuntire a controlului loco-regional i o cretere a supravieuirii (cu
excepia cazurilor cu metastaze peritoneale, diseminri ganglionare distale sau linit
plastic). n cazul CG depistat precoce, limfadenectomia sistematic poate anula
diseminarea ganglionar. Datele studiilor retrospective au artat c disecia D2 este
sigur i nu prezint o morbiditate excesiv de crescut (dei dou trialuri europene
mai recente indic o rat crescut a morbiditii i mortalitii).
Totui, innd cont de valoarea sa terapeutic, disecia D2 poate fi aplicat pe cazuri
selectate de pacieni i nu de rutin [12].
Rezecia organelor adiacente
Rezecia organelor adiacente este indicat n cazul diverselor complicaii ale CG,
cum ar fi ocluziile, perforaiile n cavitatea peritoneal sau penetrarea n organele
vecine. Splenectomia nu este indicat de rutin datorit ratei crescute a complicaiilor
ulterioare, cu excepia extensiei tumorale directe [14].
Tratamentul chirurgical paliativ
Deoarece supravieuirea pacienilor cu CG avansat este oricum redus, beneficiul
oricrei operaii efectuate, privit ca ameliorare simptomatic, trebuie s depeasc
morbiditatea i mortalitatea perioperatorie.
Indicaiile chirurgiei paliative sunt: durerea, hemoragia, disfagia i ocluzia.
Tehnica operatorie const n rezecia gastric paliativ sau by-pass-ul intestinal.
La anumii pacieni selecionai, rezecia tumorii primare realizeaz o ameliorare
simptomatic mai evident, chiar n prezena bolii reziduale macroscopice, cu o
morbiditate i o mortalitate acceptabile. Indicaiile de gastrectomie paliativ nu sunt
nc stabilite, depinznd de maniera de tratament a centrului spitalicesc n care este
internat bolnavul.
187
CANCERELE DIGESTIVE
Tratamentul loco-regional: Radioterapia
Radioterapia adjuvant
Carcinomul gastric este relativ rezistent la radioterapie (RT).
Radioterapia poate scdea rata recidivelor locale dar nu amelioreaz supravieuirea ca
modalitate unic postoperatorie. RT postoperatorie poate fi preconizat la pacienii care
nu sunt candidai pentru chimioterapie.
Pacienii cu tumori T3-T4 prezint un risc crescut de recidiv local dup tratamentul
chirurgical radical (ablaia tumorii macroscopice), chiar i cei fr adenopatii prezente
(No) avnd o supravieuire la 5 ani de doar 50%. Se pare c radioterapia extern
acioneaz asupra adenopatiilor regionale sau seroasei gastrice invadate, i sterilizeaz
marginile de rezecie [2,12].
Se poate administra o doz moderat de RT (40 Gy), eventual asociat cu
chimioterapia cu 5-fluorouracil (5-FU) i leucovorin.
Radioterapia paliativ
La pacienii cu recidiv local / metastaze, se utilizeaz uneori doze moderate de RT
extern, mai degrab n scopul paliaiei simptomelor dect al ameliorrii supravieuirii.
Recidiva gastric local/loco-regional sau adenopatiile metastatice survin n 40-65%
dintre pacieni dup o rezecie gastric cu intenie curativ. RT singur nu a
demonstrat un efect de cretere a supravieuirii, dar RT (DT 40 Gy, n 4 sptmni)
n asociaie cu 5-FU (15 mg/kg/zi I.V., n primele 3 zile de RT) poate ameliora
supravieuirea la pacienii cu boal localizat dar nerezecabil.
Aceast modalitate este limitat de posibilitile tehnice, riscurile inerente ale
iradierii abdominale, delimitarea optim necunoscut a cmpurilor de iradiere i
diminuarea statusului de performan al acestor pacieni.
La pacienii cu recidiv local focal se poate ncerca administrarea postoperatorie a
unor doze crescute de RT, n ncercarea de a prelungi supravieuirea, dei n literatura
actual nu exist date care s susin aceast indicaie [16].
n boala avansat, RT poate fi utilizat pentru paliaia hemoragiei gastrice, durerilor
i vomismentelor datorate obstruciei, metastazelor osoase sau cerebrale.
Dozele administrate pentru paliaia durerii sunt mai mici dect n terapia adjuvant
(DT
max
40 Gy).
Tratamentul sistemic: Chimioterapia
Multe citostatice au fost studiate pe parcursul a 20 ani n tratamentul CG. Dei ratele de
rspuns s-au ameliorat continuu, supravieuirea pacienilor cu boal avansat continu
s fie redus.
Monochimioterapia
Principalul chimioterapic studiat n monoterapie a fost 5-fluorouracil (5-FU), care a
demonstrat o rat de rspuns (RR) obiectiv de 21%. Ali ageni chimioterapici
investigai au fost mitomicina C (RR 30%), doxorubicina (RR 17%), cisplatin (RR
19%), ftorafur (RR 27%). Noii ageni de tipul taxanilor au demonstrat rspunsuri
obiective de 5% (paclitaxel) pn la 14% (docetaxel). Fluoropirimidinele orale (UFT,
capecitabin), camptotecin, oxaliplatin sunt n studiu. Capecitabina s-a demonstrat a nu
fi inferioar fa de 5-FU, iar eficacitatea oxaliplatin nu este inferioar cisplatin.
188
Cancerul gastric
Polichimioterapia
Asocierile de citostatice au fost utilizate pentru a ameliora rezultatele; s-au fcut
numeroase ncercri de a dezvolta protocoale de CHT mai eficiente (RR 5-50%). Pn
acum nici unul din protocoalele studiate nu s-a dovedit superior, din punct de vedere al
supravieuirii, comparativ cu monochimioterapia cu 5-FU.
Asocierea PF (cisplatin, 5-FU) a reprezentat protocolul "standard" n CG, n
principal datorit efectelor secundare relativ reduse.
Asocierea FAM (5-FU, adriamicin, mitomicina C) a fost larg utilizat n anii 1980;
RR obinute sunt de maxim 42%, cu o supravieuire median de 12,5 luni; este
asociat cu efecte secundare semnificativ mai mari dect monoterapia cu 5-FU, fr
beneficii suplimentare pentru supravieuire i durata rspunsului.
Asocierea FAMTX (5-FU, adriamicin, metotrexat), protocol ce aplic principiul
modulrii biochimice al 5-FU, determin RR de 40% (12% RC) i supravieuire
median de 7-12 luni. Nu prezint avantaje fa de monoterapia cu 5-FU.
Asocierea ECF (epirubicin, cisplatin, 5-FU) determin RR de 50-70% i supravieuiri
mediane de 10-17 luni; a devenit un standard n Canada i unele ri din Europa
(recomandare ESMO), fiind superior FAMTX [18].
Asocierea EAP (etoposid, adriamicin, cisplatin) determin RR de 50% n boala
metastatic i de 70% n boala localizat, cu supravieuiri mediane de 10-17 luni; este
mai puin benefic la pacienii cu carcinomatoz peritoneal i alte M1; determin
toxicitate important, cu decese n 10% din cazuri.
Asocierea ELF (etoposid, 5-FU modulat cu leucovorin) determin RR de 48% (12%
RC), supravieuire median de 10 luni; efectele secundare mai reduse o recomand la
pacienii vrstnici, cu funcie renal alterat.
Asocierea MLP-F (metotrexat, cisplatin, 5-FU i leucovorin) determin RR de 82%
(33% RC) i supravieuire median de 16 luni; acest regim amelioreaz rezultatele n
boala metastatic dar cu preul unei toxiciti severe la 25% din pacieni ce necesit
spitalizare; procentajul de RC este obinut i prin asocierea RT.
Asocierea FAP (5-FU, adriamicin, cisplatin) determin RR de 34% i supravieuire
median de 30 sptmni, dar cu o toxicitate secundar semnificativ.
Asocierea PELF (cisplatin, epirubicin, 5-FU cu leucovorin) determin RR de 43%,
cu preul unor efecte secundare importante.
Mai multe studii mari randomizate sunt n curs, comparnd de exemplu docetaxel i
cisplatin cu PF, sau irinotecan i cisplatin cu PF. Capecitabina i oxaliplatin ofer
alternative la 5-FU i cisplatin i sunt ncorporate n regimurile actuale de referin n
studiile clinice: ECF, ECX, EOF i EOX [23].
Foarte recent, o meta-analiz a studiilor randomizate de faz II i III care au evaluat
eficacitatea i tolerabilitatea chimioterapiei la pacienii cu cancer gastric (utiliznd
bazele de date Cochrane Controlled Trials Register, Medline, Embase i Cancerlitt)
pn n februarie 2005 ajunge la urmtoarea concluzie: Cele mai bune rezultate de
supravieuire sunt obinute prin utilizarea unei asocieri de trei citostatice coninnd
5-fluorouracil, o antraciclin i cisplatin. 5-FU administrat n bolus determin o rat mai
crescut de decese datorate toxicitii, spre deosebire de administrarea continu n
regimul cu epirubicin, cisplatin i 5-FU (ECF) [24].
189
CANCERELE DIGESTIVE
TABEL 6-5. Protocoale de chimioterapie n cancerul gastric
FAMTX
Metotrexat 1500 mg/m
2
I.V. ziua 1
5-Fluorouracil 1500 mg/m
2
I.V. (perfuzie 30), la 1h dup MTX ziua 1
Calciu folinat 15 mg/m
2
x 4/zi P.O. zilele 2-3
Doxorubicin 30 mg/m
2
I.V.(perfuzie 30) ziua 1
Se repet la fiecare 4 sptmni.
PLF
Cisplatin 50 mg/m
2
I.V. (perfuzie 15) zilele 1,15
Calciu folinat 500 mg/m
2
I.V. (perfuzie 30) nainte de 5-FU zilele 1,8,15,22
5-Fluorouracil 2600 mg/m
2
I.V. (perfuzie continu 24h) zilele 1,8,15,22
Se repet la fiecare 4 sptmni.
EFP (standard ESMO)
Epirubicin 50 mg/m
2
I.V. ziua 1
Cisplatin 60 mg/m
2
I.V. (perfuzie scurt) ziua 1
5-Fluorouracil 200 mg/m
2
I.V. (perfuzie continu 24h) ziua 1
Se repet la fiecare 3 sptmni (maxim 8 cicluri).
EAP
Etoposid 120 mg/m
2
I.V. zilele 4-6 sau
100 mg/m
2
I.V. (la pacienii cu vrste > 60 ani)
Adriamicin 20 mg/m
2
I.V. zilele 1,7
Cisplatin 40 mg/m
2
I.V. zilele 2,8
Se repet la fiecare 4 sptmni.
Protocoale experimentale, de linia a II-a
CI
Cisplatin 80 mg/m
2
I.V. (perfuzie scurt) ziua 1
Irinotecan 75 mg/m
2
I.V. (perfuzie scurt) zilele 1,15
Se repet la fiecare 3 sptmni.
DCF
Cisplatin 75 mg/m
2
I.V. (perfuzie 1h) ziua 1
Docetaxel 75mg/m
2
I.V. (perfuzie 1h) ziua 1
5-Fluorouracil 750 mg/m
2
I.V. (perfuzie continu 24h) zilele 1-5
Se repet la fiecare 3 sptmni (maxim 8 cicluri).
Chimioterapia neoadjuvant
Chimioterapia preoperatorie (nsoit sau nu de administrarea intraperitoneal de
citostatice) este n prezent studiat ntr-un numr de centre din SUA, aplicarea sa n
clinic necesitnd ns trialuri de faz III pentru confirmarea rezultatelor. Aparent,
amelioreaz procentul de rezecabilitate al tumorilor local avansate, pn la 72-77%, n
diverse studii, fr o cretere semnificativ a morbiditii i mortalitii perioperatorii.
Studiul NCRI MAGIC (503 pacieni) este primul ce identific un avantaj de
supravieuire pentru chimioterapia perioperatorie (24 luni vs. 20 luni). Pe baza
rezultatelor recente ale acestui trial, regimul ECF, preferat n Anglia i unele ri din
Europa, ar trebui considerat o opiune terapeutic preoperatorie la pacienii cu cancere
gastrice rezecabile. Beneficiile acestei atitudini sunt scderea volumului tumoral,
substadializarea, creterea susceptibilitii de rezecie curativ, a supravieuirii generale
i a intervalului liber de progresie a bolii [20].
190
Cancerul gastric
Chimioterapia adjuvant
Chimioterapia adjuvant singur nu a fost acceptat ca standard terapeutic, deoarece nu
i-a demonstrat eficacitatea n studiile mari randomizate de faz III, dei meta-analizele
sugereaz tendine spre obinerea unui beneficiu (redus). Mai mult, analiza de subset
demonstreaz c acest beneficiu se aplic numai n studiile ntreprinse n Asia i Europa
de Vest. Rolurile chimioterapiei intraperitoneale i a terapiilor biologice intite n
adjuvana CG rmn a fi definite [26].
Chimio-radioterapia
Pacienii cu CG n stadii avansate (T3-4, orice N, Mo) prezint un risc foarte crescut de
recidiv dup chirurgia potenial curativ (rezecia tuturor tumorilor macroscopice).
Asocierea chimio-radioterapiei preoperatorii la pacienii high-risk conduce la
beneficii aparente de reducere a bolii loco-regionale, de obinere a unei paliaii pe
termen lung i poate converti cancerele nerezecabile n rezecabile.
Asocierea chimio-radioterapiei postoperatorii n CG avansate este considerat un
standard n SUA, dar nu este acceptat pretutindeni n Europa datorit toxicitii
iradierii abdominale i a tipului de chirurgie recomandat.
Publicaii recente tind s acorde un beneficiu asocierii chimio-radioterapiei
postoperatorii numai n cazurile cu risc crescut de recidiv, unde aceasta poate ameliora
att supravieuirea general ct i supravieuirea fr recidiv.
Un studiu de referin (INT-0166) a demonstrat un beneficiu semnificativ de
supravieuire general (50% vs. 41%) i supravieuire fr boal (48% vs. 31%) pentru
chimio-radioterapia adjuvant comparativ cu chirurgia singur [21].
TABEL 6-6. Protocoale de chimio-radioterapie n cancerul gastric
Asociere secvenial:
5-Fluorouracil 425 mg/m
2
I.V. zilele 1-5
Acid folinic 20 mg/m
2
I.V. zilele 1-5
Se administreaz 1 ciclu naintea RT i 2 cicluri dup RT.
Asociere concomitent:
5-Fluorouracil 400 mg/m
2
I.V. zilele 1-4 i 33-35
Acid folinic 20 mg/m
2
I.V. zilele 1-4 i 33-35
Radioterapie 180 cGy, 5 zile/sptmn, 5 sptmni (DT 45 Gy)
Chimioterapia paliativ
Chimioterapia paliativ poate determina paliaia satisfctoare a simptomelor n CG
avansat (beneficiu clinic) i, uneori, remisiuni durabile.
n ultimele studii efectuate cu regimuri de tip FAMTX s-a obinut totui o ameliorare a
supravieuirii, fa de tratamentul simptomatic (supravieuire la 1 an de 40%, iar la 2 ani
de 10%, n timp ce aproape toi pacienii care primesc numai tratament simptomatic
decedeaz n cursul primului an de la diagnostic).
Asocierea DCF (docetaxel, cisplatin, 5-fluorouracil) a demonstrat un beneficiu clinic
(ameliorarea statusului Karnofsky, greutii corporale i supravieuirii fr durere), i
chiar prelungirea supravieuirii comparativ cu protocolul PF (cisplatin/5-FU) la pacienii
cu cancere gastro-esofagiene avansate (un singur studiu randomizat V325) [28].
191
CANCERELE DIGESTIVE
Chimioterapia intraperitoneal
Aplicarea chimioterapiei intraperitoneale se bazeaz pe apariia, obinuit n cancerul
gastric, a recidivelor peritoneale i hepatice, prnd capabil s trateze micrometastazele
cu aceast localizare. De asemenea, trebuie avut n vedere faptul c laparotomia crete
riscul de extensie abdominal i implantare la nivelul cavitii peritoneale.
Tratamentul se poate efectua cu mitomicin C, 5-FU i analogii si, cisplatin.
Citostaticele se introduc n timpul laparoscopiei exploratorii dup rezecia tumorii
primare i se las n cavitatea peritoneal 1-2 ore, ceea ce permite o mare intensitate
a dozei fr toxicitate sistemic. Diverse studii arat rezultate contradictorii, n ceea
ce privete ratele de rspuns i durata supravieuirii.
O modalitate deosebit o constituie perfuzia peritoneal hipertermic continu, care
se dovedete eficient numai n tratamentul bolii peritoneale de volum mic.
Principalele indicaii sunt prezena carcinomatozei peritoneale dup rezecia tumorii
primare, sau riscul crescut de recidiv cu aceeai localizare.
Procentele de supravieuire la 3 ani sunt mai crescute, comparativ cu pacienii netratai,
dar fr diferene semnificative.
Ca efecte secundare, poate afecta anastomoza operatorie sau prelungi ileusul
postoperator.
STRATEGIE TERAPEUTIC
n funcie de prezentarea bolii, se disting trei modaliti de abord terapeutic:
boala localizat chirurgia este opiunea principal, cu posibilitatea discutabil de a
utiliza radioterapia i/sau chimioterapia ca tratamente adjuvante;
boala local avansat nerezecabil radio- i/sau chimioterapia pot ameliora
supravieuirea numai la un numr redus de cazuri;
boala diseminat terapia este de obicei exclusiv paliativ i simptomatic [2].
Stadiul 0
Supravieuirea la 5 ani la pacienii tratai cu gastrectomie i limfadenectomie,
raportat n Japonia (unde CG este diagnosticat frecvent n stadiul 0), este mai mare
de 90%, fapt confirmat i de studiile americane [2,13,18].
Stadiul I
rezecie gastric subtotal (sau total n cazuri selecionate) i limfadenectomie
regional;
chimio-radioterapie postoperatorie recomandat la pacienii cu ganglioni pozitivi
(T1, N1) i cu invazia muscular (T2, No);
chimioterapie neoadjuvant n curs de evaluare clinic [2,13,18].
Stadiul II
intervenie chirurgical parial sau extins (n funcie de localizarea tumorii
primare, aa cum a fost descris anterior); rolul limfadenectomiei D2 este nesigur, i
unele studii semnaleaz o morbiditate secundar crescut;
chimioterapia adjuvant recomandat;
chimioterapia neoadjuvant n curs de evaluare clinic [2,13,18].
192
Cancerul gastric
Recomandri ESMO 2007:
Judecat prin prisma analizelor combinate, chimioterapia (CHT) pre- i postoperatorie
cu regimul ECF crete rata de rezecie R0, supravieuirea fr progresie i
supravieuirea general la pacienii cu adenocarcinoame gastrice sau eso-gastrice
(studiul european MAGIC). Pe baza acestui studiu, CHT perioperatorie cu regimuri tip
ECF poate fi considerat o alternativ la CHT-RT postoperatorie, la pacienii cu
adenocarcinoame gastrice i ale jonciunii esogastrice rezecabile.
CCHT adjuvant confer un beneficiu minim de supravieuire (III,C), dei acesta nu a
fost demonstrat n studiile individuale. Deoarece toxicitatea CHT postoperatorii este
considerabil, selecia atent a pacienilor pentru acest tratament este obligatorie [27].
Stadiul III
chirurgia radical rezecia curativ este rezervat pacienilor fr extensie
ganglionar regional la momentul explorrii chirurgicale;
chimioterapia adjuvant recomandat;
chimioterapia neoadjuvant n curs de evaluare clinic [2,13,18].
Toi pacienii cu tumori rezecabile vor fi operai, 15% din acetia putnd fi vindecai
chirurgical, n special dac extensia limfatic este minim (< 7 ganglioni regionali).
Supravieuirea general n condiiile aplicrii tratamentelor actuale uni- i multimodale
este ns sczut.
Terapia cazurilor cu rezecie incomplet/inoperabili rmne paliativ.
Toi pacienii din stadiul III de boal vor fi considerai candidai poteniali pentru
trialuri clinice.
Stadiul IV
chirurgia radical trebuie practicat ori de cte ori este posibil, urmat de CHT-RT;
chimioterapia neoadjuvant n curs de evaluare clinic.
Toi pacienii nou diagnosticai cu boal metastatic vor fi considerai candidai
poteniali pentru participarea la studii clinice.
Recomandri ESMO 2005:
Pacienii cu CG stadiul IV pot fi luai n considerare pentru chimioterapie paliativ.
Sunt utilizate n general asocieri cu cisplatin, 5-fluorouracil cu sau fr antracicline
(ECF, ECF), iar la pacienii vrstnici cu perturbri ale funcie renale se poate administra
asocierea PLF sau monoterapia cu 5-fluorouracil.
Asocierea ECF: epirubicin 50 mg/m
2
, cisplatin 60 mg/m
2
i 5-fluorouracil 200 mg/m
2
/zi
perfuzie continu 21 zile, este unul dintre cele mai active regimuri actuale (II,A).
Pot fi luate n considerare regimuri alternative ce includ: oxaliplatin, irinotecan,
docetaxel i fluoropirimidine orale (capecitabin, UFT) [24].
Boala recidivat
chimioterapia paliativ (FAP, ECF, PLF; 5-FU monoterapie);
terapia laser endoscopic / electrocauterizarea (posibil utile n leziunile obstructive);
radioterapia paliativ (combaterea hemoragiei, durerii i obstruciei) [22,24].
Pacienii selecionai vor intra n trialuri clinice de faz I i II cu noi ageni citostatici.
193
CANCERELE DIGESTIVE
REZULTATE
Rezultatele terapeutice actuale n cancerul gastric rmn nesatisfctoare.
Supravieuirea la 5 ani n absena invaziei seroasei gastrice variaz ntre 33-67%, dar
scade la valori de 15-20% n prezena acesteia. Prezena metastazelor ganglionare
reduce supravieuirea de la 35-40% (No) la 10-15% (N+).
n ciuda impactului pozitiv al CHT actual disponibile, prognosticul pacienilor cu CG
avansate inoperabile este dramatic, cu o supravieuire median de numai 7-10 luni n
majoritatea studiilor clinice. Dei beneficiile quod ad vitam ale CHT ar putea fi mai
mari la anumii pacieni, principiile tratamentului paliativ trebuie avute n vedere la
majoritatea acestora. n faa acestor cazuri trebuie mereu reamintit definiia OMS a
ngrijirii paliative: totalitatea interveniilor care asigur calitatea vieii pacientului i
familiei sale n faa problemelor asociate bolii ce amenin viaa.
Este posibil o ameliorare a rezultatelor prin utilizarea CHT i RT externe
neoadjuvante, a CHT postoperatorii n formele rezecabile i a noilor citostatice.
URMRIRE
Dei nu exist actual standarde de supraveghere a pacienilor cu CG dup tratamentul
chirurgical, efectuarea anamnezei i examenului clinic la fiecare 4 luni timp de un an,
apoi la 6 luni timp de 2 ani i ulterior anual, pare rezonabil. Vor fi solicitate examene
paraclinice i imagistice numai cnd sunt sugerate de prezena unor simptome clinice.
Deficitul de vitamin B
12
se poate dezvolta la majoritatea pacienilor cu gastrectomie
total i la 20% dintre cei cu gastrectomie subtotal, la un interval de 4-10 ani.
Suplimentarea de vitamin B
12
se face cu doze de 1000 g intramuscular lunar [18].
Urmrirea pacienilor dup rezecia gastric complet presupune inclusiv evaluarea
probelor hepatice, determinarea CEA i radiografia toracic.
Recomandri ESMO 2005:
Nu exist nici o dovad c urmrirea intensiv, regulat dup terapia iniial
amelioreaz rezultatele. n majoritatea cazurilor se recomand efectuarea vizitelor n
funcie de simptome (grad de recomandare D). n caz de apariie a simptomelor de
recidiv se va recomanda un examen fizic i teste sangvine. Investigaiile radiologice
trebuie luate n considerare la pacienii candidai pentru chimioterapie paliativ [25].
Bibliografie
1. Alberts RS, Goldberg RM. Gastrointestinal tract cancers. n: Casciato DA, ed. Manual of clinical
oncology. 5th ed. Philadelphia: Lippincott, Williams & Wilkins, 2004:185-195.
2. Pister PWT, Kelsen DP, Powell SM, et al. Cancer of the stomach. n: DeVita VT Jr, Hellman S,
Rosenberg SA, eds. Cancer - principles & practice of oncology. 7th ed. Philadelphia: Lippincott,
Williams & Wilkins, 2005:909-944.
3. Ungureanu G, Miron L. Cancerul gastric i duodenal. n: Ungureanu G, Covic M, eds. Terapeutica
medical. Iai: Editura Polirom, 2000:251-260.
4. Fine G, Chan K. Alimentary tract. n: Kissane JM, ed. Anderson's pathology. 8th ed. Saint Louis: CV
Mosby, 1985:1055-1095.
5. Maehara Y, Sakaguchi Y, Moriguchi S, et al. Signet ring cell carcinoma of the stomach. Cancer 1992;
69(7):1645-1650.
6. Gunderson LL, Donohue JH, Alberts SR. Cancer of the stomach. n: Abeloff MD, ed. Clinical oncology.
3th ed. New York: Elsevier Churchill Livingstone, 2004:1819-1862.
7. Robustelli della Cuna G, Bondadonna G. Neoplasie dell aparato dirigente. n: Bonadonna G, ed.
Medicina oncologica. 7ma ed. Milano: Masson, 2003:954-969.
194
Cancerul gastric
8. Bonin SR, Roderich E, Scwartz RE. Gastric cancer. n: Pazdur R, ed. Cancer management: a
multidisciplinary approach. 7th ed. New York: CMP, 2004:259-271.
9. American Joint Committee on Cancer. Stomach. In: AJCC Cancer Staging Manual. 6th ed. New York:
Springer, 2002:99-106.
10. Miron L. Cancerul gastric. n: Bild E, Miron L, ed. Terapia cancerului - ghid practic. Iai: Editura
Tehnopress, 2003:125-130.
11. Miron L. Cancerul gastric. n: Miron L, Miron I, eds. Chimioterapia cancerului: principii i practic.
Iai: Editura Kalos, 2005:182-217.
12. Saif MW. Gastric cancer. n: Abraham J, Allegra CJ, Gulley J, eds. Bethesda handbook of clinical
oncology. 2nd ed. Philadelphia: Lippincott Williams & Wilkins, 2005:73-90.
13. Hundahl SA, Macdonald JS, Smalley SR. Stomach.. n: Chang AE, Ganz PA, Hayes DF, eds. Oncology -
an evidence based approach.. New York: Springer, 2006:680-703.
14. Brennan MF, Karpeh MS Jr. Surgery for gastric cancer: the American view. Semin Oncol 1996;
23(3):352-9.
15. Bozzetti F, Marubini E, Bonfanti G, et al. Subtotal versus total gastrectomy for gastric cancer: five-year
survival rates in a multicenter randomized Italian trial. Italian Gastrointestinal Tumor Study Group. Ann
Surg 1999;230(2):170-8.
16. Macdonald JS, Smalley SR, Benedetti J, et al. Chemoradiotherapy after surgery compared with surgery
alone for adenocarcinoma of the stomach or gastroesophageal junction. N Engl J Med 2001;345(10):725-
730.
17. Kelsen DP. Postoperative adjuvant chemoradiation therapy for patients with resected gastric cancer:
Intergroup 116. J Clin Oncol 2000;18(suppl.21):32S-40S.
18. Benson Al B III. Carcinomas of the gastro-intestinal tract. n: Skeel RT, ed. Handbook of cancer
chemotherapy. Philadelphia: Lippincott. Williams & Wilkins, 2003:231-293.
19. Bugat R. The treatment of gastric cancer. State of the art and new drugs. n: Proceeding Book of the 15th
International Congress on Anti-Cancer Treatment (ICACT). Paris, 2004:22-23.
20. Medical Research Council Oesophageal Cancer Working Party. Surgical resection with or without
preoperative chemotherapy in oesophageal cancer: a randomised controlled trial. Lancet 2002;
359(9319):1727-1733.
21. National Comprehensive Cancer Network. Gastric cancer. n: NCCN Clinical Practice Guidelines in
Oncology, June 2006. www.nccn.org
22. Starling N, Cunningham D. The role of systemic therapy for localised gastric cancer. Ann Oncol 2006;
17(suppl.10):x115-x121.
23. Wagner AD, Grothe W, Haerting J, et al. Chemotherapy in advanced gastric cancer: a systemic review
and meta-analysis based on aggregate data. J Clin Oncol 2006;24:2903-2909.
24. Cunningham D, Jost LM, Purkalne G, et al. ESMO Minimum clinical recommendations for diagnosis,
treatment and follow-up of gastric cancer. Ann Oncol 2005;16(suppl.1):i22-i24.
25. Benson Al-B III. Carcinomas of the gastro-intestinal tract. In: Skeel RT, ed. Handbook of cancer
chemotherapy. Philadelphia: Wolter Kluwer/Lippincott, Williams & Wilkins, 2007:263-289.
26. Mahtani RL, Rodger JW, Macdonald JS. Gastric cancer: adjuvant therapy. In: Macdonald JS, ed.
Advances in the management of gastric cancer. New York: COAB CMP Oncology, 2006:35-53.
27. Cunningham D. Gastric cancer: ESMO Clinical recommendations for diagnosis, tratment and follow-up.
Ann Oncol 2007;18(suppl.2):ii17-ii18.
28. Ajani JA, Moiseyenko VM, Tjulandin S, et al. Clinical benefit with docetaxel plus fluorouracil and
cisplatin compared with cisplatin and fluorouracil in a phase III trial of advanced gastric or gastro-
esophageal cancer adenocarcinoma: The V-225 Study Group. J Clin Oncol 2007;25(22):3205-3209.
195
CANCERELE DIGESTIVE
196
Cancerele intestinului subire
EPIDEMIOLOGIE
Tumorile intestinului subire reprezint 1-2% din toate neoplaziile gastro-intestinale.
Factorii de risc pentru cancerul intestinului sunt:
sindromul Peutz-Jeghers (transformare malign 2-3%);
sindromul Gardner;
boala Crohn;
neurofibromatoza [1].
HISTOLOGIE
Marea majoritate a neoplaziilor intestinale este reprezentat de tumorile benigne (35%),
restul cazurilor fiind adenocarcinoame (> 50%), limfoame (22%), tumori carcinoide
(11%) i sarcoame (7%).
Tumorile maligne se distribuie la nivel duodenal (25%), jejunal (27%) i ileal (48%).
Adenocarcinoamele reprezint majoritatea tumorilor maligne ale intestinului subire,
mai ales duodenale (35%) supraampular/periampular/subampular i jejunale (39%).
Tumorile carcinoide ale intestinului subire sunt privite ca o entitate separat (prezentat
n capitolul Tumori endocrine) [2].
DIAGNOSTIC
Elementele sugestive pentru diagnosticul clinic sunt:
mas abdominal palpabil;
semne de ocluzie intestinal;
durere abdominal persistent;
hemoragii oculte n materiile fecale / hemoragie digestiv de origine neclar [3].
Diagnosticul paraclinic este dificil, n absena semnelor radiologice de ocluzie
intestinal, mai ales pentru tumorile primare jejunale sau ileale.
STADIALIZARE
Stadializarea carcinoamelor de intestin subire se face conform sistemului TNM UICC
1997, care a rmas nemodificat n ediia a 6-a TNM AJCC/UICC 2002 [4].
TABEL 6-7. Clasificarea TNM AJCC/UICC 2002 a carcinoamelor de intestin subire
T (tumora primar)
Tx tumora primitiv nu este definit
To fr evidena tumorii primare
Tis carcinom in situ
T1 tumora invadeaz lamina proprie sau submucoasa
T2 tumora invadeaz musculara proprie
T3 tumora depete musculara proprie, sau invadeaz submucoasa, sau trece n esutul
perimuscular, neperitonealizat (mezenter/ retroperitoneu, cu extensie 2 cm)
T4 tumora perforeaz peritoneul visceral, invadeaz direct alte organe sau esuturi
(inclusiv ansele intestinului subire), mezenterul, retroperitoneul (>2 cm), peretele
abdominal (pe cale seroas) sau duodenul, inclusiv invazia pancreasului
Cancerele intestinului subire
N (adenopatiile loco-regionale)
Nx ganglionii limfatici regionali nu sunt definii
No absena metastazelor n ganglionii regionali
N1 metastaze la nivelul ganglionilor regionali
M (metastazele la distan)
Mo absena metastazelor la distan
M1 prezena metastazelor la distan
pTNM Clasificarea patologic
Categoriile pT, pN i pM corespund categoriilor T, N, M clinice.
pNo - Examenul histologic dup limfadenectomia regional trebuie s cuprind 10 ganglioni.
Gruparea pe stadii
Stadiul 0 Tis No Mo
Stadiul I T1 No Mo
Stadiul II T2-4 No Mo
Stadiul III orice T N1 Mo
Stadiul IV orice T orice N M1
PROGNOSTIC
Majoritatea cancerelor de intestin subire sunt diagnosticate n faze avansate de boal,
datorit simptomatologiei nespecifice. n general, prognosticul nu este favorabil: dup
extirparea chirurgical complet, supravieuirea global la 5 ani este de 25%.
Stadiul bolii este cel mai important factor predictiv pentru supravieuire n
adenocarcinoamele intestinului subire; ali factori prognostici adveri sunt vrsta
(mai mare de 75 ani) i localizarea duodenal. Supravieuirea general la 5 ani este
de 20% (65%, 48%, 35% i 4% pentru stadiile I, II, III, i respectiv IV) [5].
n limfoamele intestinului subire, tratamentul multimodal asigur o supravieuire
global la 5 ani de 50%.
n general, leiomiosarcomul prezint un prognostic mai favorabil dect
adenocarcinomul, dup chirurgia cu intenie curativ supravieuirea la 5 ani fiind de
50-75%. n cazul rezeciilor paliative, supravieuirea la 5 ani este de 25%.
Carcinoidele intestinului subire tind s prezinte o evoluie clinic indolent. Acestea
rmn localizate la nivelul intestinului subire, sperana de via fiind asemntoare
cu cea a populaiei generale. Extensia la ganglionii regionali n cazul tumorilor
complet rezecabile comport o supravieuire la 5 ani de 80%. Aproximativ 50% din
pacienii cu tumori nerezecabile i circa 30% din pacienii cu diseminri hepatice
sunt n via la 5 ani. Odat cu apariia sindromului carcinoid, durata medie de
supravieuire este de circa 3 ani [7].
EVOLUIE
Adenocarcinoamele intestinului subire metastazeaz n ganglionii regionali i ulterior
n ficat, plmn i os. Sarcoamele disemineaz hematogen la nivel pulmonar, hepatic i,
mai rar, n ganglionii limfatici regionali.
Complicaiile mai frecvente sunt: ocluzia, invaginaia, perforaia intestinal i
hemoragia. Sindromul carcinoid comport apariia unor episoade paroxistice de: astm
bronic, fenomene vasomotorii i tulburri acute de tranzit [6].
197
CANCERELE DIGESTIVE
PRINCIPII DE TRATAMENT
Prima opiune terapeutic este rezecia chirurgical, cnd aceasta este posibil.
Chimioterapia (CHT) se administreaz fr rezultate semnificative; radioterapia (RT) nu
este utilizat n general.
Tratamentul loco-regional: Chirurgia
Chirurgia reprezint tratamentul de elecie i presupune rezecia segmentar cu margini
largi a intestinului (> 10 cm proximal i distal), cu ablaia ganglionilor regionali i a
mezenterului adiacent.
n neoplaziile duodenale, se practic duodeno-cefalopancreatectomia.
n localizarea ampular se practic o intervenie care s conserve pilorul, pentru a
menine activitatea funcional a stomacului.
Rolul chirurgiei de citoreducie tumoral (debulking) n formele local avansate de
cancere intestinale rmne controversat.
n prezena metastazelor hepatice, dup rezecia tumorii primare se poate recurge la
metastazectomie, lund n consideraie posibilitatea ameliorrii simptomelor (scop
paliativ) i eventual prelungirea supravieuirii.
Ca i n alte neoplazii gastro-intestinale, chirurgia reprezint modalitatea principal de
tratament i ratele de vindecare sunt proporionale cu posibilitatea de rezecie complet.
Supravieuirea general la 5 ani n tumorile complet rezecate este de numai 20%. Ratele
de supravieuire la 5 ani la pacienii cu leiomiosarcom (cea mai frecvent form de
sarcom primar a intestinului subire) rezecat sunt de aproximativ 50% [7].
Tratamentul loco-regional: Radioterapia
Radioterapia (RT) are indicaii clare (limitate) doar n limfoamele intestinului subire.
Tratamentul sistemic: Chimioterapia
Experiena utilizrii chimioterapiei n adenocarcinoamele intestinului subire este
redus, motiv pentru care se prefer aplicarea principiilor valabile n tratamentul
cancerelor de colon. n general, rezultatele sunt ns dezamgitoare.
Cele mai utilizate citostatice sunt 5-fluorouracil (5-FU) i mitomicina C, ce au demonstrat
un nivel cert, dei modest, de activitate.
Asocierea la 5-FU a doxorubicinei, BCNU sau ciclofosfamidei nu a demonstrat o ameliorare
substanial a rezultatelor.
Chimioterapia adjuvant nu se poate recomanda n adenocarcinoamele intestinului
subire pe baza datelor obiective actuale.
Chimioterapia adjuvant este indicat n cazul limfoamelor intestinale cu urmtorii
factori de risc nefavorabili prezeni:
histologia de limfom de nalt agresivitate (cu celule mari);
mas abdominal de mari dimensiuni (diametru > 7 cm);
stadiul avansat n clasificarea Ann Arbor.
Se utilizeaz asociaiile chimioterapice utilizate n limfoamele maligne cu debut
ganglionar (a se vedea capitolul Limfoame maligne non-hodgkiniene), cu supra-
vieuiri la 5 ani ntre 40-50%.
Nici n cazul leiomiosarcoamelor intestinale chimioterapia nu ntrunete suficiente
argumente de eficacitate spre a fi recomandat de rutin.
198
Cancerele intestinului subire
Chimioterapia se recomand n cazul tumorilor carcinoide n faz avansat,
nerezecabile, n prezena a cel puin 4 elemente:
afectare hepatic funcional prin progresia bolii;
tumora cu cretere rapid;
prezena de semne prognostice nefavorabile;
excreiei urinare de 5-HIAA mai mare de 150mg/zi.
Asociaia citostatic cea mai eficace include: streptozocin, 5-FU, antraciclin.
Eficacitatea terapiei cu IFN- recombinat este redus (RR < 20%), dar este n msur s
controleze satisfctor (40-50% cazuri) simptomatologia (diaree i flush cutanat) i s
reduc chiar i secreia urinar de 5-HIAA [8].
STRATEGIA TERAPEUTIC
Opiunile standard de tratament n neoplaziile intestinului subire variaz n funcie de
stadiu i de histologia tumorii.
Adenocarcinoame
Tumori de mici dimensiuni (rezecabile)
Opiunea standard este rezecia chirurgical radical.
Tumori nerezecabile / metastatice
Se opteaz pentru:
by-pass chirurgical al leziunii obstructive;
radioterapie (RT) paliativ;
tehnicile de radio-chimioterapie concomitent (CHT cu rol de radiosensibilizare) n
curs de evaluare;
testarea de noi citostatice (ex. derivaii de camptotecin) n studii de faz I i II n
boala metastatic.
Leiomiosarcoame
Opiunile terapeutice sunt identice cu cele aplicabile n adenocarcinoame.
n faa histologiei de leiomiosarcom intestinal se va avea n vedere i posibilitatea
diagnosticului de tumor gastro-intestinal stromal (TGIS), motiv pentru care trebuie
solicitat un examen imunohistochimic pentru depistarea expresiei proteinei c-Kit.
Limfoame
Tumori localizate la peretele intestinal (IE)
Opiunile terapeutice standard sunt:
rezecia chirurgical singur cu prelevarea a minimum 12 ganglioni i examen
histologic extemporaneu;
dac ganglionii sunt negativi (No) se poate recomanda chimioterapia opional;
n cazul extensiei bolii la ganglionii regionali (N+), CHT este tratamentul de elecie.
Tumori avansate nerezecabile
Se recomand:
polichimioterapie;
RT ar putea reduce riscul recidivelor n patul tumoral.
199
CANCERELE DIGESTIVE
Tumori gastro-intestinale stromale (TGIS)
Tumori rezecabile
Tratamentul standard este chirurgia radical:
rezecie intestinal segmentar, cu excizia n bloc a oricrei structuri aderente, dar
fr excizia extensiv a mezenterului (deoarece nu se cunoate riscul de metastazare
ganglionar)
Tumori nerezecabile / metastatice
Se pot avea n vedere urmtoarele opiuni terapeutice:
by-pass chirurgical (paliativ) al leziunilor obstructive / nerezecabile;
rezecie paliativ;
RT paliativ;
CHT paliativ;
imatinib mesilat n TGIS metastatice (a se vedea capitolul Tumori gastro-
intestinale stromale).
Boala recidivat
n boala recidivat local se poate recomanda:
chirurgia;
RT paliativ;
CHT paliativ:
n adenocarcinoamele sau TGIS de intestin subire recidivate nu exist o chimioterapie
considerat eficace.
n limfoamele recidivate, chimioterapia rmne tratamentul principal.
includerea n studii clinice care s evalueze noi modaliti terapeutice precum
chimio-radioterapia [6].
Bibliografie
1. Zeh H III. Cancer of the small intestine. In: DeVita VT Jr, Hellman S, Rosenberg SA, eds. Cancer:
principles & practice of oncology. 7th ed. Philadelphia: Lippincott, Williams & Wilkins, 2005:1035-48.
2. Serour F, Dona G, Birkenfeld S, et al. Primary neoplasms of the small bowel. J Surg Oncol 1992;
49(1):29-34.
3. Robustelli della Cuna G, Gennari L. Neoplasie dell apparecchio dirigente. n: Bonadonna G, ed.
Medicina oncologica. Milano: Masson, 1999:907-913.
4. American Joint Committee on Cancer. Small intestine. In: AJCC Cancer Staging Manual. 6th ed. New
York: Springer, 2002:107-112.
5. Rose DM, Hochwald SN, Klimstra DS, et al. Primary duodenal adenocarcinoma: a ten-year experience
with 79 patients. J Am Coll Surg 1996;183(2):89-96.
6. North JH, Pack MS. Malignant tumors of the small intestine: a review of 144 cases. Am Surg 2000;
66(1):46-51.
7. Coit DG. Cancer of the small intestine. In: DeVita VT Jr, Hellman S, Rosenberg SA, eds. Cancer:
principles and practice of oncology. 6th ed. Philadelphia: Lippincott, Williams & Wilkins, 2001:1204-
1216.
8. Donohue JH. Adenocarcinoma and other small intestinal malignancies. In: Chang AE, Ganz PA, Hayes
DF, eds. Oncology - an evidence based approach. New York: Springer, 2006:733- 745.
9. National Comprehensive Cancer Network. Small Intestine Cancer. In: NCCN Clinical practice guidelines
in oncology, January 2007. www.nccn.org
10. Benson Al-B III. Carcinomas of the gastro-intestinal tract. In: Skeel RT, ed. Handbook of cancer
chemotherapy. Philadelphia: Wolter Kluwer Lippincott, Williams & Wilkins, 2007: 269-270.
200
Tumorile gastro-intestinale stromale
201
Tumorile gastro-intestinale stromale
Tumorile gastrointestinale stromale (TGIS) sunt cele mai frecvente tumori
mezenchimale care survin la nivelul aparatului digestiv (80%), reprezentnd circa 5%
din toate sarcoamele de pri moi, dar numai 3% din tumorile gastrointestinale. nainte
de apariia imunohistochimiei, majoritatea sarcoamelor cu celule fusiforme ale tubului
digestiv erau clasificate ca leiomioame sau leiomiosarcoame (datorit similitudinii
histologice cu muchiul neted) i, ocazional, ca tumori neurogene [1].
Iniial, termenul de TGIS a fost unul pur descriptiv, dezvoltat n 1983 de ctre Mazur i
Clark pentru a defini neoplasmele gastrointestinale non-epiteliale care nu prezentau
trsturi imunohistochimice de celule Schwann i nici caracteristici ultrastructurale
specifice muchiului neted [2].
EPIDEMIOLOGIE
Epidemiologia TGIS este incomplet cunoscut. Incidena este de aproximativ 11-15
cazuri/milion locuitori/an, cu o prevalen de 10-20 cazuri la un milion de locuitori.
La momentul prezentrii, majoritatea pacienilor cu TGIS sunt n decada a cincea sau a
asea de via, rareori, unele TGIS sunt diagnosticate la pacienii cu vrste mai mici de
40 ani (vrsta medie 66-69 ani).
Nu este demonstrat nici o relaie de: ras, etnie, ocupaie sau distribuie geografic, dar
exist o discret predominen masculin [3].
HISTOLOGIE
TGIS sunt tumori cu celularitate moderat sau bogat, morfologic heterogene, de la
aspectul cu celule fusiforme (spindle-cell) la tipul epitelioid i variate forme mixte:
forma fusiform (70-80%):
celule alungite cu nucleu aplatizat i citoplasm bazofil sau eozinofil;
pot simula tumori de muchi neted sau tumori de teac neural;
pot prezenta vascularizaie bogat, hemoragii, hialinizare sau degenerescen mixoid.
forma epitelioid (20-30%):
celule rotunde sau poligonale cu nuclei rotunzi centrali sau excentrici; acestea pot prezenta
mitoze dar tipic prezint o evoluie mai benign spre deosebire de varianta cu celule
fusiforme [4].
Majoritatea TGIS se dezvolt din tunica extern muscular i din acest motiv sunt
predominant exofitice (se dezvolt de-a lungul peretelui intestinal, protuznd n
cavitatea abdominal). n tumorile mici, mucoasa suprajacent este frecvent intact, dar
ulcerarea poate apare n cele mari, agresive.
Agresivitatea TGIS a fost subestimat. Circa 50% din TGIS sunt metastatice sau
clasificate cu risc crescut la momentul diagnosticului [8].
Invazia organelor de vecintate poate fi semnalat n 1/3 din cazuri. Metastazele sunt
frecvente i pot fi observate n 50% din cazuri. Ficatul este cel mai frecvent afectat
(65%), urmat de peritoneu (21%). Metastazele n ganglionii limfatici, pulmonare i
osoase sunt considerate rare [10].
Majoritatea pacienilor dezvolt recidive dup rezecia chirurgical complet. Sediile
cele mai frecvente de recidiv sunt ficatul i peritoneul [5].
CANCERELE DIGESTIVE
Biologie molecular
TGIS definesc un grup distinct de tumori gastrointestinale cu originea n celulele
interstiiale Cajal (CIC), care acioneaz ca reglatoare ale peristaltismului intestinal (rol
de pace-maker). CIC exprim n mod normal c-Kit (CD117) receptor tirozinkinazic
tip III pentru factorul de cretere al celulei stem (SCF).
Aproximativ 95% din TGIS prezint coloraie pozitiv pentru c-Kit (CD117), care
reprezint cea mai bine definit caracteristic imunoreactiv a TGIS i le difereniaz
de tumorile cu origine real n muchiul neted (ex. leiomioame i leiomiosarcoame)
i de cele derivate din creasta neural (ex. schwanoame i neurofibroame) [6].
c-Kit este o glicoprotein membranar care servete ca receptor pentru SCF i prezint activitate
tirozinkinazic, corelat cu expresia receptorului de cretere a plachetelor (PDGF), factorul de
stimulare a macrofagelor i ligandul FLT3. Funcia c-Kit este critic pentru funcionarea CIC i a
precursorului celulelor hematopoietice, mastocitelor i celulelor germinale. SCF este responsabil
pentru promovarea creterii tumorale i prevenirea morii celulare n multe din aceste neoplasme.
Imunocoloraia poate fi pozitiv i pentru ali markeri: Bcl-2 (80%), CD34 (70%), actina specific
muscular (50%), actina muchiului neted (35%), proteina neural S-100 (10%) i desmina (5%).
Totui, i alte tumori maligne (melanoamele maligne, seminoamele, sarcoamele i
unele leucemii) pot exprima CD117. Din fericire, distincia dintre TGIS i acestea
poate fi efectuat pe criterii histologice [7].
TGIS sunt caracterizate i prin mutaii la nivelul genei c-Kit, localizat pe braul lung
al cromozomului 4 (4q11-q12), care codific un receptor tirozinkinazic implicat n
transducerea semnalului biologic la nivel extracelular. Proto-oncogena c-KIT
prezint un rol n dezvoltarea hematopoiezei normale, ca i n migrarea celulelor
stem, fiind exprimat pe mastocitele umane, celulele mieloide, melanocite, celulele
epiteliale mamare i CIC normale.
DIAGNOSTIC
Examen clinic
TGIS pot surveni n orice parte a tubului digestiv, cel mai frecvent n stomac (> 70%) i
intestinul subire (20-30%), dar pot apare i la nivelul rectului (5%), esofagului (2%) i
n localizri variate (5%) precum: vezica biliar, pancreas, mezenter, epiplon i
retroperitoneu. Manifestrile clinice sunt foarte variabile, depinznd de localizare i de
dimensiunea tumorii.
Frecvent, TGIS de dimensiuni reduse (obinuit asimptomatice, datorit originii
submucoase i tendinei de cretere exofitice) sunt diagnosticate ocazional, n cursul
unei explorri imagistice, endoscopice sau al unei intervenii chirurgicale.
Dimensiunile tumorilor sunt n general situate ntre 2 i 30 cm la momentul
diagnosticului. Cele mai frecvente simptome sunt: hemoragia digestiv acut
(ulceraii mucoase sau ruptur tumoral [25%]), anemia (hemoragii oculte), senzaia
de disconfort, plenitudine sau durerea abdominal; o mas abdominal palpabil se
poate ntlni la unii pacieni. Localizarea submucoas poate determina obstrucie sau
perforaie, n special n localizrile esofagiene sau de intestin subire. Tumorile
esofagiene se pot prezenta cu disfagie, iar cele care survin n duoden se pot asocia cu
compresiunea capului pancreatic cu febr i icterul. TGIS rectale se pot asocia cu
simptom de efect de mas precum: disuria, flux urinar ntrerupt datorat invaziei
vezicii urinare [10].
202
Tumorile gastro-intestinale stromale
Investigaii imagistice
Pentru evaluarea TGIS sunt disponibile mai multe metode imagistice ce includ:
ecografia abdominal, examenul computer tomografic (CT), imagistica n rezonan
magnetic (IRM) i tomografia cu emisie de pozitroni (PET).
Examenul CT este de elecie n evaluarea TGIS, fiind accesibil i cu acuratee
crescut (particular pentru metastazele hepatice). Poate furniza informaii utile pentru
diferenierea TGIS de limfoame i tumorile epiteliale gastrointestinale, i pentru
diagnosticul ocluziei intestinale (30% din TGIS). Ocazional, pot fi detectate prin CT
tumorile intestinale mici; poate, de asemenea, ghida biopsia transparietal. Odat cu
introducerea noilor terapii moleculare, examenul CT are un rol important n
evaluarea rspunsului la tratament i a recidivelor n TGIS [8,11].
Diagnostic diferenial
Deoarece TGIS prezint un spectru morfologic relativ mare, diagnosticul diferenial
include un numr de tumori mezenchimale, neurale i neuroendocrine ce pot aprea n
abdomen: leiomioame, leiomiosarcoame, schwanoame, tumori solitare fibroase, tumori
mioblastice inflamatorii, fibromatoz, sarcom sinovial, tumori neuroendocrine
pancreatice (carcinoide i insulare), tumori de glomus gastric, mezoteliom malign,
angiosarcom carcinom sarcomatoid.
Fibromatoza i leiomiosarcomul sunt entitile clinico-patologice cel mai frecvent
confundate cu TGIS.
Succesul recent n tratamentul TGIS cu imatinib mesilat (Glivec
) a deschis o nou
prioritate n a efectua acest diagnostic cu acuratee [9].
PROGNOSTIC
Majoritatea TGIS prezint un potenial malign incert. Aprecierea riscului de recidiv
este important, deoarece se va pune problema unui tratament adjuvant.
Progresia acestor tumori urmeaz o evoluie caracteristic, care include recidiva la
nivelul rezeciei, diseminarea intra-abdominal sau seroas i dezvoltarea metastazelor
hepatice. Se menioneaz c i n TGIS cu risc sczut, recidivele se pot ntlni chiar i
dup 20 ani. Din acest motiv, majoritatea experilor nu consider TGIS ca entiti cu
adevrat benigne [11,12].
Vrsta, indexul mitotic i mrimea tumorii primare (< 5 cm vs. > 5 cm) sunt factori
prognostici independeni.
Supravieuirea la 5 ani este de 20% n tumorile cu diametru > 10 cm i de aproximativ 60%
n cele cu diametru < 5 cm. Tumorile de dimensiuni mici (< 1cm) descoperite incidental
sunt aproape invariabil benigne [10].
Tumorile cu activitate mitotic crescut (> 50 de mitoze pe cmpul microscopic de nalt
rezoluie) sunt considerate agresive, cu potenial crescut de malignitate.
Pacienii cu ruptura tumorii n cavitatea abdominal nainte sau n timpul chirurgiei
prezint un risc foarte crescut de recidiv [12].
Aneuploidia este un factor prognostic negativ pentru TGIS, dar analiza prin
citometria de flux nu este utilizat n practica diagnostic curent.
O alt trstur prognostic este localizarea tumoral.
Mai multe studii au demonstrat c tumorile cu localizare primar gastric prezint un
prognostic mai bun dect cele localizate la nivelul intestinului subire sau rectului.
203
CANCERELE DIGESTIVE
TABEL 6-8. Evaluarea riscului de recidiv n TGIS rezecabile [12]
Categoria de risc Mrime T Indice mitotic
Risc foarte redus < 2 cm < 5/50 CRI
Risc sczut 2-5 cm < 5/50 CRI
Risc intermediar < 5 cm 6-10/50 CRI
5-10 cm < 10/50 CRI
Risc crescut > 5 cm > 5/50 CRI
> 10 cm orice rat mitotic
orice dimensiune > 10/50 CRI
CRI - per cmp microscopic de rezoluie nalt
TABEL 6-9. Factorii prognostici pentru TGIS localizate [12,23]
Prognostic Favorabil Intermediar Nefavorabil
Tipul histologic fusiform epiteloid mixt
Mitoze CRI <3 3-15 >15
Tipul mutaiei Kit missens exon 11 deleii, inserii exon 11 mutaii exon 9 sau 13
Mrimea tumorii <5 cm 5-10 cm >10 cm
Sex feminin masculin
CRI - per cmp microscopic de rezoluie nalt
PRINCIPII DE TRATAMENT
n general, tratamentul optim pentru TGIS este chirurgia; formele nerezecabile i
metastatice prezint un prognostic nefavorabil, cu o supravieuire median de 12 luni i
un rspuns slab la chimioterapia uzual a sarcoamele de pri moi [13].
Tratamentul loco-regional: Chirurgia
Chirurgia reprezint principala terapie la pacienii cu TGIS primare, localizate, al
crei scop principal este rezecia tumoral total.
Pentru TGIS rezecabile, confirmarea histologic preoperatorie nu este necesar (risc
crescut de ruptur, hemoragie sau diseminare).
Din aceleai motive, tumora trebuie nlturat chirurgical n bloc (margini de rezecie n
esut sntos). Limfadenectomia extins nu este necesar de rutin, deoarece
metastazele ganglionare sunt rare.
Rezultatele sunt relativ bune pentru pacienii cu tumori cu risc sczut sau
intermediar, dar recidiva este aproape inevitabil (80-90% din cazuri), chiar dup
rezecia complet, n cazul tumorilor de risc crescut; supravieuirea la 5 ani n aceste
cazuri este de 54%.
Datorit evoluiei imprevizibile postoperatorii este necesar urmrirea prin metode
imagistice pentru depistarea precoce a recidivei, ceea ce asigur un beneficiu de
supravieuire.
Dei majoritatea recidivelor survin n primii 2 ani de la rezecie, n tumorile cu index
mitotic sczut metastazarea poate surveni i dup 10 ani. Recidiva este mai frecvent la
nivel local i peritoneal, i este frecvent asociat cu metastaze hepatice (i uneori
peritoneale, spre deosebire de majoritatea sarcoamelor de pri moi, care metastazeaz
la nivel pulmonar).
Pacienii cu recidive prezint prognostic nefavorabil. Tratamentul recidivei prin
chirurgie, embolizare arterial sau iradiere este ineficace [14].
204
Tumorile gastro-intestinale stromale
Tratamentul loco-regional: (Chemo)embolizarea arterial hepatic
Embolizarea arterial hepatic sau chemoembolizarea (CHEAT) reprezint o form
atractiv de paliaie la pacienii cu TGIS metastazate hepatic.
Ocluzia arterial este eficace, deoarece tumora este hipervascularizat. Nu este clar dac
rezultatele CHEAT sunt datorate ameliorrii concentraiei locale a citostaticului sau
ntreruperii vascularizaiei tumorale [10].
Tratamentul loco-regional: Radioterapia
Eficacitatea radioterapiei (RT) n TGIS nu a fost probat.
Dei RT este esenial n terapia local a sarcoamelor de pri moi ale extremitilor, n
TGIS rolul acesteia este minim datorit potenialului toxic pentru esuturile
nconjurtoare i necesitii iradierii pe cmpuri mari.
RT poate fi utilizat ocazional pentru paliaia simptomelor TGIS, cum ar fi hemoragia la
nivelul recidivei tumorale peritoneale.
La pacienii cu boal recidivat local sau diseminat, rezultatele terapiei chirurgicale
secundare i ale RT determin rezultate uniform nefavorabile [3,6].
Tratamentul sistemic: Chimioterapia
Chimioterapia (CHT) convenional prezint o utilitate minim n tratamentul TGIS
primare sau recidivate [1,2,7].
Este dificil a se evalua rspunsul TGIS la CHT convenional. Analiza studiilor istorice
publicate a demonstrat rate de rspuns reduse (0-15%) la o varietate de ageni citostatici
clasici activi n sarcoamele de pri moi (ex. doxorubicin, ifosfamid).
Tradiional, standardul de ngrijire dup rezecia complet a tumorii primare este
observaia simpl, fr tratament adjuvant: aceasta reflect n fapt ineficacitatea CHT
convenionale. Cu aceast strategie, n TGIS localizate, supravieuirea la 1 i 3 ani a fost
de 90% i, respectiv de 58% [14].
Chimioterapia intraperitoneal
O strategie terapeutic incluznd citoreducia peritoneal i CHT intraperitoneal cu
cisplatin i doxorubicin a fost preconizat de unii clinicieni.
Deoarece metastazele peritoneale ale TGIS sunt superficiale, CHT intraperitoneal
cu mitoxantron dup citoreducia chirurgical este sigur i fezabil. Toxicitatea a
fost redus i timpul de supravieuire a crescut de la 8 la 21 luni. Astzi, CHT
intraperitoneal este rezervat pacienilor cu tumori rezistente la imatinib [11].
Tratamentul sistemic: Noile terapii moleculare
Dezvoltarea inhibitorilor de tirozinkinaz a schimbat tratamentul TGIS nerezecabile.
Imatinib mesilat (STI571, Glivec
) un inhibitor al diferite tirozinkinaze, incluznd
BCR/ABL, c-Kit i receptorului factorului de cretere plachetar (PDGF-R). Inhibiia
BCR/ABL explic activitatea spectaculoas a imatinib n leucemia mieloid cronic
(LMC), n timp ce inhibiia c-Kit explic activitatea n TGIS [15].
Experiena privind utilizarea imatinib este foarte recent. Imatinib a fost aprobat n mai
2001 pentru tratamentul LMC rezistente la terapia cu interferon, i n februarie 2002
pentru TGIS metastatice [16].
n prezent, imatinib mesilat este considerat tratamentul standard pentru formele
avansate, inoperabile i metastatice de TGIS.
205
CANCERELE DIGESTIVE
Doza optim de imatinib nu este standardizat dar, uzual, doza de atac variaz ntre 400
i 1000 mg/zi. Este bine cunoscut c doza optim variaz de la pacient la pacient i pn
ce vor fi disponibile alte date se ncepe cu doza de 400 mg/zi P.O.; la pacienii n
progresie, doza se poate crete la 600-800 mg. Nu este clar dac dozele mai mari ofer o
eficacitate superioar.
Durata optim a tratamentului nu a fost nc stabilit, dar se recomand continuarea
administrrii pn la progresia bolii.
Ratele de rspuns (RR) variaz ntre 51-75% i rata general de control al tumorii este >
90%. Aproximativ 65-70% din pacieni obin un rspuns parial i ali 15-20% aspect de
boal stabil. Durata median a rspunsului este de 12-15 sptmni. Unele TGIS
reacioneaz lent i obinerea unui rspuns parial poate dura i 1 an. Numai 5% din
pacienii cu TGIS obin un rspuns complet [13].
Sunt n curs noi studii privind rolul imatinib mesilat ca tratament adjuvant sau
neoadjuvant. Tratamentul adjuvant cu imatinib este eficace n boala minim rezidual,
dar nu i n boala local avansat [16,17].
n TGIS metastatic, rezecia chirurgical complet urmat de tratament cu imatinib nu
aduce beneficii suplimentare fa de tratamentul cu imatinib de prim linie singur
(studiul BFR14, ASCO 2006).
Efectele adverse principale ale imatinib (tratabile la majoritatea pacienilor) sunt:
astenie moderat;
dureri abdominale;
rash;
diaree;
edem periorbitar;
crampe musculare intermitente;
hemoragiile gastro-intestinale intermitente (comunicate la civa pacieni) sunt
asociate cu sinteza masiv de factor de necroz tumoral (TNF) indus de acest
agent [18].
Fenomenul de instalare a rezistenei la imatinib reprezint principalul obstacol al
tratamentului. Rezistena primar este definit ca progresia (n general multifocal) n
primele 6 luni de terapie cu imatinib; aceste tumori prezint mutaii n exonul 9 al Kit,
sau c-Kit wild type, sau mutaii la nivelul PDGFR. Rezistena secundar este definit
ca progresia care survine dup 6 luni de tratament cu imatinib i cunoate dou tipuri:
parial i multifocal.
Aproximativ 12-14% dintre pacieni manifest rezisten primar la imatinib, peste 40%
dezvolt rezisten secundar n decurs de circa 2 ani, iar o proporie redus de pacieni
nu tolereaz terapia iniial cu imatinib [19,20].
Studii preliminare sugereaz urmtoarele 4 mecanisme de rezisten la imatinib, dup
modelul LMC:
achiziia unor mutaii punctiforme la nivelul genei c-Kit sau PDGF;
amplificarea genomic a c-Kit;
supraexpresia kinazei;
activarea unei ci alternative (necunoscut nc) cu pierderea supraexpresiei c-Kit i
rezisten funcional n tumorile iniial sensibile la imatinib [21].
La pacienii cu TGIS multifocale n progresie dup imatinib sunt testate noi terapii
pentru a combate mecanismele rezistenei moleculare.
206
Tumorile gastro-intestinale stromale
Inhibitorul kinazic cu int multipl sunitinib (SU11248, Sutent
) este actual testat n
studii de faz III, fiind activ ntr-o varietate de TGIS cu mutaii dobndite, rezistente
la imatinib.
Un studiu de faz II privind utilizarea sunitinib la pacienii cu TGIS rezistente la
imatinib a determinat remisiune parial la 8% din pacieni i aspecte de boal staionar
pe o perioad > 6 luni la 37% din pacieni.
Sunitinib este asociat cu eficacitate semnificativ i tolerabilitate acceptabil la pacienii
cu TGIS rezisteni sau intolerani la imatinib. Totui, nu pare s aib o aciune
inhibitorie eficace la pacienii cu TGIS recidivate, cu mutaii genice ale c-Kit la nivelul
exonului 11 [22].
Alte medicaii n studiu vizeaz mecanismele de semnal biologic intracelular, precum
calea rapamycinei, prin administrarea combinaiei RAD001 + imatinib (la pacienii
cu TGIS cu progresie documentat dup imatinib n monoterapie), i PKC 412.
Alte asociaii sunt n curs de evaluare.
STRATEGIE TERAPEUTIC
Boala localizat
excizia chirurgical complet a tumorii, cu margini de rezecie libere (civa
centimetri):
se evit ruptura tumoral;
tratamentul adjuvant i/sau neoadjuvant cu imatinib este considerat experimental i
nu se administreaz de rutin:
ar putea fi luat n considerare la unii pacieni, pentru a obine conservarea organului;
se recomand n cazul rupturii tumorale.
radioterapia (RT) sau chimioterapia convenional (CHT) nu prezint o valoare
dovedit n adjuvan [13].
Boala recidivat/ metastatic
Terapia de prim linie
imatinib 400-600 mg/zi P.O. (doza de iniiere standard); doza de 800 mg/zi P.O.
determin un avantaj n timpul de progresie a bolii (PFS), n special la pacienii cu
mutaii n exonul 9 al c-Kit, dar fr un avantaj de supravieuire;
rezecia chirurgical a tumorilor reziduale la pacienii responsivi poate fi luat n
considerare n cazuri selectate, dar beneficiul terapeutic nu este probat n studii
clinice randomizate;
excizia metastazelor infectate sau obstructive este necesar.
Progresia TGIS n cursul terapiei cu imatinib
creterea dozelor de imatinib la 800 mg/zi, dac acest lucru este fezabil;
chirurgie sau radioterapie paliativ pentru metastazele solitare cu cretere rapid, n
cazuri selectate;
sunitinib (mai ales n TGIS cu mutaia c-Kit n exonul 9);
includerea n studii clinice [3,13,23].
207
CANCERELE DIGESTIVE
208
FIGURA 6-1. Algoritm de tratament n TGIS
Recomandri ESMO 2007:
Tratamentul de elecie n TGIS localizate este chirurgia (II,A). Pentru TGIS localizate,
tratamentul adjuvant este experimental.
n TGIS metastatice sau recidivate, imatinib este standardul de tratament (II,A), n timp
ce rolul chirurgiei nu este cunoscut.
n TGIS localizate, rezecia limitat tip wedge a stomacului i/sau cea segmental a
intestinului este considerat adecvat deoarece acestea tind s se prezinte ca tumori
exofitice, fr afectarea ganglionilor regionali (III,B).
Adesea, pentru esofag, duoden i rect, rezeciile tip wedge nu sunt fezabile, astfel nct
se efectueaz de elecie rezecii largi.
n cazul TGIS omentale sau mezenterice, sunt recomandate rezecii complete n bloc.
De asemenea, tumorile aderente de organe se vor rezeca n bloc, pentru a evita ruptura
capsulei sau diseminarea abdominal.
Dei rezecia cu margini pozitive a tumorii (rezecie intratumoral) nu este clar
detrimental pentru supravieuire, re-excizia trebuie luat n considerare n cazul
tumorilor excizate intralezional fr infiltrarea suprafeei seroase (IV,C).
1
Criterii de diagnostic:
Localizare gastro-intestinal, mezenteric
Histologie convenional tipic pentru TGIS
CD117 pozitiv (TGIS CD117 negativ trebuie tratat ca TGIS CD117 pozitiv
Blackstein, ASCO 2005, #9010)
2
inoperabil sau nu se poate efectua intervenie chirurgical conservativ
3
ASCO 2005: Rutkowski (#9037), Gronchi (#9038)
4
ESMO Consensus Guidelines, Blaz et al., Ann Oncol 2005
5
Radio Frequency Ablation, Laser Induced Thermo Therapy
P. Reichardt Optimizing therapy for GIST patients,
EJ C Supplements Vol. 4, Suppl. 1 (2006) 19-26
EVALUARE
Diagnostic de tumor intra-abdominal
Diagnostic diferenial TGIS
Stadializare
Biopsie, dac este necesar, pentru stabilirea strategiei terapeutice
Diagnostic histopatologic TGIS
1
Metastatic
Imatinib 400 mg/zi
sau 600 mg/zi
Progresie Boal stabil
Rspuns terapeutic
Se continu terapia cu
imatinib 800 mg/zi
Inoperabil
2
Imatinib 400 mg/zi
sau 600 mg/zi
Secundar operabil:
Rezecie
3
Primar operabil:
rezecie
Progresie Boal stabil
Rspuns terapeutic
Se continu terapia cu
Imatinib 400 mg/zi
sau 600 mg/zi
Rezecie incomplet
Imatinib 400 mg/zi
sau 600 mg/zi
Rezecie complet
Terapie adjuvant cu
imatinib n cadrul
studiilor clinice
Se continu terapia cu
Imatinib 400 mg/zi
sau 600 mg/zi
EVALUARE
Escaladarea dozei la
800 mg/zi
Progresie Boal stabil
Rspuns terapeutic
Progresie
local
Progresie
sistemic
800 mg/zi
4
+
Tratament local
(chirurgical, RFA, LITT
5
)
Studii clinice
Imatinib+RAD001
Imatinib+PKC412
Imatinib+AMN107
Sunutinib
Tumorile gastro-intestinale stromale
Tratamentul adjuvant cu imatinib se va administra numai n cadrul studiilor clinice
randomizate. Tratamentul preoperator cu imatinib n scop de citoreducie se va
administra numai pentru tumorile inoperabile sau cnd se preconizeaz o intervenie
chirurgical conservatorie.
Pentru tumorile inoperabile i/sau metastatice, tratamentul cu imatinib trebuie nceput
imediat, chiar dac tumora nu este evaluabil (IV,C). Nu este dovedit c rezecia
complet a tumorii dup un rspuns la imatinib ar fi util la aceti pacieni.
Imatinib 400 mg/zi este recomandat ca tratament de linia I n stadiile avansate, ct
vreme rezultatele a 2 studii randomizate ce compar dozele de 400 i 800 mg nu au fost
comunicate nc (I,A). De remarcat c cel mai mare studiu disponibil a comunicat o
tendin de cretere a supravieuirii fr progresie dup doze de imatinib de 800 mg
numai la pacienii cu mutaii n exonul 9 a genei c-Kit.
ntreruperea tratamentului cu imatinib este asociat cu un risc crescut de recidiv, chiar
la pacienii cu remisiune complet.
Dei majoritatea pacienilor (dar nu toi) rspund la tratamentul de reinducie cu
imatinib, administrarea medicamentului nu trebuie sistat dect n cadrul unor studii
clinice [23].
EVALUAREA RSPUNSULUI LA TRATAMENT
Recomandri ESMO 2007:
Examenul CT este considerat de elecie n evaluarea rspunsului (I,B). Criteriile
standard pentru evaluarea rspunsului prin examenul CT (RECIST / OMS) nu prezint
suficient acuratee pentru identificarea responsivilor. Pe lng pacienii cu rspuns
parial (RP), tratamentul cu imatinib este de asemenea benefic la pacienii cu boal
staionar (BS variaiile de mrime cuprinse ntre -30% i +20%) dup criteriile
convenionale RECIST, i chiar la pacienii care prezint o cretere iniial >20% a
volumului tumoral n primele 6 luni de tratament, asociindu-se cu o ameliorare clinic
semnificativ sau un rspuns tumoral la examenul tomografic cu emisie de pozitroni 18-
fluorodeoxiglucoz (PET-
18
FDG).
De fapt, rspunsul TGIS la tratament a fost redefinit prin intermediul examenului PET,
reducerea dimensiunilor tumorii cu >10% sau scderea densitii tumorale cu >15%
fiind identificate ca net superioare sistemului RECIST n termenii valorii prognostice.
PET-
18
FDG este foarte sensibil n depistarea rspunsului tumoral precoce, dar costul
crescut i limiteaz disponibilitatea.
Cnd TGIS rspunde la tratamentul cu imatinib, masa tumoral devine rapid
hipoatenuat la examenul CT cu substan de contrast, n timp ce reducerea
dimensiunilor tumorii poate s survin dup cteva luni sau deloc. Aceast reducere a
densitii tumorale la examenul CT (msurat n uniti Hounsfield) reflect pierderea
vascularizaiei tumorale i este asociat n general cu reducerea activitii metabolice la
examenul PET-
18
FDG scderea captrii glucozei (II,A). Ameliorarea simptomatic,
reducerea densitii tumorale la examenul CT i rspunsul PET sunt factori predictivi ai
controlului tumoral dup tratamentul cu imatinib [19,22,23].
209
CANCERELE DIGESTIVE
URMRIRE
Nu exist recomandri specifice pentru urmrirea pacienilor cu TGIS.
Recidivele survin mai frecvent la nivelul peritoneului sau ficatului. Nu se tie dac
tratamentul precoce cu imatinib al pacienilor cu TGIS avansate amelioreaz rezultatele.
Recomandri ESMO 2007:
La pacienii din grupele cu risc crescut sau intermediar, urmrirea prin examen CT la
fiecare 3-4 luni timp de 3 ani, apoi la fiecare 6 luni pn la 5 ani este considerat
rezonabil, dei ratele de recidiv la pacienii cu TGIS high risk sunt crescute, iar
recidivele tardive sunt rare (V,D).
La pacienii cu TGIS din categoriile low risk sau very low risk se recomand urmrirea
prin examen CT la fiecare 6 luni timp de 5 ani (V,D).
n prezent nu sunt date care s indice c aceste intervale sunt optime, sau c urmrirea
regulat prin examen CT ar fi benefic [23].
ntr-o perioad mai scurt de zece ani, TGIS au prsit anonimatul pentru a deveni un
model de succes a terapiilor moleculare intite. Studiile actuale tind din ce mai mult s
acrediteze ideea c aceste tumori nu reprezint o singur entitate uniform, ci mai
curnd o familie de neoplazii strns nrudite. Sunt ateptate progresele n definirea
cilor de semnal biologic care s conduc la continuarea succesele terapeutice n
tratamentul TGIS.
Odat cu ameliorarea tehnologiilor i descifrarea de noi mecanisme moleculare n
cancer, translaia spre noi terapii a tumorilor solide va continua dup modelul TGIS.
Bibliografie
1. Clary BM, De Matteo RP, Lewis JJ et al. Gastrointestinal stromal tumours and leyomiosarcoma of the
abdomen and retroperitoneum: a clinical comparison. Ann Oncol 2001;8:290-299.
2. Mazur MT, Clark HB. Gastric stromal tumors. Reappraisal of histogenesis. Am J Surg Pathol 1995;
19:507-519.
3. Joensu H. Introduction: the TGIS story in brief. n: EIS Sarcoma and TGIS ESMO International
Symposium - Gastrointestinal stromal tumors: a comprehensive update. Novartis Oncology 2006:18-22.
4. DeMateo RP, Lewis JJ, Leung D, et al. Two hundred gastrointestinal stromal tumors: recurrence patterns
and prognostic factors for survival. Ann Surg 2002;23:51-58.
5. Crian D, Olinici CD. Tumorile stromale gastro-intestinale principii de diagnostic i tratament. Rad &
Oncol Med 2003,4:213-217.
6. Demetri GD. Gastro-intestinal stromal tumors. n: DeVita VT Jr, Hellman S, Rosenberg SA, eds. Cancer:
principles & practice of oncology. 7th ed. Philadelphia: Lippincott, Williams & Wilkins, 2005: 1050-
1060.
7. Miettinem M, Sobin LH, Sarlomo-Rikala M. Immunohistochimical spectrum of TGISs at different sites
and their differential diagnosis with a refference to CD117 (KIT). Mod Pathol 2000;13:1134-1142.
8. Corless CL, Flether JA, Heinrich MC. Biology of gastrointestinal stromal tumors. J Clin Oncol 2005;
22:3813-3825.
9. Labianca R, Taino R, Messina C. An overview on management of gastro-intestinal stromal tumours
(TGIS). n: Proceeding Book of the 15th International Congress on Anti-Cancer Treatment (ICACT).
Paris 2004: 65-69.
10. Saif WM. Other gastrointestinal tumors. n: Abraham J, Allegra CJ, Gulley J, eds. Bethesda handbook of
clinical oncology. 2nd ed. Philadelphia: Lippincott Williams and Wilkins, 2005:145- 151.
11. Kamel RI, Elliot FK, Fishman EK. Imaging of gastrointestinal stromal tumor. n Chang AE, ed.
Oncology: an evidence-based approach. New York: Springer Science, 2006:413- 424.
12. Fletcher CD, Berman JJ, Cortess C et al. Diagnosis off gastrointestinal stromal tumors: A consensus
approach. Hum Pathol 2002;152:459-465.
13. Joensuu H. Gastrointestinal stromal tumor (TGIS). Ann Oncol 2006;17(suppl.10):x280-x286.
210
Tumorile gastro-intestinale stromale
14. Miron L, Miron I. Gastrointestinal stromal tumors from a poorly defined pathologic oddity to a
milestone in solid oncology. Maedica 2006;1(1):66-71.
15. Eisenberg BL. Imatinib messylate: a molecular targeted therapy for gastro-intestinal stromal tumors.
Oncology 2003;1:1615-1619.
16. Hirota S, Isozaki K, Moriyama Y, et al. Gain-of-function mutations of c-kit in human gastrointestinal
stromal tumors. Science 1998; 279:577-580.
17. Heinrich MC, Corless LC, Demetri DG, et al. Kinase mutation and imatinib response in patients with
metastatic gastro-intestinal stromal tumor. J Clin Oncol 2003;21:4342-4349.
18. Joensuu H, Roberts PJ, Sarlomo-Ricala M, et al. Effect of tyrozin kinase inbibitor STI571 in a pacient
with a metastatic gastrointestinal stromal tumor. New Engl J Med 2001;344:1052-1056.
19. Demetri GD, von Mehren M, Blanke CD, et al. Efficacy and safety of imatinib mesylate in advanced
gastrointestinal stromal tumors. N Engl J Med 2002;347-472.
20. Heinrich MC, Cortess CL, Blanke ChD, et al. Molecular correlates of imatinib resistence in
gastrointestinal stromal tumors. J Clin Oncol 2006;24(29):4764-4775.
21. Tuveson DA, Willis NA, Jacks T, et al. STI571 inactivation of the gastrointestinal stromal tumor c-KIT
oncoprotein: biological and clinical implications. Oncogene 2001;20:5054.
22. Blay JY, Bonvalot S, Casali P, et al. Consensus Meeting for the management of gastrointestinal stromal
tumors - Report of the TGIS Consensus Conference 2004. Ann Oncol 2005;16(4):566-778.
23. Blay J-Y, Le Cesne A. Gastrointestinal stromal tumors: ESMO Clinical recommandations for diagnosis,
treatment and follow-up. Ann Oncol 2007;18(suppl.2):ii27-ii29.
24. Reichardt P. Optimising therapy for GIST patients. EJC Suppl 2006;4(suppl.1):19-26.
25. Blanke CD. Gastrointestinal stromal tumors: three perspectives on current diagnosis and therapy. EJC
Suppl 2006;4(suppl.1):1-6.
211
CANCERELE DIGESTIVE
212
Cancerul colo-rectal
EPIDEMIOLOGIE
Cancerele colo-rectale (CCR) reprezint 15% din toate cancerele umane (locul doi n
lume, al treilea n Romnia la ambele sexe), cu rate crescute de morbiditate
(aproximativ 3,5 milioane cazuri anual) i mortalitate (circa 400.000 pe an).
Incidena CCR n Europa este de 58/100.000 locuitori/an, iar mortalitatea de
30/100.000 locuitori/an. n Romnia, frecvena CCR este n cretere rapid (dublarea
incidenei i mortalitii n ultimii 20 de ani!), atingnd n 2000 o inciden de
17,74/100.000 locuitori/an, care situeaz Romnia printre rile cu frecven medie a
acestui neoplasm. CCR au devenit a doua cauz de deces prin cancer (dup cele
bronho-pulmonar, dar devansnd cancerul gastric), cu un numr de 4.150 decese n
2002 (19,05/100.000 locuitori) [1].
Circa 50% din pacienii cu CCR mor datorit acestei neoplazii; boala este operabil
n 80% din cazuri, dar 35% dintre acetia se prezint cu recidive la distan [2].
ETIOLOGIE
Factorii de risc ai CCR sunt multipli [3]:
Vrsta: riscul crete cu vrsta: mai mult de 90% din CCR survin la pacienii cu vrste
de peste 50 ani, dar 3% dintre acestea survin la pacienii mai tineri de 40 ani.
Sexul: incidena cancerului de colon este mai crescut la femei, iar cancerele rectale
sunt mai frecvente la brbai.
Etnia: mai frecvente la afro-americani; mortalitatea crete la brbaii de ras neagr.
Istoric de CCR sau adenoame colonice: adenom tubular (risc sczut), tubulo-vilos
(risc intermediar), vilos (risc crescut).
Polipii colo-rectali: polipii adenomatoi prezint potenial de malignizare. Polipii de
mici dimensiuni (<1 cm) nu se asociaz cu creterea incidenei CCR, cei > 1 cm
determinnd ns incidene crescute de 4-7 ori pentru polipoza multipl; riscul de
malignizare a unui polip > 1 cm este de 2,5% la 5 ani, 8% la 10 ani i 24% la 20 ani.
Fumatul: crete riscul de adenoame/ CCR de 2,5 ori.
Obezitatea.
Dieta: dietele vegetale cu coninut bogat n fibre i srac n grsimi pot reduce riscul
de CCR. Consumul crescut de grsimi, glucide rafinate se asociaz cu un risc crescut.
Deficitul de calciu: consumul zilnic a 1.25-2 g de Ca
2+
a fost asociat cu o reducere a
riscului de adenoame recurente (studii randomizate).
Deficitul de micronutrimente: carena n folai, vitamina E i D crete riscul de CCR.
Bolile inflamatorii intestinale: 1% dintre pacienii cu CCR au un istoric de colit
ulcerativ (CU), riscul de CCR crescnd de 7-11 odat ori cu vrsta: 3% la 15 ani de
la debutul CU, 5% la 20 ani i 9% la 25 ani. Boala Crohn crete riscul de CCR de
1.5-2 ori.
Factorul genetic: 15% din toate CCR survin la pacienii cu istoric de cancere colice
la rude de gradul I.
Sindroamele polipozice familiale (polipoza adenomatoas familial (FAP), sindromul
Gardner, Turcot, Peutz-Jeghers, sindromul adenoamelor plate [flat-adenoma syndrome,
FAS], polipoza juvenil), sunt asociate cu un risc foarte crescut de CCR.
Cancerul colo-rectal
Sindromul Lynch II este un sindrom ereditar autosomal dominant (penetran familial 90%)
caracterizat prin multiple carcinoame colice, pancreatice, gastrice i extradigestive (sn,
ovar, uter). Sindromul Lynch I cuprinde cancerele colice ereditare non-polipozice (HNPCC),
sincrone i metacrone, ce survin la vrste <50 ani la cel puin 3 membri din aceeai familie,
minim 2 generaii succesive.
Ali factori: istoricul personal sau familial de alte cancere (sn, endometru, ovar);
expunerea la azbest i infeciile virale cu papiloma virusuri pot determina CCR.
HISTOLOGIE
Tipurile histologice de cancer de colon includ:
Adenocarcinoamele (majoritatea CCR);
Carcinoamele mucinoase (coloide);
Carcinoamele cu celule n inel cu pecete;
Tumorile schiroase;
Tumorile cu difereniere neuroendocrin prognostic tipic mai nefavorabil dect
variantele de adenocarcinom pur [4].
DIAGNOSTIC
Examen clinic
Elementele sugestive pentru diagnosticul CCR sunt:
colonul drept: durere abdominal, melen, mas abdominal palpabil;
colonul stng: tulburri de tranzit, dureri, modificri ale calibrului materiilor fecale;
rect: rectoragii, tenesme, dureri abdominale, masa rectal palpabil.
stadii avansate: pierdere ponderal, hepatomegalie, icter, anemie.
Examenul fizic va include obligatoriu: tueul rectal, aprecierea strii generale, a
prezenei adenopatiilor periferice i a hepatomegaliei [5].
Investigaii paraclinice
Evaluarea general: bilan hematologic, biochimic; radiografie toracic.
Rectoscopia i colonoscopia: vizualizarea tumorii, biopsia i examenul histologic,
precum i cutarea unei a doua leziuni (polip).
Clisma baritat: lacune neregulate, ulceraii, stenoze; examenul n dublu contrast
este important pentru diagnosticul leziunilor mici i al polipilor.
Examenul computer tomografic (CT) abdomino-pelvin: prezena metastazelor
hepatice sau peritoneale i evaluarea nivelului de penetraie a peretelui colic.
Ecografia endoscopic (EUS): evaluarea preoperatorie a tumorilor mari, n special
rectale (combinaia dintre tueul rectal i ecografia endorectal poate preciza
indicaia de operabilitate i defini grupul de pacieni ce beneficiaz de chimio-
radioterapie preoperatorie) [6]
Markerii tumorali: rol diagnostic redus, dar valoroi n monitorizarea recidivei.
Antigenul carcinoembrionar (CEA) este cel mai utilizat pentru urmrirea evoluiei CCR i
detecia precoce a recidivei locale i a metastazelor hepatice, dar este prea puin sensibil i
specific pentru a fi utilizat n depistarea precoce. Creterea CEA seric este corelat cu
diferenierea histologic, stadiul i gradul de afectare visceral. Ali markeri (CA19.9 i
TAG-72) sunt utilizai n monitorizarea recidivelor, n completarea dozrii CEA [7]
213
CANCERELE DIGESTIVE
TABEL 6-10. Bilanul preterapeutic n CCR [8]
Standard:
- Anamneza; antecedentele familiale i personale
- Examen clinic general
- tueu rectal (la femei: examen ginecologic prin examen cu valve i tueu vaginal)
- colon: colonoscopie (confirmare prin biopsie, verificarea tumorilor sincrone)
- rect: rectoscopie (confirmare prin biopsie), completat cu colonoscopie (tumori sincrone)
- Ecografie abdomino-pelvin
- Examen CT abdomino-pelvin
- rect: ecografie endorectal / CT / IRM pelvin (aprecierea necesitii RT preoperatorii)
- Radiografie toracic
- Markeri tumorali: antigen carcinoembrionar (CEA)
- Hemoleucograma complet, testele de coagulare
- Probe hepatice i renale
Opional:
- Clisma baritat cu dublu contrast (n caz de dificulti la colonoscopie)
- IRM abdomino-pelvin (n caz de alergie la substana de contrast)
- Dozarea CA19.9 (dac CEA este negativ)
STADIALIZARE
Se recomand utilizarea cu prioritate a ediiei a 6-a (2002) a sistemului de stadializare
TNM AJCC/UICC [9].
TABEL 6-11. Clasificarea stadial TNM AJCC/UICC 2002 a cancerelor de colon
T (tumora primar)
Tx tumora primar nu poate fi definit
To fr evidena tumorii primare
Tis carcinom in situ
T1 tumora ce invadeaz submucoasa
T2 tumora ce invadeaz muscularis propria
T3 tumora ce invadeaz peretele muscular pn la subseroas
T4 tumor ce invadeaz direct alte organe sau structuri de vecintate i/sau perforeaz
peritoneul visceral
N (adenopatiile loco-regionale)
Nx starea ganglionilor regionali nu poate fi definit
No fr metastaze n ganglionii regionali
N1 metastaze n 1-3 ganglioni pericolici sau perirectali
N2 metastaze n > 4 ganglioni limfatici pericolici sau perirectali
N3 metastaz n oricare dintre ganglionii situai n lungul arterelor ileo-colice, colic dreapt,
colic medie, colic stng, mezenteric inferioar i rectal superioar
M (metastazele la distan)
Mx prezena metastazelor la distan nu poate fi dovedit
Mo fr prezena metastazelor la distan
M1 metastaze la distan prezente
pTNM Clasificarea patologic
Categoriile pT, pN i pM corespund categoriilor T, N i M clinice.
pNo - Examinarea histologic a adenopatiilor regionale va trebui s includ minim 12 ganglioni.
214
Cancerul colo-rectal
Gruparea pe stadii Supravieuire la 5 ani (%)
Categoria TNM Dukes* Astler-Coller modificat
Stadiul 0 Tis No Mo 100
Stadiul I T1 No Mo A A 93.2
T2 No Mo A B1
Stadiul IIA T3 No Mo B B2 84.7
Stadiul IIB T4 No Mo B B3 72.2
Stadiul IIIA T1-2 N1 Mo C C1 83.4-59.8
Stadiul IIIB T3-4 N1 Mo C C2/C3 64.1-42.0
Stadiul IIIC Orice T N2 Mo C C1/C2/C3 44.3-27.3
Stadiul IV Orice T Orice N M1 D 8.1
* stadiul Dukes B este compus din 2 subgrupe prognostice: mai bun (T3NoMo) i mai puin favorabil (T4NoMo)
PRINCIPII DE TRATAMENT
CANCERUL DE COLON
Tratamentul loco-regional: Chirurgia
Chirurgia reprezint modalitatea terapeutic principal n cancerul de colon.
Radicalitatea interveniei chirurgicale presupune exereza larg a segmentului
intestinal afectat tumoral i a segmentului de drenaj limfatic; obinerea de margini
libere proximal, distal i lateral are importan capital.
Rezecabilitatea cancerelor de colon depete 90%, numai 2-7% din cazuri fiind inoperabile.
Mortalitatea perioperatorie variaz ntre 3-10%, depind 15% doar n rezecia abdomino-pelvin.
Tipul de intervenie operatorie este condiionat de localizare, dimensiunea, extensia
tumorii i starea general a pacientului, putnd consta n colectomie (dreapt/
transvers/ intermediar/ stng) sau rezecie sigmoidian.
Numrul ganglionilor limfatici rezecai i examenul histologic al acestora este foarte
important pentru o stadializare precis.
Intervenia chirurgical paliativ (pentru simptome precum obstrucia acut sau
sngerrile persistente) include colostomia sau chiar rezecia bolii metastatice.
Metastazectomia hepatic este asociat cu o mortalitate < 5% i o morbiditate perioperatorie de
30%, putnd determina o supravieuire la 5 ani de 26-38%. Rezultatele pot fi ameliorate prin
asocierea terapiilor sistemice i loco-regionale. Contraindicaii: boala extrahepatic, dimensiunile
leziunii (>10 cm), prezena metastazelor multiple sau valori ale CEA > 200 mg/ml [10].
Tratamentul loco-regional: Radioterapia
Nu sunt disponibile date din studii randomizate care s susin utilizarea radioterapiei
(RT) n tratamentul cancerelor de colon.
RT postoperatorie (DT 45 Gy, 1.8 Gy/zi) este testat la pacieni cu risc de recidiv:
n stadiul B
3
cu extensie la ntreg peretele colic, cu aderen sau invazie a structurilor
vecine i ganglioni negativi;
n stadiul C
3
ca n stadiul B
3
, dar cu ganglionii regionali pozitivi;
n cazul tumorilor suprainfectate sau fistulizate;
n cazul bolii reziduale dup excizia incomplet [1].
n aceste subgrupuri de pacieni, RT poate ameliora controlul local i supravieuirea fr
semne de boal. Asocierea chimioterapiei (5-fluorouracil cu acid folinic) reprezint o
tentativ de ameliorare a rezultatelor terapeutice.
215
CANCERELE DIGESTIVE
Tratamentul sistemic: Chimioterapia
Chimioterapia adjuvant
Tratamentul cancerelor de colon a parcurs substaniale progrese n ultimii 10-15 ani. n
baza studiilor actuale se pot deduce urmtoarele concluzii cu privire la chimioterapia
(CHT) adjuvant:
CHT adjuvant timp de 6 luni n stadiul III (Dukes C) reduce rata de recidiv (63%
vs. 58%) i amelioreaz riscul de deces cu 25-30%, i supravieuirea absolut cu 10-
15%. Oricare dintre regimurile utilizate ofer rezultate echivalente.
Valoarea CHT adjuvante n stadiul II (Dukes B) nu este nc cert; aceast opiune
poate fi rezonabil oferit pacienilor tineri, informai, cu caracteristici de risc crescut:
bine stabilite debut prin ocluzie intestinal;
perforaia peretelui intestinal;
aderen tumoral.
mai puin certe tumori puin difereniate;
invazie venoas/ limfatic/ perineural;
valori crescute preoperator ale AFP [10].
Protocolul recomandat n aceste cazuri ar fi 5-FU/AF (bine tolerat, efecte secundare
minime), dar beneficiul terapeutic este redus (ameliorare a supravieuirii de 3-4%).
Asocierea 5-FU cu levamisol este actual de importan istoric (obine reducerea cu
41% a ratelor de recidiv i cu 33% a mortalitii generale) [11,12].
Administrarea 5-FU cu acid folinic (leucovorin, AF) timp de 6 luni este echivalent
cu administrarea timp de 12 luni.
Asocierea 5-FU cu doze reduse de AF (20 mg/m) este echivalent cu administrarea
de doze mari (200-500 mg/m
2
) de AF.
Nu exist diferene ntre regimurile acceptate actual n adjuvan: administrarea 5-FU
n zilele 1-5, 6 cicluri la fiecare 4-5 sptmni, cu AF low-dose, fa de administrarea
5-FU sptmnal x 6, 4 cicluri la fiecare 8 sptmni, cu AF high-dose. Profilul de
toxicitate al acestor regimuri difer (mielosupresia i mucozita oral sunt mai
frecvente cu protocolul Mayo Clinic, n timp ce diareea este mai sever n
administrarea sptmnal) (Tabel 10).
Noile citostatice, active n cancerele de colon avansate (oxaliplatin, irinotecan,
tegafur [UFT], capecitabin), sunt susceptibile s prezinte o valoare ca tratament
adjuvant, dar acest fapt nu este probat nc n studiile clinice [13].
Oxaliplatin aduce un beneficiu n termenii riscului absolut de 4%, cu preul unei toxiciti
neurologice reversibile.
Irinotecan amelioreaz intervalul de supravieuire fr boal (DFS) n stadiul III de cancere
de colon.
Fluoropirimidinele orale prezint activitate similar cu terapia intravenoas. n adjuvan,
capecitabina nu determin rezultate inferioare fa de 5-FU/AF low-dose, devenind o
alternativ la pacienii care nu vor tolera 5-FU, AF i oxaliplatin.
Asociaerea irinotecan, 5-fluorouracil, leucovorin (IFL), administrat n adjuvan la
pacienii cu cancere de colon n stadiul III, nu amelioreaz supravieuirea general (OS) i
nici supravieuirea fr boal (DFS), dar crete toxicitatea (inclusiv letal) comparativ cu
tratamentul adjuvant cu 5-FU/AF (CALGB 89803 studiu randomizat de faz III, 1264
pacieni a demonstrat c progresele nregistrate n cancerul metastatic nu se regsesc
obligatoriu i n terapia adjuvant).
216
Cancerul colo-rectal
TABEL 6-12. Protocoale de CHT adjuvant n cancerul de colon
Mayo Clinic (Poon MA et al, J Clin Oncol 1989)
Acid folinic 20 mg/m
2
I.V. (bolus, 10 nainte de 5-FU) zilele 1-5
5-Fluorouracil 425 mg/m
2
/zi I.V. (bolus) zilele 1-5
Se repet la fiecare 4 sptmni (6 cicluri).
Roswell Park (Wolmark N et al, J Clin Oncol 1993)
Acid folinic 500 mg/m I.V. (perfuzie 2h) zilele 1,8,15,22,29,36
5-Fluorouracil 500 mg/m I.V. (bolus 1h, dup AF) zilele 1,8,15,22,29,36
Se repet la fiecare 8 sptmni (4 cicluri).
FLOX (Wolmark N et al, J Clin Oncol 2005)
Acid folinic 500mg/m
2
I.V. zilele 1,8,15,22,29,36
5-Fluorouracil 500 mg/m
2
I.V. (bolus) zilele 1,8,15,22,29,36
Oxaliplatin 85 mg/m
2
I.V. zilele 1,15,29
Se repet la fiecare 8 sptmni (3 cicluri).
Xel (Twelves C et al, N Engl J Med 2005)
Capecitabina 1250 mg/m
2
x 2/zi P.O. zilele 1-14
Se repet la fiecare 3 sptmni (8 cicluri).
FOLFOX4 (Andre T et al, N Engl J Med 2004)
Oxaliplatin 85 mg/m
2
I.V. (perfuzie 2h) ziua 1
Acid folinic 200 mg/m
2
I.V. (simultan cu oxaliplatin) ziua 1
5-Fluorouracil 400 mg/m
2
I.V. (bolus 2-4) zilele 1-2 apoi
600 mg/m
2
I.V. (perfuzie 22h) zilele 1-2
Se repet la fiecare 2 sptmni (12 cicluri).
Chimioterapia loco-regional adjuvant
Administrarea intra-tumoral de 5-FU nu a fcut proba unei eficaciti particulare.
5-FU poate fi administrat intra-portal:
Taylor et al. (1985) au comunicat reducerea semnificativ a numrului metastazelor hepatice
i creterea supravieuirii dup perfuzia portal continu cu 5-FU (1 g/zi, 7 zile) (244
pacieni). Alte 3 studii (>1.500 pacieni) nu au obinut rezultate semnificative [16].
Recomandri ESMO 2005/2007:
Tratamentul adjuvant este recomandat pentru stadiile T2-4,N1-2,Mo (stadiul III, Dukes
modificat C1-3) (I,A).
Chimioterapia adjuvant poate fi luat n consideraie la anumite cazuri selectate cu
ganglioni negativi (stadiul II), n special la pacienii cu risc crescut de recidiv. Printre
factorii cunoscui de risc n stadiul II CCR sunt: T4, adenocarcinom slab
difereniat/nedifereniat, invazie vascular sau limfatic, obstrucie sau perforaie
tumoral la momentul diagnosticului iniial i > 12 ganglioni invadai (II,A).
Opiunile terapeutice n adjuvan includ perfuzii cu asociaeri pe baz de 5-fluorouracil
(5-FU), cu sau fr oxaliplatin. 5-FU/LV plus oxaliplatin amelioreaz semnificativ
supravieuirea la 3 ani comparativ cu 5-FU/LV (II,A).
Capecitabina este cel puin la fel de eficace ca administrarea n bolus a 5-FU/leucovorin
(LV) (II,A) [17].
217
CANCERELE DIGESTIVE
TratamentuladjuvantoptimnCCRrmneafidefinit.Fiecarenoumedicamentaadus
unbeneficiuminim,asociatnscucosturiitoxicitatecrescute!
Viitorul va pune cu precdere accentul pe stratificarea pacienilor n funcie de factorii
de risc moleculari, deoarece este evident c exist fenotipuri mai agresive corelate cu
riscul crescut de metastazare. Pn atunci, n practica clinic sunt utilizai ca factori de
decizie terapeutic: statusul ganglionar, prezena ocluziei, perforaia tumoral i
invazia limfo-vascular. Ali factori precum: timidilat sintetaza, expresia K-ras, deleia
18q, regiunile coninute n gena supresoare DCC, supraexpresia markerului X,
polisomia i mutaiile receptorului EGF sunt n curs de investigaie ca elemente de
decizie n alegerea celei mai bune terapii adjuvante n cancerele de colon [18].
Chimioterapia paliativ
Recomandri ESMO 2005:
Intervenia chirurgical trebuie luat n considerare pentru metastazele unice hepatice
sau pulmonare. Pentru metastazele hepatice se poate avea n vedere CHT loco-regional.
Prima linie de chimioterapie paliativ trebuie administrat precoce i const n 5-FU n
diferite protocoale i scheme de administrare; regimurile cu 5-FU/LV perfuzabile sunt
n general mai puin toxice dect cele n bolus. Fluoropirimidina oral capecitabina este
o alternativ pentru 5-FU perfuzabil (I,B).
Se vor avea n vedere asocierile cu irinotecan sau oxaliplatin, care determin rezultate
superioare (II,A).
Administrarea noilor ageni moleculari intii (ex. anticorpii monoclonali mpotriva
VEGF i EGFR) n asociere cu chimioterapia ar putea fi luat n considerare la anumii
pacieni foarte atent selectai.
Chimioterapia de linia a doua (oxaliplatin sau irinotecan) trebuie luat n considerare la
pacieni selectai cu status bun de performan meninut (I,A) [28].
Chimioterapia este indicat n funcie de natura tumorii, statusul de performan, vrsta
i preferinele pacientului.
n formele metastatice ntrzierea administrrii CHT pn la apariia simptomelor face
prognosticul i mai nefavorabil !
Monoterapia cu 5-FU determin rate de rspuns (RR) de 20-25% i o supravieuire
median de 8-12 luni n CCR avansate; modularea 5-FU cu AF n asocierile Mayo
Clinic, Machover, de Gramont, Ardalan (Tabel 11) determin rezultate asemntoare
n termenii rspunsului i supravieuirii. Profilul toxic al acestor protocoale difer,
mielosupresia fiind mai frecvent n cazul administrrilor zilnice n bolus, iar diareea
i mucozita fiind de obicei apanajul perfuziilor continue. Rspunsul trebuie evaluat
dup un interval scurt de timp (cel mult 8-14 sptmni).
Asocierea 5-FU cu noii ageni citostatici (irinotecan, oxaliplatin, UFT, raltitrexed)
conduce la rate de rspuns crescute, fr dovada cert a ameliorrii supravieuirii;
toxicitatea secundar este considerabil i poate compromite scopul paliativ al
tratamentului.
Asocierea 5-FU, AF, irinotecan determin RR de 35-45%, supravieuire fr progresie de 7
luni i a probat o ameliorare a supravieuirii generale (numai n studiile de faz II), cu preul
unei toxiciti severe (diaree grad IV i neutropenie).
218
Cancerul colo-rectal
TABEL 6-13. Protocoale de chimioterapie recomandate actual n CCR metastatic
De Gramont
Acid folinic 200 mg/m I.V. (perfuzie 2 ore) zilele 1,2
5-FU 400 mg/m I.V. (bolus) zilele 1-2
5-FU 600 mg/m I.V. (perfuzie 46h) zilele 1-2
Se repet la fiecare 2 sptmni.
RR crescute (32.6 vs. 14.4%), DFS mai lung (27.6 luni vs. 14,4 luni), dar OS nemodificat comparativ cu 5-FU.
Roswell Park (vezi Tabel 10)
Se administreaz pn ce boala progreseaz sau toxicitatea devine intolerabil.
Mayo Clinic (vezi Tabel 10)
Se administreaz la fel ca i n adjuvan, sau cu doze de 5-FU de 370 mg/m/sptmn I.V., timp
de 30 sptmni.
5-FU monoterapie (perfuzie continu)
5-FU 750 mg/m I.V. (perfuzie continu) zilele 1-7,22-29,34-41... sau
5-FU 2600 mg/m I.V. (perfuzie continu 24h) zilele 1,8,15,22,29... sau
5-FU 50-300 mg/m I.V. (perfuzie continu 24h) zilnic*
*Se administreaz continuu pn la apariia semnelor de toxicitate (mucozit, eritrodisestezie, diaree), sau timp de
4 sptmni urmat de o sptmn pauz.
Irinotecan monoterapie
Irinotecan 125 mg/m I.V. (perfuzie 90) zilele 1,8,15,22
Se repet la fiecare 6 sptmni.
IFL (Saltz)
Irinotecan 125 mg/m I.V. (perfuzie 90) zilele 1,8,15,22(,29,36)
Leucovorin 20 mg/m I.V. (bolus) zilele 1,8,15,22(,29,36)
5-FU 400-500 mg/m I.V. (bolus) zilele 1,8,15,22(,29,36)
Se repet la fiecare 6-8 sptmni.
RR crescute (49% vs. 31%), supravieuire median mai lung (7.0 vs. 4.3 luni), OS mai lung (17,4 vs. 14,1 luni)
comparativ cu 5-FU/AF.
FOLFIRI
Irinotecan 180 mg/m I.V. (perfuzie 90) ziua 1
Leucovorin 200 mg/m I.V. (perfuzie 2h) ziua 1
5-FU 400 mg/m I.V. (bolus) ziua 1 apoi
2400-3000 mg/m I.V. (perfuzie continu 46h) zilele 1-2
Se repet la fiecare 2 sptmni.
FOLFOX4
Oxaliplatin 85 mg/m I.V. (perfuzie 120) ziua 1
Leucovorin* 200 mg/m I.V. (perfuzie 120) zilele 1-2
5-FU 400 mg/m I.V. (bolus) zilele 1-2 apoi
600 mg/m I.V. (perfuzie continu 22h) zilele 1-2
Se repet la fiecare 2 sptmni.
*Leucovorin poate fi administrat concomitent cu oxaliplatin, dar datorit incompatibilitii acestuia din urm cu
serul fiziologic, ambele se vor combina n ser glucozat 5%.
FOLFOX6
Oxaliplatin 100 mg/m I.V. (perfuzie 2h) ziua 1
Leucovorin 400 mg/m I.V. (perfuzie 2h) ziua 1
5-FU 400 mg/m I.V. (bolus) ziua 1 apoi
2400-3000 mg/m I.V. (perfuzie 46h) zilele 1-2
Se repet la fiecare 2 sptmni.
219
CANCERELE DIGESTIVE
Capecitabin monoterapie
Capecitabin 2000-2500 mg/m P.O. (2 prize/zi) zilele 1-14
Se repet la fiecare 3 sptmni.
Se prefer dozele mai reduse, datorit toxicitii secundare (eritrodisestezia i mucozita) prezente, dei limitate.
CAPOX (XELOX)
Oxaliplatin 130 mg/m I.V. ziua 1
Capecitabin 2000 mg/m
2
P.O. (2 prize/zi) zilele 1-15
Se repet la fiecare 3 sptmni.
UFT + AF
UFT* 100 mg/m P.O. (3 prize/zi) zilele 1-28
Acid folinic 30 mg/m P.O. (3 prize/zi) zilele 1-28
Se repet la fiecare 5 sptmni.
*Doza de UFT se refer la componentul tegafur (D
max
600 mg/zi).
IROX
Oxaliplatin 85 mg/m I.V. (perfuzie 2h) zilele 1,2
Irinotecan 80 (200mg)/m I.V. (perfuzie 30) ziua 1(8,15)
Se repet la fiecare 4 sptmni (cu G-CSF).
AIO
Irinotecan 80-100 mg/m I.V. (perfuzie 90) zilele 1,8,15,22(,29,36)
Leucovorin 500 mg/m I.V. (perfuzie 2h) zilele 1,8,15,22(,29,36)
5-FU 2300 mg/m I.V. (perfuzie 24h) zilele 1,8,15,22(,29,36)
Se repet la fiecare 6-8 sptmni.
Douillard
Irinotecan 180 mg/m
2
I.V. (perfuzie 2h) ziua 1
Leucovorin 200 mg/m
2
I.V. (perfuzie 2h) zilele 1-2
5-FU 400 mg/m
2
I.V. (bolus) zilele 1-2
600 mg/m
2
I.V. (perfuzie 22h) zilele 1-2
Se repet la fiecare 2 sptmni.
5-FU/LV + bevacizumab
Acid folinic 500mg/m
2
I.V. zilele 1,8,15,22,29,36
5-Fluorouracil 500 mg/m
2
I.V. (bolus) zilele 1,8,15,22,29,36
Bevacizumab 5 mg/kg I.V. (perfuzie 90) zilele 1,15,29
Se repet sptmnal pn n sptmna 6, ulterior (din ziua 43) la fiecare 2 sptmni.
Tratamentul sistemic: Noile terapii
n ultimii ani, noi molecule inteligente s-au adugat la arsenalul terapeutic utilizat n
cancerele de colon; o parte dintre acestea i-au demonstrat deja utilitatea n tratamentul
CCR metastatic.
Edrecolomab este un anticorp monoclonal IgG
2
mpotriva antigenului glicopeptidic
17-1A (sau molecula de adeziune epitelial EpCAM).
Iniial, un studiu de mici dimensiuni n CCR n stadiul III a demonstrat o reducere a
frecvenei recidivelor la pacienii tratai cu edrecolomab dup chirurgia singur [16].
Un studiu randomizat pe 2.761 pacieni cu stadii III de cancere de colon nu a demonstrat
ameliorarea rezultatelor la pacienii tratai cu 5-FU/AF + edrecolomab comparativ cu
5-FU/AF: supravieuirea la 3 ani a fost de 74,7% vs. 76,1% (p=0.53), iar intervalul liber de
boal (DFS) de 53% vs. 65,5% (p <0.0001) [14].
220
Cancerul colo-rectal
Cetuximab este un anticorp himeric care vizeaz receptorul factorului epidermal de
cretere (EGFR), activ n CCR metastatice refractare la chimioterapia cu irinotecan.
n prima linie de tratament, studiile de faz II, nerandomizate au demonstrat rezultate
promitoare cnd cetuximab a fost asociat cu protocoalele FOLFOX sau FOLFIRI n
tumorile ce exprim EGFR.
Mai multe studii mari sunt planificate n SUA i Europa pentru evaluarea rezultatelor
FOLFOX cetuximab n adjuvan (ameliorarea DFS la 3 ani la pacienii cu CCR stadii II-
III operai radical) [14,15].
Cetuximab + irinotecan amelioreaz supravieuirea fa de cetuximab singur n cazurile de
CCR metastatic rezistente la irinotecan. Cetuximab + FOLFIRI amelioreaz TTP i RR vs.
FOLFIRI n linia I de tratament (studiul CRYSTAL).
Bevacizumab este un anticorp monoclonal umanizat care intete receptorul factorului
vascular endotelial de cretere (VEGF), esenial pentru angiogenez.
Studiile randomizate au demonstrat creterea eficacitii cnd bevacizumab este asociat cu
FOLFIRI i 5-FU/AF n prima linie de tratament a CCR metastatice i cu FOLFOX n linia a
doua. Dou studii mari asupra tratamentului adjuvant al stadiilor II-III de CCR coninnd
bevacizumab sunt n curs de desfurare (NSABP C-08 i AVANT).
Bevacizumab asociat chimioterapiei amelioreaz supravieuirea att n linia I (cu IFL sau 5-
FU/AF [Horwitz et al.], FOLFOX/XELOX [N016966]), ct i n linia a II-a de tratament n
CCR metastatice (cu FOLFOX [3200]).
Circa 60% din pacienii cu CCR se prezint cu boal avansat (n principal metastaze
hepatice), care netratat determin o supravieuire median de 5-6 luni [21].
Cei cinci ageni care s-au adugat ntr-o succesiune rapid la panoplia terapeutic a
CCR (oxaliplatin, irinotecan, capecitabin, bevacizumab, cetuximab) au dublat
supravieuirea median n CCR metastatic (de la 10 la 20 luni), fa de rezultatele
obinute cu asocierea 5-FU/AF. Alegerea tratamentului se bazeaz pe eficacitate,
profilul toxic i preferina pacientului [23].
Prima linie de tratament optim n CCR metastatic se bazeaz actual pe dubla
asociaie de fluoropirimidin cu oxaliplatin sau irinotecan, care trebuie asociate cu
bevacizumab. Este bine cunoscut c, dup eecul unui regim de tip irinotecan+5-FU
n prima linie, se va continua n linia a II-a cu asocierea 5-FU+oxaliplatin, deoarece
oxaliplatin nu este foarte eficace ca monoterapie [24].
Fluoropirimidinele orale (capecitabin UFT) au demonstrat o eficacitate similar cu
regimul clasic 5-FU/AF, uurin de administrare i ameliorarea calitii vieii
Terapia cu bevacizumab poate fi responsabil pentru expunerea crescut a pacienilor
la complicaii postoperatorii, motiv pentru care aceasta trebuie efectuat la interval
de 4-6 sptmni nainte sau dup chirurgie.
TABEL 6-14. Protocol de prescriere a tratamentului cu bevacizumab
Criterii de includere
- pacieni cu CCR metastazat, ca linia I de tratament
- n asociere cu scheme de chimioterapie: FOLFOX, FOLFIRI, XELOX
- n uniti sanitare a cror dotare permite administrarea, i unde boala poate fi corect urmrit
(criterii RECIST)
- pacieni cu speran de via >6 luni, funcie renal i hepatic adecvat, rezerv medular
corespunztoare, metastaze inoperabile
221
CANCERELE DIGESTIVE
Criterii de excludere
- cardiopatie ischemic, HTA necontrolat, terapie zilnic cu aspirin (>300mg/zi) sau anticoagulant
- intervenie chirurgical major la < 1 lun de la nceputul tratamentului
- ulcer gastric/duodenal activ
- tumora colonic neoperat
- pacienii necompliani
- metastaze cerebrale
Dozare
- bevacizumab 5 mg/kg la 2 sptmni, n asociere cu FOLFOX4/FOLFIRI
- bevacizumab 7.5 mg/kg la 3 sptmni, n asociere cu oxaliplatin 130 mg/m
2
, ziua 1, i
capecitabin 1000 mg/m
2
x 2/zi, zilele 1-14, repetat la fiecare 3 sptmni.
Monitorizarea pacienilor sub tratament
- evaluarea neoplaziei dup criteriile RECIST la 2 luni (maxim la 3 luni)
- analize hematologice i biochimice n limite adecvate contiuarea terapiei
Criterii de ntrerupere a tratamentului
- progresia bolii
- toxiciti inacceptabile (beneficiul terapeutic nu justific scderea prea marcat a calitii vieii)
Chimioterapia intra-arterial hepatic
Reprezint o modalitate de tratament local al pacienilor cu metastaze hepatice de
cancere de colon, ce nu pot fi abordate chirurgical.
Citostaticele cu metabolizare hepatic rapid (ex. 5-FU, FUDR) permit o cretere a
timpului de expunere a metastazelor la CHT, cu reducerea toxicitii sistemice, atunci
cnd sunt injectate n artera hepatic.
Tehnica actual presupune instalarea chirurgical a unui cateter n artera gastro-duo-
denal i eventual ligatura arterei pilorice i colecistectomia pentru evitarea
colecistitei i ulcerelor chimice; cateterul se racordeaz la o pomp implantabil sau
la o camer sub-cutanat perfuzabil printr-o pomp extern.
Chimioterapia intra-arterial hepatic este grevat de toxicitate important: hepatit
chimic, scleroz biliar, tromboz de cateter, hemoragie digestiv.
Chimioterapia intra-arterial hepatic rmne n studiu, datorit aciunii sale modeste
asupra supravieuirii, toxicitii i costului su ridicat, precum i a incapacitii de a
mpiedica dezvoltarea altor metastaze hepatice.
STRATEGIE TERAPEUTIC
Stadiul 0
Excizia local sau polipectomia simpl cu margini libere sau rezecia segmentar de
colon (pentru leziunile mari ce nu sunt abordabile prin excizia local).
Stadiul I
Rezecie larg chirurgical i anastomoz colo-colic.
Stadiul II
Rezecie chirurgical larg i anastomoz.
CHT adjuvant, RT sau imunoterapia se pot administra numai n cadrul unor trialuri.
222
Cancerul colo-rectal
Dei unele subgrupe de pacieni cu stadiul II de boal (obstrucie complet, perforaie)
prezint un risc crescut de metastazare postoperator, nu exist argumente conform
crora chimioterapia s-ar asocia cu o ameliorare evident a supravieuirii [26].
Stadiul III
Stadiul III de cancer de colon presupune invazia ganglionar regional; numrul ganglionilor
implicai afecteaz prognosticul: pacienii cu 1-3 ganglioni invadai prezint o supravieuire mai
lung fa de cei cu 4 ganglioni cu metastaze.
Opiunile terapeutice sunt:
Rezecia chirurgical larg i anastomoza.
Chimioterapia postoperatorie cu 5-FU/AF timp de 6 luni (pentru pacienii ce nu sunt
candidai pentru studii clinice).
Chimioterapice sau terapii biologice noi (n cadrul unor studii clinice) [26].
Stadiul IV
Metastazectomia hepatic (1-3 leziuni) poate determina supravieuiri de 20-30%.
Ablaia criochirurgical a fost asociat cu controlul pe termen lung.
Chimioterapia intra-arterial hepatic cu 5-FU, fluoxuridin sau antraciclin poate
determina rspunsuri obiective la nivelul metastazelor hepatice, dar fr creterea
supravieuirii n comparaie cu chimioterapia sistemic.
Alte terapii propuse n metastazele hepatice includ: embolizarea intrahepatic i
radioterapia interstiial.
Toxicitatea local hepatic este crescut, incluznd anomalii ale funciilor hepatice i
scleroz biliar fatal.
Chimioterapia paliativ cu 5-FU n perfuzie continu este considerat standard:
RR pot crete dup modularea cu AF, dar fr un efect clar asupra supravieuirii.
IFN- asociat cu 5-FU adaug un plus de toxicitate, fr nici un beneficiu clinic.
Irinotecan (camptotecin, CPT-11) determin RR de 10-20% la pacienii n progresie
dup 5-FU, fiind considerat standard pentru acest grup de pacieni.
UFT (Tomudex
) a demonstrat o activitate similar cu 5-FU/AF n bolus [26,27].
Recomandri ESMO 2007:
Prima linie de terapie va fi administrat precoce i va consta n 5-fluorouracil n variate
asociaii i scheme. Regimurile cu 5-FU n perfuzie lung sunt mai puin toxice de ct
regimurile cu bolus. Fluoropirimidinele orale (capecitabina) sunt o alternativ la
administrarea n bolus de 5-FU/LV (I, B).
Asocierea 5-FU/LV/oxaliplatin sau 5-FU/LV/irinotecan determin supravieuri mai
lungi dect 5-FU/LV (II, A).
Anticorpii monoclonali anti-factor de cretere endotelial trebuie luai n considerare la
anumii pacieni selecionai atent. Bevacizumab crete supravieuirea general i
supravieuirea fr progresie n pima linie de tratament n asociere cu regimurile pe baz
de irinotecan. Cetuximab n asociere cu irinotecan este activ la pacienii cu CCR
metastatic, refractari la irinotecan.
Chimioterapia de linia II trebuie avut n vedere la pacienii care i menin un bun
status de performan (I,A)[29].
223
CANCERELE DIGESTIVE
TABEL 6-15. Planuri de tratament utilizate n cancerul de colon metastatic [3]
Linia I
FOLFOX4, FOLFOX6 sau CAPOX
FOLFIRI
5-FU/AF, IFL, FOLFIRI sau FOLFOX n asociaie cu bevacizumab
Alte regimuri
Capecitabina (Xeloda
) monoterapie
Irinotecan monoterapie (350 mg/m
2
) sau IFL
XELOX (oxaliplatin i capecitabin)
XELIRI (Irinotecan i capecitabina)
5-FU monoterapie, perfuzie continu
Linia a II-a
Orice regim care nu a fost utilizat n prima linie de tratament (ex. FOLFOX urmat de FOLFIRI)
Cetuximab monoterapie sau n asociere cu irinotecan
Tratamentul actual al CCR avansate reprezint o expunere continuu la toi agenii
activi, incluznd 5-fluorouracil, irinotecan, oxaliplatin i bevacizumab; aceasta va
conduce la avantajul maxim de supravieuire, estimat actual la o medie >2 ani.
Complexitatea alegerilor terapeutice i supravieuirile pe termen lung actuale oblig la
individualizare terapiei; aceasta presupune utilizarea tuturor agenilor activi n cursul
tratamentului, innd cont de un echilibru corect ntre eficacitatea i toxicitatea
regimurilor alese la fiecare etap de tratament a CCR avansate. Strategiile terapeutice
actuale vor lua n considerare terapii tip stop & go, intervale de meninere a terapiei,
intervalele fr terapie ca i reutilizarea agenilor chimioterapeutici prealabil folosii,
astfel nct conceptul liniilor convenionale de tratament dispare, evolund spre un
sistem de tratament continuu [27].
Boala recidivat
Tratamentul depinde de sediul recidivei. Opiunile terapeutice includ [26]:
Rezecia chirurgical a recidivei locale;
Rezecia chirurgical a metastazelor izolate hepatice, pulmonare, ovariene;
Radioterapia paliativ;
Chimioterapia paliativ (fluoropirimidine cu modulare biochimic, perfuzii continue,
fluoropirimidine orale, citostatice noi);
Terapii biologice (numai n cadrul unor studii clinice).
Bibliografie
1. Alberts RS, Goldberg RM. Gastrointestinal tract cancers. n: Casciato DA, ed. Manual of clinical
oncology. 5th ed. Philadelphia: Lippincott, Williams & Wilkins, 2004:195-201.
2. Miron L. Cancerele colo-rectale. n Miron L, Miron I, eds. Chimioterapia cancerului - principii i
practic. Iai: Editura Kolos 2005:269-288.
3. Kim GP, Takimoto Ch, Allegra CJ. Colorectal cancer. n: Abraham J, Allegra CJ, Gulley J, eds. Bethesda
Handbook of clinical oncology. 2nd ed. Philadelphia: Lippincott, Williams & Wilkins, 2005: 107-122.
4. Niederhuber JE, Cole CE, Grochou L. Colon cancer. n: Abeloff MD, ed. Clinical oncology. 3rd ed. New
York: Elsevier Churchill Livingstone, 2004:1977-1942
5. Libutti SK, Saltz LB, Rustgi AK, et al. Cancer of the colon. n: DeVita VT JR, Hellman S, Rosenberg
SA, eds. Cancer: principles and practice of oncology. 7th ed. Philadelphia: Lippincott, Williams &
Wilkins, 2005:1061-1109.
224
Cancerul colo-rectal
6. Robustelli della Cuna G, Gennari L. Neoplasie dell aparecchio dirigente. n: Bonadonna G, ed. Medicina
oncologica. 7ma ed. Milano: Masson, 2003:907-913.
7. Skibber JM, Minsky BD, Hohh PM. Cancer of the colon and of the rectum. n: DeVita VT Jr. Hellman S,
Rosenberg SA, eds. Cancer: principles and practice of oncology. 6th ed. Philadelphia: Lippincott,
Williams & Wilkins, 2001:1216-1319.
8. Ellernhorn JDI, Cullinane CA, Coia LR, et al. Colorectal and anal cancers. n: Pazdur R, Coia LR,
Hoskins WJ, eds. Cancer management: a multidisciplinarry approach. 8th ed. New York: CMP
Oncology, 2004:323-357.
9. UICC/AJCC Cancerele de colon i rect. n: Robin LH, Wittekind Ch, eds. TNM - clasificarea tumorilor
maligne. Ed. a 6-a (2002). Editura Ministerului Sntii, 2005:72-77.
10. Taal BG, Van Tinteren H, Zoetmulder FA. Adjuvant 5-FU plus levamisole in colonic or rectal cancer:
Improven survival in stage II and III. Br J Cancer 2001;85:1437-1443.
11. Skibber JM, Eng C. Colon, rectal, and anal cancer management. n: Chang AE, Ganz PA, Hayes DF, eds.
Oncology - an evidence based approach. New York: Springer, 2006: 704-732.
12. Sobrero A, Gugliemi A. Current controversis in the adjuvant therapy of colon cancer. Ann Oncol 2004;
15(suppl.4):iv39-iv41.
13. Cassidy J. Adjuvant chemotherapy for colon cancer. n: Perry CM, ed. Educational book of the American
Society of Clinical Oncology 41st annual meeting, 2005:260-263.
14. Tabernero J, Salazar R, Casado E. Targeted therapy in advanced colon cancer: the role of new therapies.
Ann Oncol 2004;15(suppl.4):iv55-iv62.
15. Miron L. Chimioterapia cancerelor colo-rectale. n: Stanciu C, ed. Cancerul colo-rectal: epidemiologie,
clinic, prevenie. Iai: Editura Gr.T.Popa, 2003:262-294.
16. Miron L. Tratamentul sistemic al cancerelor colo-rectale. Standarde actuale i perspective. Rev Med Chir
2003;107(4):752-775.
17. van Custem EJD, Oliveira J, Kataja VV. ESMO Minimum clinical recomandation for diagnosis, adjuvant
treatment and follow-up of colon cancer. Ann Oncol 2005;16(suppl.1):i16-i17.
18. Labianca R, Garassimo MC. Adjuvant chemotherapy for colon cancer. n: Proceedings Book of 17th
International Congress on Anti-Cancer Treatment, Paris 2006:51-54.
19. Benson Al. Carcinomas of the gastro-intestinal tract. n: Skeel RT, ed. Handbook of cancer
chemotherapy. Philadelphia: Lippincott, Williams & Wilkins, 2003:231-293.
20. de Gramont A. Management of different lines of treatment in metastatic colorectal cancer. n:
Proceedings Book of the 17
th
International Congress on Anti-Cancer Treatment, Paris 2006:147-152.
21. de Gramont A. Overview on the management of advanced colorectal cancer. n: Proceedings Book of the
15
th
International Congress on Anti-Cancer Treatment, Paris 2004:35-38.
22. Mass RD, Fyfe G, Hambleton J et al. Bevacizumab in combination with 5-FU/leucovorin improves
survival in patients with metastatic colorectal cancer: a combined analysis. J Clin Oncol 2004;22:274.
23. de Gramont A, Figer A, Seymour M, et al. Leucovorin and fluorouracil with or without oxaliplatin as
first-line treatment in advanced colorectal cancer. J Clin Oncol 2000;18(16):2938-2947
24. Miron L, Marinca M, Clement D. Tratamentul sistemic al cancerului colo-rectal metastatic: opiuni i
standarde actuale. Rev Ed Med Cont Gastroenterol 2006;1(5):53-61.
25. National Comprehensive Cancer Network. Colon cancer. n: Clinical practice guidelines in oncology.
2007, www.nccn.org
26. Ellenhorn JDI, Culliane CA, Coia LR, et al. Colon, rectal, and anal cancers. In: Pazdur R, Coia LR,
Hoskins WJ, eds. Cancer management: a multidisciplinary approach. 10th ed. New York: CMP Medica
Oncology 2007:339-365.
27. Grothey A. The continuum of care in colo-rectal cancer: eliminanting the concept of distinct lines of
treatment. In Govindan R, ed. American Society of Clinical Oncology Education Book 43rd Annual
Meeting 2007:224-228.
28. Hermann R. Colon cancer: ESMO Clinical recommendations for diagnosis, adjuvant treatment and
follow-up. Ann Oncol 2007;18(suppl.2):ii21-ii22.
29. Van Cutsem EJD. Advanced colo-rectal cancer: ESMO Clinical recommendations for diagnosis,
treatment and follow-up. Ann Oncol 2007;18(suppl.2):ii25-ii26.
225
CANCERELE DIGESTIVE
CANCERUL RECTAL
Recidiva local i/sau metastazele la distan survin la 50% din pacienii cu cancer
rectal. Factorii de risc semnificativi sunt prezena adenopatiilor metastatice i invazia
profund n peretele intestinal.
n absena adenopatiilor, rata de recidiv este de 5-19% n stadiul I i de 15-30% n
stadiul II; n stadiul III, incidena recidivelor pelvine crete la peste 50%.
Recidivele locale (n absena bolii metastatice) sunt mult mai frecvente n cancerul
rectal spre deosebire de cancerele de colon. Procedura de excizie total a mezorectului
scade semnificativ riscul, totui recidivele locale rmn frecvente la pacienii n stadiile
II i III. Din acest motiv, pe lng tehnicile chirurgicale agresive (exenteraii pelvine
anterioare, posterioare, rezecii sacrate), n cancerele rectale avansate sunt necesare alte
modaliti terapeutice asociate, cum ar fi chimio-radioterapia.
Tratamentul loco-regional: Chirurgia
Chirurgia este tratamentul primar, care poate determina vindecarea a 45% din pacienii
cu cancer rectal [1].
Cancerul rectal poate fi tratat curativ doar dac este diagnosticat n stadiul localizat,
prognosticul fiind n relaie cu profunzimea invaziei tumorale n peretele rectului i cu
prezena sau absena afectrii ganglionare.
Procedurile de stadializare preoperatorii includ examinarea digital rectal, examenul
computer tomografic sau rezonana magnetic nuclear, evaluarea endoscopic
ecografic (EUS), biopsia.
EUS este o metod sensibil de evaluare a stadiului tumoral (95%), a extensiei ganglionare
(74%) i a bolii regionale peritoneale [2].
Examenele CT, IRM i tomografia cu emisie de pozitroni (PET) pot fi utilizate i n detecia
bolii metastatice (cel mai frecvent localizat hepatic).
Stadializarea clinico-patologic este cel mai bun indicator prognostic.
Opiunile chirurgicale pentru tumorile rectale includ urmtoarele:
Rezecie anterioar rectal pentru rectul mijlociu i superior (6-15 cm de la
marginea anal);
Rezecie i anastomoz colo-anal cu/fr mpingere, excizie transanal, abord
transsfincterian i parasacrat sau rezecie abdomino-perineal pentru rectul inferior
(0-5 cm de la marginea anal):
Excizia mezorectal total (EMT);
mezorectul este definit ca esutul vascular, limfatic i neural aderent circumferenial la rect
de la promontoriul sacrat la muchii ridictori anali;
date ale unor studii europene sugereaz c ratele de recidiv local ar putea fi sczute prin
disecia n bloc a ntregului mezorect la momentul extirprii tumorale [5].
Tratamentul loco-regional: Radioterapia
Radioterapia preoperatorie (neoadjuvant) extern
Determin ameliorarea controlului local i a supravieuirii fr recidiv, fiind
administrat n urmtoarele scopuri:
creterea procentelor de rezecabilitate prin reducerea volumului tumoral (down staging);
diminuarea posibilitii de diseminare intraoperatorie a bolii neoplazice;
sterilizarea micrometastazelor i/sau a adenopatiilor regionale.
226
Cancerul colo-rectal
Se utilizeaz doze totale (DT) de:
25-35 Gy n 1-2 sptmni (fracii zilnice de 2, 3 i 5 Gy);
45 Gy n 4-5 sptmni (fracii zilnice de 1,8-2 Gy);
Riscul (singular) este cel al unui tratament excesiv al stadiilor precoce (stadiul I).
EUS poate defini mai bine invazia neoplazic local (acuratee diagnostic: 87-95%),
diminund riscul de substadializare (5%) i suprastadializare (5-18%).
Radioterapia preoperatorie (neoadjuvant) endocavitar
Pentru a se obine rezultate favorabile, tumora trebuie s ndeplineasc urmtoarele
condiii:
s fie foarte accesibil (la distan de cel mult 12 cm de orificiul anal);
s aib dimensiuni reduse ( 3-5 cm n diametru);
s fie puin infiltrativ, moderat sau bine difereniat [5].
Iradierea se poate face pe volumul-int de ordinul I (ganglionii pelvini, cicatricea
perineal), de ordinul II (pelvis), eventual de ordinul III (ganglionii para-aortici) prin:
dou cmpuri opuse izocentrice antero-posterioare cu supravoltaj;
patru cmpuri izocentrice (tehnica "box");
trei cmpuri izocentrice (unul dorsal i dou laterale, cu filtru pan);
cmp direct.
Radioterapia postoperatorie (adjuvant)
Radioterapia postoperatorie determin scderea ratei recidivelor locale, dar nu prezint
un rol cert asupra supravieuirii.
Se pot administra DT de:
45-50 Gy n 5-6 sptmni (fracii zilnice de 1.8 Gy) pe volumul-int de ordinul II (restane
tumorale) + 10-15 Gy n 1-2 sptmni pe volumele-int de ordinul I (boost)
45-50 Gy n 5-6 sptmni (fracii zilnice de 1.8 Gy) pe volumul-int de ordinul III
Radioterapia "sandwich"
Presupune administrarea RT:
preoperator: 25 Gy n 2 sptmni (fracii zilnice de 2.5 Gy)
postoperator: 25 Gy n 2 sptmni (fracii zilnice de 2.5 Gy)
Chimio-radioterapia postoperatorie
Pacienii n stadiile II-III de cancer rectal prezint un risc crescut de recidiv local i
sistemic, terapia adjuvant trebuind n aceste cazuri s combat ambele probleme.
Asocierea 5-fluorouracil (5-FU) cu RT (DT 40-44 Gy pe volum de ordinul II,
eventual "split course") este eficace i trebuie considerat ca standard actual [7].
Adugarea de derivai de nitrozuree, levamisol sau leucovorin la acest regim nu
amelioreaz rezultatele [1].
TABEL 6-16. Asocierea chimio-radioterapiei postoperatorii n cancerul rectal
5-FU 500 mg/m I.V. (bolus) zilele 1-5 (sptmnile 1,5,17,21)
Radioterapie DT 45 Gy + boost 5.4 Gy (1,8 Gy/zi) sptmnile 9-13
5-FU 500 mg/m I.V. (bolus) zilele 1-3 (sptmnile 8,12)
sau
5-FU 225 mg/m I.V. (perfuzie 24h) zilnic (pe toat durata RT)
Capecitabin 850-1250 mg/m
2
P.O. zilele 1-14,22-35 (concomitent cu RT)
227
CANCERELE DIGESTIVE
Chimioterapia paliativ
Paliaia poate fi atins cu 5-FU monoterapie la 10-20% dintre pacienii cu cancere
rectale metastatice.
Mai multe studii sugereaz c asocierea AF la 5-FU crete paliaia simptomelor i
ratele de rspuns tumoral, dar nu amelioreaz ntotdeauna i supravieuirea n
cancerul rectal.
Asocierea irinotecan sau oxaliplatin cu 5-FU/AF poate fi eficace n tratamentul
tumorilor refractare la 5-FU [2].
STRATEGIE TERAPEUTIC
Stadiul 0
Opiunile terapeutice sunt:
Excizie local sau polipectomie simpl;
Rezecie rectal complet pe cale transanal / transcoccigian (n leziunile mari, ce
nu sunt abordabile prin excizia local);
Iradiere endocavitar;
Radioterapie extern local.
Stadiul I
Opiunile terapeutice recomandate n stadiul I sunt:
Rezecie anterioar chirurgical cu anastomoz termino-terminal (cnd se poate
practica o rezecie adecvat, cu suficient rect restant distal pentru a permite o
anastomoz convenional sau endo-anal);
Excizie chirurgical larg cu rezecie abdomino-perineal (n leziunile prea distale
pentru a fi abordate prin rezecie anterioar);
Rezecie chirurgical transanal radioterapie extern perioperatorie 5-FU;
Radioterapie endocavitar radioterapie extern (n tumorile < 3 cm, mobile,
neulcerate, bine difereniate, fr adenopatii palpabile) [6].
Stadiul II
n aceste stadii pot fi invadate vaginul, uterul, parametrele, ovarele, vezica urinar sau
prostata; din acest motiv, opiunile terapeutice sunt urmtoarele:
Rezecie tumoral anterioar joas larg (cu reanastomoz, cnd aceasta este
posibil), urmat de chimioterapie i apoi de radioterapie postoperatorie.
Rezecie chirurgical larg pe cale abdomino-perineal, cu chimioterapie adjuvant i
ulterior radioterapie postoperatorie.
Exenteraie pelvin total / parial, cu chimioterapie adjuvant i apoi radioterapie
postoperatorie (cnd se documenteaz invazia celorlalte organe pelvine).
Radioterapie preoperatorie chimioterapie, urmat de chirurgie (n tentativa de a
conserva funcia sfincterian) [7].
Radioterapia intraoperatorie (IORT) cu electroni pe sediile cu boal rezidual
microscopic sau macroscopic.
IORT poate fi asociat cu RTE i CHT numai la anumii pacieni selecionai, cu intenia de
a ameliora controlul local [8].
228
Cancerul colo-rectal
Stadiul III
Opiunile terapeutice includ:
Excizie chirurgical larg i rezecie anterioar joas cu reanastomoz colo-rectal
sau colo-anal, urmat sau nu de chimioterapie i radioterapie postoperatorie;
Rezecie chirurgical larg, pe cale abdomino-perineal, urmat de chimioterapie
adjuvant i radioterapie postoperatorie;
Exenteraie pelvin total / parial, urmat de CHT i ulterior de RT adjuvant;
Radioterapie preoperatorie CHT, urmat de chirurgie (n tentativa de a conserva
funcia sfincterian), dup care se poate administra CHT adjuvant [7]:
Radioterapia preoperatorie este superioar celei postoperatorii, asocierea cu chimioterapia
determinnd o ameliorare suplimentar a controlului local;
Radioterapie postoperatorie pe sediile tumorale reziduale dup chirurgia de exerez;
IORT pe sediile cu boal rezidual microscopic sau macroscopic;
Chimio-radioterapie paliativ.
Stadiul IV
Opiunile terapeutice sunt:
Rezecie chirurgical cu anastomoz sau by-pass al leziunilor ocluzive sau rezecie
simpl pentru paliaia simptomelor (rectoragie);
Rezecia chirurgical a metastazelor izolate (pulmonare, hepatice, ovariene);
Chimio-radioterapia pentru paliaia local;
Chimioterapia singur pentru metastazele la distan, dup rezecia bolii locale;
Includerea pacientului n studii clinice de evaluare a noilor citostatice i a terapiilor
biologice antitumorale (9).
Boala recidivat
Opiunile terapeutice n formele recidivante de cancere de rect sunt:
Rezecia recidivelor locale cu intenie paliativ sau curativ n anumite cazuri
selecionate (mai ales dac intervenia iniial nu a fost adecvat);
Rezecia metastazelor hepatice sau pulmonare izolate la subgrupuri selectate de
pacieni (au fost raportate rate de vindecare la 5 ani reduse);
Radioterapia paliativ;
Chimioterapia paliativ;
Chimio-radioterapia paliativ [9].
Recomandri ESMO 2005/2007:
Boala localizat
Strategia general presupune urmrirea anumitor obiective (diminuarea riscului de
boal rezidual pelvin preferabil <5% cu preul unei morbiditi acute i cronice
reduse; conservarea funciei sfincterului anal), care ns nu pot fi atinse la majoritatea
pacienilor (<10% dintre pacienii care se prezint cu tumori fixate la peretele pelvin).
Tratamentul va ine cont de riscul terapeutic:
- n stadiile T1-2 i unele T3N0 se recomand chirurgia singur, fie ca procedur local
(microdisecie endoscopic transanal) la anumite cazuri selectate T1N0 (I,A), fie ca
disecie radical agresiv cu excizia total a mezorectului (ETM) (II,A).
229
CANCERELE DIGESTIVE
- n stadiile local avansate (majoritatea T3, unele T4N+) se recomand radioterapia (RT)
preoperatorie (DT 25 Gy/5 fracii) urmat de ETM, ca fiind o opiune mai simpl i
asociat cu mai puine efecte secundare. Mai eficace, dar mai agresiv, este RT n DT
46-50 Gy (1.8-2 Gy/fracie), cu sau fr 5-fluorouracil (5-FU) n bolus, perfuzie
continu sau oral (III,A). Cnd este posibil, tratamentul preoperator este de preferat,
fiind mai eficace i mai puin toxic dect cel postoperator (I,A).
- n formele local avansate nerezecabile (cel mai frecvent T4, unele T3) se prefer
chimio-radioterapia (CHT-RT) (DT 50.4 Gy, 1.8 Gy/fracie, concomitent cu 5-FU)
(I,A), urmat eventual de chirurgia radical dup 6-8 sptmni.
CHT-RT postoperatorie nu se mai recomand actual, dar se poate utiliza la pacienii cu
margini circumfereniale de rezecie pozitive, cu perforaie n aria tumoral sau n alte
situaii cu risc crescut de recidiv local (I,A).
n stadiile III i II cu risc crescut se poate administra CHT adjuvant, dei nu exist
dovezi suficiente ca n cazul cancerelor de colon n stadii similare (II,A).
Boala recidivat
Dac RT nu a fost administrat anterior, pacienii cu recidiv vor putea fi tratai prin
CHT-RT preoperatorie (II,A). La pacienii iradiai n prealabil se va tenta RT
suplimentar, fie extern fie intraoperatorie (IV,D).
Chirurgia radical poate fi preconizat la un interval de 6-8 sptmni dup RT (II,A).
Boala diseminat
La pacienii cu boal diseminat iniial (metastaze sincrone) se poate administra mai
nti tratamentul loco-regional i apoi cel sistemic, sau invers, conduita optim
rmnnd necunoscut (IV,D). Se vor lua n considerare: preferinele pacientului,
extensia tumorii primare i a metastazelor.
n cazuri selectate, tratamentul va include chirurgia metastazelor hepatice/pulmonare
(III,A) sau RT, ca proceduri paliative (II,A).
Chimioterapia de linia I trebuie luat n considerare, i va consta n variate asociaii pe
baz de 5-FU/AF, cu oxaliplatin sau irinotecan, i cu sau fr bevacizumab (I,A).
Chimioterapia de linia II va fi preconizat numai la anumii pacieni selectai, care i
menin statusul de performan bun (I,A) [10,11].
URMRIRE
Recomandri ESMO 2005/2007:
Urmrirea are scopul de a identifica pacienii care necesit terapie de salvare sau
paliativ i pentru a preveni cancerele colo-rectale secundare. Nu exist dovezi c
urmrirea periodic dup un tratament eficient amelioreaz rezultatele la pacienii cu
cancer rectal.
Recomandrile provizorii pentru urmrirea pacienilor cu cancer rectal sunt:
- Anamneza i rectosigmoidoscopia (cu endosonografia este disponibil) la fiecare 6 luni
timp de 2 ani (V,D);
- Istoric i colonoscopie cu rezecia polipilor la fiecare 5 ani;
- Examenul clinic, de laborator i explorrile radiologice nu prezint un beneficiu probat
i trebuie limitate la pacienii cu simptome de suspiciune [10,11].
230
Cancerul colo-rectal
Bibliografie
1. Libutti SK, Tepper JE, Saltz LB, et al. Cancer of the rectum. In: DeVita VT Jr, Hellman S, Rosenberg
SA, eds. Cancer: principles and practice of oncology. 7th ed. Philadelphia: Lippincott Williams &
Wilkins, 2005:1110-1125.
2. Skibber JM, Eng C. Colon, rectal, and anal cancer management. In: Chang AE, Ganz PA, Hayes DF, eds.
Oncology - an evidence based approach.. New York: Springer, 2006:704-732.
3. UICC/AJCC Cancerele de colon i rect. In: Robin LH, Wittekind Ch, eds. TNM - clasificarea tumorilor
maligne. Ed. a 6-a (2002). Editura Ministerului Sntii, 2005:72-77.
4. Ellernhorn JDI, Cullinane CA, Coia LR, et al. Colorectal and anal cancers. In: Pazdur R, Coia LR,
Hoskins WJ, eds. Cancer management: a multidisciplinary approach. 8th ed. New York: CMP Oncology,
2004:323-357.
5. Enker WE, Thaler HT, Cranor ML, et al. Total mesorectal excision in the operative treatment of
carcinoma of the rectum. J Am Coll Surg 1995;181(4):335-346.
6. Zaheer S, Pemberton JH, Farouk R, et al. Surgical treatment of adenocarcinoma of the rectum. Ann Surg
1998; 227(6):800-811.
7. Valentini V, Coco C, Cellini N, et al. Preoperative chemoradiation for extraperitoneal T3 rectal cancer:
acute toxicity, tumor response, and sphincter preservation. Int J Radiat Oncol Biol Phys 1998;
40(5):1067-1075.
8. Gunderson LL, Nelson H, Martenson JA, et al. Locally advanced primary colorectal cancer:
intraoperative electron and external beam irradiation +/- 5-FU. Int J Radiat Oncol Biol Phys 1997;
37(3):601-614.
9. National Comprehensive Cancer Network. Rectal cancer. In: Clinical practice guidelines in oncology.
2007, www.nccn.org
10. Tveit KM, Kataja VV. ESMO Minimum clinical recommendations for diagnosis, treatment and follow-up
of rectal cancer. Ann Oncol 2005;16(suppl.1):i20-i21.
11. Glimelius B. Rectal cancer: ESMO Clinical recommendations for diagnosis, treatment and follow-up.
Ann Oncol 2007;18(suppl.2):ii23-ii24.
12. Wsalty LB, Niedzwiecki D, Hollis D, et al. Irinotecan, fluorouracil plus leucovorin is not superior to
fluorouracil plus leucovorin alone as adjuvant treatment for stage III colon cancer: results of CALGB
89803. J Clin Oncol 2007;25:3456-3461.
231
CANCERELE DIGESTIVE
232
Cancerul anal
EPIDEMIOLOGIE
Cancerul anal (CA) reprezint 1-2% dintre cancerele intestinale i circa 4% din
totalitatea neoplaziilor tractului digestiv inferior. Peste 80% din CA survin la vrste de
50-60 ani, mai frecvent la femei (raport M/F 2:1).
Anatomic, CA sunt localizate la nivelul canalului anal (de la inelul anal la mijlocul
distanei dintre linia pectinat i marginea anal, mai frecvent la femei) i al marginilor
anale (incluznd pielea perianal, mai frecvent la brbai incidena la adultul tnr de
sex masculin este n cretere, n relaie cu infecia cu HPV i HIV) [1].
ETIOLOGIE
Etiologia este necunoscut, dar sunt considerai factori favorizani:
infecia cu HPV 16 i 18 (ar putea fi un factor etiologic) sau HIV;
ragadele / fisurile anale / hemoroizii;
istoric de boli cu transmitere sexual / condiloame i limfogranuloame veneriene;
istoric de relaii sexuale anale, mai mult de 10 parteneri sexuali n antecedente;
antecedente de cancer de col uterin, vulvar sau vaginal;
SIDA / imunosupresia dup transplantele de organe solide;
utilizarea corticosteroizilor pe termen lung;
fumatul de igarete (crete riscul de CA x 8) [2].
HISTOLOGIE
Majoritatea tumorilor sunt carcinoame epidermoide (sau adenocarcinoame):
carcinom spinocelular cel mai frecvent
carcinom cloacogenic (bazaloid)
carcinom tranziional
carcinom mucoepidermoid
carcinom nedifereniat
adenocarcinom
Tumorile anale de alte histologii includ:
limfoame
carcinoame microcelulare (small cell)
melanoame [3].
DIAGNOSTIC
Examen clinic
Simptomele sugestive pentru diagnostic sunt:
rectoragia (50%) prurit (15%);
durere (arsur) anal (40%), senzaia de corp strin intrarectal (25%), tenesme;
prezena la palpare a unei tumorete dure sau a unei ulceraii anale cu margini
infiltrate (tueu rectal);
prezena adenopatiilor inghinale [4].
Cancerul anal
Investigaii paraclinice
examinarea endoscopic (anoscopia, rectoscopia) cu descrierea leziunii i aprecierea
invaziei n organele adiacente (vezic, uretr, vagin);
biopsia incizional (eventual sub ghidaj anoscopic);
biopsia ganglionar diferenierea adenopatiei inghinale inflamatorii de o metastaz;
examenul computer tomografic (CT) pentru evaluarea adenopatiilor pelvine;
radiografie toracic standard i ecografie hepatic (dei metastazele la distan sunt
rare la momentul diagnosticului);
cistoscopie i examen ginecologic aprecierea infiltraiei n organele urogenitale [5].
STADIALIZARE
Mrimea tumorii primare este cel mai important factor prognostic pentru supravieuire
la pacienii cu carcinom anal. Stadializarea carcinoamelor anale se face conform
sistemului TNM statuat de UICC i AJCC n 1997. Noua clasificare TNM 2002 (ediia a
6-a) nu aduce modificri [6].
TABEL 6-17. Clasificarea TNM UICC/AJCC 2002 a tumorilor anale
T (tumora primar)
To fr semne de tumor primar
Tis carcinom in situ
T1 tumora 2 cm n dimensiunea maxim
T2 tumora de 2-5 cm n dimensiunea maxim
T3 tumora > 5 cm n dimensiunea maxim
T4 tumora de orice dimensiune ce infiltreaz vaginul, uretra, vezica urinar (interesarea
exclusiv a muchiului sau a sfincterului)
N (ganglionii regionali)
No fr prezena metastazelor n ganglionii regionali
N1 metastaze prezente n ganglionii perirectali (i)
N2 metastaze n ganglionii iliaci interni i/sau inghinali unilaterali
N3 metastaze n ganglionii perirectali i inghinali i/sau iliaci interni i/sau inghinali bilaterali
M (metastaze la distan)
Mo absena metastazelor
M1 prezena metastazelor
pTNM Clasificarea patologic
Categoriile T, N, M corespund categoriilor T, N, M clinice.
pNo - Examenul histologic al unui prelevat de limfadenectomie regional include 12 ganglioni.
Examenul histologic al unui prelevat de limfadenectomie inghinal include 6 ganglioni.
Gruparea pe stadii
Stadiul 0 Tis No Mo
Stadiul I T1 No Mo
Stadiul II T2-3 No Mo
Stadiul IIIA T4 No Mo
T1-3 N1 Mo
Stadiul IIIB T4 N1 Mo
orice T N2-3 Mo
Stadiul IV orice T orice N M1
233
CANCERELE DIGESTIVE
EVOLUIE
Cancerul anal tinde s disemineze prin contiguitate, pe cale limfatic i mai rar pe cale
hematogen.
Invazia local (20-30%) include pielea i esutul subcutanat al perineului, esutul
adipos al spaiilor ischio-rectale, vaginul, uterul (femei), uretra, prostata i veziculele
seminale (brbai).
Diseminarea limfatic se face preponderent (47%) pe calea ascendent (ganglionii
rectali, recto-sigmoidieni, sigmoido-colici i aortici) sau pe calea lateral (23%)
(ganglionii obturatori, hipogastrici i sacrai laterali). Calea limfatic superficial
conduce la prezena adenopatiilor inghinale.
Pe cale hematogen (3-12%), prin intermediul plexului hemoroidal, embolii tumorali
ajung n ficat naintea ptrunderii n sistemul port.
Complicaiile cele mai frecvente sunt: hemoragia, hematuria, metroragia, complicaiile
infecioase locale (abcese, proctit).
Efectele secundare majore ale tratamentului survin n corelaie cu radioterapia extern
sau interstiial: scleroza anal (ce poate face necesar practicarea colostomiei) i
necroza postradic cu formarea de fistule [7].
PROGNOSTIC
Prognosticul carcinoamelor epidermoide ale canalului anal este relativ bun.
n formele asimptomatice de tumori anale maligne supuse chirurgiei locale,
supravieuirea fr semne de boal poate atinge 100% cazuri. Supravieuirea la 5 ani
oscileaz ntre 50-80%.
Factorii prognostici majori sunt:
sediul tumorii (canal anal vs. piele perineal);
mrimea tumorii (tumorile < 2 cm prezint un prognostic mai bun);
gradul de difereniere tumoral (tumorile bine difereniate sunt de prognostic mai
favorabil fa de tumorile mai puin difereniate);
invazia ganglionar: absena afectrii ganglionare sau excizia local [8].
PRINCIPII DE TRATAMENT
Carcinoamele anale sunt neoplazii frecvent curabile.
n stadiile iniiale, tratamentul chirurgical i/sau radioterapia (RT) prezint o finalitate
curativ. n formele local avansate, abordul terapeutic actual cuprinde o asociere de
chimio-radioterapie, indicaia chirurgical fiind mult redus.
Tratamentul loco-regional: Chirurgia
Tratamentul chirurgical, considerat standard pn la apariia chimio- i radioterapiei,
const din intervenii radicale:
Amputaia abdomino-perineal (procedeul Miles), cu intenie curativ, are indicaii
limitate la cazurile recidivate sau la cele local avansate nevindecate prin tratamentul
asociat chimio-radioterapic.
Excizia local obine un bun control local, cu vindecare pentru tumorile mici,
superficiale.
Dup chirurgia singur, chiar radical, recidivele locale sunt frecvente [9].
234
Cancerul anal
Tratamentul loco-regional: Radioterapia
Radioterapia extern (RTE)
RTE primar cu energii nalte are ca scop vindecarea, cu evitarea colostomiei i cu
conservarea funciei sexuale masculine. Efectele toxice imediate i tardive sunt minime,
dezavantajul major al RTE fiind posibilitatea apariiei stricturilor sfincteriene.
RTE poate fi singura metod de tratament n tumorile T1-2No, n doze totale de 60-
70 Gy (1.8 Gy x 5/sptmn). Se poate lua n considerare administrarea split-course,
cu o pauz de 2 sptmni.
Brahiterapia intracavitar
Dup RTE (DT 45-50 Gy pe tumora primar i ariile ganglionare) se poate aduga o
doz suplimentar (boost) de 15-20 Gy prin implante intracavitare de Iridium-192
(
192
Ir) (supravieuire fr boal la 5 ani de 67%).
Supravieuirea la 5 ani a pacienilor cu cancer anal, tratai numai cu RT (DT 45-70 Gy)
este de 32-92%, cu rate de control local de 60-90%. Aceste rezultate sunt comparabile
cu cele obinute prin chirurgia radical, n funcie de mrimea tumorii [10].
Tratamentul sistemic: Chimioterapia
Dei exist citostatice active (cisplatin, doxorubicin, mitomicin C, 5-fluorouracil),
chimioterapia singur nu i gsete indicaie n cancerele anale n stadiile localizate.
La pacienii cu boal metastatic, asocierea cisplatin, mitomicin C i 5-FU poate
determina rspunsuri obiective la 50% cazuri, dar acestea sunt de scurt durat.
Tratamentul combinat: Chimio-radioterapia
Atitudinea actual n cancerele anale const n chimio-radioterapie iniial, urmat
eventual dup 4-6 sptmni de intervenia chirurgical (excizie local sau amputaie
abdomino-perineal), numai n cazul tumorilor persistente de dimensiuni mari (> 5 cm)
sau a recidivelor. Prin aceast modalitate terapeutic se poate evita de cele mai multe ori
o intervenie chirurgical mutilant [11].
Studiul RTOG-9811 a indicat c utilizarea mitomicinei C cu 5-FU i RT crete controlul
local (rata de reducere a recidivei 46%) i amelioreaz supravieuirea fr boal la 5 ani
(65%) la pacienii N+, fa de RT i 5-FU singur [12].
La pacienii cu status de performan depreciat sau cu risc crescut de toxicitate
secundar se poate administra 5-fluorouracil + radioterapie (fr mitomicin C) [13].
TABEL 6-18. Protocoale de CHT-RT concomitent n cancerul anal
Protocolul RTOG
5-Fluorouracil 1000 mg/m
2
I.V. (perfuzie continu 24h) zilele 2-4,28-32
Mitomicin C 5-15 mg/m
2
I.V. (bolus) ziua 2
RTE radical DT 45 Gy (1.8 Gy/zi x 5/spt.), boost perineal 15 Gy zilele 1-28
5-Fluorouracil 1000 mg/m
2
I.V. (perfuzie continu 24h) zilele 1-4
Cisplatin 25 mg/m
2
I.V. (perfuzie 30) zilele 1-4
RTE radical DT 45-50.4 Gy (1.8 Gy/zi x 5/spt.) zilele 1-49
235
CANCERELE DIGESTIVE
STRATEGIE TERAPEUTIC
Stadiul 0
Rezecia chirurgical este modalitatea terapeutic acceptat pentru leziunile maligne
ce nu afecteaz sfincterul (indicaia depinde i de localizarea tumorii n canalul anal).
Stadiul I
Pentru tumorile mici ale pielii perianale sau ale marginilor anale (ce nu afecteaz
sfincterul) se prefer excizia larg local.
n cancerul canalului anal sau pentru tumorile mari, opiunile terapeutice includ
excizia larg local a tumorilor de dimensiuni reduse, a pielii perianale sau a
marginilor anale, sau CHT (5-FU mitomicin) concomitent cu RT definitiv
brahiterapie cu
192
Ir pentru tumorile nerezecabile.
Rezecia radical este rezervat pacienilor cu rspunsuri incomplete sau recidiv.
Asocierea CHT-RT de salvare poate amna colostomia permanent [14].
Stadiul II
Opiunile terapeutice sunt similare celor din stadiul II de boal.
Stadiul III
Stadiul IIIA se prezint clinic ca un stadiu II n majoritatea cazurilor, fiind stadializat
corect doar intraoperator sau dup examinarea ecografic endorectal/endoanal.
Tratament similar cu cel din stadiile I-II (se prefer asocierea CHT-RT).
Rezecie abdomino-perineal cu ablaia ganglionilor femurali, abductori i iliaci,
urmat de RT postoperatorie.
Stadiul IIIB este vindecabil, dei prezena adenopatiilor inghinale metastatice
reprezint un semn de prognostic negativ. Din acest motiv, pacienii n stadiul IIIB sunt
candidai la studii clinice ce testeaz noi modaliti de abord terapeutic.
RT asociat cu CHT (ca n stadiul II), cu rezecia chirurgical (local/ abdomino-
perineal) a tumorii reziduale, sau limfadenectomia inghinal superficial/ profund
n cazul tumorilor recidivate sau reziduale [14]
Stadiul IV
Opiunile terapeutice n aceste stadii includ:
Chirurgie paliativ
Chimioterapie paliativ
Radioterapie paliativ
Chimio-radioterapie paliativ
Nu exist o schem de CHT standard pentru boala metastatic, paliaia simptomelor
constituind scopul principal al tratamentului. Un protocol eficient poate fi:
Mitomicin C 10 mg/m
2
I.V. ziua 1
Doxorubicin 30 mg/m
2
I.V. ziua 1
Cisplatin 60 mg/m
2
I.V. ziua 1
Se repet la fiecare 4 sptmni x 2, apoi la fiecare 5 sptmni (mitomicin C la 10 sptmni)
Pacienii n stadiul IV trebuie avui n vedere pentru includere n trialurile clinice [14].
236
Cancerul anal
Boala recidivat
Recidivele locale dup radioterapie, chimioterapie sau chirurgie pot fi controlate
eficient, utiliznd tratamentele alternative (ex. rezecia chirurgical dup RT i invers).
Rspunsul complet la tratamentul combinat (CHT-RT) este de ateptat la 80-90% dintre
pacienii cu cancer de canal anal. Este important evaluarea rspunsului la tratament
prin examinarea atent a canalului anal, innd cont c aceste cancere pot continua s
regreseze >3 luni dup terminarea tratamentului. Din acest motiv, biopsia recomandat
dup completarea tratamentului nu se va practica mai devreme de 3 luni dac nu apar
progresia bolii sau alte semne de recidiv precoce. Dac aceast biopsie este pozitiv, se
va practica rezecia abdomino-pelvin care permite obinerea unui control pe termen
lung i a unei supravieuiri crescute la 40-60% dintre pacieni [5].
URMRIRE
Pacienii cu cancer anal trebuie monitorizai la fiecare 3 luni n primii 3 ani, la fiecare 6
luni n urmtorii 2 ani i ulterior anual.
Monitorizarea presupune: anamneza simptomelor, examinarea fizic, hemoleucograma
complet, testele hepatice, radiografia pulmonar, ecografia abdominal i un examen
computer tomografic la fiecare 6-12 luni n primii 3 ani [2].
Bibliografie
1. Alberts RS, Goldberg RM. Gastrointestinal tract cancers. In: Casciato DA, ed. Manual of clinical
oncology. 5th ed. Philadelphia: Lippincott, Williams & Wilkins, 2004:185-195
2. Cummings BJ, Ajani JA, Swallow CJ. Cancer of the anal region. In: DeVita VT Jr, Hellman S, Rosenberg
SA, eds. Cancer: principles and practice of oncology. 7th ed. Philadelphia: Lippincott Williams &
Wilkins, 2005:1125-1138.
3. Skibber JM, Eng C. Colon, rectal, and anal cancer management. In: Chang AE, Ganz PA, Hayes DF, eds.
Oncology - an evidence based approach.. New York: Springer, 2006:704-732.
4. Robustelli della Cuna G, Bonadonna G. Neoplasie dellaparecchio dirigente. In: Bonadonna G, ed.
Medicina oncologica. 7ma ed. Milano: Masson, 2003:1013-1016.
5. Ellernhorn JDI, Culliane CA, Coia LR, et al. Colon, rectal and anal cancers. In: Pazdur R, ed. Cancer
management: a multidisciplinarry approach. 10th ed. New York: CMP Medica Oncology 2007:339-65.
6. American Joint Committee on Cancer. Anal canal. n: Robin S, Wittekind F. AJCC Cancer Staging
Manual. 6th ed. New York: Springer, 2002:125-130.
7. Malik U, Mobiuddin M. Cancer of the anal canal. n: Abeloff MD, ed. Clinical oncology. 3rd ed.
Philadelphia: Elsevier Churchill Livingstone 2004:1967-1981.
8. Minsky BD, Hoffman JP, Kelsen DP. Cancer of the anal region, n: DeVita VT Jr, Hellman S, Rosenberg
SA, eds. Cancer: principles and practice of oncology. 6th ed. Philadelphia: Lippincott Williams &
Wilkins, 2001:1319-1342.
9. Saif MW, Hamilton MJ. Anal cancer. n: Abraham J, Allegra JC, eds. Bethesda Handbook of clinical
oncology. Philadelphia: Lippincott, Williams & Wilkins, 2001:113-125.
10. Cummings BJ. Anal cancer. Int J Radiat Oncol Biol Phys 1990;19(5):1309-15.
11. Zucali R, Doci R, Bombelli L. Combined chemotherapy-radiotherapy of anal cancer. Int J Radiat Oncol
Biol Phys 1990;19(5):1221-3.
12. Wolmark N, Wieand HS, Hyams DM, et al. Randomised trial of postoperative adjuvant chemotherapy
with or without radiotherapy for carcinoma of the rectum. National Surgical Adjuvant Breast and Bowel
Project Protocol R-02. JNCI 2000;92:388-396.
13. Benson AlB III. Carcinomas of the gastro-intestinal tract. n: Skeel RT, ed. Handbook of cancer
chemotherapy. Philadelphia: Lippincott, Williams & Wilkins 2003:250-251
14. National Comprehensive Cancer Network. Anal cancer. n: Clinical Practice Guidelines in Oncology
(PDQ
). Health Professionals Version 2007. www.nccn.org
237
CANCERELE DIGESTIVE
238
Cancerul hepatic
EPIDEMIOLOGIE
Carcinomul hepatocelular (CHC) reprezint a cincea neoplazie uman (667.000 cazuri
noi n 2005 n lumea ntreag). Indicele de mortalitate prin CHC atinge 94%.
Europa inciden de la 14/100.000/an (Italia) pn la 1,7/100.000/an (Olanda) la
brbai, i de la 4/100.000/an (Spania) pn la 0,3/100.000/an (Irlanda) la femei;
mortalitate de la 1,9/100.000/an (SUA, Anglia) pn la 1,5-20/100.000/an (Austria,
Africa de Sud), respectiv 115/1.000.000 locuitori/an (China, Thailanda)
Romnia inciden 7,54/100.000/an la brbai, respectiv 3,79/100.000/an la femei;
mortalitate 6,73/100.000/an la brbai i 3,91/100.000/an la femei [1].
ETIOLOGIE
Factorii de risc pentru apariia CHC sunt:
Ciroza hepatic:
infecia cronic cu VHB/ VHC
consumul cronic de alcool
aflatoxina B1 (Aspergillus flavus)
Incidena cumulativ la 5 ani a CHC la pacientul cirotic este de 15-20%. Brbatul
cirotic cu valori mari ale AFP prezint un risc foarte crescut de a dezvolta un CHC.
Fumatul
Diabetul zaharat (insulina)
Tratamentele hormonale: contraceptivele orale, steroizii androgenici
Thorotrast
(substan de contrast radiologic) [2].
HISTOLOGIE
Tumorile maligne primare hepatice sunt n general adenocarcinoame, cu dou tipuri
majore: carcinomul hepatocelular (90%) i colangiocarcinomul (carcinomul cilor
biliare intrahepatice) [3].
Carcinomul hepatocelular varianta fibrolamelar (1% din CHC) nu se asociaz cu
ciroza hepatic, este frecvent la vrste mai tinere, prezint o evoluie clinic lent i
poate fi de obicei rezecat chirurgical.
O variant frecvent confundat cu metastazele de carcinoame renale i suprarenale este
carcinomul primitiv cu celule clare.
Mult mai rar, se ntlnesc sarcoame hepatice (hemangioendoteliom, sarcom cu celule
Kupfer). Hepatoblastomul apare rar la adult, fiind mult mai frecvent la copii i
adolesceni [5].
DIAGNOSTIC
Examen clinic
Diagnosticul de CHC este stabilit fie n stadiile avansate, fie ntmpltor n cursul unui
examen ecografic. Multicentricitatea i metastazele intrahepatice sunt tipice, n timp ce
localizrile secundare extrahepatice sunt foarte rare; metastazele osoase sunt mai
frecvente n colangiocarcinom.
Cancerul hepatic
Cele mai frecvente semne clinice (nespecifice) n CHC sunt:
durerea (91%);
pierderea ponderal (35%);
vomismentele (8%);
hepatomegalia (89%);
creterea de volum a abdomenului (43%);
icterul (7-41%);
manifestri paraneoplazice (hipoglicemie, hipercalcemie, hipercolesterolemie, febr,
sindrom carcinoid, eritrocitoz, porfirie cutanat tardiv, hipertiroidism, osteoporoz,
ginecomastie, atrofie testicular, pubertate precoce) [1,3].
Investigaii paraclinice
nivele crescute de alfa-fetoprotein (AFP) (70% - prognostic nefavorabil);
creterea transaminazelor, a fosfatazei alcaline i a -glutamil-transpeptidazei (GT),
hiperbilirubinemie.
aspecte tumorale caracteristice de scintigrafie hepatic, ecografie abdominal,
computer tomografie (CT) i imagistic n rezonan magnetic (IRM) [6].
STADIALIZARE
Sistemul de stadializare TNM a fost criticat deoarece nu evalueaz boala hepatic de
baz, care este evident un factor major prognostic la pacienii cu cancer hepatic, n afara
stadiului tumoral.
TABEL 6-19. Stadializarea TNM AJCC/UICC 2002 (ediia a 6-a) a tumorilor hepatice
i ale cilor biliare intrahepatice [7]
T (tumora primar)
Tx tumora primar nu poate fi diagnosticat
To fr evidena tumorii primare
T1 toate tumorile solitare fr invazie vascular, indiferent de dimensiune
T2 toate tumorile solitare cu invazie vascular, indiferent de stadiu i de dimensiune, sau
tumorile multiple cu dimensiuni < 5 cm.
T3 tumori unice/ multiple cu evidena invaziei vasculare majore i cu dimensiuni > 5 cm
T4 tumor sau tumori cu invazie direct la organele adiacente, altele dect vezica biliar, sau
cu perforaia peritoneului visceral
N (adenopatiile loco-regionale)
Nx ganglionii regionali nu pot fi evaluai
No fr adenopatii n ganglionii regionali
N1 adenopatii regionale metastatice prezente
M (metastazele la distan)
Mx metastazele la distan nu pot fi apreciate
Mo fr metastaze la distan
M1 metastaze la distan prezente
pTNM Clasificarea patologic
Categoriile pT, pN i pM corespund categoriilor T, N i M clinice.
pNo - Examenul histologic al materialului obinut prin limfadenectomie regional trebuie s includ >
30 ganglioni.
239
CANCERELE DIGESTIVE
Gruparea pe stadii
Stadiul I T1 No Mo
Stadiul II T2 No Mo
Stadiul III T1-2 N1 Mo
T3 No Mo
T4 Orice N Mo
Stadiul IV Orice T Orice N M1
PROGNOSTIC
AFP este un marker biologic util att n diagnosticul ct i n prognosticul CHC. Circa
50-70% dintre pacienii cu CHC prezint valori crescute ale AFP la momentul
diagnosticului, acetia avnd o supravieuire median mai redus [8].
Alte variabile cu valoare prognostic sunt:
statusul de performan;
funcia hepatic (rezerv hepatic adecvat: bilirubin <2.0 mg/dl, albumin seric
>3.5 g/dl, absena ascitei i a disfunciilor neurologice, status nutriional excelent);
prezena i severitatea cirozei n relaie cu clasificarea Child-Pugh (Tabel 19) [4,9].
Prognosticul pacienilor netratai rmne nefavorabil: supravieuirea median este de
3-6 luni i depinde de gradul afectrii hepatice.
TABEL 6-20. Clasificarea stadial conform Conferinei de consens de la Barcelona
(BCLC 2003)
Stadiul A (iniial)
Pacieni cu o singur tumor, sau trei tumori <3 cm, ce pot fi supui unei terapii radicale.
Substadiul A1: o singur tumor, fr hipertensiune portal (HTP), bilirubin normal.
Substadiul A2: o singur tumor, cu HTP, bilirubin normal.
Substadiul A3: o singur tumor, cu HTP, bilirubin crescut.
Substadiul A4: trei tumori, indiferent de funciile hepatice.
Stadiul B (intermediar)
Pacieni asimptomatici cu tumori multinodulare, fr invazie vascular sau extensie extrahepatic
Stadiul C (avansat)
Pacieni simptomatici, sau invazie tumoral vascular sau extrahepatic manifest.
Stadiul D (terminal)
Pacieni cu simptome severe (deteriorarea statusului de performan), sau alterarea avansat a
funciilor hepatice.
PRINCIPII DE TRATAMENT
Tratamentul CHC (cu intenie curativ sau paliativ) depinde n principal de extensia
local a tumorii i de boala hepatic preexistent.
Tratamentul curativ: Chirurgia
Rezecia chirurgical reprezint tratamentul de elecie la pacienii cu hepatocarcinom
localizat, asimptomatici, cu funcie hepatic conservat sau cu ciroz uoar [1,2].
240
Cancerul hepatic
TABEL 6-21. Scorul Child-Pugh
Parametru 1 punct 2 puncte 3 puncte
Bilirubina (mg/dl)
- pentru ciroza biliar primitiv
1-1.9
1-3.9
2-2.9
4-9.9
> 3.0
> 10
Timpul de protrombin (sec) 1-3 4-5 > 6
Albumina (g/dl) > 3.5 2.8-3.4 < 2.8
Ascit Absent Uoar/ Moderat Moderat/ Sever
Encefalopatie Absent Grad 1-2 Grad 3-4
Clas A
Clas B
Clas C
5-6 puncte
7-9 puncte
10-15 puncte
Ciroz bine compensat
Ciroz pe cale de decompensare
Ciroz decompensat
Hepatectomia parial/ extins
Segmentectomia/lobectomia hepatic rmne cea mai eficient metod terapeutic,
dar numai 13-35% dintre pacienii cu CHC sunt candidai la chirurgie.
Cele mai bune rezultate (supravieuire la 5 ani de 30-40%) se obin n stadiile I i II de
boal, la care pot fi obinute margini de rezecie chirurgical de cel puin 2 cm n
parenchimul hepatic normal. Supravieuirea este mai sczut (12-37%) la pacienii cu
tumori mari, cu invazie vascular i ciroz avansat. Mortalitatea perioperatorie este
< 5% (mai crescut n prezena cirozei).
Recidiva este frecvent observat n esutul restant. Extinderea hepatectomiei este
posibil la 10-29% dintre pacieni.
Tumorile mari pot fi nlturate prin hemihepatectomie extins; riscul este reprezentat
de metastazele mici n esutul hepatic. Reinterveniile pot fi de asemenea utile.
Prognosticul este sumbru: supravieuirea la 5 ani este de numai 25% chiar dup operaia
cu intenie curativ (recidive intrahepatice sau metastaze pulmonare i osoase).
Transplantul hepatic ortotopic
Este considerat actual cel mai eficace tratament al CHC (se adreseaz concomitent
tumorii primare, leziunilor hepatice secundare i cirozei). Este indicat la pacienii cu
ciroz sever sau cu rezecie extensiv dar cu rezerv minim hepatic; se efectueaz
efectiv la doar 5-15% dintre pacieni (contraindicaii numeroase, absena donorilor).
Criteriile de transplant sunt cunoscute sub numele de criteriile Milano: tumor unic
< 5 cm sau 2-3 tumori, fiecare cu diametru maxim < 3 cm i absena invaziei vasculare.
Pacienii cu colangiocarcinom intrahepatic nu sunt candidai la transplant.
Supravieuirea pe termen lung (4 ani) este de 60 pn la 75% (mortalitatea datorat
complicaiilor transplantului atinge 12-14%), dar rezultatele pot fi datorate seleciei mai
atente a pacienilor. Recidivele survin n mai puin de 15% din cazuri [10].
Tratamentul curativ: Distrucia local (tehnicile ablative)
Distrucia local reprezint cea mai recent introdus metod curativ; utilizeaz metode
simple (spitalizare scurt), bine tolerate i care pot fi administrate percutan:
chimice (alcool, acid acetic)
fizice (hipertermie, laser, crioterapie, radiofrecven, coagularea cu microunde,
radioterapie intraoperatorie, radioterapie interstiial).
Distrucia local nu este fezabil n cazurile cu ascit, hipocoagulare, localizare
subcapsular cu risc crescut de hemoragie i diseminare tumoral [11].
241
CANCERELE DIGESTIVE
Nu se nregistreaz diferene de supravieuire ntre metodele de ablaie percutan [13].
Injectarea percutan de etanol 95% (IPE) (Sugira, 1983) determin o asociere de efecte
distructive prin deshidratare celular i necroz de coagulare. Totui, aceasta nu reuete
s distrug celulele maligne de la periferia tumorii i nici nu poate fi folosit n
tratamentul tumorilor prea mici, nedetectabile la examenul ecografic. Avantajele acestei
metode sunt: simplitatea procedural, preul sczut i efectele adverse minime. Ratele
de rspuns sunt variabile, de la 90-100% (CHC < 2 cm, tumor unic, Child Pugh A) la
70% (CHC 3-5 cm, tumori multiple, Child-Pugh B) i respectiv 50% (CHC > 5 cm,
insuficien hepatic avansat). La pacienii selectai, cu rspunsuri complete,
supravieuirea la 5 ani este de 40-70%.
Ablaia termic prin radiofrecven (ARF) reprezint o alternativ de tratament percutan
la pacienii cu CHC nerezecabile dezvoltate pe ciroz cu scor Child-Pugh A sau B. Este
contraindicat n CHC localizate hilar, n organe extrahepatice, diafragm sau vase.
Determin o necroz mai mare i mai omogen, alte avantaje poteniale fa de injecia
cu etanol incluznd numrul mai mic de edine de tratament i un mai bun control
local; supravieuirea la 2 ani pare mai avantajoas pentru radiofrecven n unele studii
(96% vs. 62%) [12].
Patru studii recente, ce au comparat ARF cu IPE n CHC mici, au indicat un beneficiu
semnificativ n favoarea RF n termenii controlului local (rate de recidiv local la 2 ani
de 2-18% vs. 11-45%). Totui, aceste date nu sunt suficiente pentru a susine un
beneficiu de supravieuire dup RF [31].
Crioterapia a fost utilizat n tumorile > 3cm, dar necesit efectuarea unei laparotomii.
Radioterapia prezint un rol limitat n tratament, datorit intoleranei la iradiere a
esuturilor hepatice normale [4].
Tratamentul adjuvant i neoadjuvant: Chimioterapia
Rezultatele preveniei secundare dup (sau nainte) de interveniile terapeutice cu succes
necesit a fi ameliorate i confirmate n studii mai mari, pentru a obine un impact
asupra supravieuirii pe termen lung a pacienilor cu CHC.
Chemoembolizarea transarterial hepatic (CHEAT) poate influena pozitiv o eventual
procedur chirurgical ulterioar (scade riscul de hemoragie) i ratele de supravieuire.
CHEAT a fost testat la pacienii cu CHC aflai n ateptarea unui transplant hepatic,
unii dintre acetia prezentnd un beneficiu de supravieuire, dar care nu a fost confirmat
n alte studii. Polichimioterapia intra-arterial hepatic ar permite obinerea unor rate de
rspuns de 41-60%, cu supravieuire median de 19-20 luni [16].
CHT adjuvant sistemic a fost studiat n cteva trialuri, o meta-analiz din 2001 (de
mici dimensiuni !) relevnd un efect detrimental al acestei modaliti terapeutice.
n concluzie, la pacienii cu hepatocarcinom nu este recomandat actual chimioterapia
adjuvant/neoadjuvant cu administrare sistemic sau intraarterial hepatic [16].
Tratamentul paliativ: Chimioterapia
Chimioterapia sistemic a determinat rezultate dezamgitoare n CHC inoperabil,
posibil i datorit rezistenei multidrog native genic (MDR) a acestei neoplazii.
Chimioterapia este uzual utilizat pentru paliaia bolii nerezecabile, iar n cazul
tumorilor diseminate reprezint principala opiune de tratament la pacienii cu status
bun de performan.
242
Cancerul hepatic
Doxorubicin (adriamicin) a fost considerat mult timp citostatic de referin, dei a
demonstrat o foarte sczut eficacitate: rate de rspuns (RR) de 0-29% i nici un
beneficiu de supravieuire (media 4 luni), nregistrnd n schimb o tolerabilitate
redus i decese toxice la 25% din pacieni.
Alte citostatice clasice precum 5-FU (RR 17%), cisplatin (RR 17%) i etoposid
(RR 18%) sunt chiar mai puin active.
Citostaticele de generaia III nu au demonstrat activitate superioar (irinotecan - RR
14%, capecitabin - 13%, paclitaxel - RR 0-6%, doxorubicin liposomal - RR 0%).
Nolatrexed (Thymaq
800 mg/m
2
/zi, cicluri la 3 sptmni), un nou antimetabolit
care inhib direct i specific timidilat-sintetaza, se afl n studii de faz III, cu
rezultate preliminare promitoare.
Polichimioterapia asociaz citostatice precum: cisplatin, adriamicin, 5-FU i interferon
(PIAF) sau etoposid, cisplatin i 5-FU (ECF), care determin rate de rspuns cuprinse
ntre 15 i 35%, fr un beneficiu cert asupra supravieuirii. Nu exist n prezent un
regim de chimioterapie de referin [17,18,19].
Mai recent, regimul GEMOX (gemcitabin, oxaliplatin) a fost evaluat cu rezultate
promitoare ntr-un studiu pilot i un altul de faz II. Ratele de rspuns observate au
variat de la 17% la 40% iar controlul bolii a fost obinut n 67%, i respectiv 77% din
cazuri; supravieuirea fr boal (DFS) a fost de 6-8 luni, iar supravieuirea general
(OS) de 9-13 luni [26].
Chimioterapia sistemic nu este recomandat de rutin n cazul hepatocarcinoamelor
nerezecabile/ metastatice (20).
Tratamentul paliativ: (Chemo)embolizarea transarterial hepatic
Datorit particularitilor de vascularizaie, tumorile hepatice (primitive i secundare)
sunt candidate la proceduri de embolizare CHT regional (pe calea arterei hepatice).
Embolizarea arterei hepatice s-a dezvoltat ca o alternativ la ligatura arterial
intraoperatorie. Substana de embolizare (amidon, polivinil alcool, ulei iodat, Gelfoam,
Spherex, colagen) se va administra, eventual n mod repetat, prin cateterizarea sub
ghidaj fluoroscopic a arterei femurale pn la artera hepatic i selectiv ramurile ce irig
tumora), ct mai aproape de periferia teritoriului irigat, [22].
Chemo-embolizarea transarterial hepatic (CHEAT) este un tratament activ pentru
pacienii ce nu pot beneficia de tratamentul chirurgical curativ, dar care prezint nc o
funcie hepatic bun (Child-Pugh A), sunt asimptomatici, au un status de performan
ECOG/OMS 0-2), fr hipertensiune portal sau tromboz portal, fr insuficien
renal sau metastaze extrahepatice.
Se utilizeaz un amestec de lipiodol (colorant utilizat n limfangiografie) i citostatic,
efectul chimic fiind combinat cu embolizarea arterial. Citostaticele utilizate
antracicline (doxorubicin 40-60 mg/m I.A. zilele 1-2, epirubicin), fluoropirimidine
(5-FU, FUDR), mitomicin C, cisplatin, ifosfamid se administreaz n bolus;
lipiodolizarea crete ischemia tumoral, realiznd o microembolizare periferic.
CHEAT este indicat la circa 10% din pacieni, iar supravieuirea la 3 ani a
pacienilor bine selecionai poate atinge chiar 50%; permite obinerea unor rate de
rspuns de 41-60% (superioare CHT sistemice), cu supravieuire median de 19-20
luni. Prezena unui nodul hepatic bine vascularizat, retenia crescut de lipiodol n
interiorul tumorii dup CHEAT sunt factori de prognostic favorabil [21,24].
243
CANCERELE DIGESTIVE
Totui, studiile randomizate mai mari i meta-analizele nu au confirmat c CHEAT ar
ameliora supravieuirea fa de terapia simptomatic (best supportive care, BSC) [18].
De asemenea, studiile comparative nu au reuit s evidenieze care dintre metode este
superioar. Mai mult, comparaia chemoembolizare vs. embolizare nu a identificat nici o
diferen n rata de rspuns sau supravieuire [25].
Complicaiile embolizrii transarteriale sunt redutabile: febr (95% din cazuri),
durere abdominal (60%), anorexie (60%), toxicitate hepatobiliar (abces hepatic,
insuficien hepatic), ulceraii ale stomacului i duodenului. Decompensarea
hepatic survine n 20% din cazuri (mortalitate 3%, n special la cei cu
hiperbilirubinemie, timp de protrombin crescut i ciroz avansat), procedura fiind
riscant la pacienii cu boal avansat. Mai mult de 20% din pacieni remarc
creterea ascitei sau o cretere tranzitorie a transaminazelor. Alte complicaii relativ
frecvente sunt spasmul arterei cistice i colecistita [23,26].
Tratamentul paliativ: Imunoterapia
Interferonii (IFN) au demonstrat o oarecare eficacitate n prevenia CHC la pacienii
infectai cu virusurile hepatitei B sau C, chiar n stadiul de ciroz. Interferonul-alfa
(IFN-) reduce leziunile hepatice i progresia spre ciroz n 10-30% dintre pacienii cu
hepatit cronic B.
Totui, IFN- prezint eficacitate minim n tratamentul CHC, cu o cretere marginal
a supravieuirii generale (14,5 vs. 7,5 sptmni) comparativ cu terapia de susinere
(BSC), la pacienii fr indicaie de chirurgie, transplant, embolizare sau ablaie local.
n asociere cu CHT (protocolul PIAF), IFN- pare s creasc rspunsul tumoral, dar nu
amelioreaz supravieuirea [24].
Tratamentul paliativ: Hormonoterapia
Factorii care ar sugera dependena androgenic a CHC, conducnd la evaluarea
hormonoterapiei, sunt:
predominena masculin;
posibilitatea inducerii prin terapia androgenic;
expresia fiziologic a receptorilor androgeni n ficatul normal (valori mari n CHC);
prezena receptorilor pentru hormoni gonadotrofinici n unele linii celulare de CHC.
Antiestrogenii nu au demonstrat eficacitate nici singuri, nici n asociere cu agonitii
hipofizari (LH-RH) cum ar fi flutamida i triptorelina. Tamoxifen a determinat rezultate
ncurajatoare, cu rate de supravieuire > 1an, dar pe loturi de pacieni foarte bine
selecionai; datele nu au fost reproductibile [18].
Analogii de somatostatin inhib proliferarea celular prin stimularea subtipurilor de
receptori (SRS) care sunt exprimai diferit n CHC. Nu au confirmat nici un avantaj de
supravieuire n ciuda obinerii unor aspecte de boal staionar [28].
Tratamentul paliativ: Radioterapia
Radioterapia extern (RT) are rol limitat n CHC, datorit toleranei slabe a iradierii
de ctre ficat. Totui, doze sigure i eficace pot fi administrate pentru paliaia durerii.
Administrarea pe artera hepatic de izotopi radioactivi, precum Iod-131 (
131
I),
asociai cu lipiodol, poate determina ameliorarea intervalului liber de boal (un
singur studiu) [1,2].
244
Cancerul hepatic
Terapii viitoare
Inhibitorii de receptori ai factorului de cretere epidermal (EGFR)
Hepatocitele (att normale, ct i maligne) prezint capacitate de regenerare prin
intermediul a numeroi factori de cretere, inclusiv factorul de cretere epidermal (EGF)
i factorul de transformare alfa (TGF-).
Prin utilizarea inhibitorilor de transducie, n special ai EGFR, incluznd gefitinib
(Iressa
), erlotinib (Tarceva
) i cetuximab (Erbitux
) au fost ateptate rezultate
promitoare n tumorile ce supraexprim EGFR.
Administrarea de cetuximab monoterapie a demonstrat un bun profil de siguran, dar
cu rspuns slab tumoral i efect minim asupra supravieuirii. Noi combinaii cu
chimioterapia sau cu alte terapii biologice (ex. asociaia GEMOX plus cetuximab)
sunt n curs de studiu [24].
Genistein, un inhibitor specific de tirozin-kinaz prezint activitate n celulele de
hepatocarcinom uman (HepG2), ceea ce sugereaz un rol n tratamentul acestei boli.
Agenii antiangiogenetici
CHC sunt tumori bogat vascularizate asociate cu nivele crescute de factor de cretere
endotelial (VEGF) i fibroblastic (bFGF).
Thalidomida determin, singur sau n asociere cu chimioterapia (doxorubicin
liposomal pegilat, gemcitabin), o rat de rspuns de 5% n CHC. Deoarece
toxicitatea thalidomidei este minim, cu excepia neuropatiei periferice, aceasta pare
o opiune atractiv n formele avansate de CHC.
Sorafenib, inhibitor al receptorului VEGF i al kinazei raf, a demonstrat o activitate
clinic semnificativ: sorafenib 400 mg x 2/zi determin creterea OS cu 44% fa de
placebo la pacienii cu CHC avansat (studiul SHARP, 602 pacieni, ASCO 2007),
creterea supravieuirii generale (10,7 luni vs. 7,9 luni), un timp crescut pn la
progresia radiologic (5,5 vs. 2,8 luni) i status de boal staionar mai frecvent (71%
vs. 67%), cu o toxicitate tratabil cel mai frecvent reacii cutanate tip hand-foot
syndrome (31%), diaree (43%), astenie (30%), rash (17%) i vrsturi (16%).
Sorafenib apare astfel ca primul agent molecular testat riguros care determin un
beneficiu de supravieuire la pacienii cu CHC avansate. Asocierea sorafenib plus
doxorubicin determin de asemenea rezultate ncurajatoare [31].
Bevacizumab, inhibitor de VEGF administrat n doz de 10 mg/kg, determin rate de
rspuns parial de 12,5% i boal staionar n 54% din cazuri. Asocierea
bevacizumab cu erlotinib determin rezultate ncurajatoare, cu un bun profil toxic.
Inhibitorii de farnesil-transferaz, de metaloproteinaz, agenii antisens i noi
molecule cu efect antiangiogenetic NP70, AM1470, PTK787 (vatalanib), SU5416
(semaxinib) sunt de asemenea studiai n tratamentul CHC, rezultatele fiind
ateptate cu interes.
Inhibitorii de 2-ciclooxigenaz (COX2) sunt n curs de studiu n CHC.
Pravastatin (inhibitor de HMG-CoA reductaz) prezint activitate citostatic pe
celulele canceroase, demonstrnd (n asociere cu embolizarea transarterial) un
beneficiu de supravieuire (19 luni vs. 9 luni) ntr-un studiu japonez recent [24].
245
CANCERELE DIGESTIVE
Tratamentul simptomatic
Tratamentul paliativ simptomatic trebuie luat n considerare la mai mult de 50% din
pacienii cu cancere hepatice. n absena posibilitii de vindecare, scopul tratamentului
este ameliorarea calitii vieii i eventual prelungirea supravieuirii.
Tratamente precum: octreotid, radioterapia intern cu
131
I, radioterapia cu protoni,
antiandrogenii, IFN-, tamoxifen au fost studiate numai n trialuri mici, necomparative,
unele fiind asociate cu rate de rspuns crescute, fr o ameliorare a supravieuirii.
n Fig. 2 este prezentat un arbore decizional n funcie de stadializarea TNM, prezena/
absena cirozei hepatice i scorul Child-Pugh.
STRATEGIE TERAPEUTIC
Stadiul I
Rezecia hepatic i injectarea percutan de etanol sunt posibiliti terapeutice cu
rezultate comparabile asupra supravieuirii pe termen lung. Date recente sugereaz c
hepatocarcinoamele de mici dimensiuni rezecate, chiar cele aprute n contextul
cirozei, pot prezenta supravieuiri la 5 ani de peste 70%.
Transplantul hepatic este o metod curativ.
Stadiul II
Tratamentul este similar cu cel din stadiul I.
Modalitile terapeutice sunt mai puin bine precizate, deoarece prognosticul este
nefavorabil, dar transplantul hepatic pare superior rezeciei (40-60% vs. 20-40%).
Rezultatele pot fi semnificativ ameliorate prin utilizarea chimioterapiei intra-arteriale
hepatice (CHEAT). Supravieuirea pe termen lung se situeaz ntre 40-65%.
Stadiul III
Terapia primar const n CHEAT, cu sau fr embolizare. La pacieni selecionai,
opiunile terapeutice standard pot include:
Ablaia cu radiofrecven, criochirurgia, injectarea percutan de etanol;
Transplantul hepatic - potenial curativ la anumii pacieni selecionai cu boal
localizat, nerezecabil, particular la pacienii cu hepatom fibrolamelar;
Chimioterapia regional (administrare intraarterial hepatic pe calea unui porth
subcutan cu pomp implantabil); poate fi asociat cu radioterapia extern;
Chimioterapia sistemic - au fost comunicate remisiuni durabile, dar nu a demonstrat
un beneficiu de supravieuire concludent.
Chirurgia asociat cu chimioterapia intrahepatic i radioterapia cu hipertermie/
radiosensibilizatori - studii clinice, mai ales n tumorile mari, multifocale [23].
Stadiul IV
Nu exist standarde de tratament.
Tratament simptomatic;
Chimioterapia - beneficiu minim,
Studii clinice cu noi ageni biologici.
246
Cancerul hepatic
CHC carcinom hepato-celular, CH ciroz hepatic
FIGURA 6-2. Algoritm decizional n CHC [28]
CARCINOMUL HEPATOCELULAR FIBROLAMELAR
Carcinomul hepatocelular fibrolamelar este o variant mai indolent ca evoluie, ns
majoritatea pacienilor se prezint la medic ntr-un stadiu avansat.
Spre deosebire de hepatocarcinom, carcinomul fibrolamelar pare a avea o predominan
discret la sexul feminin. Nu se asociaz cu fibroza, hepatita B sau C, sau nivele
crescute de AFP. Dei gama-carboxiprotrombina este specific crescut, uneori exist i
nivele serice crescute de neurotensin. Diferenierea neuroendocrin a tumorii permite
identificarea imunohistochimic a neuron-specific enolazei (NSE), VIP i serotoninei.
Examenul CT evideniaz frecvent calcificri intratumorale patognomonice, similare
ntructva cu cele din hiperplazia focal nodular.
Supravieuirea pe termen lung este posibil dup rezecie sau transplant hepatic.
Chimioterapia de orice tip, sau tratamentul cu izotopi radioactivi nu ofer nici un
avantaj semnificativ din punct de vedere al supravieuirii [27].
SARCOAMELE FICATULUI
Angiosarcomul este o tumor hepatic rar. Vrsta pacienilor variaz ntre 24-93 ani,
cu un vrf de inciden n decadele 6-7 de via; 85% din pacieni sunt de sex masculin.
Simptomul iniial cel mai frecvent este durerea abdominal. Alte sarcoame de esuturi
moi cu implicare hepatic (fibrosarcom, leiomiosarcom) sunt foarte rare. Diagnosticul
diferenial se face cu metastazele de tumori gastro-intestinale sau genitale.
Rezecia chirurgical este principala opiune terapeutic pentru sarcoamele primare.
Tumorile nerezecabile au n general un prognostic nefavorabil.
Ficatul poate fi uneori situsul primar pentru un rabdomiosarcom, mai frecvent la copii
dect la aduli. Este tratat similar cu rabdomiosarcomul cu alte localizri, prin excizie
chirurgical (atunci cnd este posibil) i chimioterapie.
Sarcoamele nedifereniate ale ficatului sunt foarte rare i apar de obicei la copii ntre
6-15 ani, sunt de obicei nerezecabile i rspund slab la radio- i chimioterapie [28].
247
CANCERELE DIGESTIVE
HEPATOBLASTOMUL
Hepatoblastomul afecteaz 1/100.000 de copii (n special naintea vrstei de 3 ani, cu o
inciden de 2 ori mai mare la sexul masculin) i este cea mai frecvent tumor hepatic
malign primar la acetia. Principalul simptom este prezena masei tumorale
abdominale. AFP seric este crescut la 75-96% din pacieni. Examenul CT pune n
eviden o mas tumoral hepatic, solitar n 80% din cazuri, sau calcificri
diseminate, n mai mult de 50% din cazuri. Angiografia este utilizat pentru localizare
(tumori hipervascularizate, cu margini imprecis definite) i aprecierea rezecabilitii.
Supravieuirea pe termen lung variaz ntre 15 i 37%. Principalii factori de prognostic
nefavorabil sunt aneuploidia i gradul mic de difereniere.
Rezecia complet este posibil la 50-65% din copii cu hepatoblastoame i este
asociat cu rate de vindecare de 30-70%.
Chimioterapia preoperatorie a fost folosit cu oarecare succes pentru reconvertirea
tumorilor nerezecabile.
Unele studii crediteaz chimioterapia adjuvant cu obinerea unor perioade libere de
semne de boal de 8 pn la 42 luni.
Radioterapia a fost utilizat n tratamentul hepatoblastoamelor nerezecabile, dar rolul
su este controversat.
Transplantul ortotopic de ficat pare a avea un rol la copiii cu hepatoblastoame
nerezecabile, dac reconversia nu poate fi obinut prin chimioterapie (a se vedea
capitolul Cancere pediatrice) [1,2].
Bibliografie
1. Barlett DL, Carr BI, Marsh JW. Cancer of the liver. n: DeVita VT Jr, Hellman S, Rosenberg SA, eds.
Cancer: principles and practice of oncology. 7th ed. Philadelphia: Lippincott, Williams & Wilkins,
2005:986-1008.
2. Alberts RS, Goldberg RM. Gastrointestinal tract cancers. n: Casciato DA, ed. Manual of clinical
oncology. 5th ed. Philadelphia: Lippincott, Williams & Wilkins, 2004:185-232.
3. Leonard GD, Jarnagin WR, Allegra CJ. Primary cancers of the liver. n Abraham J, Allegra CJ, Gulley J,
eds. Bethesda Handbook of clinical oncology. 2nd ed. Philadelphia: Lippincott, Williams & Wilkins,
2005:99-105.
4. Engstrom PF, Sigurdson ER, Evans AA, Pingpank JF. Primary neoplasms of the liver. n: Holland JF,
Frei BC, eds. Cancer medicine. 6th ed. Hamilton: Decker, 2003:1543-1553.
5. Fong Y, Kemeny N, Lawrence TS. Cancer of the liver and biliary tree. n: DeVita VT Jr, Hellman S,
Rosenberg SA, eds. Cancer: principles and practice of oncology. 6th ed. Philadelphia: Lippincott,
Williams & Wilkins, 2001:1162-1187.
6. Weber S, OReilly MO, Abou-Alfa GK. Liver and bile duct cancer. n: Abeloff MD, ed. Clinical
oncology, 3th ed. Philadelphia: Elsevier Churchill Livingstone 2004:1981-2015.
7. American Joint Committee on Cancer. Liver (including intrahepatic bile ducts). n: Robin S, Wittekind F.
AJCC Cancer Staging Manual. 6th ed. New York: Springer, 2002,131-138.
8. Izumi R, Shimizu K, Kiriyama M, et al. Alpha-fetoprotein production by hepatocellular carcinoma is
prognostic of poor patient survival. J Surg Oncol 1992;49(3):151-5.
9. Yamashita Y, Takahashi M, Koga Y, et al. Prognostic factors in the treatment of hepatocellular carcinoma
with transcatheter arterial embolization and arterial infusion. Cancer 1991;67(2):385-391.
10. Hegate U, Grem J. Primary cancers of the liver. n: Abraham J, Allegra CJ, ed. Bethesda Handbook of
clinical oncology. Philadelphia: Lippincott, Williams & Wilkins, 2001:87-93.
11. Hemming AW, Cattral MS, Reed AI, et al. Liver transplantation for hepatocellular carcinoma. Ann Surg
2001;233(5):652-259.
12. Livraghi T, Goldberg SN, Lazzaroni S, et al. Small hepatocellular carcinoma: treatment with radio-
frequency ablation versus ethanol injection. Radiology 1999;210(3):655-661.
13. Dannielle B, DeSio I, Izzo F et al. Hepatic resection and percutaneous ethanol injection as treatment of
small hepatocellular carcinoma: a Cancer of the Liver Italian Program (CLP 08) retrospective case-
control study. J Clin Gastroenterol 2003:36:63-67.
248
Cancerul hepatic
14. Livraghi T, Bolondi L, Lazzaroni S, et al. Percutaneous ethanol injection in the treatment of
hepatocellular carcinoma in cirrhosis. A study on 207 patients. Cancer 1992;69(4):925-629.
15. Groupe d'Etude et de Traitement du Carcinome Hpatocellulaire. A comparison of lipiodol
chemoembolization and conservative treatment for unresectable hepatocellular carcinoma. N Engl J Med
1995;332(19):1256-1261.
16. Zhou XD, Tang ZY. Cryotherapy for primary liver cancer. Semin Surg Oncol 1998;14(2):171-4.
17. Ciuleanu TE. Aportul chimioterapiei n tratamentul tumorilor hepatice primitive. Rad & Oncol Med
2003;9(4):250-257.
18. Epstein B, Ettinger D, Leichner PK, et al. Multimodality cisplatin treatment in nonresectable alpha-
fetoprotein-positive hepatoma. Cancer 1991;67(4):896-900.
19. Sitzmann JV, Abrams R: Improved survival for hepatocellular cancer with combination surgery and
multimodality treatment. Ann Surg 1993;217(2):149-154.
20. Farmer DG, Rosove MH, Shaked A, et al. Current treatment modalities for hepatocellular carcinoma. Ann
Surg 1994;219(3):236-47.
21. Iwatsuki S, Starzl TE, Sheahan DG, et al. Hepatic resection versus transplantation for hepatocellular
carcinoma. Ann Surg 1991;214(3): 221-8.
22. Venook AP: Treatment of hepatocellular carcinoma: too many options? J Clin Oncol 1994;12(6):1323-
34.
23. Bruix JB, Lovet MJ. Is there an optimal loco-regional therapy for hepato-celular carcinoma? American
Society of Clinical Oncology 26th Meeting Educational Book, 2002:316-320.
24. Johnson PJ. Is there a role for sistemic therapy in hepatocellular carcinoma and if so, can we assess
responses? American Society of Clinical Oncology 26th Meeting Educational Book, 2002: 310-315.
25. Ruff P. Therapeutic options in hepatocellular carcinoma. Am J Cancer 2004;3(2):119-131.
26. Taieb J, Barbare JC, Rougier P. Medical treatments for hepatocellular carcinoma (HCC): whats next ?
Ann Oncol 2006;17(10):x308-x314.
27. Mor E, Kaspa RT, Sheiner P, et al. Treatment of hepatocellular carcinoma associated with cirrhosis in the
era of liver transplantation. Ann Intern Med 1998;129(8):643-53.
28. Kendrick LM, Grambihler A, Gores GJ, et al. Cancer of the liver and bile ducts. n: Chang AE, Ganz PF,
eds. Oncology: an evidence-based approach, New York: Springer, 2006:745-763.
29. Wagman LD, Robertson JM, ONeill B. Liver, gallbladder, and billiary tract cancers. In: Pazdur R, Coia
LR, Hoskins WJ, eds. Cancer management: a multidisciplinary approach. 10th ed. New York: CMP
Medica Oncology 2007:319- 337.
30. Chaudhary RT. Carcinomas of the pancreas, liver, gallbladder, and bile ducts. In: Skeel RT, ed.
Handbook of cancer chemotherapy, 7th ed. Philadelphia: Wolters Kluwer/Lippincott, Williams &
Wilkins, 2007:294-297.
31. Lopez PM, Patel P, Uva P, et al. Current management of liver cancer. Eur J Cancer 2007;5(5):444-446.
249
CANCERELE DIGESTIVE
250
Cancerul veziculei biliare
EPIDEMIOLOGIE
Carcinomul primar al veziculei biliare (CVB) este cea mai frecvent malignitate a
tractului biliar i cea de-a cincea neoplazie ca prevalen a tubului digestiv.
Se nregistreaz o predominen la sexul feminin, CVB fiind de 2-6 ori mai frecvent
dect la brbai. Vrsta median la momentul diagnosticului este de 65 ani. Din punct de
vedere al distribuiei geografice, CVB este mai frecvent n America de Sud (Peru,
Ecuador) [1].
ETIOLOGIE
Factorii de risc pentru CVB sunt:
Litiaza biliar vezicular:
65-90% dintre pacienii cu pacienii cu CVB prezint calculi biliari, dar numai 1-3% dintre
pacienii cu colelitiaz dezvolt CVB; riscul crete direct proporional cu dimensiunea
calculilor.
Infeciile (Salmonella typhy, Escherichia coli, Helicobacter pylori).
Polipii vezicali sau vezicula de porelan:
polipii peste 1 cm n diametru prezint riscul cel mai crescut de malignizare;
vezicula de porelan este o entitate patologic datorat depunerii excesive de calciu n
peretele veziculei biliare, care poate fi asociat cu CVB (< 20% dintre pacieni).
Diverse:
anomaliile pancreatico-biliare de jonciune care determin refluxul biliar i staza biliar pot
cauza CVB. Obezitatea, estrogenii i chimicalele din industria de colorani sunt asociate, de
asemenea cu aceast neoplazie.
HISTOLOGIE
Adenocarcinomul de vezicul biliar reprezint mai mult de 85% din cazuri; este
submprit n: papilar, tubular, mucinos sau cu celule n inel cu pecete. Alte tipuri
histologice includ: carcinomul anaplazic, scuamos, cu celule mici i carcinosarcomul.
Unele subtipuri (ex. carcinomul papilar) prezint un prognostic mai bun [2].
DIAGNOSTIC
Examen clinic
La momentul diagnosticului, CVB este obinuit avansat, dar fr metastaze la distan.
Simptomele precoce se pot ntlni numai n ampulomul vaterian datorit prezenei
icterului obstructiv.
Elementele sugestive pentru diagnostic sunt:
durere la nivelul hipocondrului drept (82%);
pierdere ponderal (72%);
anorexie, greuri i vrsturi (68%);
mas tumoral palpabil n hipocondrul drept (65%);
distensie abdominal (30%);
icter obstructiv (44%);
prurit (20%).
Cancerul veziculei biliare
Investigaii paraclinice
ecografia abdominal;
examenul computer tomografic (CT);
colangiografia transhepatic (n prezena icterului);
colangiopancreatografia endoscopic retrograd (ERCP);
puncia-citologie cu ac fin;
CA19.9 cel mai bun marker pentru CVB (valori mai mari de 20 UI/ml prezint o
sensibilitate i specificitate de 79%);
CEA 93% specific pentru CVB.
STADIALIZARE
TABEL 6-22. Sistemul de stadializare TNM AJCC/UICC 2002 (ediia a 6-a) a CVB [3]
T (tumora primar)
Tx tumora primar nu poate fi evaluat
To fr evidena tumorii primare
Tis carcinom in situ
T1 tumora invadeaz mucoasa sau musculara veziculei biliare
T1a tumora invadeaz mucoasa
T1b tumora invadeaz musculara
T2 tumora invadeaz esutul conjunctiv perimuscular, fr extensie dincolo de seroas sau
n ficat
T3 tumora perforeaz seroasa (peritoneul visceral) i/sau invadeaz direct ficatul sau una
dintre urmtoarele structuri: stomac, duoden, colon, pancreas, epiploon, ci biliare
extrahepatice
T4 tumora invadeaz vena port principal sau artera hepatic sau invadeaz multiple
organe sau structuri extrahepatice
N (adenopatiile loco-regionale)
Nx ganglionii regionali nu pot fi evaluai
No ganglioni regionali fr metastaze
N1 metastaze n ganglionii regionali (ai canalului cistic, pericoledocieni i/sau hilari, ai
ligamentului hepato-duodenal), peripancreatici (exclusiv pericefalici), periduodenali,
periportali, celiaci i/sau mezenterici superiori
M (metastazele la distan)
Mx metastazele la distan nu pot fi evaluate
Mo fr metastaze la distan
M1 metastaze la distan prezente
pTNM Clasificarea patologic
Categoriile pT, pN i pM corespund categoriilor T, N i M clinice.
pNo - Examenul histologic dup limfadenectoma regional trebuie s cuprind 3 ganglioni.
Gruparea pe stadii
Stadiul 0 Tis No Mo
Stadiul IA T1 No Mo
Stadiul IB T2 No Mo
Stadiul IIA T3 No Mo
Stadiul IIB T1 N1 Mo
T2-3 No Mo
Stadiul III T4 Orice N Mo
Stadiul IV Orice T Orice N M1
251
CANCERELE DIGESTIVE
PROGNOSTIC
Factorii prognostici recunoscui sunt: stadiul bolii (cel mai important), tipul histologic
(prognostic mai favorabil n subtipul papilar), gradul de difereniere tumoral, invazia
vascular [4].
Cnd CVB este descoperit incidental, n absena simptomelor clinice i tumora este
localizat la nivelul mucoasei vezicale, supravieuirea la 5 ani este > 80% din cazuri.
Peste 70% din pacienii cu CVB/ colangiocarcinom prezint extensie local, implicare
ganglionar sau diseminare la distan la momentul diagnosticului. La pacienii cu
tumori T2-4 supravieuirea la 5 ani pentru grupa cu No se apreciaz a fi de 42,5%, iar
pentru grupa cu N+ de 31 6,2%. Supravieuirea median a pacienilor care se prezint
cu boal avansat este de 2-6 luni, cu rate de supravieuire la 1 an de 5%, iar
probabilitatea de a fi n via la 2 ani este foarte sczut. Nici unul dintre pacienii care
primesc terapie paliativ nu supravieuiete la 5 ani; durata medie de via pentru cei n
stadiul IV, cu metastaze hepatice i peritoneale la diagnostic, este de 1-3 luni.
PRINCIPII DE TRATAMENT
n ciuda ameliorrii metodelor diagnostice, CVB rmne o boal fatal n majoritatea
cazurilor. Colecistectomia este singurul tratament eficace, rezecia curativ trebuind
adaptat la extensia tumorii.
Tratamentul loco-regional: Chirurgia
Numai 10-30% din pacieni pot fi considerai candidai poteniali la chirurgia
curativ, care poate fi o colecistectomie simpl (rate de supravieuire > 85% n
stadiul I) sau o rezecie radical extins. Limfadenectomia este obligatorie.
Procedura radical presupune rezecia n eav de puc a patului veziculei biliare i a
segmentelor hepatice V i VI, excizia supraduodenal a coledocului, rezecia n bloc a
ganglionilor limfatici (unii chirurgi preconizeaz pancreato-duodenectomia) [5].
Unele studii au comunicat supravieuiri prelungite dup chirurgia radical chiar n
stadiul IV [1,5].
Tratamentul loco-regional: Radioterapia
Unele studii (nerandomizate) au raportat ameliorri ale ratelor de supravieuire dup
radioterapia intraoperatorie sau adjuvant [1].
Radioterapia postoperatorie (DT 45-60 Gy n 5-6 sptmni) este utilizat la pacienii
care dup intervenie chirurgical macroscopic radical prezint un risc crescut de
recidiv. Asocierea RT cu 5-FU ofer avantajul potenial al creterii controlului local.
Experiena japonez indic obinerea de rezultate prin radioterapia intraoperatorie cu
electroni (24-40 Gy n doz unic) [6].
La pacienii cu tumori nerezecabile, radioterapia (RT) singur este o procedur
paliativ rareori de succes.
Tratamentul sistemic: Chimioterapia
Datorit raritii acestor tumori, studiile clinice au inclus att tumorile veziculei biliare,
ct i pe cele ale cilor biliare. Este deci dificil a decela diferene n rspunsul la CHT
ntre carcinoamele de vezicul biliar i colangiocarcinoame (vezi capitolul Cancerul
cilor biliare).
252
Cancerul veziculei biliare
STRATEGIE TERAPEUTIC
Boala localizat
Include urmtoarele stadii: Tis, T1, T2 cazuri selectate, rareori T3; No; Mo.
Intervenia chirurgical este curativ, fr a fi necesar alt terapie.
Boala avansat / metastatic
Include: orice T, N1, Mo; orice T, orice N, M1; majoritatea T3, toate T4, No, Mo).
Aceti pacieni nu sunt curabili. Tratamentul de combatere a obstruciei biliare poate
obine un beneficiu clinic. Un numr redus de pacieni pot prezenta tumori cu cretere
foarte lent i pot supravieui mai muli ani.
Opiunile terapeutice standard sunt:
Rezecia hepatic n jurul patului veziculei biliare sau hepatectomia extins i
limfadenectomia care s includ ganglionii N1 i N2 se pot asocia cu creterea
intervalului pn la recidiv i ameliorarea supravieuirii. La pacienii cu icter
(stadiile III-IV) se va ncerca preoperator drenajul biliar percutan transhepatic pentru
eliminarea obstacolului biliar.
Radioterapia extern (RTE) cu sau fr chimioterapie (ca tratament definitiv sau
postoperator) poate obine rate de rspuns pe termen scurt [7].
Tratamentul paliativ:
Chirurgie paliativ (colecisto-duodenoanastomoz) n caz de obstrucie biliar simptomatic
(icter, prurit, disfuncie hepatic, colangit);
Drenaj biliar transhepatic cu cateter ghidat radiologic sau plasare endoscopic de stent;
RTE poate ridica obstrucia biliar la unii pacieni, suplinind procedurile de by-pass;
Chimioterapia nu este eficace dect ocazional, la unii pacieni simptomatici [7].
EVOLUIE I COMPLICAII
Ameliorarea calitii vieii pacienilor se poate obine prin tratamentul simptomatic al
icterului, durerii, pruritului, senzaiei de grea i al vrsturilor.
Controlul durerii splanhnicectomie cu etanol, percutan/intraoperatorie.
Prurit i icter plasarea endoscopic/ percutan de stenturi.
Obstrucia duodenal tardiv gastrojejunostomie [2].
Bibliografie
1. Leonard GD, OReilly EM. Primary cancers of the liver. n: Abraham J, Allegra CJ, Gulley J, eds.
Bethesda handbook of clinical oncology. 2nd ed. Philadelphia: Lippincott Williams &Wilkins 2005:91-94
2. Barlett DL, Ramanathan RK, Deutsch M. Cancer of the billiary tree - tumors of the gall bladder. n:
DeVita VT Jr, Hellman S, Rosenberg SA, eds. Cancer: principles & practice of oncology. 7th ed.
Philadelphia: Lippincott, Williams & Wilkins, 2005:1022-1030.
3. American Joint Committee on Cancer. Gallbladder. In: AJCC Cancer Staging Manual. 6th ed. New York:
Springer, 2002, 139-144.
4. Chao TC, Greager JA. Primary carcinoma of the gallbladder. J Surg Oncol 1991;46 (4):215-21.
5. Shoup M, Fong Y: Surgical indications and extent of resection in gallbladder cancer. Surg Oncol Clin N
Am 2002;11(4):985-994.
6. Kendrick LM, Grambihler A, Gores GJ, et al. Cancer of the liver and bile ducts. n: Chang AE, Ganz P,
eds. Oncology: an evidence-based approach. New York: Springer, 2006:745-763.
7. National Comprehensive Cancer Network. Gallbladder Cancer. n: Clinical Practice Guidelines in
Oncology. Health Proffessional Version, 2007. Available at www.nccn.org
253
CANCERELE DIGESTIVE
254
Cancerul cilor biliare (colangiocarcinomul)
Termenul de colangiocarcinom a fost iniial utilizat pentru a desemna tumori ale
ductului biliar intrahepatic dar, mai recent, nglobeaz ntregul spectru al tumorilor cu
origine n ductele intrahepatice, perihilare i distale.
Colangiocarcinoamele pot fi clasificate ca: extrahepatice proximale (perihilar, tumora
Klatskin, 50-60%), extrahepatice distale (20-25%), intrahepatice (tumora periferic,
20-25%) i multifocale (5%) [1].
EPIDEMIOLOGIE
Colangiocarcinoamele sunt tumori maligne rare, cu oarecare predominen masculin
(survin cu frecven egal la sexul feminin i masculin dup vrsta de 70 ani) [2].
ETIOLOGIE
Factorii de risc pentru apariia colangiocarcinoamelor sunt:
condiiile inflamatorii (colecistita primar sclerozant, colita ulcerativ);
anomaliile de coledoc (boala Caroli - dilataia chistic a ductelor intrahepatice);
infeciile cu parazii (Opistorchis viverrini, O. felineus i Clonorchis sinensis);
hepatita / ciroza hepatic cu VHC;
fumatul;
azbestoza;
radonul;
nitrozaminele.
HISTOLOGIE
Subtipurile histologice de colangiocarcinom sunt urmtoarele: adenocarcinom NOS,
de tip intestinal, mucinos, cu celule clare; carcinom cu celule n inel cu pecete,
scuamos, cu celule mici (oat-cell), anaplazic, papilar neinvaziv/invaziv; tumori
mezenchimale maligne (rabdomiosarcom embrionar, leiomiosarcom, histiocitom
fibros malign) [3].
DIAGNOSTIC
Examen clinic
Colangiocarcinomul intrahepatic se prezint ca mas tumoral asimptomatic sau cu
simptome vagi: durere, pierdere ponderal, transpiraii nocturne i stare de ru.
Colangiocarcinomul extrahepatic se prezint uzual cu simptome i semne de
colestaz (icter, fecale decolorate, urin hipercrom, prurit) sau colangit (febr,
durere, icter) [4].
Investigaii paraclinice
funcia hepatic;
ecografie abdominal;
examen CT abdominal.
Cancerul cilor biliare
STADIALIZARE
Mai mult de 50% din pacieni prezint afectare ganglionar la momentul prezentrii i
10-20% din pacieni prezint carcinomatoz peritoneal.
Stadializarea se bazeaz pe clasificarea TNM. Alte clasificri, precum cea aparinnd lui
Bismuth i colab. definesc extensia afectrii ductale n:
Tip I tumor deasupra confluenei dintre ductele hepatice drept i stng.
Tip II tumora afectnd confluena dar fr invazia ductului hepatic drept/ stng.
Tip III tumora ocluzioneaz hepaticul comun i un duct hepatic, drept sau stng.
Tip IV tumora este multicentric sau invadeaz ductele hepatice drept i stng.
TABEL 6-23. Stadializarea TNM AJCC/UICC 2002 (ediia a 6-a) a tumorilor de duct
biliar [5]
T (tumora primar)
Tx tumora primar nu poate fi evaluat
To fr evidena tumorii primare
Tis carcinom in situ
T1 tumora limitat la ductul biliar
T2 tumora invadeaz dincolo de peretele ductului biliar
T3 tumora invadeaz ficatul, vezica biliar, pancreasul i/sau ramul unilateral al venei porte
(drepte sau stngi) sau artera hepatic (dreapt sau stng)
T4 tumora invadeaz una dintre urmtoarele structuri: vena port principal sau ramurile
sale bilaterale, artera hepatic comun sau structurile adiacente precum: colon, stomac, duoden
sau perete abdominal.
N (adenopatiile loco-regionale)
Nx ganglionii regionali nu pot fi evaluai
No fr metastaze n ganglionii regionali
N1 metastaze n ganglionii regionali
M (metastazele la distan)
Mx metastazele la distan nu pot fi evaluate
Mo fr metastaze la distan
M1 metastaze la distan prezente
pTNM Clasificarea patologic
Categoriile pT, pN i pM corespund categoriilor T, N i M clinice.
Stadiul depinde de definirea limitelor tumorii prin mijloace imagistice, prin explorarea chirurgical i
prin examenul histopatologic.
pNo - Examenul histologic al materialului obinut prin limfadenectomie regional trebuie s cuprind
3 ganglioni.
Gruparea pe stadii
Stadiu 0 Tis No Mo
Stadiul IA T1 No Mo
Stadiul IB T2 No Mo
Stadiul IIA T3 No Mo
Stadiul IIB T1-3 N1 Mo
Stadiul III T4 orice N Mo
Stadiul IV orice T orice N M1
255
CANCERELE DIGESTIVE
PRINCIPII DE TRATAMENT
Tratamentul loco-regional: Chirurgia
Chirurgia este singura opiune curativ posibil la 30-60% dintre pacieni. Scopurile
interveniei sunt nlturarea tumorii i restaurarea drenajului biliar [1].
n cazuri izolate, cu localizare nalt pe bifurcaia canalului hepatic (tumora
Klatskin), se recomand extinderea interveniei dincolo de hemihepatectomie
(chirurgia extensiv, cu transplant hepatic, prin procedura Whipple).
n tumorile foarte avansate se recomand chirurgia paliativ (combaterea obstruciei:
anastomoze (hepato-/gastrojejunostomia) sau implantare endoscopic de stent [6].
Explorarea intraoperatorie este util pentru:
stabilirea diagnosticului,
nlturarea veziculei biliare (profilaxia colecistitei),
injectarea plexului celiac cu alcool (splanhnicectomia) pentru controlul durerii,
prevenirea sau tratamentul obstruciei polului inferior gastric.
Tratamentul loco-regional: Radioterapia
n boala nerezecabil, utilizarea CHT-RT obine uneori supravieuiri pe termen lung.
RT adjuvant nu este recomandat, deoarece datele disponibile despre acest subiect
sunt limitate i conflictuale.
Tratamentul sistemic: Chimioterapia
Chimioterapia (CHT) determin beneficii paliative la pacienii cu cancer de ci biliare,
dei nu exist dovezi c poate ameliora supravieuirea, iar RR nu depesc 10-20%.
Nu se recomand chimioterapia adjuvant.
n scop paliativ, la pacienii cu o stare general bun i fr afectare bio-metabolic
sever poate fi luat n consideraie monochimioterapia (gemcitabin, 5-FU,
epirubicin sau mitomicin C). Dozele trebuie reduse la pacienii cu icter.
Asociaiile cu gemcitabin i cisplatin sau 5-FU au demonstrat RR de 20-60% i o
supravieuire median >20 luni. Nu exist studii comparative cu monoterapia [9].
Capecitabina (Xeloda
) determin rate de rspuns la 4 din 8 cazuri de carcinom de
vezic biliar, i la numai 1 din 18 cazuri de colangiocarcinoame.
TABEL 6-24. Chimioterapia n cancerele de tract biliar avansate [9]
Monoterapia
Gemcitabin 1000 mg/m I.V. perfuzie 30 zilele 1,8,15
Se repet la fiecare 4 sptmni.
5-Fluorouracil 500-600 mg/m I.V. (bolus) zilele 1-5 sau
5-Fluorouracil 500 mg/m I.V. zilele 1,8,15,22,29,36
Se repet la fiecare 4, sau respectiv 8 sptmni.
Epirubicin 20 mg/m
2
I.V. zilele 1,8,15
Se repet la fiecare 4 sptmni.
Docetaxel 100 mg/m I.V. (perfuzie 1h) ziua 1
Se repet la fiecare 3 sptmni.
256
Cancerul cilor biliare
Polichimioterapia
GLF
Gemcitabin 1000 mg/m I.V. (perfuzie 30) zilele 1,8,15
Acid folinic 20 mg/m I.V. (bolus) zilele 1,8,15
5-Fluorouracil 600 mg/m I.V. (bolus) zilele 1,8,15
Se repet la fiecare 4 sptmni (doar la pacienii cu status de performan bun).
GEMOX
Gemcitabin 1000 mg/m I.V. (perfuzie 30) zilele 1,8
Oxaliplatin 130 mg/m
2
I.V. (perfuzie 2h) ziua 8
Se repet la fiecare 3 sptmni (doar la pacienii cu status de performan bun).
FS
5-Fluorouracil 400 mg/m I.V. zilele 1-5
Streptozocin 500 mg/m I.V. zilele 1-5
Se repet la fiecare 4 sptmni.
GemCap
Capecitabin 750 mg/m x 2/zi P.O. zilele 1-14
Gemcitabin 1000 mg/m I.V. zilele 1,8
Se repet la fiecare 3 sptmni.
XELOX
Capecitabin 750 mg/m x 2/zi P.O. zilele 1-14
Oxaliplatin 130 mg/m I.V. ziua 1
Se repet la fiecare 3 sptmni.
FLM
5-Fluorouracil 400 mg/m I.V. zilele 1-4
Acid folinic 200 mg/m I.V. zilele 1-4
Mitomicin C 8 mg/m I.V. ziua 1
Se repet la fiecare 4 sptmni.
CEF
Cisplatin 60 mg/m I.V. ziua 1
Epirubicin 50 mg/m I.V. ziua 1
5-Fluorouracil 200 mg/m I.V. (perfuzie continu 24h) zilele 1-21
Se repet la fiecare 6 sptmni.
n absena studiilor clinice, pacienii cu cancere biliare pot fi tratai cu gemcitabin
i/sau 5-FU leucovorin (sau capecitabin). Pot fi asociai i ali ageni citostatici
(doxorubicin, cisplatin), dar nu exist evidene c CHT ar determina beneficii
substaniale n ameliorarea supravieuirii sau a calitii vieii [10].
Tratamentul paliativ
Pacienii cu boal nerezecabil sau metastatic pot beneficia de chirurgie paliativ,
radioterapie, chimioterapie sau o asociaie a acestora. O alt opiune este blocarea sau
terapia fotodinamic.
Drenajul biliar poate fi obinut prin coledoco-jejunostomie, by-pass al canalului
hepatic drept sau stng sau montarea endoscopic/ percutan de stent-uri.
Stent-urile metalice au diametru mai mare i un risc de ocluzie / migraie mai redus, fiind
utilizate preferenial la pacienii cu speran de via >6 luni i/sau cu boal nerezecabil.
257
CANCERELE DIGESTIVE
STRATEGIE TERAPEUTIC
Boala localizat
Opiunile terapeutice standard includ:
Chirurgia posibilitatea de rezecie chirurgical optimal variaz n funcie de
localizare, extensia afectrii parenchimului hepatic i statusul ganglionilor limfatici
regionali.
Interveniile chirurgicale cu viz curativ pentru cancerele ductelor biliare sunt extensive
(procedura Whipple) i asociate cu o mortalitate operatorie crescut (5-10%) i curabilitate
sczut.
Rezecia chirurgical complet este posibil doar la o minoritate de pacieni cu cancere ale
cilor biliare proximale, spre deosebire de tumorile cu origine n ductul biliar distal, pentru
care supravieuirea la 5 ani atinge 25% [10,12].
La pacienii cu icter obstructiv sunt necesare proceduri paliative (uneori de urgen,
mai ales cnd icterul este sever i este prezent azotemia): plasarea endoscopic de
stent-uri sau drenaj biliar percutan [10,12].
Radioterapia extern poate fi utilizat n asociaie cu rezecia chirurgical [2].
Boala nerezecabil / metastatic
Majoritatea cancerelor ductelor biliare extrahepatice nu pot fi complet rezecate
chirurgical. Frecvent, tumorile proximale invadeaz direct structurile parenchimului
hepatic adiacent, artera hepatic sau vena port (hipertensiune portal). Diseminarea la
distan, pe cale hematogen sau transperitoneal, este rar.
Aceti pacieni nu pot fi vindecai; primeaz tratamentul paliativ pentru combaterea
durerii, icterului i pruritului.
Paliaia poate fi obinut prin anastomoza ductului biliar cu intestinul sau prin
montarea de stent-uri n ductul biliar (intraoperatorie, endoscopic sau prin tehnici
percutane).
Radioterapia paliativ dup practicarea unui by-pass biliar/ stentare poate fi benefic
pentru unii pacieni. n centrele cu dotare corespunztoare, dac a fost montat un
cateter percutan, acesta poate fi utilizat drept conduct pentru plasarea unei surse
pentru brahiterapie [11].
Bibliografie
1. Leonard GD, OReilly EM, Allegra CJ. Billiary tract cancer. In: Abraham J, Allegra CJ, Gulley J, eds.
Bethesda Handbook of clinical oncology. 2nd ed. Philadelphia: Lippincott, Williams & Wilkins, 2005:
94-97.
2. Barlett DL, Ramanathan RK, Deutsch M. Cancer of the billiary tree - colangiocarcinomas. In: DeVita VT
Jr, Hellman S, Rosenberg SA, eds. Cancer: principles & practice of oncology. 7th ed. Philadelphia:
Lippincott, Williams & Wilkins, 2005:1009-1021.
3. Henson DE, Albores-Saavedra J, Corle D. Carcinoma of the extrahepatic bile ducts. Histologic types,
stage of disease, grade, and survival rates. Cancer 1992;70(6):1498-1501.
4. Alberts RS, Goldberg RM. Gastrointestinal tract cancers. In: Casciato DA, ed. Manual of clinical
oncology. 5th ed. Philadelphia: Lippincott, Williams & Wilkins, 2004:185-232.
5. American Joint Committee on Cancer. Extrahepatic bile ducts. In: AJCC Cancer Staging Manual. 6th ed.
New York: Springer, 2002:145-150.
6. Stain SC, Baer HU, Dennison AR, et al. Current management of hilar cholangiocarcinoma. Surg Gynecol
Obstet 1992;175(6):579-588.
7. de Groen PC, Gores GJ, LaRusso NF, et al. Biliary tract cancers. N Engl J Med 1999:341(18):1368-1378.
8. Bhuiya MR, Nimura Y, Kamiya J, et al. Clinicopathologic studies on perineural invasion of bile duct
carcinoma. Ann Surg 1992;215(4):344-349.
258
Cancerul cilor biliare
9. Chaudhari RT. Carcinomas of the pancreas, liver, gallbladder and bile ducts. In: Skeel RT, ed. Handbook
of cancer chemotherapy. 7th ed. Philadelphia: Lippincott Williams & Wilkins, 2003:285-297
10. Wagman LD, Robertson JM, ONeil B. Liver, gallbladder, and billiary tract cancers. In: Pazdur R, Coia
LR, Hoskins WJ, eds. Cancer management: a multidisciplinary approach. 10th ed. New York: CMP
Medica Oncology 2007:319-337.
11. Fong Y, Kemeny N, Lawrence TS. Cancer of the liver and biliary tree. In: DeVita VT Jr, Hellman S,
Rosenberg SA, eds. Cancer: principles & practice of oncology. 6th ed. Philadelphia: Lippincott, Williams
& Wilkins, 2001:1187-1199.
12. Kendrick LM, Grambihler A, Gores GJ, et al. Cancer of the liver and bile ducts. n: Chang AE, Ganz PF,
eds. Oncology: an evidence-based approach. New York: Springer, 2006:745-763.
13. National Comprehensive Cancer Network. Cholangiocarcinoma. n: Clinical Practice Guidelines in
Oncology: Treatment. Health Proffessional Version 2007. Available at www.nccn.org
259
S-ar putea să vă placă și
- Prevenirea cancerului. 10 reguli obligatorii pentru sănătate și viață lungăDe la EverandPrevenirea cancerului. 10 reguli obligatorii pentru sănătate și viață lungăÎncă nu există evaluări
- C. Cxorp UterinDocument21 paginiC. Cxorp UterinZorin SvetlanaÎncă nu există evaluări
- Alte ORL PDFDocument5 paginiAlte ORL PDFCosmin-AdrianaZirbauÎncă nu există evaluări
- OncologieDocument63 paginiOncologieVoicu DanielaÎncă nu există evaluări
- Cancerul RectuluiDocument8 paginiCancerul RectuluiionelatriÎncă nu există evaluări
- Durerea La Copilul Cu CancerDocument32 paginiDurerea La Copilul Cu Cancerelenaconstantin1Încă nu există evaluări
- 03 MironDocument2 pagini03 MironAgache AnamariaÎncă nu există evaluări
- Opţiuni Terapeutice În Cancerul Glandei Mamare - Evaluare Critica, RezultateDocument31 paginiOpţiuni Terapeutice În Cancerul Glandei Mamare - Evaluare Critica, RezultaterenovatiumÎncă nu există evaluări
- Reconstructia San (CURS)Document60 paginiReconstructia San (CURS)LaviniaPurcaru100% (1)
- Curs 3 Oncologie - Rolul ChirurgieiDocument44 paginiCurs 3 Oncologie - Rolul ChirurgieiIoana Monica Marinescu100% (1)
- Rolul Chirurgiei in OncologieDocument6 paginiRolul Chirurgiei in OncologieIacobescu GeorgianÎncă nu există evaluări
- Curs 9 LimfoscintigrafiaDocument51 paginiCurs 9 LimfoscintigrafiaCARLAÎncă nu există evaluări
- Cancerul-Mamar-09 03 2019Document94 paginiCancerul-Mamar-09 03 2019Epure Loreta DianaÎncă nu există evaluări
- Diagnosticul Şi Stadializarea CanceruluiDocument31 paginiDiagnosticul Şi Stadializarea CanceruluiCristina Anca RobuÎncă nu există evaluări
- Tratamentul Chirurgical in Cancerul MamarDocument11 paginiTratamentul Chirurgical in Cancerul MamarMacrineanu IonutÎncă nu există evaluări
- 16 - Patologia Glandei MamareDocument55 pagini16 - Patologia Glandei MamareCosmin LibrimirÎncă nu există evaluări
- Oncologie 2Document83 paginiOncologie 2alexxsaruÎncă nu există evaluări
- Imunologia Cancerului Si Principii de ImunoterapieDocument1 paginăImunologia Cancerului Si Principii de ImunoterapieTheo TheodoraÎncă nu există evaluări
- Curs Oncologie IOBDocument68 paginiCurs Oncologie IOBovidiu-george manaila100% (1)
- 09 - Factorii de PrognosticDocument6 pagini09 - Factorii de PrognosticBERBECE MARIA LILIANAÎncă nu există evaluări
- Elemente de Oncologie Parti MoiDocument128 paginiElemente de Oncologie Parti MoiBianca DinescuÎncă nu există evaluări
- Cancer Prostata Rezistent La CastrareDocument96 paginiCancer Prostata Rezistent La CastrareCristian TomaÎncă nu există evaluări
- Cancer ColDocument15 paginiCancer ColBirca Marius100% (1)
- 74 Determinari Secundare Cu Punct de Plecare NeprecizarDocument2 pagini74 Determinari Secundare Cu Punct de Plecare NeprecizarobrejaÎncă nu există evaluări
- Tumorile Solide Ale CopiluluiDocument200 paginiTumorile Solide Ale CopiluluiPopa MihaiÎncă nu există evaluări
- Oncologie Medicala DefinitieDocument4 paginiOncologie Medicala DefinitieDaniela Greere100% (3)
- Curriculum Vitae 8Document4 paginiCurriculum Vitae 8Vlad FărăuÎncă nu există evaluări
- Oncologie: Curs nr.1Document109 paginiOncologie: Curs nr.1Ecaterina CapusneacÎncă nu există evaluări
- 15 San BenignDocument39 pagini15 San BenignAlexandra BataniÎncă nu există evaluări
- Oncologie - Subiecte Rezolvate ModificateDocument53 paginiOncologie - Subiecte Rezolvate ModificateLazaros TsiatsiosÎncă nu există evaluări
- LP 7+8 - DigestivDocument99 paginiLP 7+8 - DigestivEduard SimaderÎncă nu există evaluări
- Cancer Pulmonar NSCLC AvansatDocument12 paginiCancer Pulmonar NSCLC AvansatAndreea Mare100% (1)
- CC RenalDocument21 paginiCC RenalEliza SabinaÎncă nu există evaluări
- 71 Mieloproliferari MaligneDocument12 pagini71 Mieloproliferari MaligneobrejaÎncă nu există evaluări
- 5 Tumori Epiteliale CursDocument102 pagini5 Tumori Epiteliale CursDenisa NeaguÎncă nu există evaluări
- Durerea in Cancer (Sub.28)Document11 paginiDurerea in Cancer (Sub.28)Popa Mihai100% (1)
- Oncologie TotDocument71 paginiOncologie TotAnda Madalina ZahariaÎncă nu există evaluări
- Preventie Si Depistare in CancerDocument44 paginiPreventie Si Depistare in Cancerralu_5Încă nu există evaluări
- Curs 1 Oncologie - Definitie - IstoricDocument76 paginiCurs 1 Oncologie - Definitie - IstoricIoana Monica Marinescu100% (2)
- Curs 4 Cancerul MamarDocument51 paginiCurs 4 Cancerul MamarDr Diana Enachescu100% (1)
- Cancerul de Col Si de Corp UterinDocument18 paginiCancerul de Col Si de Corp UterinSpataru VirgilÎncă nu există evaluări
- Oncologie NormDocument41 paginiOncologie NormPătîrnichi ConstantinÎncă nu există evaluări
- Oncologie Intrebari xcsscscscsc1-80 LPDocument20 paginiOncologie Intrebari xcsscscscsc1-80 LPiremÎncă nu există evaluări
- Ciclul Celular Si CancerulDocument19 paginiCiclul Celular Si CancerulAndrei DraganÎncă nu există evaluări
- Cancerul Mamar - Material InformativDocument36 paginiCancerul Mamar - Material InformativSju Târgu JiuÎncă nu există evaluări
- Brahiterapia Cu Implant Permanent de Iod 125Document10 paginiBrahiterapia Cu Implant Permanent de Iod 125Buleteanu ManuelaÎncă nu există evaluări
- Patologia Mamara Benigna Si MalignaDocument22 paginiPatologia Mamara Benigna Si MalignaDJ ATBÎncă nu există evaluări
- Subiecte OncologieDocument47 paginiSubiecte OncologieMarius PasatÎncă nu există evaluări
- 59 - Cancerul TesticularDocument9 pagini59 - Cancerul TesticularAdrian PetrosÎncă nu există evaluări
- 62 - Cancerul RinichiuluiDocument13 pagini62 - Cancerul RinichiuluiAdrian PetrosÎncă nu există evaluări
- 5555 Cancer Colon 55Document142 pagini5555 Cancer Colon 55Alinuch Matei100% (1)
- Curs 8 Oncologie - GASTRICDocument34 paginiCurs 8 Oncologie - GASTRICIoana Monica Marinescu100% (1)
- OncologieDocument96 paginiOncologielacramioraÎncă nu există evaluări
- Cancerul OvarianDocument6 paginiCancerul OvarianlascaricasÎncă nu există evaluări
- Cancerul Gastric Carol DavilaDocument30 paginiCancerul Gastric Carol DavilaDenise DnsÎncă nu există evaluări
- Cancer GastricDocument38 paginiCancer GastricIrina PopoviciÎncă nu există evaluări
- Cancerul EsofagianDocument20 paginiCancerul Esofagianmarian comanÎncă nu există evaluări
- 57 - C - VaginDocument5 pagini57 - C - Vaginiloretaa123Încă nu există evaluări
- Cancerul EsofagianDocument4 paginiCancerul EsofagianvalcovemiÎncă nu există evaluări
- Cancerul ColorectalDocument5 paginiCancerul ColorectalOANAÎncă nu există evaluări