Documente Academic
Documente Profesional
Documente Cultură
Unitate de Invatare 10
Încărcat de
jicamihaiDrepturi de autor
Formate disponibile
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentDrepturi de autor:
Formate disponibile
Unitate de Invatare 10
Încărcat de
jicamihaiDrepturi de autor:
Formate disponibile
238
UNITATE DE NVARE 10
HIDROCARBURI AROMATICE: STRUCTURA, PROPRIETI
FIZICE, CARACTERUL AROMATIC. REGULA HCKEL
Unitate de nvare 10. Hidrocarburi aromatice: structura, proprieti fizice,
caracterul aromatic. Regula hckel.............................................................238
Obiectivele unitatii de invatare nr.10 .........................................................238
10.1 Structura benzenului ...........................................................................238
10.1.1 structura de rezonanta a benzenului; orbitalii moleculari ............243
10.2 Proprietati fizice .................................................................................245
10.3 Caracterul aromatic. Regula huckel....................................................245
10.4 Metode de obtinere.............................................................................242
10.4.1 Distilarea uscat a crbunilor ......................................................249
10.4.2. Reformarea catalitic ..................................................................250
10.4.3. Piroliza benzinelor alifatice ........................................................250
10.4.4. Transformarea funciunilor adiacente .........................................250
10.4.5. Prin reacii fittig-wurtz ...............................................................251
10.5 Reactivitatea relativ si orientarea substituiei electrofile in benzenul
mono- si disubstituit...................................................................................244
10.5.1.Reactivitatea relativ a hidrocarburilor aromatice la substituia
electrofil ................................................................................................251
10.5.2. Orientarea substituiei n benzenul monosubstituit ....................252
10.5.3. Orientarea substituiei la compuii benzenului disubstituit ........257
Teste de autoevaluare .................................................................................260
Lucrare de verificare ...................................................................................261
OBIECTIVELE UNITATII DE INVATARE NR.10
1.
2.
3.
4.
Insusirea metodelor de obtinere si a proprietatilor fizice ale arenelor;
Intelegerea notiunilor de caracter aromatic;
Intelegerea regulii Huckel
Evaluarea cunostintelor insusite pe baza testelor de autoevaluare si a
lucrarilor de evaluare
10.1 STRUCTURA BENZENULUI
Denumirea acestei clase de hidrocarburi provine de la mirosul
particular al reprezentanilor ei. Compuii aromatici sunt substane,
asemntoare benzenului ca proprieti fizice i chimice, datorit unei
configuraii electronice comune (chiar dac aparent sunt diferite)
difereniindu-se de compuii alifatici, asemntori oarecum grsimilor.
Proprietatea chimic dominant a compuilor aromatici este stabilitatea lor
239
termodinamic, n raport cu alte hidrocarburi i tendina de a da substituii
cu reactani electrofili (avnd afinitate pentru electronii ai compuilor
aromatici). Substituenii alifatici ai hidrocarburilor aromatice dau de obicei
reaciile caracteristice compuilor alifatici.
Dei benzenul (C6H6) este cunoscut de foarte mult timp, structura sa a
fost lmurit satisfctor numai n jurul anilor 1930, datorit dificultilor
provenite dintr-o reprezentare neadecvat a teoriei structurii.
a) Pentru formula brut a benzenului, Kekul a propus structura I, dar
aceleiai formule brute i pot corespunde i alte structuri, propuse
de ali autori :
H
H
H
H
H
H
H
I
II
Kekule'
CH2
C CH3
H2C
CH
IV
Hueckel
Ladenburg
III
Dewar
H3C
C CH
CH2
VI
VII
Din structurile prezentate, numai structura Kekul concord cu numrul real
de izomeri i anume :
b) Benzenul d un singur produs monosubstituit, C6H5-Z, adic numai
un singur nitrobenzen etc, deci toi atomii de hidrogen sunt echivaleni, ceea
ce este valabil doar pentru structurile I, III i VI.
c) Benzenul d 3 izomeri disubstituii, C6H4Z2 sau C6H4ZY i deci
structurile III i VI nu pot intra nici ele n discuie. Pentru izomerul orto, ar
putea ns fi scris i o alt structur, echivalent, n care poziia dublelor
legturi s-ar schimba (ntre carbonii care poart substituenii; ar putea fi o
legtur simpl sau dubl) i ar fi vorba de o tautomerie, susinut de un
echilibru continuu (delocalizare de electroni ?)
Br
Br
Br
Br
Br
Br
;
Br
orto
meta
Br
para
240
d) Structura Kekul rspunde satisfctor numrului de izomeri posibili dar
nu poate explica de ce benzenul este att de stabil termodinamic i d
preponderent un singur fel de reacii;
e) Benzenul d mai ales reacii de substituie, electrofil :
Br
Br 2
HBr
H2O
(Fe)
brombenze n
NO2
HNO3
( H2SO 4)
nitrobenzen
SO 3H
H2SO 4
H2O
(SO3)
acid benzensulfonic
H3CCl
CH3
(AlCl3)
HCl
metilbenzen
n reaciile de substituie electrofil (bromurare, nitrare, sulfonare, alchilare
i acilare Friedel-Crafts, etc.) un atom de hidrogen din ciclul benzenic este
nlocuit prin substituentul corespunztor i ciclul poate fi substituit n
continuare.
f) Reaciile de adiie ale benzenului decurg greu, cu aport mare de
energie i implic specii reactive (atomi, radicali liberi, carbene, sisteme
catalitice). Dac ar fi o adevrat ciclohexatrien, cum o reprezint
structura Kekul, el ar trebui s reacioneze similar alchenelor sau dienelor,
adic s dea o reacie de oxidare rapid (cu soluie KMnO4 la rece), adiie
rapid de Br2 n soluie de CCl4, la ntuneric, adiie rapid de soluie de acid
iodhidric, ceea ce nu se observ experimental. Reaciile prin care dispar
legturile multiple se petrec doar n condiii energice, cu reactani i sisteme
catalitice puternice, sau sub influena radiaiei:
241
3H2, catalizatori
ciclohexan
100 atm 100-200 C
O3
3O2
O3
triozonida
O3
3Cl 2
Cl
H
H Cl
H
Cl
H
Cl
Cl
hexaclorociclohexan
H Cl
: CH2
CH2
carbena
norcaradiena
g) Ciclul aromatic are o influen acidifiant asupra grupelor legate de
el, adic fenolul este un acid mai puternic dect alcoolii, acidul benzoic este
mai puternic dect acizii alifatici, iar anilina este o baz mai slab dect
aminele alifatice:
OH
fenol
COOH
acid benzoic
NH2
anilina
acid mai puternic (Ka 10-10-) mai puternic (Ka 6x10-5) baz mai slab (Kb 10-10)
dect alcoolii (Ka 10-16)
dect acizii alifatici (Ka 1,5x10-5)
dect
aminele alifatice (Kb 10-4)
Stabilitatea ciclului benzenic. Cldura de hidrogenare i de ardere
Din reaciile prezentate anterior, rezult calitativ, c benzenul este mai
stabil dect ciclohexatriena corespunztoare. Ca i n cazul altor substane
studiate (alchene, diene conjugate, acetilene) evaluarea cldurilor de
hidrogenare i de ardere ne ofer o msur obiectiv a stabilitii lor
relative: cu ct cldurile de hidrogenare i de ardere sunt mai mici, cu att
substanele respective sunt mai stabile. Cldura de hidrogenare pentru o
dubl legtur este de -2830 Kcal/mol (ciclohexen -28,6 ; ciclohexadien
-55,4) i deci ciclohexatriena ar trebui s aib cldura de hidrogenare de (28,6 x 3) = -85,8 Kcal/mol. n realitate cldura de hidrogenare msurat
experimental este de numai -49,8 Kcal/mol, adic cu 36 Kcal/mol, mai
mic, dect cea calculat. Reprezentarea energiei poteniale, n funcie de
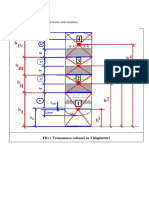
gradul de hidrogenare este redat n fig. 14.1.
242
ciclohexatriena
ipotetica
+ 3H2
Energie potentiala
1,3-ciclohexadiena
energia de
rezonanta
benzen
+ 2H2
-85,8
(calc.)
ciclohexena
+ 3H2
36 kcal/mol
+ H2
-57,2
(calc.)
-49,8
-55,4
-28,6
ciclohexan
Fig 14.1 Clduri de hidrogenare calculate i experimentale (Kcal/mol) i
stabilitatea relativ, fa de ciclohexan, a ciclohexenei; ciclohexadienei i a
ciclohexatrienei (ipotetice) fa de benzen. Energia de rezonan a benzenului = 36
Kcal/mol
Cldurile de ardere, comparate pentru cei trei compui, conduc la
aceiai concluzie, c benzenul este mai stabil, dect ciclohexatriena
ipotetic, cu 36 Kcal/mol, egal cu energia de rezonan a benzenului. Este
uor de observat c toate reaciile de hidrogenare sunt exoterme (chiar dac
uneori, cum e cazul benzenului decurg n condiii energice) deoarece se rup
legturi C=C, relativ slabe i se formeaz legturi C-H puternice. Este
evident c toate reaciile de dehidrogenare sunt endoterme. Totui reacia
de dehidrogenare a 1,3-ciclohexadienei la benzen este slab exoterm (H
-5,5 Kcal/mol).
- H2
1,3- ciclohexadiena
H = -5,5 Kcal/mol
benzen
ceea ce adeverete, c intervine puternic energia de conjugare (de rezonan)
care stabilizeaz molecula benzenului. Este evident c reacia invers,
hidrogenarea primei legturi din benzen duce la diminuarea energiei de
conjugare i este o reacie endoterm (contrar tuturor reaciilor de
hidrogenare a dublei legturi) i ca urmare, practic nu se poate realiza
hidrogenarea parial a benzenului, pentru a obine ciclohexadien sau
ciclohexen, dect n condiii speciale.
243
10.1.1 STRUCTURA DE REZONANTA A BENZENULUI;
ORBITALII MOLECULARI
Cu ajutorul metodelor fizice (difracia de raze X, difracia de electroni,
spectroscopia IR i Raman) s-a demonstrat c geometria moleculei
benzenului corespunde unui hexagon regulat, plan, cu toate legturile
carbon-carbon, egale ntre ele. Lungimea acestor legturi este intermediar,
ntre lungimea unei legturi simple C-C (1,54) i a uneia duble C=C
(1,34), fiind de 1,397. De asemenea toate legturile C-H sunt egale ntre
ele, dar mai scurte dect
n alcani i n alchene (1,084) iar toate
unghiurile de legtur sunt de 120. n concordan cu aceste date, cldura
de disociere a legturilor C-H este egal cu 112 Kcal/mol, mult mai mare
dect n ciclohexan i chiar n alchene.
;
I
II
Structuri limit
III
hibrid de rezonan
Structura Kekul, redat prin cele dou structuri limit (I i II)
particip cu egal probabilitate la structura real a moleculei (deoarece sunt
echivalente energetic) care este redat mai bine prin hibridul de rezonan
III, n acord fidel, cu cele 6 legturi C-C egale i echivalente, de 1,397,
adic ntre lungimea legturii duble i simple.
O reprezentare mai exact a structurii benzenului se obine prin luarea
n consideraie a orbitalilor de legtur. Un atom de carbon legat cu ali trei
atomi, cum este i cazul benzenului, folosete trei orbitali hibrizi sp2, ca n
etilen, ceea ce conduce la plasarea tuturor atomilor carbonului ntr-un
singur plan i formarea legturilor prin ntreptrunderea orbitalilor hibrizi
sp2, pe direcia legturii :
Legturile din benzen,
Norii electronici ,
formate cu orbitalii hibrizi sp2
i dedesubtul planului
ai carbonului
legturilor din benzen
Formarea legturilor , prin
ntreptrunderea lateral a orbitalilor p,
deasupra
perpendiculari pe planul moleculei
benzenului
Fiecare orbital p, perpendicular pe planul legturilor , ocupat cu un
singur electron se ntreptrunde, prin lateral, cu orbitalii p vecini, astfel c
din cei 6 orbitali p rezult o structur de electroni , delocalizai pe ntregul
nucleu, ceea ce confer o stabilitate mai mare a moleculei. Electronii
244
delocalizai sunt mai slab legai dect electronii din legturile i de aceea
sunt mai uor accesibili unui reactant electrofil. Reaciile tipice ale ciclului
benzenic sunt cele n care el cedeaz electronii (este o baz Lewis)
agentului electrofil (acid Lewis) i are loc o reacie de substituie, pentru a
conserva caracterul aromatic.
Prin combinarea linear a celor ase orbitali atomici, trebuie s rezulte
ase orbitali moleculari 1-6 (vezi principiile de combinare a orbitalilor
atomici) ale cror energii i simetrii au fost calculate, folosind metoda
orbitalilor moleculari. (vezi fig 14.2)
Orbitalii moleculari 1,2, 3 sunt orbitali moleculari , de legtur
ocupai cu cte doi electroni cu spin mperechiat : orbitalul 1 de energie
minim, i 2 cu 3 cu aceeai energie (orbitali degenerai). Aceti trei
orbitali de legtur se suprapun geometric, sub forma a doi nori toroidali,
fiind plasai imediat deasupra i dedesubtul planului legturilor ,
constituind aa zisul sextet aromatic. Deoarece energiile orbitalilor se
exprim prin suma sau diferena a dou valori: = energia orbitalului 2p
nainte de ntreptrundere iar = integrala de rezonan = energia de
stabilizare rezultat n urma suprapunerii ; valorile rezultate din calcul
sunt redate pe verticala din fig 12.2. Energia total a electronilor din cei trei
orbitali ocupai (din care doi de energie egal = degenerai, + ) este egal
cu suma: 2( + 2) + 2( + ) + 2( + ) = 6 +8 , i este mai mic dect
energia a trei legturi duble izolate = 3(2 + 2). Diferena dintre aceste
energii, egal cu 2 reprezint energia de conjugare (de rezonan, de
delocalizare) i n metoda Hckel 2 = 36Kcal/mol, deci = 18 Kcal/mol.
Fig 14.2 Cei ase orbitali moleculari ai benzenului, ocupai cu electroni, n stare
fundamental
245
Reprezentarea corect a ciclului benzenic este redat
suprapunerea celor dou structuri limit (mezomere) Kekul (I i II).
prin
legaturi
;
I
II
structuri limita
III
hibrid de rezonanta
Adesea structura aromatic a benzenului este redat prin formula III,
hibridul de rezonan, respectndu-se convenia c hexagonul reprezint
legturile iar inelul interior legturile (sextetul aromatic). Extinderea
acestei reprezentri la hidrocarburile aromatice policiclice este incorect
cci acolo cercul nu mai red sextetul aromatic de electroni (vezi i
13.1.2).
10.2 PROPRIETATI FIZICE
Hidrocarburile aromatice sunt puin polare, au miros caracteristic,
particular, sunt insolubile n ap dar solubile n solveni nepolari: CCl4, eter
de petrol, eter etilic. Ele au densitate mai mic dect apa iar punctul de
fierbere crete cu masa molecular, aproximativ cu 20-30 pentru un atom
de carbon. Punctul de topire depinde de masa molecular dar mai ales de
poziia relativ a substituenilor, izomerii para avnd puncte de topire mai
ridicate dect ceilali izomeri (xilen, o, m = -25C i 43C, dar para =
+13C) i deci aceti izomeri sunt mai puin solubili ntr-un anumit solvent
(structurile cristaline sunt mai compacte din cauza simetriei moleculare mai
ridicate) cci forele intermoleculare sunt mai puternice.
10.3 CARACTERUL AROMATIC. REGULA HUCKEL
Exist multiple structuri asemntoare benzenului (dar diferite de
benzen) care posed caracter aromatic i seamn cu el, dar n ce msur ?
n general ele au stabilitate termodinamic mai ridicat dect congenerii
lor, sunt plane, cu legturi conjugate; dau preferenial reacii de substituie
i au clduri de hidrogenare i de ardere mai mici dect cele ateptate, iar
n spectrul de rezonan magnetic nuclear (RMN) indic deplasri
chimice asemntoare.
Din punct de vedere teoretic un compus este aromatic dac conine un
nor electronic deasupra i dedesubtul unui ciclu plan, format n total din
(4n + 2) electroni , adic trebuie s avem pentru n = 0,1,2,3, etc, un numr
determinat de electroni : 2,6,10,14 etc sau numr impar de perechi de
electroni : 1,3,5,7,etc. Aceast regul, a lui Hckel, decurge din calcule
mecanic cuantice i depinde de umplerea diferiilor orbitali cu electroni .
Regula lui Hckel a fost verificat de numeroase date experimentale. n
afara benzenului cu sextet de electroni (n=1) sunt i alte hidrocarburi ca
246
naftalina, antracenul, fenantrenul, azulena sau compui heterociclici
(piridina, tiofenul, pirimidine, etc) care posed tot sextet electronic i deci
au caracter aromatic.
Dac examinm cele ase structuri ale radicalilor, cationilor i
anionilor, corespunztoare ciclopentadienei i cicloheptatrienei, (care n-au
caracter aromatic deoarece sistemul de legturi nu este conjugat), fiecare
redat prin 5, respectiv 7 structuri de rezonan echivalente, n care
electronul nemperecheat sau sarcina este delocalizat la alt atom din ciclu,
se observ c stabilitate deosebit au numai anionul ciclopentadienilic, i
cationul cicloheptatrienilic (tropiliu):
cation ciclopentadienilic
4 electroni
nearomatic
H
+
H
H
cation cicloheptatrienilic
6 electroni (tropiliu)
aromatic
radical ciclopentadienilic
5 electroni
nearomatic
anion ciclopentadienilic
6 electroni
aromatic
H
H
H
H
H
radical cicloheptatrienilic
7 electroni
nearomatic
H
H
H
anion cicloheptatrienilic
8 electroni
nearomatic
Dei fiecare molecul (cation, radical sau anion) reprezint un hibrid
de rezonan cu 5, respectiv 7 structuri echivalente, numai anionul
ciclopentadienilic i cationul tropiliu, cu cte un sextet de electroni au
stabilitate deosebit, deoarece numai ei ndeplinesc regula Hckel cu (4n+2)
electroni (n=1). Deci pentru a avea caracter aromatic, nu sistemul conjugat
de duble legturi i/sau numrul structurilor de rezonan echivalente
energetic sunt decisive, ci satisfacerea condiiei de a poseda un sistem de
(4n+2) electroni sau numr impar de perechi de electroni : 1,3,5,7.
Dealtfel ciclopentadiena este o substan cu caracter acid neateptat
(Ka 10-15) mai puternic dect alcoolii (Ka10-16) fa de cicloheptatrien
(Ka 10-45) avnd chiar 7 structuri de rezonan, deoarece ciclopentadiena
prin cedarea unui proton se transform ntr-un anion cu sextet aromatic de
electroni, stabil (anion de ciclopentadieniliu) pe cnd cicloheptatriena se
transform prin cedarea unui proton, ntr-un anion cicloheptatrienilic (cu 8
electroni ) care n-are caracter aromatic, pentru c nu ndeplinete regula
Hckel.
247
Caracterul aromatic al anionului ciclopentadienilic se pune n eviden prin
sarea de Fe2+, a doi anioni (C5H5-)2 de diciclopentadien care formeaz o
molecul covalent, stabil, (p.t.=174C ; p.f.=245), cu structur de
sandvi, n care toate legturile C-C sunt egale (1,4) iar ciclurile dau
reacii de substituie aromatic tipice, (sulfonare, alchilare i acilare FriedelCrafts), fr a afecta structura moleculei, sensibil la ageni oxidani.
3,22
Fe
Ferocenul (metalocen)
Din motive similare cationul cicloheptatrienilic (sextet aromatic
realizat formal prin cedarea unui electron i a unui atom de hidrogen din
cicloheptatrien) este stabil. Spre exemplu bromura de tropiliu C7H7Br se
topete peste 200 este solubil n ap i insolubil n solveni nepolari,
dnd cu soluie de AgNO3, imediat, precipitatul alb de AgBr. Nici un
compus bromurat organic, (n care legtura este n general covalent i este
insolubil n ap), nu are asemenea comportare de compus ionic, R+Br-, i ea
se datoreaz stabilitii carbocationului cicloheptatrienilic, cu sextet
aromatic de electroni .
Configuraia electronic a anionului ciclopentadienilic este dat de
cinci atomi de carbon, legai prin orbitali hibrizi sp2, cu ei nsi i fiecare cu
cte un atom de hidrogen (molecul plan). Pentagonul cu unghi de 108
este apropiat de 120 (pentru sp2 ) i o oarecare tensiune unghiular n ciclu
este compensat de delocalizarea electronilor . Acetia formeaz norul
electronic de sextet, prin combinarea a patru orbitali p, cu cte un electron i
un orbital p cu doi electroni (cel care a cedat protonul), distribuit deasupra i
dedesubtul ciclului aromatic.
248
ntr-un mod analog se formeaz cationul aromatic cicloheptatrienilic
(tropiliu) i ei se redau prin ciclurile
, respectiv
.
Pentru a poseda caracter aromatic substanele trebuie s aib un ciclu
format din legturi , cu hibridizare sp2, plan i ca urmare un unghi de
legtur apropiat de 120, pentru ca orbitalii p s se poat ntreptrund,
pentru ntregul ciclu. Ar trebui s fie deci aromatice, substanele cu 5-6-7
atomi n ciclu, deoarece n acest mod se confer structurii respective
stabilitate maxim i aceasta este adevrat pentru multe substane.
i alte substane monociclice cu 2,10,14,18 electroni care se supun
regulii lui Hckel, au caracter aromatic, dar nu apropiat benzenului, ci sunt
mai stabile dect compuii nrudii ca structur, cci ciclul lor este tensionat
(fie prea mic, fie prea mare) raportul la legturile rezultate din contopirea
orbitalilor hibrizi sp2. De exemplu 3-clorociclopropena d cu SbCl5 o
substan cristalin, insolubil n solveni nepolari, dar solubil n solveni
polari:
H
H
+
SbCl 6
SbCl 5
H
+
H Cl
n care toi protonii sunt echivaleni n 1H-RMN i care d cu AgBF4 un
precipitat alb de AgCl. Dac se adaug ioni de Cl- se obine din nou 3-clorociclopropena.
1,3,5,7-Ciclooctatetraen d reaciile obinuite ale compuilor
nesaturai (oxidare cu sol. dil. de KMnO4, adiie de Br2 n CCl4 la ntuneric)
dar atunci cnd este tratat cu K metalic se obine un compus stabil C8H822K+, deoarece anionul su are 10 electroni i satisface regula lui Hckel,
pentru cicluri aromatice, relativ slabe :
o
+2K
+2e
2-
2K+
Numai hidrocarburile ciclice cu legturi conjugate (anulene) care
ndeplinesc regula lui Hckel, privind numrul electronilor , au caracter
aromatic: astfel anulena (16) este nesaturat i instabil, iar anulena ( 18) are
caracter aromatic.
H
H
H
H
H
H
anulena (16) nesaturat, instabil
aromatic
anulena (18)
249
Substanele care posed numai 4n electroni (sau numr par de
perechi de electroni) sunt nestabile i considerate antiaromatice, cum sunt :
ciclobutadiena (4 electroni )
(antiaromatic)
2 perechi de electroni
pentalena (8 electroni )
(antiaromatic)
4 perechi de electroni
n schimb caracterul aromatic se pstreaz la sisteme homoaromatice (cu
grupe CH2 adiionale), la compuii mezoionici ; la ciclofani, la sisteme
heterociclice care ndeplinesc regula Hckel etc :
H
+
p-ciclofan
(aromatic)
cation homotropiliu
(homoaromatic)
C
+ C
N C
sidnon mezoionic
(aromatic)
N
azulen
(aromatic)
piridin
(aromatic)
10.4 OBINEREA HIDROCARBURILOR AROMATICE.
Att benzenul ct i homologii si reprezint materiile prime de
baz pentru fabricarea tuturor compuilor aromatici. De obicei nimeni nu
ncearc s-i sintetizeze nucleul benzenic n scopuri preparative. n general
hidrocarburile aromatice provin din dou surse: crbunele i petrolul.
10.4.1 Distilarea uscat a crbunilor
La distilarea uscat (la 800-1000C) a crbunilor se obin gaze (H2,
metan, H2O, NH3) i fraciuni lichide, provenite din descompunerea parial
a crbunelui iar ca reziduu se obine cocsul pentru metalurgie (aproape 80%
din total). Dintr-o ton de crbune cocsificabil se obin 40-50 Kg de
fraciuni de lichide n care exist aproximativ 1 Kg benzen, 0,250 g toluen,
0,050 Kg xileni, 0,250 Kg fenol, 1 Kg crezoli (metilfenoli, izomeri) i 2,5
Kg naftalin. Dei se prelucreaz anual, cantiti enorme de crbune i deci
250
sursa de hidrocarburi aromatice este semnificativ, ea nu satisface
necesitile industriale i peste 90% din hidrocarburile aromatice provin din
procesele de prelucrare a petrolului.
10.4.2. Reformarea catalitic
Reformarea catalitic const n trecerea benzinelor de distilare
primar (cu pf<200C) la temperaturi de 450-500C peste catalizatori
bimetalici (cu funciune acid i hidrogenant: Pt/Al2O3) n atmosfer de
hidrogen. Aromatele se obin nu numai prin dehidrogenarea ciclurilor
corespunztoare, ci i prin reacii de ciclizare, izomerizare i
dehidrociclizare a alcanilor i a cicloalcanilor, formndu-se de exemplu
toluen din n-heptan sau din 1,2-dimetilciclopentan. Benzenul se poate forma
din dehidrogenarea ciclohexanului, din metilciclopentan (izomerizare,
dehidrogenare) sau din hidrodezalchilarea toluenului. La benzinele de
reformare, n fraciunea BTX (benzen-toluen-xilen) predomin toluenul.
10.4.3. Piroliza benzinelor alifatice
Cantiti importante de aromate se formeaz i la piroliza benzinelor
alifatice pentru producerea olefinelor inferioare (eten, propen, alturi de
butadien i izopren) unde se formeaz aromate i prin reacii periciclice
(cicloadiii, electrociclizare) i dehidrogenare. n fraciunea BTX a
benzinelor de piroliz predomin benzenul.
Att din benzinele de reformare ct i din cele de piroliz
hidrocarburile aromatice se pot separa prin extracie cu solveni potrivii
(sulfolan, SO2 lichid, N-metilpirolidon, polietilenglicol) urmat de
rectificarea pentru separarea de aromate individuale pure, sau pentru a
folosi, alturi de benzinele provenite din cracare catalitic (bogate n
hidrocarburi aromatice) la ridicarea cifrei octanice a benzinelor comerciale.
10.4.4. Transformarea funciunilor adiacente
O cale important pentru obinerea alchilaromatelor o reprezint
transformarea catenei laterale, purttoare de anumite funciuni ca de
exemplu:
A) Hidrogenarea alchenil-aromatelor
CH=CH-R
H2
Ni(cat)
CH2-CH2-R
Ea se practic la prelucrarea fraciunilor aromate, cu coninut
apreciabil de alchenilaromate, provenite din procesele de piroliz a
alcanilor.
B. Reducerea aril-cetonelor
251
Aril-cetonele, uor de obinut prin acilare Friedel-Crafts a
aromatelor, cu halogenuri acide, n prezena AlCl3, se pot reduce la alchilaromate pe dou ci:
a) reducere Clemensen
O
C-R
a) Zn(Hg)HCl
b) reducere Wolff-Kishner
CH2-R
sau b) N2H4 + KOH conc., To
10.4.5. Prin reacii Fittig-Wurtz
Reacia Wurtz, aplicat la sinteza alcanilor, se poate folosi i la
condensarea unui derivat halogenat aromatic, cu un derivat halogenat
alifatic i conduce la un omolog al hidrocarburii alchil-aromatice, fr a
avea loc izomerizarea catenelor:
o
C6H5Br
BrCH2(CH2)4CH3
bromobenzen
2Na
C6H5CH2(CH2)4CH3
-2NaBr
1-bromohexan
n-hexilbenzen
Intermediar se formeaz compui organo-metalici aromatici care sunt
alchilai ulterior de ctre derivatul halogenat alifatic.
o
C6H5Cl +
C6H5Na +
2 Na
clorbenzen
C6H5Na
fenilsodiu
NaCl
fenilsodiu
C6H5CH2CH3 + NaCl
ClCH2CH3
clorura de etil
etilbenzen
10.5. REACTIVITATEA RELATIVA SI ORIENTAREA
SUBSTITUTIEI ELECTROFILE IN BENZENUL MONO- SI
DISUBSTITUIT
10.5.1.Reactivitatea relativ a hidrocarburilor aromatice la substituia
electrofil
Dac se examineaz comparativ etapa lent, determinant de vitez, n
cazul benzenului (I) cu alte hidrocarburi, purtnd substitueni donori de
electroni (toluenul) (II) sau atrgtori de electroni (nitrobenzenul) (III):
E
+
CH 3
II
NO 2
III
252
se observ c un substituent donor de electroni, cum e grupa CH3 din II,
favorizeaz preluarea sarcinii pozitive de ctre nucleul aromatic i prin
urmare stabilizeaz ionul de carbeniu, ceea ce va determina formarea lui mai
uoar n etapa de tranziie, dect n cazul benzenului nesubstituit (I).
Substituenii cu efect inductiv +I, de ordinul unu (avnd numai legturi
simple) vor accelara reacia de substituie electrofil. Grupa NO2 are
dimpotriv un efect puternic atrgtor de electroni (-I i -E) care amplific
sarcina pozitiv a nucleului, scade stabilitatea ionului de carbeniu i
micoreaz viteza de reacie.
Reactivitatea la substituia aromatic electrofil depinde de
capacitatea substituentului de a ceda sau de a atrage electronii (prin efecte
inductive I i/sau prin efecte de rezonan E). Substituenii care cedeaz
electroni activeaz nucleul aromatic iar cei care atrag electroni
dezactiveaz nucleul n reacia de substituie electrofil.
E
+ E+
+
G
G=
G este electrodonator,
stabilizeaza carbocationul,
activeaza substitutia,
orienteaza in orto/para
- O- NR2
- OH
- OCH3
mai ales prin +E
- NHCOCH3
- C6H5
- CH3 si alti alchili;
E
+ E+
+
G
G este electronoacceptor,
destabilizeaza carbocationul,
dezactiveaza substitutia, mai
ales in orto/para, si deci
orienteaza in meta
G=
- NR3+
- NH3+
- NO2
- CN
- SO3H
- COOH
- CHO
- COR
sarcina pozitiva sau
grupa cu legaturi
multiple, orienteaza
meta
Dac grupa alchil este la rndul su substituit cu ali atomi, ca de exemplu
pentru grupa metil, rezultatul const n creterea dezactivrii, pe msura
introducerii elementelor electronegative:
CH3
activare
+I
CH2Cl
dezactivare
slaba
CHCl2
dezactivare
insemnata
CCl3
dezactivare
puternica
10.5.2. Orientarea substituiei n benzenul monosubstituit
Din discuia efectului substituenilor asupra subtituiei aromatice
electrofile a rezultat c :
253
a) o grup activatoare activeaz toate poziiile din nucleul benzenic, dar
mai puin pe cea din meta, de aceea substituia este dirijat preferenial
n orto-para:
b) o grup dezactivatoare, dezactiveaz toate poziiile benzenului, dar
n mai mare msur poziiile orto i para, de aceea substituia se
dirijeaz n poziia meta, mai puin dezactivat.
Deci n general substituenii i exercit efectul activator sau dezactivator n
poziiile orto-para i mai puin n meta. De ce are loc o semenea orientare
preferenial? Dac se examineaz, n cazul toluenului toate structurile de
rezonan pentru substituiile n orto, meta, para cu reactantul +E se va
observa c :
CH3
CH3
CH3
Atac n poziia para. Structura
III este preferat cci sarcina
pozitiv se exercit la atomul cu
substituent donor de electroni, cu
efect inductiv maxim iar
carbocationul este teriar
+
+
H E
H E
H E
II
CH3
CH3
E
III
IV
E
H
CH3
+
H
VII
VI
CH3
CH3
E
+
Atac n poziia orto. Structura
VI este preferat energetic cci
sarcina pozitiv se exercit la
substituentul donor de electroni
iar carbocationul este teriar.
CH3
H
VIII
Atac n poziia meta. Nici una
din structurile limit nu
beneficiaz direct de aportul
donorului de electroni iar
carbocationul este secundar.
E
H
IX
Evident c toluenul va fi substituit mai repede dect benzenul nesubstituit
(pentru condiii echivalente de reacie) datorit efectului grupei CH3 iar
orientarea substituiei va fi preferenial pentru poziiile orto i para. Dac
n locul grupei CH3 vom avea substitueni mai voluminoi, ca t-butil, din
motive sterice, izomerul para va fi preponderent.
254
O examinare similar pentru un substituent atrgtor de electroni, ca
de exemplu NO2, conduce la concluzia c atacul electrofilului +E se
produce preferenial n meta :
NO2
NO2
NO2
Atac n para: structura XII este
energetic deosebit de nefavorabil,
cu sarcina pozitiv la carbonul
srcit de substituentul atrgtor de
electroni i particip numai dou
structuri echivalente, la rezonan.
+
+
E H
E H
E H
XI
XII
NO2
NO2
E
+
XIII
NO2
E
+
XVI
NO2
E
+
XIV
XV
NO2
NO2
H
XVII
E
H
Atac n orto: Structura XV este
energetic foarte defavorabil,
deci particip la rezonan numai
dou structuri echivalente.
Atac n meta: Toate structurile
particip n mod egal la hibridul
de rezonan, deci substituia
preferat este n meta.
H
XVIII
Am examinat pn acum efectul grupelor donatoare sau atrgtoare de
electroni, numai prin efectul inductiv, care se manifest din aproape n
aproape i devine nesemnificativ la al 3-lea atom. Unele grupe cu efect
inductiv I, ca -NH2, -OR sau derivaii lor, mai electronegativi dect C,
datorit electronilor neparticipani, acioneaz ca activatori puternici n
substituia aromatic electrofil, prin efect electrodinamic +E, (de
rezonan) la cererea reactantului.
Efectul acestor grupe se poate explica prin contribuia electronilor
neparticipani la legtura cu nucleul aromatic, prelund o parte din sarcina
sa pozitiv. Pe aceast cale numrul structurilor de rezonan se amplific
i favorizeaz substituia, n poziiile para i orto. Pentru o grup NH2, la
atacul electrofilului +E, se pot scrie urmtoarele structuri de rezonan :
255
NH2
NH2
NH2
Atac n para : structura de
rezonan IV este favorizat
energetic, cci ea corespunde
unei sri de amoniu, cu octet de
electroni la C i N i nu unui
carbocation, ca n structurile IIII.
NH2
+
+
H E
H E
H E
II
NH2
III
NH2
VI
VII
NH2
NH2
NH2
IX
NH2
E
H
VIII
Atac n meta : Nu se poate scrie
o structur limit, cu sarcina
pozitiv preluat de N. Atacul
este defavorizat.
IV
NH2
E
H E
E
H
XI
Pentru ceilali derivai, ca fenolii i aminele substituite se pot scrie structuri
limit similare, corespunztoare unor sruri de oniu (amoniu, oxoniu etc) :
+ OH
+ OH
+ OCH
+ OCH
E
H ;
E
para
+ NR
E
H
orto
+ NR
H
para
+ NH-COCH
E
H ;
H
para
orto
E
H
E
orto
+ NHCOCH3
H
para
orto
Atac n orto :
Structura
limit XI, ca
sare de
amoniu, cu
octet de
electroni la C
i N este
favorizat
energetic.
256
Este evident c efectul electrodinamic +E este mult mai puternic dect
efectul inductiv +I i consecinele sunt importante :
a) Derivaii monosubstituii ai benzenului care poart asemenea grupe
reacioneaz nu numai cu electrofilii tari, ci i cu cei slabi (+NO,
ArN+N]X-, CO2, :CX2 etc) ;
b) Orientarea substituiei se face preferenial n para, deoarece
structurile limit corespunztoare includ delocalizarea electronilor pe un
numr mai mare de atomi, dect poziia orto. Numai dac poziia para este
ocupat sau reactantul este implicat n structuri chelatice, substituia are loc
n poziia orto.
Influena halogenilor din nucleu asupra substituiei aromatice electrofile
Existena halogenilor din nucleul aromatic infueneaz aparent n mod
straniu substituia aromatic electrofil. Fiind puternic atrgtori de
electroni, halogenii dezactiveaz nucleul aromatic (i deci ar trebui s
orienteze n meta) dar n realitate orienteaz substituia n orto-para.
Explicaia const n efectul inductiv, atrgtor de electroni al halogenilor i
prin efectul electronodonator datorat rezonanei.
E
+
Cl
Prin efectul I, halogenii dezactiveaz ntreg nucleul benzenic ; mai
puternic pentru substituiile din poziiile orto-para i mai puin n meta (vezi
i efectul grupei NO2, atrgtoare de electroni). Dar un atom de halogen
poate prelua sarcina pozitiv a nucleului, transformndu-se n ion de haloniu
(vezi adiia halogenilor la olefine) i poate participa la stabilizarea strii de
tranziie a substituiilor din orto i para:
Cl
Cl
E
+
Cl
E
E
H
carbon cu sextet de electroni,
mai putin stabil, caci sarcina + este
la carbonul cu substituentul -I
Cl
E
H;
Cl
sau
relativ stabil,
ion dehaloniu,
cu octet de electroni
la carbon
H E
pentru para
Efectul inductiv I este puternic i depete efectul salb de rezonan +E al
halogenilor, de aceea prin efectul inductiv I se dezactiveaz toate poziiile
nucleului benzenic. Efectul su de rezonan este opus efectului inductiv
pentru poziiile orto i para i de aceea acestea sunt mai puin dezactivate
dect meta. n acest mod, dei efectul inductiv este mai puternic, el transfer
257
efectului de rezonan (mai selectiv) orientarea orto-para n substituia
nucleului aromatic. Caracterul parial de dubl legtur a halogenului la
compui vinilici i la cei aromatici (mpreun cu tipul diferit de hibridizare,
sp2, care intervine n legturile ) ofer ntr-o oarecare msur explicaia, de
ce atomii de halogen din asemenea compui sunt att de puin reactivi.
10.5.3.Orientarea substituiei la compuii benzenului disubstituit
Prezena a doi substitueni n acelai ciclu poate s complice ntr-o
msur nsemnat orientarea substituiei.
i) Dac din ntmplare, natura substituenilor i poziia relativ este
convenabil, efectul lor de orientare se nsumeaz, ca de exemplu:
NO2
CH3
NH-COCH3
CN
SO 3H
NO2
Dac subtituenii orienteaz n poziii diferite, atunci orientarea
substituiei este decis de grupele activatoare.
ii) Grupele activatoare puternice (mai ales cu efect +E)
contrabalanseaz orientarea substituenilor dezactivatori sau a celor cu
capacitate slab de orientare. Ordinea de orietare se plaseaz n seria :
-O-, -NR2, -NH2, -OH, -OCH3, -NHCOCH3, -C6H5, -CH3 > grupe ce orienteaz meta,
(dezactivatoare)
Exemple:
NHCOCH3
OH
OH
NO2
HNO 3
CH3
CH3
FeBr3
CH3
singurul produs
COOR
COOR
Br
Br2
FeBr3
OH
Br
Br2
H2SO4
NHCOCH3
OH
produs principal
n alte cazuri este dificil de prevzut orientarea substituiei :
CH3
produs principal
258
Cl
Cl
Cl
NO2
HNO 3
H2SO4
NO2
CH3
CH3
CH3
58%
42%
iii) ntre doi substitueni aflai n meta, n general substituia se face greu din
cauza efectului steric : De exemplu :
CH3
CH3
CH3
NO2
HNO 3
sau
H2SO4
CH3
CH3
CH3
NO2
85%
37%
Cl
15%
59%
1%
CH3
9%
;
Cl
Br
62%
la nitrare
32%
Toate aceste indicaii sunt foarte utile pentru conceperea sintezei unui
anumit compus, cci ne arat locul unde va intra substituentul i ordinea
preferenial de introducere, dependent de substitueni. Exemple:
259
COOH
COOH
CH3
HNO 3
H2SO4
oxidare
NO2
principalul produs
CH3
NO2
HNO 3
H2SO4
CH3
+
oxidare
NO2
oxidare
COOH
NO2
COOH
NO2
sau
NO2
NO2
Br2
Fe
HNO 3
H2SO4
Br
produs principal
Br
Br2
Fe
Br
Br
NO2
HNO 3
H2SO4
+
38%
NO2
62%
260
TESTE DE AUTOEVALUARE
1. Precizai dac reacia are loc sau nu, precum i produii care rezult
pentru sistemul benzen + 2CH3Cl + AlCl3
2. Cati produi se vor forma la monohalogenarea cu Cl2 + FeCl3 a pxilenului i a m-xilenului.
3. Cunoscnd cldura de hidrogenare a benzenului (DH = -49,8
kcal/mol) i a ciclohexenei (DH = -28,6 kcal/mol) calculai energia
de conjugare a benzenului.
4. Alegeti raspunsul correct:
I) Se numesc arene:
a) substanele compuse din atomi de C, H i O care au n structura
lor unul sau mai multe nuclee benzenice;
b) substanele compuse din atomi de C i H care au n structura
lor unul sau mai multe nuclee benzenice;
c) hidrocarburile saturate cu structur ciclic;
II) Formulei moleculare C9H12 i corespunde un numr de izomeri:
a) 4; b) 6; c) 8;
III) Care din urmtoarele afirmaii referitoare la structura moleculei
de benzen nu este adevrat?
a) particip cu uurin la reacii de adiie;
b) distanele ntre atomii de carbon sunt intermediare ntre
legtura simpl i cea dubl;
c) cei ase electroni aparin ntregului sistem
IV) Tratarea toluenului cu clor, n prezen de clorur de aluminiu
anhidr (AlCl3), conduce, la:
a) clorur de benzil;
b) meta-clor-toluen;
c) un amestec de orto i para clor toluen;
V) Prin reacia toluenului cu clorul, la lumin, se obine n principal:
a) clorur de benzil;
b) o-clor-toluen;
c) p-clor-toluen;
5. Se supun reaciei de nitrare 156 kg benzen. Dac s-au obinut 196,8
kg nitrobenzen, care este randamentul reaciei ?
261
LUCRARE DE VERIFICARE
1. La tratarea p-metil-fenolului (p-crezol) cu Br2 se formeaz n
majoritate un singur produs monosubstituit. Care este structura
produsului majoritar.
2. Prezentati influena halogenilor din nucleu asupra substituiei
aromatice electrofile.
3. Ordonai grupele de substane n ordinea descreterii reactivitii la
substituia electrofil: benzen, etilbenzen, clorobenzen, nitrobenzen,
fenol.
4. Scriei toate structurile de rezonan pentru substituiile n orto,meta
i para pentru cazul toluenului .
5. Ce mas de benzen este necesar pentru a obine 202 g mbromnitrobenzen, daca randamentul reaciei este de 90% ? Scriei
ecuaiile reaciei chimice.
REZUMAT
Dei benzenul (C6H6) este cunoscut de foarte mult timp, structura sa a
fost lmurit satisfctor numai n jurul anilor 1930, datorit dificultilor
provenite dintr-o reprezentare neadecvat a teoriei structurii. Proprietatea
chimic dominant a compuilor aromatici este stabilitatea lor
termodinamic, n raport cu alte hidrocarburi i tendina de a da substituii
cu reactani electrofili (avnd afinitate pentru electronii ai compuilor
aromatici).Cu ajutorul metodelor fizice (difracia de raze X, difracia de
electroni, spectroscopia IR i Raman) s-a demonstrat c geometria moleculei
benzenului corespunde unui hexagon regulat, plan, cu toate legturile
carbon-carbon, egale ntre ele. Electronii delocalizai sunt mai slab legai
dect electronii din legturile i de aceea sunt mai uor accesibili unui
reactant electrofil. Reaciile tipice ale ciclului benzenic sunt cele n care el
cedeaz electronii (este o baz Lewis) agentului electrofil (acid Lewis) i
are loc o reacie de substituie, pentru a conserva caracterul aromatic.
Hidrocarburile aromatice sunt puin polare, au miros caracteristic,
particular, sunt insolubile n ap dar solubile n solveni nepolari: CCl4, eter
de petrol, eter etilic. Ele au densitate mai mic dect apa iar punctul de
fierbere crete cu masa molecular, aproximativ cu 20-30 pentru un atom
de carbon. Punctul de topire depinde de masa molecular dar mai ales de
poziia relativ a substituenilor, izomerii para avnd puncte de topire mai
ridicate dect ceilali izomeri (xilen, o, m = -25C i 43C, dar para =
+13C) i deci aceti izomeri sunt mai puin solubili ntr-un anumit solvent
(structurile cristaline sunt mai compacte din cauza simetriei moleculare mai
ridicate) cci forele intermoleculare sunt mai puternice.
Din punct de vedere teoretic un compus este aromatic dac conine un
nor electronic deasupra i dedesubtul unui ciclu plan, format n total din
(4n + 2) electroni , adic trebuie s avem pentru n = 0,1,2,3, etc, un numr
determinat de electroni : 2,6,10,14 etc sau numr impar de perechi de
electroni : 1,3,5,7,etc. Deci pentru a avea caracter aromatic, nu sistemul
262
conjugat de duble legturi i/sau numrul structurilor de rezonan
echivalente energetic sunt decisive, ci satisfacerea condiiei de a poseda un
sistem de (4n+2) electroni sau numr impar de perechi de electroni :
1,3,5,7. Numai hidrocarburile ciclice cu legturi conjugate (anulene) care
ndeplinesc regula lui Hckel, privind numrul electronilor , au caracter
aromatic.
Reactivitatea la substituia aromatic electrofil depinde de capacitatea
substituentului de a ceda sau de a atrage electronii (prin efecte inductive I
i/sau prin efecte de rezonan E). Substituenii care cedeaz electroni
activeaz nucleul aromatic iar cei care atrag electroni dezactiveaz nucleul
n reacia de substituie electrofil.
Din discuia efectului substituenilor asupra subtituiei aromatice
electrofile a rezultat c o grup activatoare activeaz toate poziiile din
nucleul benzenic, dar mai puin pe cea din meta, de aceea substituia este
dirijat preferenial n orto-para, iar o grup dezactivatoare, dezactiveaz
toate poziiile benzenului, dar n mai mare msur poziiile orto i para, de
aceea substituia se dirijeaz n poziia meta, mai puin dezactivat. Deci n
general substituenii i exercit efectul activator sau dezactivator n
poziiile orto-para i mai puin n meta.
Unele grupe cu efect inductiv I, ca -NH2, -OR sau derivaii lor, mai
electronegativi dect C, datorit electronilor neparticipani, acioneaz ca
activatori puternici n substituia aromatic electrofil, prin efect
electrodinamic +E, (de rezonan) la cererea reactantului.
Efectul acestor grupe se poate explica prin contribuia electronilor
neparticipani la legtura cu nucleul aromatic, prelund o parte din sarcina
sa pozitiv.
Efectul inductiv I este puternic i depete efectul salb de rezonan
+E al halogenilor, de aceea prin efectul inductiv I se dezactiveaz toate
poziiile nucleului benzenic. Efectul su de rezonan este opus efectului
inductiv pentru poziiile orto i para i de aceea acestea sunt mai puin
dezactivate dect meta.
Prezena a doi substitueni n acelai ciclu poate s complice ntr-o
msur nsemnat orientarea substituiei. Astfel daca natura substituenilor
i poziia relativ este convenabil, efectul lor de orientare se nsumeaz, iar
dac subtituenii orienteaz n poziii diferite, atunci orientarea substituiei
este decis de grupele activatoare. Grupele activatoare puternice (mai ales
cu efect +E) contrabalanseaz orientarea substituenilor dezactivatori sau a
celor cu capacitate slab de orientare.
Bibliografie selectiv
1. Cuiban F., Bolocan I., Barbu E., Chimie organica moderna, vol I, Ed.
UPG Ploiesti, 2004
2. Avram, M., Chimie Organic, vol.I, Bucureti: Editura Academiei, 1983.
3. Cuiban, F.; Anghelache, I.; Bolocan, I.; Popescu, M., Probleme de chimie
organic, Ploieti: Ed. UPG, 1989.
4. Petrescu O., Petrescu G., Probleme si teste de chimie organica, Editura
PROREP, 1996
263
S-ar putea să vă placă și
- Arene MononucleareDocument19 paginiArene MononucleareDaniel AndronacheÎncă nu există evaluări
- Hidrocarburi AromaticeDocument14 paginiHidrocarburi AromaticeAnamaria Botan100% (1)
- Suport Curs Chimie Organica Compusi Cu Functiuni PDFDocument78 paginiSuport Curs Chimie Organica Compusi Cu Functiuni PDFTeodorina TeoÎncă nu există evaluări
- Acizi Carboxilici RCOFS 2018Document34 paginiAcizi Carboxilici RCOFS 2018Diana RalucaÎncă nu există evaluări
- Curs ChimieDocument28 paginiCurs ChimieMatthew EdwardsÎncă nu există evaluări
- Chimie Organica RED AndreiDocument145 paginiChimie Organica RED Andreijust meÎncă nu există evaluări
- Chimia Verde - Curs 1 - 2010Document38 paginiChimia Verde - Curs 1 - 2010Lavinia MotoroiuÎncă nu există evaluări
- Structura Benzenului Si Starea AromaticaDocument50 paginiStructura Benzenului Si Starea AromaticaMihaela SaviucÎncă nu există evaluări
- Carmen Pop - Curs 4Document48 paginiCarmen Pop - Curs 4Dana Elena LupuleasaÎncă nu există evaluări
- Mase PlasticeDocument222 paginiMase PlasticeSilviu C100% (9)
- 01 Teste Chimie Organica, FII, Sem I, 2011-2012Document344 pagini01 Teste Chimie Organica, FII, Sem I, 2011-2012Adi SoareÎncă nu există evaluări
- Laborator 5 OrganicaDocument6 paginiLaborator 5 OrganicaElena GheorghițăÎncă nu există evaluări
- MODEL Declaratie Proprie RaspundereDocument1 paginăMODEL Declaratie Proprie RaspundereAlina Mihai86% (136)
- Pproiectdidactic 9D CHIMIEDocument11 paginiPproiectdidactic 9D CHIMIEpopescuv_2Încă nu există evaluări
- Curs de Pregatire - Carbonilici - Acizi Si Derivati - 2013Document48 paginiCurs de Pregatire - Carbonilici - Acizi Si Derivati - 2013Cristina MariaÎncă nu există evaluări
- Reactii de SubstitutieDocument7 paginiReactii de SubstitutieFlorina VisanÎncă nu există evaluări
- Curs 5 Si Curs 6 - Echilibrul Ionic Şi Teorii Acido-BaziceDocument16 paginiCurs 5 Si Curs 6 - Echilibrul Ionic Şi Teorii Acido-BaziceMarianaBurloiuÎncă nu există evaluări
- Fisa de Lucru HidrocarburiDocument11 paginiFisa de Lucru HidrocarburiAlexÎncă nu există evaluări
- F 29 Formular Necesar MaterialeDocument1 paginăF 29 Formular Necesar MaterialejicamihaiÎncă nu există evaluări
- Determinare Grad de EpurareDocument4 paginiDeterminare Grad de EpurareGhita Alexandra MarianaÎncă nu există evaluări
- Metoda ChaulnesDocument5 paginiMetoda ChaulnesRaluca VasilacheÎncă nu există evaluări
- Curs 11Document19 paginiCurs 11Oana Andreea UrsicăÎncă nu există evaluări
- Fisa Mijlocului FixDocument2 paginiFisa Mijlocului FixRadoi Bogdan100% (1)
- Test Chimie OrganicăDocument15 paginiTest Chimie OrganicăMirela DumitraÎncă nu există evaluări
- Curs Autocad PDFDocument124 paginiCurs Autocad PDFNicolae TabircaÎncă nu există evaluări
- Tipuri de Reactii in Chimia Organica - Reactia de AditieDocument8 paginiTipuri de Reactii in Chimia Organica - Reactia de AditieSteven CojoÎncă nu există evaluări
- AminoaciziDocument5 paginiAminoaciziIonutz BoteÎncă nu există evaluări
- Afirmaţii:: A. Scrieţi, Pe Foaia de Test, Termenul Din Paranteză Care Completează Corect UrmătoareleDocument3 paginiAfirmaţii:: A. Scrieţi, Pe Foaia de Test, Termenul Din Paranteză Care Completează Corect UrmătoareleNadejda CazaciocÎncă nu există evaluări
- Lipide ComplexeDocument3 paginiLipide ComplexeDORINA BOBOCÎncă nu există evaluări
- Chimie Organica - 2009 - Clasa A XII-ADocument23 paginiChimie Organica - 2009 - Clasa A XII-Amihaialex_butnaruÎncă nu există evaluări
- Teste Admitere Chimie Organica SIA 2015Document44 paginiTeste Admitere Chimie Organica SIA 2015Mitchell CarterÎncă nu există evaluări
- Cursuri de ChimieDocument34 paginiCursuri de ChimieCalin Catalin Cristian100% (1)
- Acizi Carboxilici X Cazan DidacticDocument4 paginiAcizi Carboxilici X Cazan DidacticSimona Turcanu100% (1)
- Manualul de Identitate Vizuală Al AFIR PDFDocument30 paginiManualul de Identitate Vizuală Al AFIR PDFAna MÎncă nu există evaluări
- Combinații Complexe Cu CobaltDocument7 paginiCombinații Complexe Cu CobaltIlenuca SacalasÎncă nu există evaluări
- Efectul InductivDocument2 paginiEfectul InductivDaniel AndronacheÎncă nu există evaluări
- Proiect Didactic Comb ComplexeDocument5 paginiProiect Didactic Comb ComplexeBadea IonelaÎncă nu există evaluări
- Curs 13Document25 paginiCurs 13Oana Andreea UrsicăÎncă nu există evaluări
- Hidratii de CarbonDocument57 paginiHidratii de CarbonpopaalexxÎncă nu există evaluări
- Carmen Pop - Curs 3Document48 paginiCarmen Pop - Curs 3Dana Elena LupuleasaÎncă nu există evaluări
- C6 Derivati Cu Azot Ai Acizilor CarboxiliciDocument24 paginiC6 Derivati Cu Azot Ai Acizilor CarboxiliciAlexandru Viorel100% (1)
- Plan Managerial Chimie BiologieDocument3 paginiPlan Managerial Chimie BiologieMonica DobrogeanuÎncă nu există evaluări
- Aplicatii Ale Chimiei in Viata Cotidiana 00935Document18 paginiAplicatii Ale Chimiei in Viata Cotidiana 00935Vitalie FilipÎncă nu există evaluări
- GLUCOZADocument18 paginiGLUCOZAOprea GabrielÎncă nu există evaluări
- Eseu MotivationalDocument2 paginiEseu MotivationalCornel DiaconuÎncă nu există evaluări
- CursDocument37 paginiCursRoxana AndreeaÎncă nu există evaluări
- Testex3e 61811012Document74 paginiTestex3e 61811012Dan Masson100% (1)
- Clasificarea Compusilor Organici Cu FunctiuniDocument1 paginăClasificarea Compusilor Organici Cu FunctiunistiinteÎncă nu există evaluări
- 7296Document13 pagini7296Catalina Dinu0% (1)
- 21 16 28 32partea A 7a - Nomenclatura Hidrocarburi PDFDocument23 pagini21 16 28 32partea A 7a - Nomenclatura Hidrocarburi PDFLili LiliÎncă nu există evaluări
- AlcaniDocument38 paginiAlcanime_bruxinha9231Încă nu există evaluări
- LectieDocument6 paginiLectieiugaÎncă nu există evaluări
- Energia Si Reactiile ChimiceDocument9 paginiEnergia Si Reactiile ChimiceVartolomeiDumitruÎncă nu există evaluări
- Amine Si NitroderivatiDocument13 paginiAmine Si NitroderivatiandreiÎncă nu există evaluări
- Curs 13-14Document37 paginiCurs 13-14Ileana Mariaa StoenescuÎncă nu există evaluări
- Model Subiect Olimpiada Chimie 2014.Document1 paginăModel Subiect Olimpiada Chimie 2014.Eusebiu TunsuÎncă nu există evaluări
- C8 Halo-Alcooli Fenoli CarbonilDocument20 paginiC8 Halo-Alcooli Fenoli CarbonilDenisa Ana GheorgheÎncă nu există evaluări
- CHIMIEDocument2 paginiCHIMIEmaraÎncă nu există evaluări
- Aminoalc Aminoac Peptide ProteineDocument85 paginiAminoalc Aminoac Peptide ProteineLupu AlexandruÎncă nu există evaluări
- Arene MonoDocument16 paginiArene MonoBubuOanaÎncă nu există evaluări
- AreneleDocument6 paginiAreneleNicolae Alexandru100% (1)
- Aromatice Curs 20dec 2011Document15 paginiAromatice Curs 20dec 2011andra_cool07Încă nu există evaluări
- Curs 9Document21 paginiCurs 9Ștefan MihăilăÎncă nu există evaluări
- Cap 2 5Document17 paginiCap 2 5Amalia IordachescuÎncă nu există evaluări
- Curs 05Document21 paginiCurs 05Marius Ciprian IlieÎncă nu există evaluări
- CURS 4 5 Chimie Anul II 2020 2021Document16 paginiCURS 4 5 Chimie Anul II 2020 2021Maria GabrielaÎncă nu există evaluări
- Roman PunteDocument28 paginiRoman PuntejicamihaiÎncă nu există evaluări
- Caracteristici Tehnice Difuzori DiscDocument4 paginiCaracteristici Tehnice Difuzori DiscjicamihaiÎncă nu există evaluări
- Grundfos Document3500Document15 paginiGrundfos Document3500jicamihaiÎncă nu există evaluări
- S2100300500462es289qnd511Document23 paginiS2100300500462es289qnd511jicamihaiÎncă nu există evaluări
- Grundfos DocumentDocument17 paginiGrundfos DocumentjicamihaiÎncă nu există evaluări
- Launch Pack 3225Document2 paginiLaunch Pack 3225jicamihaiÎncă nu există evaluări
- OPTDocument6 paginiOPTjicamihaiÎncă nu există evaluări
- Fisa Mijlocului FixDocument1 paginăFisa Mijlocului FixAnonymous ADLVfwepÎncă nu există evaluări
- Proiect Ieap PT Inv FR PDFDocument65 paginiProiect Ieap PT Inv FR PDFjicamihaiÎncă nu există evaluări
- Statie Tratare Apa CazanDocument80 paginiStatie Tratare Apa CazanjicamihaiÎncă nu există evaluări
- Regulamet 733 - 2014 PDFDocument54 paginiRegulamet 733 - 2014 PDFjicamihaiÎncă nu există evaluări
- Unitatea de Invatare NR 1 Tear ProiectDocument9 paginiUnitatea de Invatare NR 1 Tear ProiectjicamihaiÎncă nu există evaluări
- Manual de Procedura SM 19.2 v02Document361 paginiManual de Procedura SM 19.2 v02jicamihaiÎncă nu există evaluări
- Subiecte Procese HidrodinamiceDocument1 paginăSubiecte Procese HidrodinamicejicamihaiÎncă nu există evaluări
- Cap Conditii de RezistentaDocument13 paginiCap Conditii de RezistentajicamihaiÎncă nu există evaluări
- Regulament 2150 2002 PDFDocument54 paginiRegulament 2150 2002 PDFjicamihaiÎncă nu există evaluări
- Monitorizarea Poluarii Mediului III IPM FRDocument153 paginiMonitorizarea Poluarii Mediului III IPM FRjicamihaiÎncă nu există evaluări
- Tratarea Apelor RezidualeDocument12 paginiTratarea Apelor RezidualejicamihaiÎncă nu există evaluări
- Dimensionarea DecantoruluiDocument2 paginiDimensionarea DecantoruluijicamihaiÎncă nu există evaluări
- Ipb U.i.1Document20 paginiIpb U.i.1jicamihaiÎncă nu există evaluări
- Lucrarea de Laborator 4Document4 paginiLucrarea de Laborator 4jicamihaiÎncă nu există evaluări
- Directiva1999 - 31 Depoz DesDocument26 paginiDirectiva1999 - 31 Depoz DesOana ModoiÎncă nu există evaluări
- Portofoliu. ReciclareDocument15 paginiPortofoliu. ReciclareBatîru MihailÎncă nu există evaluări