Documente Academic
Documente Profesional
Documente Cultură
Enzime Digestive Hormoni Estrogeni Prezentare in Farmacii PDF
Încărcat de
Dorin Hagatis Dranca0 evaluări0% au considerat acest document util (0 voturi)
418 vizualizări0 paginieizime digestive
Titlu original
133256123 Enzime Digestive Hormoni Estrogeni Prezentare in Farmacii PDF
Drepturi de autor
© Attribution Non-Commercial (BY-NC)
Formate disponibile
PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documenteizime digestive
Drepturi de autor:
Attribution Non-Commercial (BY-NC)
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
418 vizualizări0 paginiEnzime Digestive Hormoni Estrogeni Prezentare in Farmacii PDF
Încărcat de
Dorin Hagatis Drancaeizime digestive
Drepturi de autor:
Attribution Non-Commercial (BY-NC)
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 0
1
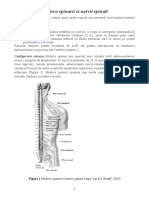
Prof. Dr. BBEANU ILEANA CRISTINA
BIOCHIMIE
Manual universitar pentru nvmntul la distan.
CRAIOVA, 2010
2
3
CUPRINS
Tema nr. 1 GLUCIDE........................................................................
1.1 Monoglucide: structur, proprieti, rol metabolic. .......................
1. 2. Oligoglucide naturale....................................................................
1.3 Poliglucide: clasificare, structur, rol biochimic............................
Rezumatul temei....................................................................................
Tema nr. 2 LIPIDE ...........................................................................
2.1 Acizi grasi......................................................................................
2.2 Lipide simple: clasificare, structur, rol biochimic........................
2.3 Lipide complexe..............................................................................
Rezumatul temei....................................................................................
Tema nr. 3 PROTIDE......................................................................
3.1. Aminoacizi; Structur general, clasificare, proprieti chimice..
3.2 Proteine; structur i proprieti.......................................................
3.3 Holoproteine i heteroproteine........................................................
Rezumatul temei....................................................................................
Tema nr. 4 ACIZI NUCLEICI..........................................................
4.1 Structura bazelor azotate. Structura nucleozidelor si nucleotidelor
4.2 Tipuri de acizi nucleici ..................................................................
Rezumatul temei....................................................................................
Tema nr. 5 VITAMINE ....................................................................
5. 1 Vitamine liposolubile ...................................................................
5.2 Vitamine hidrosolubile....................................................................
Rezumatul temei....................................................................................
Tema nr. 6 ENZIME..........................................................................
6.1 Generaliti despre enzime, structura i specificitatea
enzimelor..........................................................................................
6.2 Mecanisme generale de actiune i clasificarea
enzimelor..........................................................................................
Rezumatul temei....................................................................................
TEST RECAPITULATIV...................................................................
BIBLIOGRAFIE.................................................................................
5
5
10
11
14
15
15
17
21
25
26
26
31
35
38
39
39
44
47
48
49
52
56
57
57
61
63
64
67
4
5
Tema nr. 1
GLUCIDE
Uniti de nvare:
Monoglucide: structur, proprieti, rol metabolic.
Oligoglucide naturale
Poliglucide: clasificare, structur, rol biochimic
Obiectivele temei :
- Cunoaterea aspectelor biochimice privind structura, izomeria,
proprietile si rolul metabolic al glucidelor
- Studiul principalelor oligoglucide naturale, structura si rolul lor
biochimic
- Studiul structurii si al proprietilor fizico-chimice ale
poliglucidelor.
- Utilizarea de metode, tehnici i procedee specifice laboratorului de
biochimie pentru determinarea cantitativa si calitativa a glucidelor
Timpul alocat temei : 6 ore
Bibliografie recomandat :
1. Babeanu C., 2003, - Biochimie vegetal, Ed Universitaria, Craiova
2. Babeanu C., 2010, Biochimie. Manual universitar pentru nvmntul
la distan. Editura Universitaria, Craiova
3. Glodeanu E., 1997 - Biochimie Metabolica, Ed Gorjeanul
4. Marinescu G., Glodeanu E., 1995- Biochimie General, Ed.
Universitaria, Craiova
5. Neamu G., Cimpeanu Ghe., Socaciu C., 1993- Biochimie Vegetal, Ed.
Didactic i Pedagogic Bucureti.
1.1. Monoglucide: structur, proprieti, rol metabolic.
Clasificarea glucidelor
Dup reacia de hidroliz, glucidele se mpart n dou grupe: n oze
i ozide. Ozele se mai numesc i monoglucide. Ozidele sunt substane
formate din mai multe resturi de monoglucide prin eliminare de ap. Dup
structura molecular, ozidele se mpart, de asemenea, n dou grupe: n
oligoglucide i n poliglucide. Dup natura compuilor care intr n
constituia lor, ozidele se clasific n holozide i heterozide. Holozidele sunt
formate numai din resturi de monoglucide (aceleai sau diferite), iar
heterozidele conin n molecula lor pe lng resturi de monoglucide i alte
resturi de substane neglucidice (alcooli, fenoli, alcaloizi, pigmeni, etc)
numite agliconi.
Monoglucidele sunt compui cu funciuni mixte ce conin n
molecula lor o grupare carbonil i grupri hidroxil alcoolice. Dup natura
grupei carbonil se clasific n: aldoze i cetoze. Dup numrul atomilor de
carbon din molecul se clasific n: trioze, tetroze, pentoze, hexoze, etc.
Cele mai simple glucide sunt aldehida gliceric, ca reprezentant al
polihidroxi-aldehidelor i dihidroxi-acetona, ca reprezentant al polihidroxi-
cetonelor.
6
H C = O CH2 OH
| |
H C OH C = O
| |
CH2OH CH2 OH
aldehida gliceric dihidroxiacetona
Retinem: monoglucidele prezint mai multe tipuri de izomerie:
Izomeri datorit gruprii carbonilice; Acesti izomeri sunt determinai de
natura gruprii carbonilice. Se ntlnesc aldoze i cetoze.
Izomeri datorit activitii optice i stereoizomeria D i L ; Monoglucidele
avnd n molecula lor atomi de carbon asimetrici prezint izomerie optic.
Ele pot roti planul luminii polarizate spre dreapta (dextrogire) se noteaz cu
(+) sau pot roti planul luminii polarizate spre stnga, sunt levogire i se
noteaz cu (-). Din motive de sistematizare, glucidele s-au mprit n dou
serii D i L dup configuraia lor nrudit cu Dgliceraldehida sau L
gliceraldehida. Se consider c ozele care au configuraia atomului asimetric
cel mai ndeprtat de gruparea carbonil, identic cu cea a carbonului
asimetric din Dgliceraldehida aparin seriei D, iar cele avnd configuraia
ultimului atom de carbon asimetric cel mai ndeprtat de gruparea carbonil
din molecula identic cu cea a atomului de carbon asimetric din L
gliceraldehid, aparin seriei L. Izomerii optic activi au aceleai proprieti
cu excepia sensului de rotire a luminii polarizate. Amesctecul n pri egale,
din enentiomerul dextrogir i cel levogir al aceleiai substane se numete
amestec racemic i este optic inactiv prin compensaie
Izomeri datorit structurii moleculare. Monoglucidele prezint dou
structuri: aciclic i ciclic. Forma ciclic ia natere printr-o reacie de
semiacetalizare (adiie de alcool la gruparea carbonil) intra-molecular.
Semiacetalizarea are loc ntre grupa carbonil i hidroxilul alcoolic din
molecula respectiv, care conduce la formarea unui ciclu fr tensiune.
Astfel iau natere formele semiacetilice, heterociclice, cu ciclu de 6 atomi ce
deriv de la heterociclul piran, numite forme piranozice i formele cu ciclul
de 5 atomi ce deriv de la heterociclul furan, numite forme furanozice.
-D-glucofuranoza D-glucoza -D-glucopiranoza
D-fructofuranoza D-fructoza D-fructopiranoza
C
C
C
C
C
C
OH
H
OH
OH
OH
H
2
HO
H
H
H
2
O
H
2
H
H
HO
H
2
OH
OH
H
OH
C
C
C
C
C
C
H
2
H
H
HO
H
2
OH
OH
H
OH
C
C
C
C
C
C
O
O
O
C
C
C
C
C
C
H
OH
HO
H
H
H
2
C
C
C
C
C
C
H
OH
HO
H
H
H
2 H
2
H
H
HO
OH
OH
OH
H
OH
C
C
C
C
C
C
O
H
OH
OH
H
OH
O
H
H OH
H
OH
OH
H
7
D-glucofuranoza D-glucopiranoza
D-fructofuranoza D-fructopiranoza
Izomeri datorit hidroxilului semiacetalic. Dup poziia hidroxilului
semiacetalic din molecula monoglucidelor ciclice, se cunosc doi
stereoizomeri. Cnd hidroxilul semiacetalic se gsete n partea dreapt a
catenei de carbon (in partea de jos la formulele perspectivice) se obine
izomerul , iar cnd hidroxilul semiacetalic se gsete n partea stng (n
partea de sus la formulele perspectivice) se obine izomerul . Trecerea
izomerilor n izomeri se face prin intermediul formei carbonilice. Aceti
izomeri i se numesc anomeri.
-D-glucopiranoza -D-glucopiranoza
-D-fructofuranoza -D- fructofuranoza
Epimeria Epimeria const n modificarea configuraiei la un atom de carbon
asimetric. Se menioneaz ca structuri epimere: D-riboza i D-arabinoza; D-
glucoza, D-galactoza, D-manoza.
Observatie Monoglucidele prezint proprietile chimice caracteristice
gruprii funcionale carbonil si hidroxil.
Reacia de hidrogenare Aldozele i cetozele prin hidrogenare formeaz
polialcooli. Prin reducerea fructozei se obine un amestec de doi polioli
diastereoizomeri: D-sorbitol i D-manitol.
D-sorbitol D-fructoz D-manitol
C
C
C
C
C
C
OH
H
OH
OH
H
2
HO
H
H
H
2
C
C
C
C
C
C
OH
H
OH
OH
H
2
HO
H
H
H
2
O
H
2
H
H
HO
H
2
OH
OH
OH
H
OH
C
C
C
C
C
C
+2H +2H
OH
OH
H
OH
HO H
O
OH
H
OH H
OH
H
CH
2
OH
HO
H
O
H
OH CH
2
H
OH
H OH
OH
H
2 HO C
O
H
H
OH
H
HO
H
OH CH
2
H
HO
OH
H
HO
OH CH2
H
OH
H OH
H
OH
O
H
HO
OH CH2
H
OH
H OH
H
OH O
C HOH2
OH
OH H
OH
H
CH2OH
H
O C HOH2 OH
OH H
OH
H
CH2OH
H
O
8
Reacia de oxidare. Produii de oxidare ai monoglucidelor depind de natura
oxidantului. Folosind oxidani slabi, energici sau prin oxidare protejt
rezult: acizi aldonici, acizi zaharici i acizi uronici.
Oxidare blnd Oxidanii slabi n mediu alcalin oxideaz gruparea carbonil
obinndu-se acizi aldonici sau onici. Cetozele sunt stabile la oxidare.
acidul D-gluconic acidul D-galactonic acidul D-manonic
Oxidare energic; Oxidanii energici formeaz acizi zaharici.
Acid D-glucozaharic Acid galactozaharic Acid manozaharic
Oxidarea protejat. Dac funcia aldehidic este blocat (prin reacii de
esterificare sau condensare a hidroxilului semiacetalic), oxidarea are loc la
funcia alcool primar rezultnd acizi uronici.
Acidul glucuronic Acidul galacturonic Acidul manuronic
Reacii ale gruprilor hidroxil; In molecula monoglucidelor ciclice se pot
afla o grupare OH glicozidic i mai multe grupri OH alcoolice, fiecare
dintre aceste grupri avnd proprieti caracteristice.
Derivai ai monoglucidelor; ntre derivaii glucidelor se menioneaz
dezoxiglucidele, metilglucidele, tioglucidele i aminoglucidele. Se pot
considera derivai ai glucidelor i acizii uronici, produii de eterificare.
Dezoxiglucide
Sunt derivai ai monozaharidelor care au o grup OH nlocuit cu un atom
de hidrogen. Dintre acestea mai importante pentru organismele vii sunt: 2-
Dezoxi--riboza, 6-Dezoxi-Galactoza i 6-Dezoxi-L-Manoza.
Dezoxiriboza intr n structura ADN.
H HO
OH
H
OH
OH
C
C
C
C
C
C
H
OH
OH
HO
H
H
2
H
2
H
H
HO
OH
OH
H
C
C
C
C
C
C
H
2
H
H
HO
OH
OH
H
C
C
C
C
C
COOH OOH
OOH
H
OH
H HO
H HO
OH
H OH
C
C
C
C
C
C
H
OH
HO
H
H
H
HO
OH
OH
H
C
C
C
C
C
C
H
H
HO
OH
H
C
C
C
C
C
COOH OOH
OOH
H
OH
H HO
OOH OOH
OOH
H
HO
H
OH
H OH
H
OH
O
H
HO
H
OH
H
OH
H
OH
O O
OH
H
OH H
OH
H
HO
H
COOH COOH
COOH
H
H H
9
2-dezoxiriboza 6-dezoxi-L-galactoza 6-dezoxi-L-manoza
TEST DE EVALUARE
Ce compui rezult la oxidarea glucidelor ?
Rspuns:
Glucidele formeaz la oxidare blnd acizi aldonici, la oxidare protejat
acizi uronici si la oxidare energic acizi zaharici.
Ce tipuri de izomerie prezint glucidele ?
Rspuns
Exerciii.
Exemplu rezolvat:
1. Prin reducerea fructozei se obine:
a) D- glucoz
b) Acid aldonic
c) D-sorbitol i D-manitol
d) D- glucoz si D galactoz
e) -D-glucopiranoza
Rezolvare : c
De rezolvat:
2. Ce reprezint urmtoarea formul?
a) -D-fructofuranoza
b) -D- fructofuranoza
c) -D-glucopiranoza
d) -D- glucofuranoza
e) acid glucuronic
Rezolvare:
O
H OH
H
OH
H
H
2 HO C
H
H
HO
HO
C
H
H
C
OH C
OH
H
C
C
C
H
O H
H
3
H
HO
H
OH
H
O
C
C
C
OH
C
C
H
3
H
H
C
HO
10
1.2. Oligoglucide naturale
Oligozidele sunt produi de condensare a 2 pn la 8 molecule de oze. ntre
resturile de monozaharide este o legtur eteric numit legtura glicozidic.
Reinem: n funcie de felul grupei OH glicozidic care particip la reacie se
pot forma legturi i -glicozidice. Oligozidele se clasific dup numrul
resturilor de oze din molecul: dioligozide (dizaharide), trioligozide, etc.
Dup caracterul chimic se mpart n oligozide reductoare i nereductoare,
iar dup felul ozelor constituente n oligozaharide omogene i heterogene.
Diglucide Diglucidele sunt alctuite din dou resturi de monoglucide
identice sau diferite, unite prin legturi de tipul -; -; - i -
glicozidice. .
Diglucide reductoare
Celobioza; 4-[-D-glucopiranozil]-D-glucopiranoza este un diglucid format
din dou resturi de -glucopiranoz, legate 1-4 glicozidic. Frecvent se
ntlnete sub form policondensat (celuloz).
Maltoza 4-[-D-glucopiranozil]-D-glucopiranoza, este format din dou
molecule de D-glucoz unite prin legtura 14 glicozidic. Se gsete n
seminele germinale ale cerealelor, ca produi de hidroliz a amidonului.
Lactoza; 4-[-D-galactopiranozil]-D-glucopiranoza (zahrul din lapte) este
format din resturi de -D-galactopiranoz i de -D-glucopiranoz, legate
1-4 glicozidic. Se gsete n laptele mamiferelor
Diglucide nereductoare
Zaharoza Zaharoza 2-[ -D-glucopiranozil]--D-fructofuranoza,
este rspndit n multe organe vegetale (fructe, semine, frunze). Este un
dizaharid nereductor, constituit dintr-o molecul de -D-glucopiranoz i
una de -D-fructofuranoz unite printr-o legtur - 1-2 dicarbonilic.
H
HO
OH CH2
H
OH
H OH
H
O
H
HO
OH CH2
H
OH
H OH
H
O
H O
H
H
HO
OH CH2
H
OH
H OH
H
O
H
O
H
O H
OH H
OH
H
CH2OH
HO
H
H
HO
OH CH
2
H
OH
H OH
H
O
CH
2
H
O H
H
O H
OH
H
OH
HO
H
HO
O
H
OH CH2
OH
H OH
H2 HO C
H
HO
OH CH2
H
OH
H OH
H
O
O
H
H
11
TEST DE EVALUARE
1. Ce grupare funcional din molecul confer caracterul reductor
sau nereductor la oligoglucide.
Rspuns:
Caracterul reductor este dat de gruparea OH glicozidic liber. Dac
OH glicozidic este blocat in legtur eteric de tip glicozidic aceast
proprietate nu se manifest, molecula are caracter nereductor.
2. Ce compui rezult la hidroliza zaharozei?
Rspuns:
Exerciii.
Exemplu rezolvat:
1. Care dintre urmtoarele oligoglucide au caracter reductor ?
a) maltoza si lactoza,
b) maltoza si celobioza
c) zaharoza si celobioza
d) maltoz i zaharoz
e) lactoz i celobioz
Rezolvare : a, b, e
De rezolvat:
2. Ce substane se formeaz la hidroliza maltozei ?
a) 2 molecule de glucoz
b) 2 molecule de glucoz
c) o molecula de glucoz si o molecul de glucoz
d) 2 molecule de fructoz
e) o molecula de glucoz si o o molecul de fructoz
Rezolvare:
1.3 Poliglucide: clasificare, structur, rol biochimic
Poliglucidele sunt compui macromoleculari constituii dintr-un
numr mare de resturi de monoglucide legate ntre ele prin legturi
glicozidice. Au proprietatea de a hidroliza n mod treptat, formnd produi
intermediari cu un grad de polimerizare din ce n ce mai mic. Prin hidroliz
total se obin monoglucidele componente. Clasificarea poliglucidelor se
face dup structura lor n: homopoliglucide (poliglucide unitare sau
omogene) i heteropoliglucide (poliglucide mixte, complexe sau
neomogene).
Homopoliglucide
Amidonul este un poliglucid foarte rspndit n regnul vegetal, reprezentnd
o important surs de glucide alimentare pentru om i animale. Este
insolubil n ap rece iar n ap cald formeaz o dispersie coloidal care prin
rcire se transform n gel (coca).
12
Reinem: Amidonul nu este o substan unitar. Granulele sale sunt formate
din dou componente: amiloz i amilopectin care se gsesc uniform
repartizate. Aceste componente se deosebesc ntre ele att sub aspect
structural ct i prin proprietile fizice i chimice.
Amiloza este alctuit dintr-un numr mare de molecule de -D(+) glucoz,
unite ntre ele -glicozidic n poziiile 14. Are o structur liniar. Masa
molecular variaz n funcie de natura plantei, fiind cuprins ntre 10000 i
100000. Amiloza se dizolv uor n ap rece. Cu apa cald formeaz coca
caracteristic amidonului. Cu iodul d o coloraie albastru-nchis care
dispare la cald i reapare la rece.
rest terminal resturi interne rest terminal
amiloza (fragment macromolecular)
Amilopectina reprezint 70-80% din totalul amidonului avnd gradul
de polimerizare de 1000-6000 i greutatea molecular 200000-1000000. Are
o structur ramificat. Macromolecula amilopectinei prezint caten format
din resturi de -D(+) glucoz legate -glicozidic n poziiile 14 i conine
i cteva laterale formate din 25-30 resturi de -glucoz legate -glicozidic
de catena liniar n poziiile 16. Raportul dintre amiloz i amilopectin n
granule de amidon variaz n funcie de plant. Cu iodul amilopectina d o
coloraie rou-violet.
rest terminal resturi interne rest terminal
amilopectina (fragment macromolecular)
Observaie: Cea mai important reacie a amidonului este hidroliza.
Hidroliza, acid sau sub influenta enzimelor, se produce treptat, rezult
iniial produi macromoleculari nedefinii, dextrinele, apoi maltoza i n
final glucoza. Produii intermediari ai hidrolizei se pot pune n eviden prin
reacii de culoare. Hidroliza enzimatic a amidonului este realizat de -
amilaze si amilaze.
13
Celuloza
Celuloza este constituentul principal al pereilor celulelor vegetale.
Este cea mai rspndit substan organic n natur. Celuloza n general se
afl sub form de fibre amestecate cu alte substane ca: lignina,
hemicelulozele, materiile pectice, lipide, rini, taninuri, pigmeni, sruri
minerale i alte substane ncrustante.
Reinem: Celuloza este format prin policondensarea unui numr mare de
molecule de -glucoz, gradul de policondensare este diferit n funcie de
provenien. n macromolecula celulozei resturile de -glucoz sunt unite -
glicozidic n poziiile 1 4.
fragment din molecula de celuloz
Masa molecular a celulozei variaz mult cu proveniena sa. Hidroliza
enzimatic se produce sub aciunea celulazei, care duce la celobioz i apoi
celobiaza o hidrolizeaz pn la -glucoz.
Observaie: Cu toate c organismul uman nu posed enzimele necesare
hidrolizei, prezena celulozei n hran, n cantiti foarte mici este necesar,
avnd un rol important n peristaltismul i tranzitul intestinal.
TEST DE EVALUARE
1. Care este cea mai important reacie chimic a amidonului?
Rspuns
Cea mai important reacie a amidonului este hidroliza. Hidroliza, acid
sau sub influenta enzimelor, se produce treptat, rezult iniial produi
macromoleculari nedefinii, dextrinele, apoi maltoza i n final glucoza.
2. Ce compus rezult la hidroliza total a amidolului?
Rspuns
Exerciii.
Exemplu rezolvat:
1. Din ce molecule este format amiloza?
a) -glucoz unite -glicozidic n poziiile 14.
b) -glucoz unite -glicozidic n poziiile 14.
c) -glucoz unite -glicozidic n poziiile 16.
d) -glucoz unite -glicozidic n poziiile 16.
e) -glucoz i -glucoz unite glicozidic n poziiile 11.
Rezolvare : b
H
O
H
O
H
OH H
OH
H
CH
2OH
H
O
H
OH H
OH
H
CH2OH
H
H
OH CH2
H
OH
H OH
H
O
H
OH CH2
H
OH
H OH
H
O
H
O
H
O O
14
De rezolvat:
2. Din ce molecule este format celuloza?
a) -glucoz unite -glicozidic n poziiile 14.
b) -glucoz unite -glicozidic n poziiile 14.
c) -glucoz unite -glicozidic n poziiile 16.
d) -glucoz unite -glicozidic n poziiile 16.
e) -glucoz i -glucoz unite glicozidic n poziiile 11.
Rezolvare :
Rezumatul temei
Glucidele sunt biomolecule, universal rspndite n lumea vie. Cu
excepia unor derivai azotai glucidele sunt substane ternare formate din
carbon, hidrogen i oxigen. Dup reacia de hidroliz, glucidele se mpart n
dou grupe: oze i ozide. Ozele se mai numesc i monoglucide iar ozidele
sunt substane formate din mai multe molecule de monoglucide prin
eliminare de ap. Dup structura molecular, ozidele se mpart n dou
grupe: oligoglucide i poliglucide. Oligoglucidele sunt formate dintr-un
numr mic de resturi de monoglucide (2-8) iar poliglucidele sunt formate
dintr-un numr mare de resturi de monoglucide.
Ozele sau monoglucidele sunt compui cu funciuni mixte care
conin n molecula lor o grupare carbonil i grupri hidroxil alcoolice.
Monoglucidele prezint mai multe tipuri de izomerie. Se prezint n form
ciclic sau aciclic. Monoglucidele coninnd n molecul grupri carbonil
i hidroxil (alcoolic sau glicozidic) vor prezenta proprietile chimice
caracteristice acestor grupri funcionale. Dintre reaciile specifice gruprii
carbonil amintim: reaciile de hidrogenare, oxidare, condensare. Gruparea
carbonil din oze prezint i o serie de reacii prin care se poate identifica i
doza.
Oligozidele sunt produi de condensare a 2 pn la 8 molecule de
oze. n funcie de felul grupei OH glicozidic care particip la reacie se pot
forma legturi i -glicozidice. Dintre diglucidele reductoare cele mai
raspndite amintim celobioza, maltoza i lactoza iar dintre cele
nereductoare zaharoza.
Poliglucidele sunt compui macromoleculari constituii dintr-un
numr mare de resturi de monoglucide legate ntre ele prin legturi
glicozidice. Clasificarea poliglucidelor se face dup structura lor n:
homopoliglucide i heteropoliglucide. Amidonul este un poliglucid foarte
rspndit n regnul vegetal si din punct de vedere structural nu este o
substan unitar. Granulele sale sunt formate din dou componente:
amiloz i amilopectin. Aceste componente se deosebesc ntre ele att sub
aspect structural ct i prin proprietile fizice i chimice. Raportul dintre
amiloz i amilopectin n granule de amidon variaz n funcie de plant.
Celuloza este format prin policondensarea unui numr mare de
molecule de -glucoz, gradul de policondensare fiind diferit n funcie de
provenien. n macromolecula celulozei resturile de -glucoz sunt unite -
glicozidic n poziiile 1 4.
15
Tema nr. 2
LIPIDE
Uniti de nvare :
Acizi grasi.
Lipide simple: clasificare, structur, rol biochimic.
Lipide complexe: clasificare, structur, rol biochimic.
Obiectivele temei :
- Cunoaterea aspectelor biochimice privind clasificarea, structura i
proprietile lipidelor.
- Inelegerea conceptelor i analizarea corelatiei structur, proprieti, rol
biochimic.
- Cunoaterea principalilor reprezentani ai lipidelor simple si ai lipidelor
complexe.
- Dezbaterea metodelor si procedeelor de caracterizare calitativ i
cantitativ a lipidelor
Timpul alocat temei : 6 ore
Bibliografie recomandat :
1. Babeanu C., 2003, - Biochimie vegetal, Ed Universitaria, Craiova
2. Babeanu C., 2010, Biochimie. Manual universitar pentru nvmntul
la distan. Editura Universitaria, Craiova
3. Campbell P.N, Smith A. D., 2004- Biochimie ilustrat, Ed. Academiei
Romane, Bucuresti
4. Cristea Popa E., Popescu A., Truia E., Dinu V., 1991, Tratat de
biochimie medical, Ed Medical, Bucuresti,
5. Grban Z., 1999, Biochimie Tratat comprehensiv, vol I, ediia 2, Ed.
Didactic i Pedagogic Bucureti
6. Leninger A.L., 1987, Biochimie, vol. I, Ed. Tehnic, Bucureti
1.1. Acizi grai
Lipidele reprezint o clas de biomolecule organice, larg rspndite
n natur att n regnul vegetal ct i n cel animal. Ele se caracterizeaz prin
heterogenitatea structurii i proprietilor. Comun tuturor lipidelor le este
insolubilitatea n ap i solubilitatea n solveni organici.
Clasificarea general a lipidelor Natura chimic a lipidelor este foarte
variat. Lipidele se pot clasifica dup mai multe criterii. Astfel dup rolul
lor biologic se pot grupa n lipide de rezerv i lipide de constituie. n
funcie de compoziia chimic, lipidele se clasific n trei grupe: lipide
simple, lipide complexe, lipide derivate.
Acizi grai. Acizii organici care intr n constituia lipidelor se numesc n
mod curent acizi grai.
Reinem: Majoritatea acizilor grai din lipide sunt acizi monocarboxilici, cu
caten normal, cu numr par de atomi de carbon n molecul, saturai sau
nesaturai. Proprietile lipidelor sunt determinate de felul, lungimea i
configuraia catenei de carbon a acizilor grai, de felul i numrul legturilor
interatomice, de felul i numrul gruprilor funcionale. Majoritatea acizilor
grai din organismele vegetale se gsesc sub form de esteri i sruri. Puini
16
acizi grai se gsesc n celule i esuturi n stare liber, fiind disociai la pH-
ul optim al mediului. n plantele superioare predomin cantitativ acizii
lauric, miristic, palmitic i stearic. n uleiurile vegetale acizii grai saturai
se gsesc n cantitate mult mai redus, dect acizii grai nesaturai.
Principalii acizi grai saturai liniari, aciclici
Denumirea acidului gras Structura
Obinuit sistematic
Butiric n-butanoic COOH CH CH
2 2 3
) (
Caproic n-hexanoic COOH CH CH
4 2 3
) (
Caprilic n-octanoic COOH CH CH
6 2 3
) (
Caprinic n-decanoic COOH CH CH
8 2 3
) (
Lauric n-duodecanoic COOH CH CH
10 2 3
) (
Miristic n-tetradecanoic COOH CH CH
12 2 3
) (
Palmitic n-hexadecanoic COOH CH CH
14 2 3
) (
Stearic n-octodecanoic COOH CH CH
16 2 3
) (
Arachic n-eicosanoic COOH CH CH
18 2 3
) (
Acizii grai nesaturai sunt acizi monocarboxilici, cu caten liniar
care conin n molecula lor una sau mai multe duble legturi. Difer ntre ei
prin lungimea lanului i prin numrul i poziia dublelor legturi. Prezena
dublei legturi se noteaz cu litera greceasc care se aeaz dup atomul
de carbon de la care ncepe dubla legtur.
Observaie: Acizii grai nesaturai cu una sau mai multe duble
legturi ndeplinesc un rol foarte important n organismul animal. Cei mai
importani sunt acidul linoleic, linolenic arahidonic. In organismul uman i
animal aceti acizi care au un rol foarte important nu pot fi sintetizai n
cantitile necesare i se impune un aport alimetar, numindu-se acizi grai
eseniali. Acizii linoleic i linolenic nu sunt sintetizai n organismul
mamiferelor, ci numai n plante. Carena n acizii grai eseniali conduce la
unele tulburri cum sunt oprirea creterii, perturbarea proceselor de
circulaie, determin o fragilitate a capilarelor ct i alte dereglri.
TEST DE EVALUARE
1. Ce sunt acizii grai?
Rspuns
Acizii grai din lipide sunt acizi monocarboxilici, cu caten normal, cu
numr par de atomi de carbon n molecul, saturai sau nesaturai.
2. Ce sunt acizii grai eseniali?
Rspuns
17
Exerciii.
Exemplu rezolvat:
1. Care sunt cei mai importani acizi grai eseniali?
a) acid stearic si acid oleic
b) acid stearic si acid palmitic
c) acid oleic si acid palmitic
d) acid stearic, acid lauric si acid palmitic
e) acid linoleic si acid linolenic
Rezolvare : e
De rezolvat:
2. In structura acidului stearic intlnim:
a) 20 atomi de carbon in molecul si o dubl legtur
b) 16 atomi de carbon in molecul
c) 18 atomi de carbon in molecul
d) 18 atomi de carbon in molecul si o dubl legtur
e) 16 atomi de carbon in molecul si dou duble legturi
Rezolvare:
2.2 Lipide simple: clasificare, structur, rol biochimic.
Clasificare Lipidele simple se clasific n funcie de natura alcoolului din
structura lor n: gliceride, steride, ceride, etolide.
Gliceride (Acilgliceroli) sau grsimi neutre
Sunt lipidele cele mai abundente din natur. Sunt componente ale
grsimilor vegetale de rezerv din esuturi. Sunt esteri ai glicerolului
(propantriol) cu acizi grai, acilgliceroli. Dup numrul gruprilor alcoolice
din glicerol esterificate se mpart n monoacilgliceroli (monogliceride),
diacilgliceroli (digliceride) i triacilgliceroli (trigliceride). Mono i
digliceridele nu apar ns dect n cantitate foarte mic.
-monoacilglicerol -monoacilglicerol
-diacilglicerol '-diacilglicerol
CH
2
O
C
O
R
CH OH
CH
2
OH
OH CH
2
H C
O CH
2
H
O
C R
O
OH CH
2
H C O
C R
O
R
O
C O CH
CH
2
H C
R
O
C
O CH
2
O
C R
O HO
18
Triglicerid mixt
Grsimile de rezerv sunt alctuite aproape exclusiv din trigliceride.
Mono i digliceridele sunt intermediari n cursul sintezei i degradrii
trigliceridelor i se gsesc n esuturi n cantiti mici. Cele mai rspndite
sunt trigliceridele mixte. Trigliceridele mixte pot exista sub numeroase
forme de izomerie de poziie.
Observaie: n uleiurile vegetale predomin gliceridele cu un
coninut ridicat n acizi grai nesaturai. Proprietile fizice i chimice ale
gliceridelor sunt determinate n mare msur de natura acizilor grai din
compoziie. Starea de agregare a triacilglicerolilor depinde de compoziia n
acizi grai: cele bogate n acizi saturai inferiori sau acizi nesaturai sunt
lichide; cele cu un coninut ridicat n acizi saturai superiori sunt solide.
Grsimile naturale sunt amestecuri de diveri triacilgliceroli, ele nu au un
punct de fierbere sau de topire net. Gliceridele vegetale sunt solubile n eter
de petrol, eter, cloroform, sulfur de carbon i ali solveni organici.
Cea mai important reacie chimic a gliceridelor este hidroliza.
nclzite cu ap sub presiune trigliceridele sunt hidrolizate cu formare de
glicerol i acizi grai. Hidroliza are loc n etape, se formeaz mai nti o
diglicerid, apoi o monoglicerid i n final glicerol liber. Reacia este
catalizat de ctre acizi minerali tari, ca HCl, H
2
SO
4
i n special de acizi
sulfonici.
Hidroliza gliceridelor are loc i sub aciunea enzimelor specifice, numite
lipaze.
Reinem : Dac reacia de hidroliz are loc n mediu bazic, cu
hidroxizi alcalini Ca(OH)
2
, Mg(OH)
2
sau cu oxizi ai metalelor grele se
formeaz glicerol i sruri ale acizilor grai i se numete reacie de
saponificare. Srurile acizilor grai sunt numite spunuri. Pentru
caracterizarea calitativ i cantitativ a uleiurilor i grsimilor se utilizeaz
indicele de saponificare care reprezint numrul de mg KOH necesar
saponificrii unei cantiti de 1g ulei sau grsime. Gliceridele care conin n
molecul acizi grai nesaturai se pot halogena. Pentru caracterizarea unei
gliceride se folosete i "indicele de iod" care reprezint cantitatea de iod
adiionat de 100g ulei sau grsime, i care ne d indicaii privind gradul de
nesaturare al acizilor grai din constituia gliceridei.
Gliceridele care conin n molecul acizi grai nesaturai adiioneaz
i hidrogen n prezen de catalizatori. n urma hidrogenrii gliceridele
nesaturate de consisten uleuioas sau grsimile uor fuzibile sunt
transformate n grsimi consistente.
CH
2 O
CH
CH
2
CO
R
1
R
2
CO O
R
CO O
3
CH
2 O
CH
CH
2
CO
R
1
R
2
CO O
R
CO O
3
H
2
O
3
+
O
O
CH
2
CH
O
CH
2 H
H
H
R
1
COOH
R
2
COOH
R
3
COOH
+
19
n contact cu oxigenul i vaporii de ap din atmosfer, gliceridele
naturale sufer o serie de transformri nedorite, complexe care duc la
rncezirea acestora.
Steride
Steridele sunt esteri ai sterolilor cu acizii grai. Alcoolii din steride
sunt alcooli policiclici numii steroli. Ei sunt esterificai de obicei cu acizii
palmitic, stearic sau oleic. Sterolii sunt monoalcooli secundari care deriv de
la hidrocarbura numit steran.
Steran
Sterolii difer prin gruprile funcionale i catenele laterale grefate
pe nucleul steranic, prin prezena unor duble legturi i prin existena unui
numr foarte mare de stereoizomeri. n aceeai surs vegetal se gsesc de
obicei mai muli fitosteroli. Ei se gsesc n plante att n stare liber, ct i
sub form de fitosteride, glicozide cardiotonice, saponine, alcaloizi
steroidici, etc. Conin n molecul 29 atomi de carbon i prezint importan
biologic important n biosinteza hormonilor steroidici, a vitaminelor D,
acizilor colici, etc.
Sitosterol Stigmasterol
Colesterol
Retinem Dintre zoosteroli cel mai important din punct de vedere
biologic este colesterolul. Predomin n organismele animale dar a fost
identificat i n plante. El are un rol structural, este prezent n majoritatea
membranelor celulare i n acelai timp este precursorul tuturor celorlali
compui steroidici.
Ceride
Ceridele sunt esteri naturali ai acizilor grai cu monoalcooli
superiori. n regnul vegetal se gsesc sub form de cutin pe suprafaa
fructelor, frunzelor, florilor, constituind un nveli protector mpotriva
evaporrii apei, a cldurii i luminii excesive i ca un strat protector
mecanic. ndeprtarea cerurilor de pe suprafaa fructelor la recoltare
micoreaz foarte mult rezistena lor la pstrare. Cerurile animale se gsesc
att la mamifere ct i la insecte i psri. Ceara de albine este format din
ceroat de ceril i palmitatul de miricil (33%).
Formula general a unei ceride este
A B
C D
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
HO
C
2
H
5
C
2
H
5
HO
HO
20
Etolide
Etolidele sunt esteri intermoleculari ai unor hidroxiacizi superiori. Se gsesc
numai n regnul vegetal, predominant n cerurile unor conifere. n structura
unei etolide se gsesc dou resturi de molecule ale aceluiai hidroxiacid, dar
la formarea etolidelor particip i 3-5 molecule de hidroxiacid.
TEST DE EVALUARE
1. Ce rezult la hidroliza bazic a unei gliceride (triacilglicerol) ?
Rspuns
In urma hidrolizei bazice a unei gliceride se formeaz glicerin si sruri
ale acizilor grai (spunuri).
2. Care este cel mai rspndit si cel mai important sterol din
organismul animalelor superioare ?
Rspuns
Exerciii.
Exemplu rezolvat:
1. Care este starea de agregare a triacilglicerolilor in funcie de
compoziia in acizi grai?
a) cele in care predomin acizi saturati sunt solide
b) cele in care predomin acizi saturati sunt lichide
c) cele in care predomin acizi nesaturati sunt lichide
d) cele in care predomin acizi nesaturati sunt solide
e) cele in care predomin acizi saturati sunt att lichide ct si solide
Rezolvare : a, c
De rezolvat:
2. Care dintre urmtoarele reacii sunt date de trigliceride?
a) aditie de hidrogen daca in molecul exist resturi de acizi grai
nesaturai
b) reacie de hidroliz (bazic, acid sau enzimatic)
c) aditie de hidrogen daca in molecul exist resturi de acizi grai
saturai
d) reacie de oxidare
e) aditie de halogen daca in molecul exist resturi de acizi grai
saturai
Rezolvare :
CH
3
(CH
2)n
C
O
O CH
2
(CH
2)n1 CH
3
O CH
2 (CH
2)
n
C O
C O
)
n
(CH
2 CH
2
O
21
2.3 Lipide complexe
Lipidele complexe sunt esteri ai acizilor grai la constituia crora
mai particip pe lng alcooli fr azot i aminoalcooli, acidul fosforic,
serina, un rest de acid sulfuric, iar n unele cazuri inozitolul, una sau mai
multe monolucide. Acidul fosforic fiind un component al marii majoriti a
lipidelor vegetale complexe ele sunt denumite i fosfatide sau fosfolipide.
Proporia de lipide complexe n regnul vegetal este relativ mic,
predominnd n regnul animal. Lipidele complexe se gsesc n constituia
membranelor cloroplastelor, n mitocondrii, reticul endoplasmatic, n
membrane celulare. Ele nu se depun sub form de lipide de rezerv. n ap
formeaz emulsii i sunt solubile n aceton, deosebindu-se n acest fel de
lipidele simple. n organismele vii lipidele complexe mai apar asociate cu
proteinele formnd lipoprotein, substane cu rol fiziologic important.
n funcie de natura alcoolului din structura lor se clasific n:
glicerofosfolipide i sfingolipide.
Lipidele complexe care conin n molecul un rest de acid fosforic au
fost denumite i fosfatide sau fosfolipide iar cele care nu conin acid fosforic
n molecul au fost denumite glicolipide.
Fosfatide sau fosfolipide
Majoritatea fosfatidelor vegetale sunt esteri ai glicerolului cu acizi
grai i cu acid fosforic; la rndul su acidul fosforic este esterificat cu un
aminoalcool, un aminoacid sau un inozitol.
Reinem: Fosfatidele corespund deci urmtoarelor formule generale,
care se deosebesc prin poziia acidului fosforic n molecul.
Fosfatida Fosfatida
n care R i R reprezint resturi de acizi grai saturai sau nesaturai, iar R
restul de aminoalcool, aminoacid sau inozitol. Toate fosfatidele vegetale
sunt optic active.
Principalii aminoalcooli care intr n compoziia fosfatidelor
vegetale sunt: colamina, colina, sfingozina i fitosfingozina.
Glicerofosfolipide
Glicerofosfolipidele la hidroliz formeaz glicerin, dou molecule
de acid gras, acid fosforic, aminoalcool sau inozitol. n cadrul
glicerofosfolipidelor se include: acizii fosfatidici, etanolaminfosfatide
(cefaline), colinfosfatide (lecitine), serinfosfatide, inozitolfosfatide,
acetalfosfatide (plasmologenii) i fosfatidiglicerolii. Glicerofosfolipidele
sunt cele mai rspndite lipide complexe, se gsesc n plante n cantitate
mare n cloroplaste i semine.
CH
2
OCOR
CHOCOR"
CH
2
OP
OH
OR"
O CH
2
OCOR
O
OR"
OH
CHOP
CH
2
OCOR
22
Acizii fosfatidici
Acizii fosfatidici sunt cele mai simple lipide complexe i sunt
substana de baz a glicerofosfolipidelor. Acizii fosfatidici conin n
molecula lor glicerin esterificat cu dou molecule de acizi grai, cea de-a
treia grup hidroxil a glicerinei fiind esterificat cu acid fosforic.
CH2 O CO R1
|
R2 OC O CH O
|
CH2 O P OH
|
OH
Acid fosfatidic
Observaie: S-a dovedit c acizii fosfatidici reprezint produi intermediari
n sinteza unor fosfatide mai complexe, cum sunt lecitinele, sau produi de
hidroliz enzimatic ai fosfatidelor complexe. n urma hidrolizei acizilor
fosfatidici s-au gsit urmtorii acizi grai: lauric, miristic, palmitic, stearic,
oleic, linolic i linolenic. Acizii fosfatidici naturali fac parte din seria L.
Colinfosfatidele (lecitinele)
Colinfosfatidele (lecitinele) sunt cele mai rspndite lipide complexe. n
plante se gsesc n embrionii seminelor de leguminoase i de cereale, n
proporie de 2%.
Reinem: Sunt formate dintr-un rest de acid fosfatidic legat de
aminoalcoolul colin OH CH N CH CH OH ] ) ( [
3 3 2 2
+
Lecitinele sunt
substane cu caracter bipolar
CH2 O CO R
|
R - OC O CH O
|
CH2 O P -
+
OH CH N CH CH O ] ) (
3 3 2 2
|
OH
Fosfatil colina
CH2 O CO R
|
R - OC O CH O
|
CH2 O P -
3 3 2 2
) (CH N CH CH O
+
|
O
Structura amfionic a fosfatidil colinei
Lecitinele se prezint ca o mas ceroas, unsuroas, de culoare
glbuie sau, n stare pur, brun. Lecitinele perfect pure sunt cristalizabile.
n solveni organici, cu excepia acetonei, lecitinele sunt solubile. Ele se
solv de asemenea n grsimi. Cu ap puin se gonfleaz, cu ap mult dau
emulsii stabile.
23
Observaie: Comportarea fa de ap i grsimi se explic prin
caracterul hidrofil al componentului fosforic i caracterul hidrofob al
restului moleculei.
Lizolecitine - Prin lizolecitine se neleg lecitine, cu puternic aciune
hemolitic, care se obin prin hidroliza enzimatic parial a lecitinelor,
cauzat de lecitinaza A.
CH
2
OCOR
|
CHOH
| O
CH
2
OP OCH
2
CH
2
N(CH
3
)
3
||
O
Lizolecitin
Etanolaminfosfatide (Cefaline)
Etanolaminfosfatidele sunt esteri ai acizilor fosfatidici cu restul de
acid fosforic esterificat cu colamin HO-CH
2
CH
2
NH
2
(etanolamin). Ele
nsoesc lecitinele n organismele vegetale i animale.
CH2 O CO R
|
R - OC O C - H O
|
CH2 O P -
2 2 2
NH CH CH O
|
OH Etanolaminfosfatida
CH2 O CO R
|
R - OC O CH O
|
CH2 O P -
+
3 2 2
NH CH CH O
|
O
Structura amfiionica a cefalinei
S-au identificat i n germenii de gru, semine de floarea soarelui,
in, lupin, soia. ntre proprietile lor se remarc caracterul amfiionic al
acestora molecula devenind bipolar. Cefalinele prezint proprieti fizico-
chimice asemntoare lecitinelor iar rolul lor n organism este asemntor
lecitinelor.
Serinfosfatide
Serinfosfatide sunt compui cu molecula format din acid fosfatidic n care
restul de acid fosforic este esterificat cu serin. Similar cefalinelor i
lecitinelor, esterificarea se poate face n poziia sau .
24
CH
2
O CO R
|
R - OC O CH O
|
CH
2
O P O CH
2
CH COOH
| |
O + NH
3
Serinofosfatida
Serinfosfatidele nsoesc celelalte fosfatide, de exemplu cele din
arachide i din soia. Proprietile fizico-chimice sunt similare cu ale
celorlalte lipide complexe.
Inozitolfosfatide
Inozitolfosfatidele sunt lipide complexe n structura crora se afl
resturi de acid fosfatidic i inozitol. Aceste lipide complexe se afl n
cantiti mici n diferite esuturi, n cantiti mai mari gsindu-se n lipide
din creier i muchi. Fosfatide vegetale coninnd inozitol au fost gsite n
fasolea soia, germenii de gru, arahide, pere, mazre, fasole, boabe de
porumb, bacterii acidorezistente.
Sfingolipidele
Sfingolipidele sunt lipide complexe n constituia crora intr un
aminoalcool, un acid gras, acid fosforic, baz azotat sau un glucid.
Aminoalcoolii pot fi sfingozina sau derivai ai acestuia: sfinganina
(dihidrosfingozina) sau fitosfingozina (4hidroxisfingozina). n sfingolipide
acidul gras este legat amidic la grupa NH
2
- a sfingozinei.
TEST DE EVALUARE
1. Ce sunt din punct de vedere structural acizii fosfatidici?
Rspuns:
Acizii fosfatidici conin n molecula lor glicerin esterificat cu dou
molecule de acizi grai, cea de-a treia grup hidroxil a glicerinei fiind
esterificat cu acid fosforic.
2. Care este aminoalcoolul din structura unei lecitine?
Rspuns:
Exerciii.
Exemplu rezolvat:
1. Prin ce tip de legtur este legat acidul gras in structura unei
sfingozine?
a) legtur eteric de tip alcoolic
b legtur eteric de tip glicozidic
c) legtur amidic
d) legtur esteric
e) legtur de hidrogen
Rezolvare: c
25
De rezolvat:
2. Care este aminoalcoolul din structura unei cefaline?
a) colin
b) etanolamin
c) serin
d) inozitol
e) sfingozin
Rezolvare:
Rezumatul temei
Lipidele reprezint o clas de biomolecule larg rspndite n natur
caracterizate prin heterogenitatea structurii i proprietilor. Sunt insolubile
n ap i solubile n solveni organici. n plante, lipidele se gsesc att libere,
predominat ca substane de rezerv ct i asociate cu proteinele i glucidele
sub forma unor compui numii lipoproteine respectiv lipoglucide, care se
gsesc n cantitate mai mare n constitueni celulari cu activitate fiziologic
intens. Lipidele se pot clasifica dup mai multe criterii. Dup rolul lor
biologic se pot grupa n lipide de rezerv i lipide de constituie. n funcie
de compoziia chimic, lipidele se clasific n: lipide simple, lipide
complexe, lipide derivate. La rndul lor lipidele simple se clasific n funcie
de natura alcoolului din structura lor n: gliceride, steride, ceride, etolide.
Lipidele complexe se clasific n: glicerofosfolipide i sfingolipide.
Acizii grai sunt acizi monocarboxilici, cu caten normal, cu numr
par de atomi de carbon n molecul, saturai sau nesaturai. Majoritatea
acizilor grai din organismele vegetale se gsesc sub form de esteri i
sruri. Acizii grai nesaturai ndeplinesc un rol foarte important n
organismul animal, numindu-se acizi grai eseniali (nu pot fi sintetizai de
organismul animal). Cei mai importani sunt acidul linoleic, linolenic
arahidonic.
Gliceridele sunt esteri ai glicerolului cu acizi grai, steridele esteri ai
sterolilor cu acizii grai, ceridele esteri naturali ai acizilor grai cu
monoalcooli superiori iar etolidele sunt esteri intermoleculari ai unor
hidroxiacizi superiori.
Lipidele complexe sunt esteri ai acizilor grai la constituia crora
mai particip pe lng alcooli fr azot i aminoalcooli, acidul fosforic,
serina, un rest de acid sulfuric, iar n unele cazuri inozitolul, una sau mai
multe monoglucide. Avnd acid fosforic in molecul lipidele vegetale
complexe sunt denumite i fosfatide sau fosfolipide. n funcie de natura
alcoolului din structura lor se clasific n: glicerofosfolipide i sfingolipide.
Acizii fosfatidici sunt cele mai simple lipide complexe i sunt
substana de baz a glicerofosfolipidelor. Acizii fosfatidici conin n
molecula lor glicerin esterificat cu dou molecule de acizi grai si cu un
rest de acid fosforic. Cele mai rspndite lipide complexe sunt lecitinele i
cefalinele. Ele sunt formate dintr-un rest de acid fosfatidic legat de
aminoalcoolul colin respectiv etanolamin.
26
Tema nr. 3
PROTIDE
Uniti de nvare :
Aminoacizi; Structur general, clasificare, proprieti
chimice. Peptide.
Proteine; structur i proprieti
Holoproteine i heteroproteine.
Obiectivele temei :
- Cunoaterea aspectelor biochimice privind structura proteinelor
- Inelegerea conceptelor i analizarea corelatiei structur, proprieti, rol
biochimic.
- Dezbaterea metodelor si procedeelor de separare, identificare i dozare a
proteinelor
Timpul alocat temei : 6 ore
Bibliografie recomandat :
1. Babeanu C., 2003, - Biochimie vegetal, Ed Universitaria, Craiova
2. Babeanu C., 2010, Biochimie. Manual universitar pentru nvmntul
la distan. Editura Universitaria, Craiova
3. Campbell P.N, Smith A. D., 2004- Biochimie ilustrat, Ed. Academiei
Romane, Bucuresti
5. Dinu V., Trutia E., Cristea Popa E., Popescu A., 2002, Biochimie
medical, Mic tratat, Ed Medical, Bucuresti,
6. Garban Z. 1981, Tratat elementar de biochimie, Ed Mirton Timisoara
3.1. Aminoacizi; Structur general, clasificare, proprieti chimice.
Consideraii generale i clasificare
Aminoacizii sunt unitile constituente ale proteinelor. Dei se cunoate un
numr mare de aminoacizi naturali, exist doar 20 aminoacizi prezeni n
toate organismele vii, de la cele mai simple pn la om. Alturi de aceti 20
aminoacizi fundamentali, n proteine se mai ntlnesc ali civa, care rezult
de fapt prin modificri chimice ale acestora dup ncorporarea n lanurile
polipeptidice.
Aminoacizii naturali au formula :
Toi aminoacizii care intr n structura proteinelor sunt -
aminoacizi, cu excepia prolinei care are o grupare aminic secundar.
Diversitatea aminoacizilor naturali este dat de natura radicalului R.
Clasificarea aminoacizilor naturali se face dup mai multe criterii: Dup
criteriul biologic aminoacizii naturali se clasific n: a) aminoacizi proteici
i neproteici ; b) aminoacizi eseniali i neeseniali
R
CH
COOH
NH
2
27
Observaie: Nu toi aminoacizii proteici sunt sintetizai de ctre organismul
animal. Dintre aminoacizii proteici, 8 aminoacizi sunt absolut necesari
organismului animal i uman, dar ei nu pot fi sintetizai de aceste
organisme, sunt sintetizate doar n organismele vegetale. Aminoacizii
eseniali sunt: valina, leucina, izoleucina, lisina, metionina, treonina,
fenilalanina i triptofanul.
Reinem: Dup structura chimic aminoacizii pot fi clasificai astfel:
Aminoacizi monoaminomonocarboxilici alifatici
Acid aminoacetic Acid -aminopropionic
Glicocol (glicina) (Gly) Alanina (Ala)
Acid -aminoizovalerianic Acid -aminoizocapronic
Valina (Val) Leucina (leu)
Acid -amino- metil- valerianic (Izoleucina - Ile)
Aminoacizi monoaminodicarboxilici
Acidul aspartic i acidul glutamic sunt aminoacizii iar asparagina i
glutamina sunt amidele lor.
Acid aminosuccinic Acid aminoglutaric
Acid aspartic (Asp) Acid glutamic (Glu)
Asparagina (Asn) Glutamina (Glu)
Aminoacizi diaminomonocarboxilici:
Acid , -diaminovalerianic Acid , -diaminocapronic
Ornitina Lisina (Lis)
Acid -amino- -guanidivalerianic guanidin
Arginina (Arg)
Arginina conine o grupare guanidil derivat de la guanidin.
CH
3
CH COOH
NH
2
NH
2
COOH CH CH
2
CH CH
3
CH
3
CH COOH
NH
2
CH
2
HOOC
NH
2
COOH CH
2
CH COOH
NH
2
CH COOH
NH
2
CH CH
3
CH
3
CH COOH
NH
2
CH COOH
NH
2
CH
3
CH
CH
3
CH
2
CH COOH
NH
2
CH
2
HOOC
CH
2
CH COOH
NH
2
CH
2
H
2
NOC
CH
2
NH
2
COOH CH CH
2
H
2
NOC
CH (CH
2
CH COOH
NH
2
)
2
2
H
2
N
)
3
NH
2
COOH CH
(CH
2
HN
C HN
NH
2
CH (CH
2
CH COOH
NH
2
)
3
2
H
2
N
HN
C NH
2
NH
2
28
Aminoacizi cu alte grupe functionale:
Acid -amino--hidroxipropionic Acid -amino--hidroxibutiric
Serina (Ser) Treonina (Thr)
Acid -amino--tiometilbutiric Acid -amino-- tiopropionic
Metionina (Met) Cisteina (Cys)
Cistina Acid -amino-imidazolil propionic
Histidina (Hys)
Acid -amino--fenil propionic Acid -amino-(parafenil)propionic
Fenilalanina (Phe) Tirozina (Tyr)
Acid pirolidin -2-carboxilic Acid 4-hidroxipirolidin -2-carboxilic
Prolina (Pro) Hidroxiprolina (Pro-OH)
Acid -amino--indolil propionic
Triptofan (Trp)
Proprieti chimice ale aminoacizilor
Aminoacizii au caracter amfoter. Avnd n molecul o grupare -NH
2
bazic
i o grupare -COOH acid ntre acestea poate avea loc transferul de protoni:
Ion bipolar (amfion)
S
CH
2
CH
2
CH COOH
NH
2
CH
3
OH
CH
NH
2
COOH CH
NH
2
COOH CH
2
CH
3
CH COOH
NH
2
CH COOH
NH
2
CH
OH
SH
CH
NH
2
COOH CH
NH
2
COOH CH
2
CH
2
S S CH
2
CH CH NH
2
COOH COOH
NH
2
CH
2
CH COOH
NH
2
N
N
H
NH
2
COOH CH CH
2
R
CH
COOH
NH
2
NH
3
COO
CH
R
+
-
CH
2
CH COOH
NH
2
OH
N
CH
2
CH COOH
H
2
C
H
2
C
H
N
CH
2
CH COOH H
2
C
H
HC HO
H
N NH
2
COOH CH CH
2
29
La pH-ul fiziologic, ca i n stare cristalin, aminoacizii prezint o astfel de
structur amfiionic. Datorit caracterului lor amfoter, aminoacizii se
comport n mediu acid ca baze iar n mediu bazic ca acizi.
Observaie: Proprietatea aminoacizilor de a reaciona att cu ionii
hidroxil ct i cu ionii de hidroniu permite utilizarea lor ca substane
tampon. Punctul izoionic se definete ca PH-ul pentru care sarcina electric
net a moleculei de aminoacizi este nul. n funcie de sarcina electric net
la un anumit pH, aminoacizii se deplaseaz sub influena unui cmp electric,
manifest proprieti electroforetice. Punctul izoelectric (pHi) este pH-ul la
care aminoacizii nu migreaz ntr-un cmp electric, ei se afl disociai ca
anioni i cationi n proporii egale. Solubilitatea lor este redus la acest pHi
datorit atraciei electrostatice dintre anionii i cationii existeni.
Reinem: Aminoacizii avnd n molecula lor gruparea -NH
2
i
gruparea -COOH prezint proprietile chimice ale acestor grupri
funcionale, precum i proprieti chimice specifice, datorate prezenei
radicalului R de la carbonul C.
Reacii chimice caracteristice gruprii carboxil:
1) Ca i acizii organici, aminoacizii formeaz sruri cu bazele:
2) Aminoacizii reacioneaz cu alcoolii formnd esteri.
3) Aminoacizii reacioneaz cu pentaclorura de fosfor. Clorurile
aminoacizilor sunt deosebit de reactive i sunt folosite n sinteza
peptidelor.
4) Prin decarboxilare aminoacizii formeaz amine, multe dintre ele au
proprieti fiziologice i farmacologice importante. Decarboxilarea are lor n
organism sub aciunea unor enzime specifice (decarboxilaze) i aminele
obinute se numesc amine biogene.
4) Prin reducere energic aminoacizii se transform n aminoalcooli
Reacii chimice caracteristice gruprii amino
1) Aminoacizii formeaz sruri cu acizii minerali ca i aminele.
2) Aminoacizii se alchileaz, de exemplu prin metilare, n prezena iodurii
sau sulfatului de metil, formnd sruri cuaternare de amoniu.
3) Prin acilare rezult N-acilderivai. De exemplu, prin tratarea glicocolului
cu clorura de benzoil, n mediu alcalin, se formeaz acidul hipuric. Acidul
benzoic este un produs toxic, este cuplat sub form de acid hipuric i astfel
este eliminat pe cale renal.
Reacii datorate catenelor laterale
n funcie de natura catenelor laterale unii aminoacizi reacioneaz cu
anumii reactivi, formnd compui specifici (colorai sau precipitate) care
servesc la identificarea lor.
R
C
COO
NH
3
COO
C
R
+
+ H
3
O
+
H
H
H
+
H
2
O
+
NH
3
-
R
C
COO
NH
2
COO
C
R
+
H H
+
H
2
O
+
NH
3
-
HO
-
-
30
Reacii datorate ambelor grupri funcionale
Aminoacizii particip la reacii de condensare i policondensare formnd
peptide i protide. Peptidele sunt produi de policondensare a dou sau mai
multe molecule de aminoacizi. Resturile de aminoacizi sunt legate prin
legtur amidic, numit legtur peptidic. Sunt substane naturale care se
gsesc n plante n stare liber sau apar ca intermediari la hidroliza
proteinelor. Structura i funciile peptidelor sunt determinate de secvena de
aminoacizi din molecul.
Peptidele se clasific n:oligopeptide i polipeptide
Oligopeptidele se formeaz din condensarea a 2 pn la 10 molecule de
aminoacizi (dipeptide, tripeptide, etc.) iar polipeptidele prin condensarea
unui numr mai mare de 10 molecule de aminoacizi.
Din dou molecule de aminoacizi se formeaz o dipeptid:
Datorit posibilitilor de legare a acelorai aminoacizi n secvene diferite,
peptidele pot prezenta fenomenul de izomerie de structur. n diferitele
organe vegetale se gsesc peptide i polipeptide, care indeplinesc anumite
roluri fiziologice sau constituie produi intermediari n anabolismul i
catabolismul proteidelor. Una din primele peptide naturale cunoscut,
izolat din drojdia de bere este glutationul. Glutationul se gsete i n
numeroase organe vegetale, ndeosebi n semine, unde cantitatea lui
sporete n cursul ncolirii. Glutationul este o tripeptid format din acid
glutamic, cistein i glicocol.
Glutamil Cistenil Glicocol
n celule glutationul se poate gsi sub form redus G-SH, ca tiol ct i sub
form oxidat, ca disulfur G-S-S-G. Trecerea glutationului din forma
redus n forma oxidat este un proces reversibil i constituie unul din cele
mai importante siteme de oxidoreducere din celule.
R
CH COOH
NH
2
+
NH
2
COOH CH
R
NH
2
CO CH R
COOH CH NH
R
-
H
2
O
HOOC CH (CH
2
)
2
CO NH
CH CO NH
CH
2 COOH
NH
2 CH
2
SH
G SH G S S
G
H
H
-2
+2
31
TEST DE EVALUARE
1. Cum se explic comportarea ca soluii tampon a soluiilor de
aminoacizi?
Rspuns:
In soluie apoas aminoacizii se gsesc sub form de amfiioni i prezint
caracter amfoter, comportndu-se ca solutii tampon (in mediu acid se
comport ca baze iar in mediu bazic se comport ca acizi)
2. Cum se clasific aminoacizii naturali dup criteriul biologic?
Rspuns:
Exerciii.
Exemplu rezolvat:
1. Ce fel de reacii chimice prezint aminoacizii?
a) reacii de alchilare
b) reactii de acilare
c) reacii de hidroliz
d) reacii de condensare
e) reacii de decarboxilare
Rezolvare : a, b, d, e
De rezolvat:
2. Care dintre urmtoarele reacii chimice sunt datorate gruprii
amino?
a) reactia de hidroliz
b) reactia de esterificare
c) reactia de decarboxilare
d) reactia cu ninhidrina
e) reactia de acilare
Rezolvare :
3.2. Proteine; Structur si proprieti
Proteinele sunt macromolecule care exist ntr-o varietate foarte
mare i care au o structur deosebit de complex. Au o structur
polipeptidic care asigur proteinelor diversitate molecular i specificitate.
Structura proteinelor.
Cu ajutorul celor 20 aminoacizi proteici se pot obine combinaii
multiple, deosebite prin numrul i secvena resturilor de aminoacizi.
Lanurile polipeptidice, unidimensionale i flexibile, se aeaz spontan n
arhitecturi moleculare, edificii cu trei dimensiuni, cu forme caracteristice
pentru o anumit secven de aminoacizi.
Reinem: Complexitatea proteinelor a impus introducerea mai multor trepte
de organizare structural denumite structur primar, secundar, teriar i
cuaternar astfel c structura de ansamblu a unei proteine este dat de
existena i interaciunea acestor structuri. ntre aceste nivele de organizare
32
structural exist interdependen i mpreun determin particularitile
structurale i proprietile funcionale specifice fiecrei proteine.
Structura primar
Structura primar este dat de numrul, felul i secvena resturilor
aminoacizilor din molecul. n legtura peptidic exist efectul de rezonan
care conduce la un caracter parial de dubl legtur pentru legtura dintre
azot i carbon.
Acest caracter se explic prin urmtoarele structuri limit de
rezonan ale legturii peptidice. Ca o consecin a caracterului parial de
dubl legtur al legturii peptidice este apariia izomeriei cis-trans. n
proteine, ca i n peptide catena este n zig-zag, atomii implicai n legtura
peptidic sunt coplanari, iar resturile aminoacizilor R sunt aezai alternativ
deasupra i dedesuptul planului legturilor peptidice.
Structura secundar
Structura secundar definete orientarea spaial a lanului
polipeptidic. Pauling i Corey (1951) au postulat dou structuri secundare
pentru lanurile polipeptidice: modelul elicoidal (-helix) i structura
(planuri pliate). O structur elicoidal distinct de cea descris de Pauling
este ntlnit la colagen, care are o compoziie aminoacidic particular.
Modelul -helix. Acest model prevede dobndirea de ctre o caten
polipeptidic a unei conformaii elicoidale numit -helix, rezultat i
stabilizat prin legturi de hidrogen intracatenare. Legturile de hidrogen
sunt dispuse aproape perfect paralel cu axa -helixului. Radicalii R ai
aminoacizilor constitueni ai -helixului sunt aezai alternativ, deasupra i
sub planurile legturii peptidice i proiectate radial n jurul elicei.
Figura 1. Structura secundar de helice a unui lan polipeptidic
Modelul planurilor pliate (foaie pliat) i acest model reprezint o
conformaie ordonat i stabilizat prin legturi de hidrogen dar
intercatenare, dispuse aproape perpendicular pe axa catenei polipeptidice.
C N
H
R
O O
R
H
N C
+
-
C N C N C N
C
H
O
H
C
O
H
C
H
R
1
R
2
H
H
R
3
33
Lanurile polipeptidice se aeaz n foi. Structura secundar n foaie pliat
este ntlnit n proporie de aproape 100% n proteina din mtase, fibroina.
Figura 2. Structurain foaie pliat
Structura teriar
Aceast structur reprezint un stadiu avansat de organizare spaial a
proteinelor i const n replierea catenelor polipeptidice elicoidale asupra lor
nile. Catena polipeptidic sufer o nfurare spontan, avnd loc o
repliere ordonat combinat cu plieri care nu sunt regulat ordonate n spaiu.
Structura teriar se constituie pe baza unor legiti i este meninut prin
stabilirea unor legturi i interaciuni diferite. Aceste legturi sunt de
urmtoarele tipuri:
- Legturi covalente disulfurice-S-S-, sunt legturi care se stabilesc ntre
dou resturi de cistein, la nivelul gruprilor tiolice -SH
- Legturi ionice - aceste legturi se stabilesc ntre grupri polare de sens
contrar.
- Legturi de hidrogen-
- Interaciuni dipol-dipol.
- Fore Van der Waals i interaciuni hidrofobe. Acestea sunt stabilite
ntre radicalii hidrocarbonai ai aminoacizilor.
Structura teriar prezint un grad mare de labilitate n raport cu diferii
factori fizici i chimici, desfacerea legturilor implicate n organizarea
structurii teriare determin denaturarea proteinelor, proces nsoit de regul
de pierderea proprietilor biologice.
Structura cuaternar
Structura cuaternar a unei proteine oligomere indic modul n care
lanurile polipeptidice individuale, se asociaz, se asambleaz pentru a
realiza structura proteinei date, structura sa funcional. Structura cuaternar
este un nivel de organizare care rezult prin interaciunea dintre lanurile
polipeptidice independente care au deja o structura primar, secundar i
teriar bine definit. Suprastructura cuaternar reprezint asocierea unor
catene polipeptiodice numite protomeri ntr-un ansamblu sau agregat numit
oligomer. Interaciunile prin care se asambleaz agregatul molecular nu sunt
de natur covalent, ci sunt legturi de hidrogen i legturi electrostatice. Un
exemplu tipic pentru organizarea structurii cuaternare este globina din
hemoglobin (Hb) care are o molecul tetramer format din patru lanuri
polipeptidice, fiecare cu structura sa primar, secundar i teriar bine
definit, legate ntre ele prin legturi de hidrogen, fore Van der Waals i
legturi polare. Funcia specific a unei proteine oligomere se manifest
numai la nivelul structurii cuaternare, protomerii separai sunt inactivi.
34
Proprietile proteinelor
Proprieti fizice
Solubilitatea Proteinele fibrilare sunt insolubile n ap, pe cnd cele
globulare prezint grade diferite de solubilitate. Soluiile apoase ale
proteinelor sunt soluii coloidale n care diametrul particulelor variaz ntre
5-100 milimicroni. Proteinele au caracter amfoter. Aceasta se datoreaz
gruprilor acide sau bazice din resturile de aminoacizi mono-
aminodicarboxilici sau diaminomonocarboxilici. La pH-ul fiziologic toate
aceste grupri acide sau bazice sunt ionizate i proteina apare ca un
poliamfolit. n soluie apoas, n funcie de pH proteina migreaz n cmp
electric i pe aceast proprietate se bazeaz separarea i purificarea
proteinelor prin electroforez.
Observaie: Exist un pH la care proteina apare cu sarcin electric
nul, numit punct izoelectric sau pH izoelectric cnd numrul sarcinilor
negative este egal cu numrul sarcinilor pozitive i proteina nu mai
migreaz n cmp electric. Datorit caracterului lor amfoter proteinele
ndeplinesc n organism rol de soluii tampon. Ele contribuie la meninerea
echilibrului acido-bazic.
Precipitarea. Conformaiile native ale proteinelor pot fi uor
perturbate sub aciunea unei multitudini de ageni care afecteaz
interaciunile necovalente din cuprinsul moleculei. Precipitarea unei
proteine este provocat de diferii factori fizici i diferii ageni chimici.
Precipitarea poate fi reversibil i ireversibil.
Proprieti chimice
Proteinele dau numeroase reacii chimice datorit gruprilor amino i
carboxil libere ale aminoacizilor constitueni, legturii peptidice i diferiilor
radicali din molecul. Pe baza unora dintre proprietile chimice ele se pot
identifica i determina cantitativ. Proteinele sunt substane macromoleculare
care hidrolizeaz n mediu acid, bazic sau sub aciunea enzimelor
proteolitice. Hidroliza proteinelor poate fi total sau parial. Hidroliza
total duce la obinerea de aminoacizi iar hidroliza parial la obinerea de
fragmente polipeptidice.
TEST DE EVALUARE
1. Cum se definete structura primar a unei proteine ?
Rspuns:
Structura primar este dat de numrul, felul i secvena resturilor
aminoacizilor din molecul.
Cum se definete structura secundar a unei proteine ?
Exerciii.
Exemplu rezolvat:
1. Care sunt tipurile de legturi si interaciuni care menin stabilitatea
structurii teriare a unei proteine?
a)legturi covalente disulfurice
b) legturi ionice
35
c) legturi de hidrogen
d) legturi prin fore Van der Waals
e) interactiuni dipol-dipol
Rezolvare : a, b, c, d, e
De rezolvat:
2. Care dintre urmtoarele afirmaii sunt adevrate?
a) proteinele prezint caracter amfoter
b) proteinele nu migreaz in cmp electric
c) proteinele prezint proprieti imunologice
d) proteinele precipit reversibil sau ireversibil
e) proteinele sunt molecule mici foarte solubile in ap
Rezolvare :
3.3. Holoproteide si heteroproteide
Clasificarea holoproteidelor
Datorit complexitii structurii lor, clasificarea proteinelor nu se
poate face dup un criteriu unic. La baza clasificrii stau de obicei dou
criterii: conformaia tridimensional (globulare i fibrilare) i constituia lor
chimic.
Reinem: Dup solubilitate i caracterul lor chimic proteinele
globulare se clasific n: albumine, globuline, prolamine, gluteline, histone
i protamine.
Albumine. Albuminele sunt proteine cu caracter acid, solubile n ap i n
soluii diluate de electrolii.
Globuline Globulinele sunt proteine cu caracter acid mai pronunat datorit
prezenei acidului aspartic i acidului glutamic n structura lor. Sunt
insolubile n ap dar se dizolv n soluii diluate de electrolii.
Prolamine. Prolaminele au fost identificate numai n seminele de
graminee, sunt proteine vegetale cu caracter acid pronunat datorit
coninutului ridicat n prolin, acid glutamic i acid aspartic. Prolamine sunt
insolubile n ap, n soluii neutre de electrolii salini i n alcool absolut.
Sunt uor solubile n soluii apoase alcaline i alcool 70%. Gluteline.
Glutelinele sunt proteine cu caracter acid pronunat datorit coninutului
ridicat n acid glutamic i acid aspartic. Sunt insolubile n ap, alcool i
soluii de sruri neutre. Se dizolv n soluii bazice si precipit din aceste
soluii la acidulare.
Histone. Histonele sunt proteine cu caracter bazic care predomin n regnul
animal. Au un coninut ridicat de arginin i lizin. Se dizolv uor n soluii
diluate de acid sulfuric.
Protamine Protamine sunt proteine cu caracter bazic pronunat datorit
coninutului n aminoacizi bazici: lizin, histidin i mai ales arginin.
Protaminele sunt proteine care se gsesc numai n regnul animal.
Scleroproteine Scleroproteinele sunt proteine fibrilare, alctuite aproape
exclusiv din aminoacizi monoaminomonocarboxilici. Ele au proprieti
mecanice bune i un rol plastic i de susinere n organismele animale., sunt
de consisten solid, sunt insolubile n ap, soluii acide sau bazice i sunt
stabile fa de aciunea enzimelor proteolitice.
36
Heteroproteide
Heteroproteidele sunt proteide complexe formate dintr-o
holoproteid i o grupare de natur neproteic numit grupare prostetic.
Observaie: Gruparea prostetic se leag de componenta proteic prin
legturi covalente, ionice, legturi de hidrogen sau fore Van der Waals,
legturi care sunt mai slabe dect legturile peptidice. Prin hidroliz total
pun n libertate aminoacizi i diferite grupri prostetice.
Heteroproteidele se clasific n funcie de natura gruprii prostetice n
- Fosfoproteide;
- Glicoproteide;
- Lipoproteide;
- Cromoproteide;
- Metalproteide;
- Nucleoproteide;
Fosfoproteide- sunt heteroproteide n care componenta prostetic este acidul
ortofosforic legat esteric cu gruparea -OH din serin (cel mai frecvent) sau
din treonin.
Observaie: Fosfoproteidele au un caracter acid datorit restului fosforic
din molecul. Sunt substane solide, insolubile n ap i n acizi. Se dizolv
n baze diluate. Sunt substane care se gsesc n organismele animale i n
microorganisme, in plante neientificndu-se dect n polenul de porumb.
Cele mai importante fosfoproteide sunt cazeina din lapte i vitelina din
glbenuul de ou.
Glicoproteide- sunt heteroproteide n care componenta prostetic este
format din glucide, de obicei poliglucide complexe. Ele sunt proteide
caracteristice regnului animal, dar s-au identificat i n plante.
Lipoproteide -sunt heteroproteide n care componenta prostetic este
format din lipide (acizi grai, gliceride, lecitine, cefaline, etc.) se gsesc n
toate organismele vegetale i animale. n lipoproteide legturile stabilite
ntre lipide i partea proteic sunt de obicei de natur ionic i se stabilesc
ntre grupe -COO
-
libere din proteine i grupe -NH
3
+
din colin sau restul
fosforic al fosfolipidelor i -NH
3
+
din protein. Lipoproteinele sunt substane
de constituie ale celulelor, mitocondriilor, membranelor celulare.
Metaloproteide- sunt heteroproteide care au ca grupare prostetic metale
(Fe, Cu, Mg, Zn, Mn, etc.) Ele au un rol nsemnat n depozitarea i
transportul diferitelor metale. Metalul sub form ionic este legat complex
prin stabilirea unor legturi coordinative ntre metal i anumite grupri din
componenta proteic. Dintre metalproteide cele mai importante sunt cele cu
rol enzimatic. n cloroplaste se afl feredoxina, enzim care conine fier n
molecul i are rol important n reaciile de oxido-reducere.
Cromoproteide- sunt heteroproteide care au ca grupare prostetic o
substan colorat. Se gsesc n toate organismele animale i vegetale, fiind
universal rspndite n lumea vie. Dup structura gruprii prostetice
cromoproteidele se mpart n
- a) cromoproteide porfirinice, care au drept grupare prostetic un nucleu
porfirinic
- b) cromoproteide neporfirinice
HN CH
CO
CH
2
O
PO
3
H
2
37
Dup rolul pe care l ndeplinesc n organism ambele grupe se mpart n
cromoproteide cu funcie respiratorie i cromoproteide fr funcie
respiratorie.
a) Cromoproteide porfirinice
Aceast clas de cromoproteide are drept component prostetic un
nucleu porfirinic. Din punct de vedere biochimic sunt importante
cromoproteidele cu funcie respiratorie: hemoglobina, citocromii, catalazele,
peroxidazele. La plante cromoproteidele feroporfirinice s-au identificat n
boabele de gru, ovz, migdale, n drojdia de bere. Grupa cromoproteidelor
porfirinice fr funcie respiratorie cuprinde cloroplastinele, ficoeritrinele i
ficocianinele.
Toate cromoproteidele porfirinice au in gruparea prostetic un inel
porfirinic, care se formeaz din patru nuclee pirolice unite prin grupri
metinice. Prin introducerea unui atom de metal n interiorul porfirinelor se
obine gruparea prostetic. Cromoproteidele se deosebesc ntre ele prin
natura componentei proteice i prin atomul de metal din gruparea prostetic.
Dintre cromoproteidele porfirinice fac parte i hemoglobina i cloroplastina.
B) Cromoproteide neporfirinice
Sunt cromoproteide care conin o grupare prostetic colorat de
natur neporfirinic. Din grupa cromoproteide neporfirinice cu funcie
respiratorie fac parte hemocianinele, flavinenzimele. Hemocianinele conin
cupru n molecul. Din grupa cromoproteide neporfirinice fr funcie
respiratorie fac parte carotenoproteidele i flavinproteidele.
Nucleoproteide- sunt heteroproteide formate dintr-o protein cu caracter
bazic i o grupare prostetic constituit din acizi nucleici. Deoarece
componenta proteic are in majoritatea cazurilor caracter bazic iar gruparea
prostetic caracter acid pronunat, nucleoproteidele pot fi considerate sruri
ale acizilor nucleici. Nucleoproteidele se clasific dup tipul acidului
nucleic din constituia sa n ribonucleoproteide i deoxiribonucleoproteide.
Se gsesc n toate celulele vegetale i animale, n protoplasm i n lichidele
biologice, formeaz masa principal a nucleelor celulare i a materialului
cromatic.
TEST DE EVALUARE
1. Cum se clasific heteroproteidele dup natura gruprii prostetice?
Rspuns:
Dup natura gruprii prostetice heteroproteidele se clasific n:
fosfoproteide, glicoproteide, lipoproteide, cromoproteide, metalproteide i
nucleoproteide;
2. Cum se clasific holoproteidele dup caracterul lor chimic i dup
solubilitate?
Rspuns:
Exerciii.
Exemplu rezolvat:
1. Care dintre urmtoarele afirmaii sunt adevrate?
38
a) n fosfoproteide componenta prostetic este acidul ortofosforic
legat esteric de gruparea -OH din serin
b) fosfoproteidele au caracter bazic
c) glicoproteidele au drept component prostetic glicerolul
d) globulinele sunt proteine cu caracter bazic foarte uor solubile in
ap
e) globulinele sunt proteine cu caracter acid, greu solubile in ap
Rezolvare : a, e
De rezolvat:
2. Care dintre urmtoarele afirmaii sunt adevrate?
a) albuminele sunt proteine cu caracter acid solubile in ap
b) globulinele sunt proteine cu caracter acid, solubile in soluii de
sruri
c) glutelinele sunt proteine cu caracter acid i au coninut ridicat de
acid glutamic
d) nucleoproteidele au drept component prostetic acizi nucleici
e) nucleoproteidele au drept component prostetic nuclee aromatice
Rezolvare :
Rezumatul temei
Protidele sunt cele mai rspndite biomolecule din celulele vii. Ele
sunt eseniale pentru toate aspectele structurii i funciilor celulare. Cea mai
mare parte din informaia genetic este exprimat prin proteine. Structura
moleculelor proteice i relaia structurii cu funcia lor biologic i cu
activitatea lor sunt probleme centrale ale biochimiei.
Proteinele au o structur polipeptidic. Complexitatea proteinelor a
impus introducerea mai multor trepte de organizare structural denumite
structur primar, secundar, teriar i cuaternar astfel c structura de
ansamblu a unei proteine este dat de existena i interaciunea acestor
structuri. ntre aceste nivele de organizare structural exist interdependen
i mpreun determin particularitile structurale i proprietile funcionale
specifice fiecrei proteine.
Structura primar este dat de numrul, felul i secvena resturilor
aminoacizilor din molecul. Structura secundar definete orientarea
spaial a lanului polipeptidic. Structura teriar reprezint un stadiu avansat
de organizare spaial a proteinelor i const n replierea catenelor
polipeptidice elicoidale asupra lor nile. Structura teriar se constituie pe
baza unor legiti i este meninut prin stabilirea unor legturi i
interaciuni diferite. Structura cuaternar a unei proteine oligomere indic
modul n care lanurile polipeptidice individuale, se asociaz, se asambleaz
pentru a realiza structura proteinei date, structura sa funcional.
Proteinele dau numeroase reacii chimice datorit gruprilor amino i
carboxil libere ale aminoacizilor constitueni, legturii peptidice i diferiilor
radicali din molecul. Datorit complexitii structurii lor, clasificarea
proteinelor nu se poate face dup un criteriu unic. La baza clasificrii stau
de obicei dou criterii: conformaia tridimensional (globulare i fibrilare) i
constituia lor chimic.
39
Tema nr. 4
ACIZI NUCLEICI
Uniti de nvare :
Structura bazelor azotate. Structura nucleozidelor si
nucleotidelor.
Tipuri de acizi nucleici
Obiectivele temei :
- Cunoaterea si studiul principalilor componeni ai acizilor
nucleici
- Cunoaterea aspectelor biochimice privind proprietile si rolul
metabolic al acizilor nucleici
- Explicarea si interpretarea corecta a structurii lanului
polinucleotidic
Timpul alocat temei : 4 ore
Bibliografie recomandat :
1. Babeanu C., 2003, - Biochimie vegetal, Ed Universitaria, Craiova
2. Babeanu C., 2010, Biochimie. Manual universitar pentru nvmntul
la distan. Editura Universitaria, Craiova
3. Campbell P.N, Smith A. D., 2004- Biochimie ilustrat, Ed. Academiei
Romane, Bucuresti
4. Dumitru I. F., Biochimie, 1980, Ed Didactic si Pedagogic, Bucuresti
5. Marinescu G., Glodeanu E., 1995- Biochimie General, Ed. Universitaria,
Craiova
4.1 Structura bazelor azotate. Structura nucleozidelor si nucleotidelor.
Acizii nucleici sunt din punct de vedere chimic, produi de
policondensare ai nucleotidelor. Se cunosc dou tipuri de acizi nucleici:
acizi dezoxiribonucleici (ADN) i acizi ribonucleici. Att ADN ct i ARN
sunt macromolecule informaionale care permit stocarea, transmiterea i
exprimarea informaiei genetice. Molecula de ADN reprezint baza
molecular a ereditii, ea conine informaia genetic cu privire la
biosinteza proteinelor. Coninutul informaional al ADN, nscris n secvena
nucleotidelor, permite specificarea fiecrei proteine, determin
individualitatea organismului.
Reinem: Acizii nucleici sunt substane macromoleculare a cror
unitate de baz este nucleotidul. Hidroliza acid a acizilor nucleici formeaz
baze azotate, pentoze i acid fosforic.
Pentoza din structura acizilor ribonucleici este D- riboza, iar cea
din structura acizilor dezoxiribonucleici este D-2dezoxi riboza. n structura
acizilor nucleici pentozele se gsesc sub form ciclic, furanozic.
40
-riboza 2-dezoxi--riboza
Bazele azotate din structura acizilor nucleici
Bazele azotate care intr n structura acizilor nucleici deriv din dou
structuri heterociclice: purina i pirimidina.
Pirimidin Purin
Bazele purinice din structura acizilor nucleici sunt adenina (6 amino-
purina) i guanina (2-amino-6-hidroxipurina) Ca baze pirimidinice s-au
identificat trei baze majore: uracilul (2,4-dihidroxi-pirimidin), timin (2,4-
dihidroxi-5-metil-pirimidin) i citozin (2-hidroxi-4amino- pirimidin)
Citozina Uracil Timina
Adenina Guanina
Bazele purinice i pirimidinice prezint fenomenul de tautomerie.
Bazele azotate prezint tautomerie lactam-lactim.
Observaie: La pH-ul fiziologic predomin forma lactam. Bazele
azotate care nu conin OH prezint i ele tautomerie imino-amino, dar
echilibrul este deplasat spre forma amino, mai stabil.
forma lactam forma lactim
N
N
NH
2
HO
N
N
HO
OH
N
N
OH
HO
CH
3
N
N
N
N
H
OH
H
2
N
H
N
N
N
N
NH
2
N
N
H
N
N
N
N
O
H
2
C HO
OH
OH OH
HO H
2
C
O
H OH
OH
C NH C N
O OH
41
Nucleozide
Nucleozidele sunt compui care rezult prin stabilirea unei legturi
N-glicozidice ntre hidroxilul semiacetalic (de la C1) al pentozei i atomul
de azot din poziia 9 a unei baze purinice sau din poziia 3 a unei baze
pirimidinice. Bazele azotate se leag glicozidic de pentoz.
Ribonucleozidele conin ca pentoz riboza iar dezoxiribonucleozidele conin
2-dezoxiriboza. n structura nucleozidelor atomii de carbon ai pentozei se
noteaz cu 1'-5' pentru a se deosebi de cei ai bazelor azotate.
Adenozina Guanozina
Uridina Citidina Dezoxitimidina
n funcie de structura bazei azotate componente se cunosc
urmtoarele nucleozide: citidina, uridina, timidina, adenozina, guanozina.
Observaie: Denumirea nucleozidelor provine de la denumirea bazei
azotate la care se adaug sufixul idin pentru derivaii pirimidinici i ozin
pentru cei purinici. Dezoxiribonucleozidele se denumesc adugnd prefixul
dezoxi la numele ribonucleozidului corespunztor. Nucleozidele libere se
gsesc doar n urme, ca produi de hidroliz ai nucleotidelor. Hidroliza
enzimatic a ambelor tipuri de nucleozide are loc sub aciunea
nucleozidazelor.
Nucleotide
Nucleotidele sunt esteri fosforici ai nucleozidelor n care acidul
fosforic este esterificat la gruparea alcool de la C5', C3' sau C2' ai ribozei
sau C5' sau C3' ai dezoxiribozei. n structura acizilor nucleici intr
predominant nucleozid 5' fosfai.
Dezoxiguanozin- 5'-monofosfat (dGMP) Guanozin- 5'-monofosfat (GMP)
(Acid dezoxiguanilic) Acid guanilic
42
Adenozin -5'-monofosfat (AMP)
(Acid adenilic)
Observaie: Deoarece nucleotidele conin un rest de acid fosforic, ele au
caracter acid i se mai numesc acizi nucleozid-5'-monofosforici. Principalele
nucleotide care intr n structura ARN sunt: citidin-5'-monofosfatul, uridin-
5'-monofosfatul, adenozin-5'-monofosfatul, i guanozin-5'-monofosfatul.
Principalele dezoxiribonucleotide din structura ADN sunt dezoxicitidin-5'-
monofosfatul(dCMP),dezoxitimidin-5'-monofosfatul(dTMP)
dezoxiadenozin-5'-monofosfatul (dAMP), i dezoxiguanozin-5'-
monofosfatul(dGMP).
Dezoxicitidin 5'-monofosfatul (dCMP) Citidin 5'-monofosfatul (CMP)
Acid dezoxicitidilic Acid citidilic
Uridin 5'-monofosfatul (UMP) Dezoxitimidin 5'-monofosfatul (dTMP)
Acid uridilic Acid dezoxitimidinic
43
Dac un nucleozid sau un dezoxinucleozid este di sau trifosforilat se
obin nucleozid sau dezoxinucleozid di i trifosfai. De exemplu n cazul
adeninei se obin adenozin-difosfatul (ADP) i adenozin-trifosfatul (ATP).
Resturile de acizi fosforici sunt unite prin legturi macroergice (legturi cu
energie ridicat).
Nucleotidele rezult prin hidroliza parial a acizilor nucleici dar se
gsesc i libere n celule unde ndeplinesc funcii biochimice importante.
Alturi de nucleozid 5'-fosfaii descrii mai exist i nucleotide care conin
grupri fosfat n alte poziii. Astfel exist ribonucleozid 2',3' fosfai ciclici i
ribonucleozid 3'- fosfai cu rol biochimic important. Acidul adenozin 3', 5'
monofosforic ciclic (AMPc) i acidul guanozin 3', 5' monofosforic ciclic
(GMPc) au roluri importante n n mecanismele de aciune ale hormonilor la
nivel celular. La plante este nc controversat rolul regulator al AMPc i
GMPc, prin analogie cu celula animal. Nucleotidele intr i n constituia
unor coenzime cum sunt nicotinamid-dinucleotidele (NAD
+
, NADH+H
+
,
NADP
+
) sau flavinadenin-dinucleotidele (FAD, FADH2) implicate n
procesele oxidoreductoare ale respiraiei celulare.
TEST DE EVALUARE
Care sunt compuii care se formeaz la hidroliza nucleotidelor?
Rspuns:
La hidroliza nucleotidelor rezult baze azotate, pentoze i acid fosforic.
2. Care sunt substanele care intr n constituia nucleozidelor?
Rspuns:
Exerciii.
Exemplu rezolvat:
1. Care dintre urmtoarele substane intr n constituia acizilor
nucleici?
a) uracil si timin
b) timin si riboz
c) ribuloz i dezoxiriboz
d) adenin si guanin
e) citozin si dezoxiglucoz
44
Rezolvare: a, b, d
De rezolvat:
2. Care dintre urmtoarele afirmaii sunt adevrate?
a) acizii nucleici sunt produi de policondensare ai nucleotidelor
b) pentoza din structura acizilor ribonucleici este fructofuranoza
c) bazele purinice din structura acizilor nucleici sunt adenina i
guanina
d) bazele azotate se leag amidic de pentoz.
e) bazele azotate se leag glicozidic de pentoz.
Rezolvare :
4.2 Tipuri de acizi nucleici
Acizii nucleici sunt polinucleotide rezultate din policondensarea
nucleotidelor, care se succed n lan. Gruparea 5' hidroxi a unui nucleotid
este legat la gruparea 3' hidroxi a nucleotidului urmtor prin legtur fosfat
diesteric. Orice caten polinucleotidic are o direcie specific, n sensul c
toate legturile internucleotidice au aceeai orientare de-a lungul lanului.
Fiecare caten polinucleotidic va avea dou capete: captul 5', la care
gruparea -OH de la C5' este liber i captul 3', la care gruparea -OH de la
C3' nu este angajat ntr-o legtur internucleotidic. Lanurile de
dezoxiribonucleotide legate covalent formeaz acidul dezoxiribonucleic
(ADN) iar lanurile de ribonucleotide legate covalent formeaz acizii
ribonucleici.
Acizii Dezoxiribonucleici
ADN-ul conine patru baze azotate i anume: adenina, guanina,
timina i citozina. n secvena nucleotidelor din molecula de ADN este
nscris informaia genetic pe care acestea o cuprind, astfel nct
succesiunea a trei baze din structura ADN codific includerea unui anumit
aminoacid n biosinteza proteinelor. Structura primar a ADN este
reprezentat de lanul de polidezoxiribonucleotide, caracterizat prin natura,
proporia i secvena nucleotidelor constituente.
Figura 3. Structura primar a unui lan
polinucleotidic dezoxiribonucleic.
(fragment de ADN)
H
H
C H2
H
H
OH H
O
H
H
C H2
H
H
H
O
Baza
Baza
HO O
O
O
P
P
O
O
O HO
Baza
O
H
H
H
H2C
H
H
P
O
O
O HO
Baza
O
H
H
H
H2C
H
H
P
O
O HO
45
I.D.Watson, F. Willkins i F.H.C.Crick, n 1953, pe baza unor date
experimentale privind spectrometria cu raze X propun pentru ADN structura
de dublu helix. Modelul este confirmat ulterior de numeroase date
experimentale fapt pentru care aceti cercettori au primit premiul Nobel.
Reinem: Analiza cromatografic efectuat pe molecule de AND stabilete
o anumit relaie cantitativ ntre cele patru baze azotate. n toate tipurile de
ADN studiate s-a demonstrat c bazele purinice i pirimidinice se gsesc n
cantiti echimoleculare, A+G=T+C i A/T=1, G/C=1. Molecula de ADN
este format din dou lanuri polinucleotidice complementare i antiparalele,
rsucite elicoidal spre dreapta n jurul unei axe comune de simetrie.
Figura 4. Structura dublu helicoidal a ADN Baze complementare unite
prin legturi de hidrogen
Stabilitatea dublului helix este asigurat att de interaciunile
hidrofobe dintre bazele azotate ct i de legturile de hidrogen ce se
stabilesc ntre bazele azotate de pe o caten i cele complementare de pe
cealalt caten. Legturile de hidrogen se stabilesc, invariabil, ntre o baz
azotat purinic de pe o caten i una pirimidinic de pe cealalt caten fiind
de tipul A=T, G=C. Cuplarea a dou baze purinice este exclus ntruct s-ar
depi spaiul oferit de dublul helix, iar cuplarea a dou baze pirimidinice ar
face imposibil stabilirea legturilor de hidrogen, bazele fiind prea departe
una de alta. Bazele pereche sunt adenina-timina i guanina-citozina, ntruct
numai acestea pot stabili numrul maxim de legturi de hidrogen, asigurnd
astfel conformaia cu energia liber cea mai mic, deci cea mai stabil,
moleculei de ADN: Adenina se leag de timin prin dou legturi de
hidrogen iar guanina de citozin prin trei legturi. Cele dou catene nu sunt
identice ci complementare. Succesiunea bazelor azotate dintr-o caten
dicteaz succesiunea bazelor azotate din cea de a doua caten, o caten este
replica celeilalte. Stabilitatea sistemului este suplimentat i de fore Van
der Waals, dipol-dipol sau hidrofobe ntre cele dou catene. Bazele azotate
46
sunt plasate spre interiorul dublului helix cu planurile ciclurilor n poziii
orizontale, reciproc paralele i perpendiculare pe axa helixului.
Acizii ribonucleici
Sunt produi macromoleculari rezultai prin policondensarea
ribonuceotidelor. Ribonucleotidele care alctuiesc molecula de ARN
stabilesc legturi fosfat diesterice ntre gruparea OH din poziia 3' a unui
nucleotid i gruparea OH din poziia 5' a nucleotidului succesiv. ARN
conine guanina, citozina, adenina i uracilul. Pe lng aceste baze, ARN
conine i baze aa-zise "minore" rezultate prin metilri sau tiolri ale
bazelor "majore". Componenta glucidic din ARN este riboza. n lanul
ribonucleotidic al moleculei de ARN, raportul A/U i G/C nu mai este 1,
ntruct nu exist un lan complemantar ca i la AND. Cantitatea de ARN
spre deosebire de cea de AND, variaz de la o celul la alta i chiar n cadrul
aceleiai celule, n funcie de intensitatea procesului de biosintez a
proteinelor la un moment dat.
Figura 5. Structura primar a unui lan
polinucleotidic ribonucleic. (fragment de
ARN)
Baze azotate: guanina, citozina, adenina i
uracil.
Observaie: Exist diferite tipuri de ARN n celule: ARN ribozomal
(ARNr), ARN de transfer (ARNt), i ARN mesager (ARNm), cu structuri
caracteristice. Toi au n comun aceeai structur primar iar structura
secundar i teriar este specific fiecrui tip de ARN, i anume difer prin
masa molecular, coeficieni de sedimentare, stabilitate.
Moleculele de ARN sunt monocatenare dar pe anumite poriuni,
acolo unde o permite complementaritatea bazelor se organizeaz n structuri
dublu elicoidale, formate prin rsucirea catenei n jurul propriului ax i
formarea de legturi de hidrogen conform principiului complementaritii
bazelor. Poriunile de baze necomplementare sunt expulzate ca bucle n
afara zonelor de dublu helix.
Figura 6. Structura secundar a
ARN monocatenar coninnd
poriuni cu baze complementare
asociate prin legturi de hidrogen
i poriuni cu baze
necomplementare
H
H
C H2
H
OH
H
OH
O
H
H
C H2
H
OH
H
O
OH
OH
Baza
Baza
HO O
O
O
P
P
O
O
O HO
Baza
O
H
H
H2C
H
H
P
O
O
O HO
Baza O
H
H
H2C
H
H
P
O
O HO
47
ARN-mesager (ARNm) se sintetizeaz n nucleu prin procesul de
transcripie, prin care secvena bazelor dintr-o caten de ADN este copiat
enzimatic (ARN-polimeraz) realizndu-se o caten complementar.
Funcia biochimic a ARNm este de a transmite informaia preluat de la
ADN la nivelul ribozomilor unde are loc biosinteza proteinelor.
ARN de transfer (ARNt) are rolul de a transporta aminoacizii la
ribozomi unde are loc procesul de biosintez al proteinelor i este localizat
n citoplasm. Fiecruia dintre cei 20 aminoacizi care intr n structura
proteinelor i corespunde cel puin un ARNt specific. n general exist mai
multe tipuri de ARNt pentru un aminoacid.
ARN ribozomal (ARNr), sunt molecule flexibile i deformabile,
care conin zone dublu catenare ntrerupte de zone monocatenare. ARNr
este o component esenial a ribozomilor i constituie 75-80% din totalul
ARN celular i cel mai stabil metabolic. ARNr se deosebesc ntre ei prin
masele lor moleculare i prin coeficienii de sedimentare. ARNr nu se
gsesc n stare liber ci combinai cu proteine diverse, constituind particule
ribonucleoproteice denumite ribozomi. La nivelul ribozomilor are loc
biosinteza proteinelor, acetia permind conlucrarea ARNt, ARNm, i
ARNr n vederea desfurrii acestui proces.
TEST DE EVALUARE
1. Care este funcia biochimic a ARNm?
Rspuns:
Funcia biochimic a ARNm este de a transmite informaia preluat de la
ADN la nivelul ribozomilor unde are loc biosinteza proteinelor.
2. Care sunt bazele azotate din structura ADN ?
Rspuns:
Exerciii.
Exemplu rezolvat:
1. Care dintre urmtoarele afirmaii sunt adevrate?
a) ADN are structura de dublu helix.
b) ADN are structura monocatenar
c) Adenina se leag de timin prin dou legturi de hidrogen iar
guanina de citozin prin trei legturi.
d) Adenina se leag de timin prin trei legturi de hidrogen iar
guanina de citozin prin dou legturi.
e) Bazele pereche sunt adenina-timina i guanina-citozina
Rezolvare : a, c, e
De rezolvat:
2. Care dintre urmtoarele afirmaii sunt adevrate?
a) In ARN raportul A/U i G/C este 1
b) In ARN raportul A/U i G/C este diferit de 1
c) ARN conine guanina, citozina, adenina i uracilul.
d) ARN conine guanina, citozina, adenina i timin.
48
e) In ADN bazele purinice i pirimidinice se gsesc n cantiti
echimoleculare
Rezolvare :
Rezumatul temei
Acizii nucleici sunt din punct de vedere chimic, produi de
policondensare ai nucleotidelor. Se cunosc dou tipuri de acizi nucleici:
acizi dezoxiribonucleici (ADN) i acizi ribonucleici. Att ADN ct i ARN
sunt macromolecule informaionale care permit stocarea, transmiterea i
exprimarea informaiei genetice. Acizii nucleici sunt substane
macromoleculare a cror unitate de baz este nucleotidul. Hidroliza acid a
acizilor nucleici formeaz baze azotate, pentoze i acid fosforic.
Pentoza din structura acizilor ribonucleici este D- riboza, iar cea
din structura acizilor dezoxiribonucleici este D-2dezoxi--riboza. n
structura acizilor nucleici pentozele se gsesc sub form ciclic,
furanozic. Bazele azotate care intr n structura acizilor nucleici deriv din
dou structuri heterociclice: purina i pirimidina.
Bazele purinice din structura acizilor nucleici sunt adenina i
guanina iar ca baze pirimidinice s-au identificat trei baze majore: uracilul,
timin i citozin.
Nucleozidele sunt compui care rezult prin stabilirea unei legturi N-
glicozidice ntre hidroxilul semiacetalic (de la C1) al pentozei i atomul de
azot din poziia 9 a unei baze purinice sau din poziia 3 a unei baze
pirimidinice. Bazele azotate se leag glicozidic de pentoz.
n funcie de structura bazei azotate componente se cunosc urmtoarele
nucleozide: citidina, uridina, timidina, adenozina, guanozina.
Nucleotidele sunt esteri fosforici ai nucleozidelor, n structura
acizilor nucleici intrnd predominant nucleozid 5' fosfai. Nucleotidele
rezult prin hidroliza parial a acizilor nucleici dar se gsesc i libere n
celule unde ndeplinesc funcii biochimice importante.
Acizii nucleici sunt polinucleotide rezultate din policondensarea
nucleotidelor, care se succed n lan. Lanurile de dezoxiribonucleotide
legate covalent formeaz acidul dezoxiribonucleic (ADN) iar lanurile de
ribonucleotide formeaz acizii ribonucleici.
ADN-ul conine patru baze azotate i anume: adenina, guanina, timina i
citozina. ADN are structura de dublu helix. Bazele purinice i pirimidinice
se gsesc n cantiti echimoleculare, A+G=T+C i A/T=1, G/C=1.
Molecula de ADN este format din dou lanuri polinucleotidice
complementare i antiparalele, rsucite elicoidal spre dreapta n jurul unei
axe comune de simetrie.
ARN conine guanina, citozina, adenina i uracilul. n lanul
ribonucleotidic al moleculei de ARN, raportul A/U i G/C nu mai este 1,
ntruct nu exist un lan complemantar ca i la AND. Cantitatea de ARN
spre deosebire de cea de AND, variaz de la o celul la alta i chiar n cadrul
aceleiai celule, n funcie de intensitatea procesului de biosintez a
proteinelor la un moment dat. Exist diferite tipuri de ARN n celule: ARN
ribozomal (ARNr), ARN de transfer (ARNt), i ARN mesager (ARNm), cu
structuri caracteristice. Toi au n comun aceeai structur primar iar
structura secundar i teriar este specific fiecrui tip de ARN, i anume
difer prin masa molecular, coeficieni de sedimentare, stabilitate.
49
Tema nr. 5
VITAMINE
Uniti de nvare :
Vitamine liposolubile
Vitamine hidrosolubile
Obiectivele temei :
- Cunoaterea aspectelor biochimice privind clasificarea, structura i
proprietile vitaminelor
- Analizarea corelatiei structur, proprieti, rol biochimic.
- Cunoaterea principalelor vitamine naturale
Timpul alocat temei : 4 ore
Bibliografie recomandat :
1. Babeanu C., 2003, - Biochimie vegetal, Ed Universitaria, Craiova
2. Babeanu C., 2010, Biochimie. Manual universitar pentru nvmntul
la distan. Editura Universitaria, Craiova
3. Campbell P.N, Smith A. D., 2004- Biochimie ilustrat, Ed. Academiei
Romane, Bucuresti
4. Leninger A.L., Biochimie, 1992, vol. II , Ed. Tehnic, Bucureti
5. Marinescu G., Glodeanu E., 1995- Biochimie General, Ed. Universitaria,
Craiova
5.1. Vitamine liposolubile
Vitaminele sunt o categorie de substane care se gsesc n organism
n cantiti foarte mici i sunt indispensabile pentru reglarea proceselor
metabolice. Vitaminele sunt sintetizate de organismele vegetale i numai n
mic msur de cele animale. Animalele i procur vitaminele din hran.
Deoarece vitaminele nu se pot depozita, organismele animale au nevoie
permanent de vitamine. Acestea nu au rol plastic sau energetic ci regleaz i
stimuleaz principalele procese metabolice. Majoritatea vitaminelor
alctuiesc coenzime sau cofactori ai unor enzime. Lipsa sau insuficiena
vitaminelor din organism determin tulburri metabolice i apariia unor
boli (avitaminoze, hipovitaminoze) care constituie boli careniale.
n plante i animale s-au identificat unele substane organice care au
o aciune fiziologic i biochimic opus vitaminelor. Aceste substane se
numesc antivitamine i acioneaz n dou moduri: sunt analogi structurali
ai vitaminelor dar nu posed activitatea biologic a vitaminelor sau au
structur diferit dar acioneaz asupra vitaminelor inactivndu-le.
Reinem: Vitaminele au structuri chimice foarte variate. Din aceast
cauz ele nu s-au clasificat conform structurii i s-a fixat drept criteriu de
clasicare solubilitatea. Din punct de vedere al solubilitii, vitaminele se
grupeaz n vitamine hidrosolubile (cele cu molecule polare, solubile n ap)
i vitamine liposolubile (cele cu molecule nepolare) solubile n grsimi.
Vitamine liposolubile
Vitaminele liposolubile sunt substane solubile n grsimi, n solveni
organici i insolubil n ap. Din aceast grup fac parte vitaminele A, D, E,
K i F.
50
Vitamina A (Retinol)
Vitaminele A se gsesc n natur att ca atare ct i ca provitamine.
Reinem: Se cunosc vitaminele A
1
(retinol) i A
2
(dehidroretinol). Cea mai
important este vitamina A
1
, vitamina antixeroftalmic sau vitamina
creterii. Vitamina A
2
se gsete frecvent n petii de ap dulce. Vitamina A
1
pur este o substan de culoare galben, cristalizat iar vitamina A
2
este un
ulei galben.. i vitamina A
1
i vitamina A
2
sunt autooxidabile, termostabile
n absena aerului, sensibile la aciunea oxidanilor i a luminii n special a
radiaiilor UV. n regnul vegetal, vitaminele A se gsesc predominat sub
form de provitamine. Provitaminele A sunt carotenoizii , i din care la
nivelul peretelui intestinal are loc formarea vitaminelor A printr-o scindare
oxidativ n prezena enzimei carotinaz.
Observaie: Vitaminele A au un rol important n creterea
organismelor tinere, n protejarea esuturilor epiteliale i n procesul vederii.
n avitaminoz A se oprete creterea organismelor tinere, se produc
dereglri ale esuturilor epiteliale, din tubul digestiv, din aparatul respirator
i aparatul urogenital. Se produc tulburri oculare i apare xeroftalmia
(orbul ginilor) Lipsa vitaminei A n organismul omului determin
incapacitatea de regenerare a rodopsinei (purpura retinian) urmat de
tulburri oculare specifice, cum sunt pierderea vederii crepusculare sau
tulburri de adaptare a vederii la ntuneric.
Vitamine D
Ca i vitaminele A, vitamina D are mai multe vitamine i mai multe
provitamine D. Ele se gsesc n natur mai ales n regnul vegetal.
Reinem: Din punct de vedere structural, provitaminele D sunt
steroli care difer ntre ei prin catena lateral fixat n poziia 21.
Transformarea sterolilor n vitamine D se face n piele i esutul subcutanat
sub aciunea energiei solare, a radiaiilor UV (256-313nm) printr-un proces
fotochimic cu consum de energie.
Vitaminele D sunt termostabile i rezistente la aciunea oxigenului.
n cantitate mai mare se gsesc n uleiul de pete, ficat, unt, ou, lapte, piele,
drojdie de bere.
Observaie: Vitaminele D se mai numesc i antirahitice, deoarece previn i
vindec rahitismul. Vitaminele D favorizeaz absorbia calciului i a
fosforului i formarea sistemului osos. n avitaminoze D apare rahitismul la
copii i osteoporoza i osteomalacia la aduli. Osteomalacia se manifest
prin nmuierea oaselor, micorarea lor n volum i deformarea lor.
Osteoporoza se caracterizeaz prin rarefierea sitemului osos. Excesul de
vitamine D duce la demineralizare oaselor i apariia calculilor (renali,
hepatici, etc)
Vitamine E (Tocoferoli)
Vitamina E se mai numete i tocoferol. Aceste nume este legat de
principala ei funcie biologic de a favoriza fertilitatea (n grecete tokos =
natere i pherin = a purta) . Tocoferolii sunt sintetizai n plante i se gsesc
n frunze, uleiuri vegetale, semine n stare de germinaie.
Reinem: Tocoferolii sunt derivai ai benzopiranului, numit croman. Se
cunosc mai muli tocoferoli, notai cu litere greceti , , , etc., toi avnd
ca structur de baz tocolul. Tocoferolii intervin n n procesul de fertilitate,
asigurnd la masculi formarea spermatozoizilor iar la femele influeneaz
favorabil procesul de gestaie. Se mai numete vitamina antisterilitii
deoarece la animale lipsa vitaminei E duce la sterilitate. Vitamina E
stimuleaz biosinteza proteinelor i manifest activitate antioxidant,
51
protejnd mpotriva oxidrii acizii grai nesaturai, carotenoizi, retinolii.
Avitaminoza E determin la om i animale scderea capacitii de
reproducere, sterilitate, dereglri metabolice, decalcefiere, slbirea
rezistenei organismului la infecii, stri nervoase. De asemenea apar
tulburri la nivelul ficatului i al glandelor suprarenale.
Vitamine K
Vitaminele K se mai numesc vitamine antihemoragice sau vitamine
pentru coagularea sngelui. Lipsa lor din organism, la om i animale duce la
hemoragii. Vitaminele K sunt sintetizate numai de plante i de
microorganismele din tubul digestiv. Aceast flor intestinal constituie o
surs important de vitamina K pentru organismul animal.
Reinem: Nucleul de baz al vitaminelor K este format din 1,4-
naftochinon substituit. Ca i celelalte vitamine liposolubile, vitamina K
are mai multe vitamine cu structuri chimice asemntoare. Mai importante
sunt vitaminele K
1
, izolat din vegetale i K
2
izolat din esuturi animale i
bacterii intestinale.
Cea mai important funcie a vitaminei K n organism este
implicarea ei n procesul coagulrii. Este implicat n biosinteza
protrombinei i a altor factori de coagulare, biosintetizai n ficat sub forma
unor precursori inactivi, care sunt activai prin intervenia vitaminei K.
TEST DE EVALUARE
1. Care sunt provitaminele A naturale?
Rspuns
Provitaminele A sunt carotenoizii , i din care la nivelul peretelui
intestinal are loc formarea vitaminelor A printr-o scindare oxidativ n
prezena enzimei carotinaz.
2. Ce sunt provitaminele D din punct devedere structural?
Rspuns
Exerciii.
Exemplu rezolvat:
1. Care este numele dat vitaminei K datorit aciunii sale?
a) vitamina antixeroftalmic sau vitamina creterii.
b) antirahitice
c) vitamina antisterilitii
d) vitamine antihemoragice
e) vitamina antipelagroas
Rezolvare: d
De rezolvat:
2. Care dintre urmtoarele proprieti sunt prezentate de vitamina D?
a) au un rol important n creterea organismelor tinere i n procesul
vederii.
b) favorizeaz absorbia calciului i a fosforului i formarea
sistemului osos.
52
c) in avitaminoze D apare rahitismul la copii i osteoporoza i
osteomalacia la aduli.
d) intervin n n procesul de fertilitate,
e) cea mai important funcie n organism este implicarea ei n
procesul coagulrii.
Rezolvare:
5.2 Vitamine hidrosolubile
Complexul B
n grupul vitaminelor B intr mai multe substane cu structur
chimic diferit. Vitaminele B intr ca atare sau puin modificate n
structura enzimelor alctuind coenzime sau grupri prostetice. Din grupa
vitaminelor B fac parte: vitamina B
1
, B
2,
B
12,
acidul pantotenic,
nicotinamida, acidul paraaminobenzoic, acizii pteroilglutamici, biotina,
mezoinozitolul, etc. Drojdia de bere i cortexul cerealelor conin n cantitate
mare vitamine din complexul B. .
Vitamina B
1
(tiamina)
Vitamina B
1
se mai numete tiamin, aneurin sau vitamin
antiberiberic. Majoritatea microorganismelor sunt capabile s o sintetizeze
total iar cteva specii vegetale primesc tiamina de la organismele simbiotice.
Vertebratele, ciupercile i unele microorganisme sunt incapabile de sintez.
Vitamina B1 se gsete n drojdia de bere, seminele cerealelor i
leguminoaselor, n cojile de orez, frunze, flori, polen, etc.
Reinem: Vitamina B
1
este format dintr-un nucleu pirimidinic i unul
tiazolic unite printr-o grupare metilenic. Principala funcie a vitaminei B
1
este cea de coenzim, sub form de tiaminpirofosfat (TTP), pentru enzimele
participante la metabolizarea -cetoacizilor i -cetolilor. Lipsa vitaminelor
B
1
din hran produce la animale polinevrit iar la om se manifest prin
tulburri ale sistemului nervos, pierderea apetitului, oboseal, tulburri
gastrointestinale. Boala beri-beri apare n cazul avitaminozelor prelungite.
Ea se manifest prin tulburri pshihice, digestive, nervoase, cardiace.
Vitamina B
2
(lactoflavina, riboflavina)
Vitamina B
2
se mai numete i riboflavin datorit structurii sale de
flavin (pigment galben).
Reinem: Vitamina B
2
este format dintr-un nucleu izoaloxazinic i
din ribitol. n organism riboflavina formeaz cu ATP dou flavinnucleotide
numite flavinmononucleotid (FMN) i flavinadenindinucleotid (FAD).
Vitamina B
2
se gsete n aproape toate celulele vegetale i animale
att n form liber ct i sub forma celor dou coenzime nucleotidice. La
mamifere ficatul, rinichiul, inima, splina i creierul sunt organele n care
riboflavina se gsete n cantitate mare. De asemenea cantiti importante se
gsesc n ficatul petilor, retin, glandele lacrimale i lacrimile mamiferelor.
n cazuri de avitaminoz, organismele au o slab rezisten la infecii, se
produc dereglri ale epidermei, cderea prului, conjunctivite.
Nicotinamida (Vitamina PP)
Vitamina PP este vitamina antipelagroas (pellagra preventiae).
Numele de niacin corespunde structurii chimice de niacin, acid nicotinic.
Aceeai aciune vitaminic antipelagroas o are i amida acidului nicotinic,
nicotinamida sau niacinamida. Vitamina PP se gsete n trele cerealelor,
ciuperci, lapte, ficat. Ambele substane sunt vitamine PP. Formele active ale
53
vitaminei PP sunt cofactorii NAD
+
i NADP
+
implicai n marea majoritate
a reaciilor de oxido-reducere din organismele vii.
Carena de vitamin PP duce la simptome caracteristice bolii numite
pelagr. Pelagra apare n urma unui consum ndelungat de porumb sau in
urma unui consum excesiv de alcool i melas. Simptomele acestei boli
cuprind leziuni ale pielii, mucoaselor, afeciuni ale sistemului nervos central
i periferic i degenerescen hepatic gras. Ca simptome caracteristice
sunt dermatita, diareea i demena, simptomele celor trei "D". Necesarul
zilnic de vitamina PP este de 15 mg.
Vitamina B
6
Numele de piridoxin corespunde structurii chimice a vitaminei B
6
deoarece ea este un alcool cu inel piridinic. Se mai numete adermin sau
vitamina antipelagroas a obolanului.
Reinem: Cele mai importante sunt piridoxina, piridoxalul i piridoxamina.
Aceste trei substane sunt mult rspndite n natur, de obieci mpreun i se
pot transforma reciproc una n alta. Toate formele vitaminei B6 sunt
fotosensibile. Vitaminele B6 sunt larg rspndite n organismele vegetale i
animale. Ca toate vitaminele complexului B se gsete n cantiti mari n
drojdia de bere. Cantiti importante se afl i n coaja bobului de orez,
polen, seminele cerealelor, ficatul animalelor, pete, glbenuul de ou.
Lptiorul de matc este foarte bogat n piridoxin (5000g/g) i n alte
vitamine ale complexului B. n stri careniale se produc modificri
cutanate, tulburri nervoase, anemie. In cauza abundenei vitaminei n
alimente i a biosintezei acesteia de ctre flora intestinal, stri de caren se
evidenaiz rar. Pentru unele microorganisme vitaminele B6 constituie
factori de cretere.
Vitamina B
12
Vitamina B
12
ndeplinete rol de vitamin antipernicioas pentru om
i este factor de cretere pentru microorganisme. Are o importan deosebit
n cretere, hematopoez i funcionarea celulei nervoase.
Reinem: Se mai numete cianocobalamin, datorit structurii chimice,
fiind format dintr-un nucleu porfirinic care conine central un atom de
cobalt i o grupare cian, grupri metilice i amidice legate de nucleii pirolici,
un nucleu dimetilbenzoimidazolic, riboz, acid fosforic i alcool izopropilic.
Rolul biochimic i fiziologic al vitaminei B
12
este ndeplinit de coenzima
B
12
. Aceasta particip drept coenzim n procesele de carboxilare, la
biosinteza hemului, la biosinteza ADN, n biosinteza proteinelor i lipidelor.
Carena n vitamina B
12
produce anemia pernicioas, demineralizri ale
sistemului nervos i ntrzieri n creterea organismelor tinere. Necesarul
zilnic de vitamina B
12
este de 30mg.
Acidul pantotenic (Vitamina B3)
Acidul pantotenic poart acest nume (n grecete, pan = tot, peste
tot) pentru c este foarte rspndit n esuturile vegetale i animale cu toate
c nu este sintetizat dect de plante i microorganisme. n cantitate mai mare
se gsete n lptilorul de matc, fina de fasole, soia, drojdia de bere,
arahide, migdale.
Observaie: Principalul rol al acidului pantotenic este cel de component al
coenzimei A. Coenzima A particip la numeroase procese biochimice
fundamentale, att de biosintez ct i de degradare.
La om nu a fost evideniat o avitaminoz provocat de acidul
pantotenic, aceasta explicndu-se probabil prin faptul c se gsete n
aproape toate alimentele i pentru c este sintetizat i n organism de flora
54
intestinal. Strile de hipovitaminoz care se pot instala, sunt de cele mai
multe ori datorate unei policarene generale sau alterrii capacitii de
absorbie intestinal. Necesarul zilnic pentru omul adult este de 4-5mg.
Biotina
Unele organisme necesit n mediul de cultur prezena unor factori
de cretere denumii bios. Ulterior s-a constatat c biosul este alctuit din
mai multe substane printre care i un grup de trei vitamine hidrosolubile:
mezoinozitolul, biotina i acidul pantotenic. Aceste trei vitamine sunt i
factori de cretere pentru animalele superioare. n structura biotinei intr un
ciclu tetrahidrotiofenic substituit. Exist dou biotine naturale i cu
activitate vitaminic. Biocitina reprezint forma vitaminic natural cea mai
activ i mai rspndit. Biotina are un rol important n creterea i
funcionarea normal a organismelor animale i vegetale, intervenind n
metabolismul glucidelor, lipidelor i proteinelor, precum i n metabolismul
energetic, face parte din structura unor sisteme enzimatice implicate n
biosinteza acizilor grai i a unor aminoacizi i glucide. Este factor de
cretere pentru drojdii i numeroase microorganisme. Biotina are capacitatea
de a lega peptide i proteine, formnd complexe stabile care nu se absorb la
nivelul intestinului.
Observaie: Un exemplu este complexul inactiv biotinavidin format cu
avidina din albuul de ou. Hipovitaminoza cauzat de insuficiena
alimentar a biotinei este foarte rar. Strile de caren biotinic sunt bine
descrise i sunt cunoscute sub numele "sindromul deficitului carboxilazic",
manifestate prin: dermatite, leziuni cutanate, micri insuficient coordonate.
Acizii folici (acizi pteroilglutamici)
Acizii folici sunt cofactori eseniali hidrosolubili, produi de
organismele vegetale. Grupul generic al "acizilor folici" este constituit dintr-
un complex de vitamine, corelate din punct de vedere structural cu acidul
pteroilglutamic. Au aciune hematopoetic i leucopoetic dar se
difereniaz prin aciunea specific pe care o au asupra diferitelor specii de
animale i microorganisme. Din acest grup fac parte acidul folic i derivaii
si acidul folinic, acidul tetrahidrofolic, acidul dihidrofolic, vitaminele U.
Acidul folic este larg rspndit n natur, att n esuturile vegetale ct i
animale. Simptomul deficienei n folai este anemia megaloblastc care se
caracterizeaz prin apariia de celule gigantice i a unor eritrocite imature, n
mduva spinrii. Ca efecte secundare apar ulceraii, infecii, tulburri gastro-
intestinale, neuropatii periferice. Dintre toate acestea cele mai caracteristice
sunt modificrile hematologice.
Acidul para-aminobenzoic (PABA)
Acidul para-aminobenzoic se numete i vitamina H. Este un factor de
cretere pentru numeroase microorganisme. Este sintetizat de flora
intestinal n cantiti suficiente pentru om. Se gsete liber sau combinat cu
anumii aminoacizi sau n structura acizilor folici. Acidul p-aminobenzoic la
animale previne depigmentarea pielii i a prului. Se presupune c are o
aciune antiinfecioas general.
Vitamina C
Vitamina C, acidul ascorbic este una din cele mai cunoscute vitamine. Are o
larg rspndire n natur fiind biosintetizat att de organismele vegetale,
animale (cu excepia omului, maimuei i cobaiului) ct i de numeroase
microorganisme. Se gsete n stare liber i asociat cu proteinele, formnd
un complex protein-acid ascorbic, numit ascorbigen, care servete ca
55
rezerv. Se gsete n toate plantele, iar n cantitate mai mare se afl n
fructele citrice, mcee, coarne, coacze negre, ctin, nuci necoapte, mere.
Reinem: Acidul ascorbic este lactona acidului 2,3-dienol-L-gulonic, are
formula brut C
6
H
8
O
6
, i are 4 atomi de hidrogen mai puin dect o hexoz.
Este o substan optic activ, dextrogir. Vitamina C are activitate
antiinfecioas activnd sistemul imun al organismului. Acidul ascorbic
stimuleaz rspunsul imun al leucocitelor i aprarea antibacterian prin
creterea mobilitii acestor celule i prin protecia membranei acestora fa
de ageni oxidani.
Acidul ascorbic i acidul dehidroascorbic formeaz n celule un
sistem redox foarte important, care ia parte n numeroase procese
metabolice din organism.
Acid L ascorbic Acid dehidro-L-ascorbic
Acest sistem regleaz potenialul de oxidoreducere celular i
contribuie la transportul hidrogenului pe cale neenzimatic. Vitamina C are
un rol important n stimularea sau inhibarea unor sisteme enzimatice, n
lanul oxidrilor celulare. Are o aciune antioxidant de aprare a
vitaminelor liposolubile i a glutationului.
Observaie: n avitaminoz se produce la om boala numit scorbut,
caracterizat prin hemoragii la nivelul gingiilor, apariia de hematoame,
tulburri digestive, anemie, stare de subfebrilitate, etc. n stadiu mai avansat
al scorbutului apar cangrene, hemoragii viscerale, necroze osoase. Necesarul
zilnic de vitamina C pentru un adult este de 50-100mg.
TEST DE EVALUARE
1. Care este, n celule, rolul sistemului redox acid ascorbic/acid
dehidroascorbic?
Rspuns
Acest sistem ia parte n numeroase procese metabolice din organism,
regleaz potenialul de oxidoreducere celular i contribuie la transportul
hidrogenului pe cale neenzimatic.
2. Care este principalul rol al acidului pantotenic?
Rspuns:
Exerciii.
Exemplu rezolvat:
1. Care este numele dat vitaminei B
1
datorit aciunii sale?
H
CH
2OH
HO
H
HO
HO
O
O
C
C
C
C
C
H
CH
2OH
HO
H
HO
HO
O
O
C
C
C
C
C
H
CH
2OH
HO
O
O
C
C
C
C
C
O
O
O
-2H
+
+2H
+
56
a) se mai numete tiamin, aneurin sau vitamin antiberiberic.
b) este vitamina antipelagroas (pellagra preventiae)
c) se mai numeste piridoxamina sau piridoxal.
d) este vitamina antipernicioas
e) vitamina antixeroftalmic
Rezolvare: a
De rezolvat:
2. Care dintre urmtoarele proprieti sunt caracteristice vitaminei C?
a) principala funcie este aceea de coenzim, sub form de
tiaminpirofosfat (TTP)
b) formele active ale vitaminei sunt cofactorii NAD
+
i NADP
+
c) formeaz n celule un sistem redox foarte important,
d) se gsete n stare liber i asociat cu proteinele, formnd un
complex protein-acid ascorbic
e) protejeaz diferite substane contra agentilor oxidani
Rezolvare
Rezumatul temei
Vitaminele sunt o categorie de substane care se gsesc n organism
n cantiti foarte mici i sunt indispensabile pentru reglarea proceselor
metabolice. Vitaminele sunt sintetizate de organismele vegetale i numai n
msur foarte mic de unele specii animale. Animalele i procur
vitaminele din hran, fie n stare liber, fie sub form de provitamine, care
n organism sunt transformate n vitamine. Acestea nu au rol plastic sau
energetic ci intervin n reglarea i stimularea principalelor procese
metabolice. Majoritatea vitaminelor alctuiesc coenzime sau cofactori ai
unor enzime. Lipsa sau insuficiena vitaminelor din organism determin
tulburri metabolice i apariia unor boli numite avitaminoze sau
hipovitaminoze, care constituie boli careniale. n plante i animale s-au
identificat unele substane organice care au o aciune fiziologic i
biochimic opus vitaminelor, antivitamine care acioneaz n dou moduri:
sunt analogi structurali ai vitaminelor dar nu posed activitatea biologic a
vitaminelor sau au structur diferit dar acioneaz asupra vitaminelor
inactivndu-le.
Vitaminele au structuri chimice foarte variate, din aceast cauz s-a
fixat drept criteriu de clasicare solubilitatea. Din punct de vedere al
solubilitii, vitaminele se grupeaz n vitamine hidrosolubile (cele cu
molecule polare, solubile n ap) i vitamine liposolubile (cele cu molecule
nepolare) solubile n grsimi.
O alt clasificare a vitaminelor se face dup mecanismul lor de
aciune n vitamine cu funcie de coenzime i vitamine fr funcie de
coenzime. Nomenclatura vitaminelor se poate stabili dup trei criterii: dup
nomenclatura veche, dup rolul fiziologic i dup structura chimic.
Vitaminele liposolubile sunt substane solubile n grsimi, n solveni
organici i insolubil n ap. Din aceast grup fac parte vitaminele A, D, E,
K, i F. Dintre vitaminele hidrosolubile amintim complexul B. Din grupa
vitaminelor B fac parte: vitamina B
1
, B
2,
B
12,
acidul pantotenic,
nicotinamida, acidul paraaminobenzoic, acizii pteroilglutamici, biotina,
mezoinozitolul, colina, etc. Drojdia de bere i cortexul cerealelor conin n
cantitate mare vitamine din complexul B. .
57
Tema nr. 6
ENZIME
Uniti de nvare :
Generaliti despre enzime, structura i specificitatea
enzimelor.
Mecanisme generale de actiune i clasificarea enzimelor
Obiectivele temei :
- Cunoaterea aspectelor biochimice privind structura si specificitatea
enzimelor;
- Studiul mecanismelor de actiune i criterii de clasificare a enzimelor;
- Utilizarea de metode i procedee specifice pentru determinarea
activitii enzimatice
Timpul alocat temei : 2 ore
Bibliografie recomandat :
1. Babeanu C., 2003, - Biochimie vegetal, Ed Universitaria, Craiova
2. Babeanu C., 2010, Biochimie. Manual universitar pentru nvmntul
la distan. Editura Universitaria, Craiova
3. Babeanu C., 2006, Biochimie metabolic, Editura Universitaria, Craiova
4. Campbell P.N, Smith A. D., 2004- Biochimie ilustrat, Ed. Academiei
Romane, Bucuresti
5. Dinu V., Trutia E., Cristea Popa E., Popescu A., 2002, Biochimie
medical, Mic tratat, Ed Medical, Bucuresti,
6. Neamu G., Cimpeanu Ghe., Socaciu C., 1993- Biochimie Vegetal, Ed.
Didactic i Pedagogic Bucureti
6.1 Generaliti despre enzime, structura i specificitatea enzimelor.
Enzimele sunt substane care catalizeaz reaciile biochimice.
Enzimele au un rol fundamental n reglarea proceselor metabolice din
organism. Din punct de vedere chimic enzimele sunt proteine sau proteide
cu rol funcional foarte important. Dup locul unde i manifest activitatea,
enzimele se pot clasifica n exoenzime i endoenzime.
Reinem: Enzimele au toate proprietile catalizatorilor utilizai n
reaciile chimice: acioneaz n cantiti extrem de mici; nu se consum i nu
se transform n reacia catalizat; catalizeaz reacii termodinamic posibile;
nu modific starea final de echilibru a reaciilor ci doar orienteaz i
mresc viteza reaciilor biochimice.
Structura enzimelor
Structura chimic de ansamblu a enzimelor reprezint un aranjament
spaial macromolecular complex determinat de nivelurile de organizare
structural ale proteinelor.
Dup structur enzimele se clasific n dou categorii:
- enzime de natur exclusiv proteic formate numai dintr-o holoproteid
- enzime de natur heteroproteic, formate din dou componente, una de
natur proteic, numit apoenzim i alta de natur neproteic numit
coenzim. mpreun cele dou pri alctuiesc holoenzima.
58
Enzime cu structur proteic
Enzime cu structur proteic sunt relativ puine. n cazul acestor
enzime att legarea substratului ct i cataliza se realizeaz de ctre
gruprile funcionale ale resturilor de aminoacizi. Se caracterizeaz, sub
aspect structural prin existena anumitor zone, denumite situsuri,
caracterizate printr-o anumit secven de aminoacizi i o conformaie
caracteristic, zone care sunt eseniale pentru manifestarea activitii
catalitice (situs catalitic) sau pentru funcia de reglare (situs alosteric).
Observaie: n structura molecular a enzimelor exist anumite
regiuni sau zone, formate dintr-un numr restrns de aminoacizi care se
numesc situs catalitic sau situs activ.
Substratul enzimelor (S) reprezint un compus chimic care se poate lega
specific, la o enzim (E) . n urma aciunii enzimei substratul este
transformat n produi (P)
E+S [ES] E+P
Substratul trebuie s prezinte o dispunere spaial bine definit care
s-i permit accesul la molecula de enzim, s prezinte o complementaritate
structural i conformaional, cu situsul catalitic al enzimei. Enzimele au
capacitatea de a aciona preferenial numai asupra unor anumite substraturi,
proprietate numit specificitate enzimatic.
Unele enzime cu rol de reglare enzimatic, denumite enzime
allosterice conin n molecula lor pe lng situsul catalitic i un al doilea
situs numit situs allosteric. n aceste mecanisme prin interaciuni allosterice
intervine un efector allosteric (activator sau inhibitor) care se leag la situsul
allosteric i moduleaz tranziiile moleculei de enzim ntre diferite
conformaii posibile pe care le poate lua, realizndu-se efectul de reglare
Enzime de natur heteroproteidic
Aceste enzime necesit pentru activitatea lor catalitic, prezena unor
cofactori enzimatici (coenzime, grupri prostetice, metale) Centrul catalitic
reprezint ansamblul gruprilor chimice active care particip efectiv la
reacia catalizat. n cazul enzimelor holoproteice centrul catalitic este
sinonim cu situsul catalitic. n cazul enzimelor heteroproteidice, care
necesit pentru activitatea lor catalitic, prezena unor cofactori, centrul
catalitic include situsul catalitic i regiunea din molecul la care se ataeaz
cofactorul (coenzima i/sau metal). Centrul activ = situs catalitic + coenzim
+ metal
Apoenzime i cofactori enzimatici
Pentru funcia catalitic a enzimelor sunt determinante structura i
organizarea spaial a moleculei proteice care poart situsul catalitic. La
unele enzime, proprietile catalitice sunt date de interacia i cooperarea
dintre componenta proteic i anumite micromolecule sau ioni metalici
numii cofactori. Apoenzima sau cofactorul separat sunt inactive catalitic.
Ele formeaz un complex molecular enzim-cofactor denumit holoenzim,
complex cu activitate catalitic. Cofactorul este indispensabil activitii
catalitice a enzimei iar n unele cazuri o poteneaz. S-a observat c
specificitatea este determinat n totalitate de apoenzime n timp ce
coenzimele sunt gruprile responsabile n cea mai mare parte de
transformarea chimic.
Apoenzim + cofactor = holoenzim
59
Cofactori enzimatici
Reinem Termenul cofactor se utilizeaz pentru totalitatea compuilor
neproteici din structura heteroenzimelor. Termenul coenzim se utilizeaz
numai pentru componentele neproteice de natur organic care se leag prin
legturi foarte slabe, labile de apoenzime i care sunt uor disociabile de
aceast.Termenul de grupare prostetic se utilizeaz tot pentru cofactori de
natur organic dar care se leag de apoenzime prin legturi puternice,
inclusiv covalente.
Sisteme multienzimatice
n cazul unor ci metabolice toate enzimele care catalizeaz reacii
individuale sunt asociate n form de complexe multienzimatice. Enzimele
sunt fixate prin legturi slabe, ntr-o ordine corespunztoare intrrii lor n
aciune, pe o protein central. Se asigur pe ansamblu o vitez mai mare
dect cea corespunztoare aciunii enzimelor neasociate.
Izoenzime
Reinem: O parte din enzimele care au structur cuaternar se prezint sub
mai multe forme moleculare. Pentru o enzim dat, formele moleculare sub
care ea apare se numesc izoenzime. Toate izoenzimele unei enzime
catalizeaz aceeai reacie i i au originea n aceeai celul, esut sau lichid
biologic dintr-un anumit organism. Izoenzimele prezint configuraii
spaiale diferite i se deosebesc ntre ele printr-o serie de proprieti fizico-
chimice (mobilitate electroforetic, compoziie n aminoacizi, cinetic de
reacie, tipuri de inhibiie).
Observaie: Izoenzimele apar din diferene determinate genetic, n structura
primar a enzimei respective. Nu pot fi considerate izoenzime acele forme
moleculare rezultate prin modificarea aceleiai structuri primare.
Specificitatea enzimelor
O proprietate remarcabil a enzimelor este nalta lor specificitate. O enzim
are capacitatea de a selecta numai un substrat sau un numr limitat de
substraturi asupra crora acioneaz condiionnd o reacie bine definit.
Enzimele prezint o specificitate dubl: specificitate de substrat i
specificitate de aciune.
Specificitatea de substrat
Specificitatea de substrat este o proprietate caracteristic enzimelor
i const n capacitatea lor de a aciona preferenial numai asupra unui
anumitor substraturi. Aceast specificitate include mai multe tipuri:
Specificitate absolut
Enzima acioneaz strict asupra unui anumit substrat: de exemplu
enzima ureaza acioneaz numai asupra ureei ca substrat. Ca variante ale
specificitii absolute sunt stereospecificitatea i specificitatea geometric.
Specificitate relativ de grup
Enzima acioneaz asupra unui grup de substane care au o
constituie chimic asemntoare i care conin acelai tip de legtur
chimic.
Specificitate absolut de grup
Enzimele care prezint acest tip de specificitate catalizeaz reacia unui grup
de substrate care conin acelai tip de legtura dar i o anumit structur a
unei pri din substrat.
Specificitate de aciune
Enzimele, n funcie de specificitatea lor pentru substrat i de modul
de aciune asupra acestuia, catalizeaz un anumit tip de reacie, bine
60
determinat. Un substrat sub aciunea unor enzime care catalizeaz reacii
diferite formeaz produi diferii de reacie.
TEST DE EVALUARE
1. . Cum se clasific enzimele dup structura lor chimic?
Rspuns:
Dup structur enzimele se clasific n dou categorii: enzime de natur
exclusiv proteic formate numai dintr-o holoproteid; enzime de natur
heteroproteic, formate dintr-o component de natur proteic si o
component de natur neproteic numit coenzim.
2. Ce este specificitatea enzimatic?
Rspuns:
Exerciii.
Exemplu rezolvat:
1. Care dintre urmtoarele proprieti aparin izoenzimelor?
a) toate izoenzimele unei enzime catalizeaz aceeai reacie
b) i au originea n aceeai celul, esut sau lichid biologic
c) se deosebesc ntre ele printr-o serie de proprieti fizico-chimice
d) izoenzimele apar din diferene determinate genetic,
e) forme moleculare rezultate prin modificarea aceleiai structuri
primare.
Rezolvare: a , b, c, d
De rezolvat:
2. Ce reprezinta centrul catalitic in cazul unei enzime?
a) n cazul enzimelor holoproteice centrul catalitic este sinonim cu
situsul catalitic.
b) reprezint ansamblul gruprilor chimice active care particip
efectiv la reacia catalizat.
c) centrul catalitic include situsul catalitic i regiunea din molecul la
care se ataeaz cofactorul (coenzima i/sau metal)
d) n cazul enzimelor heteroproteidice centrul catalitic este sinonim
cu situsul catalitic.
e) reprezint apoenzima sau cofactorul care separat manifest
activitate catalitic
Rezolvare:
61
6.2 Mecanisme generale de actiune i clasificarea enzimelor
Mecanisme implicate n cataliza enzimatic
S-au emis diferite ipoteze cu privire la mecanismele de interaciune dintre
enzim i subtrat. n orice reacie catalizat enzimatic formarea
intermediarului enzim substrat, [ES] este obligatorie.
Reinem: S-au elaborat dou modele implicate in cataliza enzimatic:
Modelul clasic- lact-cheie consider c potrivirea substratului cu centrul
activ al enzimei este analoag cu potrivirea "lact-cheie". Acest model
presupune o rigiditate a structurii enzimei n zona centrului activ.
Modelul centrului activ indus presupune o flexibilitate a zonei n care acesta
se afl. n enzima liber centrul activ are o configuraie spaial uor diferit
de cea necesar fixrii substratului. Apropierea substratului induce o
modificare conformaional a zonei centrului activ realizndu-se
configuraia optim fixrii.
Observaie: Activatori enzimatici - Activatorii enzimatici influeneaz
pozitiv activitatea enzimatic. Ei i pot exercita aciunea pe diferite ci n
funcie de natura lor. Inhibitori enzimatici - Activitatea multor enzime este
inhibat de compui chimici diveri. n sistemele vii asemenea compui pot
fi de origine endogen (diferii metabolii) sau de origine exogen. Inhibiia
enzimelor poate fi reversibil i ireversibil, aceasta din urm numindu-se
inactivare. Inhibitorii enzimatici pot afecta fie situsul catalitic fie alt
regiune a moleculei de enzim, n ambele cazuri legarea substratului fiind
influenat.
Clasificarea i nomenclatura enzimelor
Uniunea Internaional de Biochimie a decis la cel de-al III-lea Congres
Internaional de Biochimie (Bruxelles, 1955) nfiinarea unei Comisii
Internaionale de Enzimologie a crei sarcin era printre altele elaborarea
unei clasificri i nomenclaturi a enzimelor i coenzimelor. n 1964 a fost
adoptat oficial clasificarea i nomenclatura enzimelor.
Reinem: n funcie de tipul de reacie pe care l catalizeaz, enzimele se
clasific n ase mari clase:
1.oxidoreductaze
2. transferaze
3. hidrolaze
4. liaze
5. izomeraze
6.ligaze sau sintetaze
Enzimele reunite ntr-o anumit clas sunt ulterior clasificate n subclase, i
subsubclase n funcie de unele detalii privind gruprile chimice asupra
crora acioneaz, cofactorii implicai n reacia respectiv. Fiecare enzim
este caracterizat de un cod numeric format din patru cifre, care conine
informaii despre enzima respectiv. Prima cifr din cod indic apartenena
la una din cele ase mari clase de enzime. A doua cifr din codul enzimei
indic subclasele care sunt alctuite dup criterii caracteristice fiecrei clase
(natura substratului transformat, tipul legturii scindate, natura gruprii
transferate, etc. Pentru unele enzime se utilizeaz denumiri empirice, uzuale.
Astfel denumirea multor enzime rezult prin adugarea sufixului az la
numele substratului, exemplu: maltaz are ca substrat maltoza, ureeaza are
ca substrat ureea.
62
TEST DE EVALUARE
1. Ce sunt activatorii enzimatici?
Rspuns
Activatorii enzimatici influeneaz pozitiv activitatea enzimatic i i pot
exercita aciunea pe diferite ci n funcie de natura lor.
2. Care este clasificarea enzimelor n funcie de tipul de reacie pe care
l catalizeaz?
Rspuns:
Exerciii.
Exemplu rezolvat:
1. Care din urmtoarele afirmaii privitoare la modul de actiune al
enzimelor sunt adevrate ?
a) n orice reacie catalizat enzimatic formarea intermediarului
enzim substrat, [ES] este obligatorie.
b) modelul clasic: lact-cheie presupune o rigiditate a structurii
enzimei n zona centrului activ.
c) modelul clasic: lact-cheie presupune o flexibilitate a structurii
enzimei n zona centrului activ.
d) modelul centrului activ indus presupune o flexibilitate a zonei n
care acesta se afl
e) inhibitorii enzimatici pot afecta fie situsul catalitic fie alt regiune
a moleculei de enzim, n ambele cazuri legarea substratului fiind
afectat
Rezolvare: a, b, d, e
De rezolvat:
Care dintre afirmaiile urmtoare sunt adevrate in cazul
mecanismului centrului activ indus?
a) n enzima liber centrul activ are o configuraie spaial uor diferit de
cea necesar fixrii substratului.
b) apropierea substratului induce o modificare conformaional a zonei
centrului activ realizndu-se configuraia optim fixrii.
c) formarea complexului ES se realizeaz prin legarea esteric a substratului
la la situsul alosteric al enzimei
d) mecanismul se bazeaz pe complementaritatea structural reciproc intre
molecula de substart si enzim
e) potrivirea riguroas a substratului la situsul catalitic in enzima liber
conduce la formarea complexului ES
Rezolvare:
63
Rezumatul temei
Enzimele sunt substane care catalizeaz reaciile biochimice. Dup
structur se mpart n dou categorii: enzime de natur exclusiv proteic i
enzime de natur heteroproteic . Enzimele de natur exclusiv proteic se
caracterizeaz prin existena anumitor zone (situsuri) caracterizate printr-o
anumit secven de aminoacizi i o conformaie caracteristic, care sunt
eseniale pentru manifestarea activitii catalitice (situs catalitic) sau pentru
funcia de reglare (situs alosteric). Enzimele de natur heteroproteic
necesit pentru activitatea lor catalitic, prezena unor cofactori enzimatici.
Enzimele au capacitatea de a aciona preferenial numai asupra unor
anumite substraturi, proprietate numit specificitate enzimatic. O enzim
are capacitatea de a selecta numai un substrat sau un numr limitat de
substraturi asupra crora acioneaz condiionnd o reacie bine definit.
Enzimele prezint o specificitate dubl: specificitate de substrat i
specificitate de aciune.
S-au emis diferite ipoteze cu privire la mecanismele de interaciune
dintre enzim i substrat. n orice reacie catalizat enzimatic formarea
intermediarului enzim substrat, [ES] este obligatorie. S-au elaborat dou
modele implicate in cataliza enzimatic: Modelul clasic-lact-cheie
consider c potrivirea substratului cu centrul activ al enzimei este analoag
cu potrivirea "lact-cheie". Modelul centrului activ indus presupune o
flexibilitate a zonei n care acesta se afl. n enzima liber centrul activ are o
configuraie relaxat, diferit de cea necesar fixrii substratului. Apropierea
substratului induce o modificare conformaional a zonei centrului activ
realizndu-se configuraia optim fixrii.
n funcie de tipul de reacie pe care l catalizeaz, enzimele se
clasific n ase mari clase: 1.oxidoreductaze; 2. transferaze; 3. hidrolaze; 4.
liaze; 5. izomeraze; 6.ligaze sau sintetaze
Enzimele reunite ntr-o anumit clas sunt ulterior clasificate n subclase, i
subsubclase n funcie de unele detalii privind gruprile chimice asupra
crora acioneaz.
64
TEST RECAPITULATIV
1. Monoglucidele prezinta izomerie:
a) geometric
b) de caten
c) optic
d) de functiune
e) anomerie
2. Dezoxiglucidele sunt derivati ai monozaharidelor care au :
a) o grupare OH inlocuit cu NH
2
b) o grupare OH inlocuit cu H
c) o grupare H inlocuit cu OH
d) o grupare OH inlocuit cu COOH
e) o grupare C=O inlocuit cu NH
2
3. Amidonul este:
a) substan cu rol informaional
b) substan de rezerv
c) substan de structur
d) eter al glucozei cu alcooli
e) ester al glucozei cu acizi
4. Oxidarea blnd a glucozei formeaz:
a) amestec de acizi zaharici
b) acizi uronici
c) acizi aldonici
d) acizi nucleici
e) amestec de acizi grasi
5. Lipidele simple sunt:
a) gliceride, fosfatide, etolide, cerebrozide
b) ceride, fosfatide, gliceride, etolide,
c) gliceride, etolide, steride, ceride
d) gliceride, fosfatide, sfingolipide
e) gangliozide, gliceride, ceride
6. Apartenena la seria D i L se refer la:
a) sensul de rotatie al luminii polarizate
b) configuraia atomului de carbon asimetric cel mai indepartat de
gruparea carbonil
c) att in funcie de sensul de rotatie al luminii polarizate ct i de
configuraia atomului de carbon asimetric cel mai indepartat de
gruparea carbonil
d) configuratia fiecrui atom de carbon asimetric
e) ) configuraia atomului de carbon asimetric cel mai apropiat de
gruparea carbonil
7. Dintre cele trei structuri prezentate mai jos structura D(-)
fructofuranozei este:
C
C
C
C
C
C
OH
H
OH
OH
OH
H
2
HO
H
H
H
2
O
H
2
H
H
HO
H
2
OH
OH
H
OH
C
C
C
C
C
C
H
2
H
H
HO
H
2
OH
OH
H
OH
C
C
C
C
C
C
O
O
1 2
3
65
a) 1 si 3 b) 2 si 3 c) 1 si 2 d) 1 e) 3
8. Urmtoarea structur reprezint:
a) maltoz b) celobioz c) zaharoz d) lactoza e)
galactoza
9. La hidroliza bazic a grsimilor alturi de glicerin rezult:
a) spun
b)amestec de sruri de sodiu ale acizilor grai
c) acizi grai liberi
d) lipide complexe
e) lecitine
10. Monoglucidele sunt compusi care au in molecula lor:
a) o grupare carbonil si o grupare alcool
b) o grupare carbonil si mai multe grupri carboxil
c) mai multe grupri hidroxil i o grupare carbonil
d) o grupare aldehidica sau cetonica si mai multe grupari hidroxil
e) mai multe grupri hidroxil i o grupare amino
11. Structura secundar a unei proteine :
a) este determinat de numrul, felul, proporia i secvena
aminoacizilor constitueni;
b) arat conformaia lanurilor polipeptidice
c) reprezint formula chimic a proteinei
d) este determinat de tipul fortelor care stabilizeaza protomerii
e) arat conformaia lanurilor polinucleotidice
12. Din punct de vedere chimic acizii nucleici sunt formai din:
a) o baz anorganic, o pentoz i acid fosforic
b) o baz azotat si o pentoz
c) o baz azotat, o pentoz i acid fosforic
d) o baz anorganic, o molecula de glucid cu 6 atomi carbon i
acid fosforic
e) o baz organic, o molecula de glucid cu 6 atomi carbon i acid
fosforic
13. O baz purinic de pe o caten ADN stabilete legturi de hidrogen
intercatenare:
a) numai cu o baz purinic de pe celalalt caten;
b) numai cu o baz pirimidinic de pe celalalt caten;
c) att cu o baz purinic ct i cu o baz pirimidinic de pe cealalt
caten
d) numai cu o pentoza de pe celalalt caten;
e) att cu o baz purinic ct i cu o pentoza de pe cealalt caten
14. Molecula de ARN are:
a) structur monocatenar
b) structur dublu catenar
c) structur n straturi pliate
d) structura helicoidala
e) structura care prezinta izomerie geometrica (cisd-trans)
H
HO
OH CH2
H
OH
H OH
H
O
H
HO
OH CH2
H
OH
H OH
H
O
H O
H
66
15. Molecula de ADN are:
a) structur monocatenar
b) structur dublu catenar
c) structur n straturi pliate
d) structura helicoidala
e) structura care prezinta izomerie geometrica (cisd-trans)
16. Urmatoarea formula reprezinta:
CH
2
O COR
|
R -OCOCH O
|
CH
2
OP OCH
2
CHCOOH
| |
O + NH
3
a) lecitina b) cefalina c) serinfosfatida d) acid fosfatidic e) sfingozina
17. Urmatoarea formula reprezinta:
CH2 OCOR
|
R OCO C- H O
|
CH2 O P -
2 2 2
NH CH CH O
|
OH
a) lecitina b) cefalina c) serinfosfatida d) acid fosfatidic e) sfingozina
18. Principalele nucleotide din structura ARN sunt:
a) citidin-5' monofosfat (CMP) uridin 5'monofosfat (UMP), adenozin
5'-monofosfat (AMP) i guanozin-5' monofosfat (GMP)
b) uridin-5'-monofosfat (UMP), adenozin-5'-monofosfat (AMP) i
guanozin-5'-monofosfat (GMP)
c) citidin-5' monofosfat (CMP) uridin 5'monofosfat (UMP), adenozin
5'-monofosfat (AMP) i timidin-5'-monofosfat (TMP)
d) dezoxiuridin-5'-monofosfat (dUMP), dezoxiadenozin-5'-monofosfat
(dAMP) i dezoxiguanozin-5'-monofosfat (dGMP)
e) dezoxicitidin-5' monofosfat (dCMP) dezoxitimidin-5'monofosfat
(dTMP), dezoxiadenozin-5'-monofosfat (dAMP) dezoxiguanozin-
5'monofosfat (dGMP)
19. Vitaminele sunt:
a) substante de origine exogen indispensabile pentru cresterea si
dezvoltarea vieuitoarelor
b) substane care intervin in stimularea i reglarea principalelor
procese metabolice
c) substante care exercit rol de coordonare si reglare la nivelul
intregului organism
d) substante care in anumite conditii anuleaz sau suprim activitatea
unei enzime
e) substante care indeplinesc rol plastic si energetic
67
BIBLIOGRAFIE
6. Babeanu C., 2003, - Biochimie vegetal, Ed Universitaria, Craiova
7. Babeanu C., 2010, Biochimie. Manual universitar pentru nvmntul
la distan. Editura Universitaria, Craiova
8. Babeanu C., 2006, Biochimie metabolica, Editura Universitaria,
Craiova
9. Campbell P.N, Smith A. D., 2004- Biochimie ilustrat, Ed. Academiei
Romane, Bucuresti
10. Cristea Popa E., Popescu A., Truia E., Dinu V., 1991, Tratat de
biochimie medical, Ed Medical, Bucuresti
11. Dinu V., Trutia E., Cristea Popa E., Popescu A., 2002, Biochimie
medical, Mic tratat, Ed Medical, Bucuresti
12. Dumitru I. F., Biochimie, 1980, Ed Didactic si Pedagogic, Bucuresti
13. Grban Z., 1999, Biochimie Tratat comprehensiv, vol I, ediia 2, Ed.
Didactic i Pedagogic Bucureti
14. Garban Z. 1981, Tratat elementar de biochimie, Ed Mirton Timisoara
15. Glodeanu E., 1997 - Biochimie Metabolica, Ed Gorjeanul
16. Leninger A.L., 1987, Biochimie, vol. I, Ed. Tehnic, Bucureti
17. Leninger A.L., 1992, Biochimie, vol. II , Ed. Tehnic, Bucureti
18. Marinescu G., Glodeanu E., 1995- Biochimie General, Ed.
Universitaria, Craiova
19. Neamu G., Cimpeanu Ghe., Socaciu C., 1993- Biochimie Vegetal, Ed.
Didactic i Pedagogic Bucureti.
S-ar putea să vă placă și
- BiochimieDocument14 paginiBiochimieOvidiu GhitaÎncă nu există evaluări
- Dezvoltarea Aparatului ReproducaorDocument2 paginiDezvoltarea Aparatului ReproducaorAndreea VieruÎncă nu există evaluări
- Oasele Si MuschiiDocument60 paginiOasele Si MuschiiPetru Enea100% (1)
- Farmacognozie Produse FarmaceuticeDocument25 paginiFarmacognozie Produse FarmaceuticeVladÎncă nu există evaluări
- Referat 1. Metabolismul Materiei VIIDocument6 paginiReferat 1. Metabolismul Materiei VIILavinia KostovÎncă nu există evaluări
- .CELULA Tesuturi, LECTIIDocument15 pagini.CELULA Tesuturi, LECTIIAdelle BioÎncă nu există evaluări
- Curs AMG 13 - Sistem Endocrin HemolimfaticDocument24 paginiCurs AMG 13 - Sistem Endocrin HemolimfaticAndreea Gheorghiță100% (1)
- Compusii OrganiciDocument30 paginiCompusii OrganiciLifeStyle of TobyÎncă nu există evaluări
- Exemple de PH-metre, Spectrofotometre EtcDocument7 paginiExemple de PH-metre, Spectrofotometre Etcghinitaflorin100% (1)
- Reglarea Nervoasa Si Umorala A Activitatii UrineiDocument20 paginiReglarea Nervoasa Si Umorala A Activitatii UrineiAdelina Cadar100% (1)
- Sistemul ExcretorDocument11 paginiSistemul ExcretorElena DeduÎncă nu există evaluări
- Sistemul OsosDocument19 paginiSistemul Ososmihaelaborza90Încă nu există evaluări
- SangeleDocument3 paginiSangeleely_ely3395Încă nu există evaluări
- Tesutul MuscularDocument6 paginiTesutul MuscularSorina SmarandoiuÎncă nu există evaluări
- UreterDocument4 paginiUreterRoxanaÎncă nu există evaluări
- ProteineDocument3 paginiProteineAnnaMincaÎncă nu există evaluări
- EnzimeleDocument3 paginiEnzimeleBianca CiobanuÎncă nu există evaluări
- Aminoacizii BiochimiaDocument62 paginiAminoacizii BiochimiaTatiana Manic MunteanuÎncă nu există evaluări
- COAPSADocument51 paginiCOAPSACorina Lovin100% (1)
- Aminoacizi NaturaliDocument16 paginiAminoacizi NaturaliDaniel Ionuț BogdanÎncă nu există evaluări
- Dezvoltarea Aparatului ExcretorDocument3 paginiDezvoltarea Aparatului ExcretorAna-Maria AvadaneiÎncă nu există evaluări
- Sistemul NervosDocument24 paginiSistemul NervoslpdeeaÎncă nu există evaluări
- Biofizică 1Document28 paginiBiofizică 1Crina ClimaÎncă nu există evaluări
- Curs VizualDocument31 paginiCurs VizualLarisa P. OanceaÎncă nu există evaluări
- Maduva Spinarii Si Nervii SpinaliDocument9 paginiMaduva Spinarii Si Nervii SpinalinetprintÎncă nu există evaluări
- Schimbul de Gaze În PlămîniDocument23 paginiSchimbul de Gaze În PlămîniEva MeLLiSSa100% (1)
- RenalDocument24 paginiRenalMelina PopescuÎncă nu există evaluări
- Leuco Cite LeDocument5 paginiLeuco Cite LeciprianÎncă nu există evaluări
- Fiziologie TotDocument45 paginiFiziologie TotPasvantu DanielÎncă nu există evaluări
- EicosanoiziiDocument7 paginiEicosanoiziiAndreea ChiochiuÎncă nu există evaluări
- Sinteza AGDocument71 paginiSinteza AGConstantin UntilaÎncă nu există evaluări
- Fiziologia Analizatorului OpticDocument3 paginiFiziologia Analizatorului OpticAlexandru MituÎncă nu există evaluări
- 4 Inhibitia EnzimaticaDocument4 pagini4 Inhibitia EnzimaticaDragan StefanÎncă nu există evaluări
- Met Intermediar Al Proteinelor Simple Si CromoproteinelorDocument96 paginiMet Intermediar Al Proteinelor Simple Si CromoproteinelorIuliana MîrzaÎncă nu există evaluări
- Reglarea Activitatii InimiiDocument1 paginăReglarea Activitatii InimiiMusgociu NelaÎncă nu există evaluări
- Subiectul 10 Rectul - Configuratie Externa Si Interna, Structura, Vascularizatie, InervatieDocument5 paginiSubiectul 10 Rectul - Configuratie Externa Si Interna, Structura, Vascularizatie, InervatieNicusor OnaciuÎncă nu există evaluări
- Sistemul DigestivDocument7 paginiSistemul DigestivGurgu Ana-MariaÎncă nu există evaluări
- Metabolismul ProteinelorDocument12 paginiMetabolismul ProteinelorCalin-Sorin CimpeanuÎncă nu există evaluări
- Fiziologie SangeleDocument28 paginiFiziologie SangeleLorincz MartaÎncă nu există evaluări
- Subexlpmed10-11-Rezolvate BiochimieDocument8 paginiSubexlpmed10-11-Rezolvate BiochimieAndreea PatrascuÎncă nu există evaluări
- Referat - Microbiologie (Genul Vibrio)Document5 paginiReferat - Microbiologie (Genul Vibrio)Delia W.Încă nu există evaluări
- 4 Proteine Si AminoaciziDocument3 pagini4 Proteine Si AminoaciziMazilu CatalinaÎncă nu există evaluări
- SangeleDocument11 paginiSangelePopoiu GeorgeÎncă nu există evaluări
- C6 Microcirculatia Si Sistemul LimfaticDocument4 paginiC6 Microcirculatia Si Sistemul LimfaticcnajesrnasiferfÎncă nu există evaluări
- 14 Telencefal-Comformatie ExternaDocument5 pagini14 Telencefal-Comformatie ExternaMarian Dan IngridÎncă nu există evaluări
- Oase Si ArticulatiiDocument14 paginiOase Si ArticulatiiFlorina BodenciuÎncă nu există evaluări
- HapteneDocument1 paginăHapteneDana CopoiuÎncă nu există evaluări
- Curs 9 Biochimie Anul I MedicinaDocument75 paginiCurs 9 Biochimie Anul I MedicinaAlexandru BarbuÎncă nu există evaluări
- GlucideDocument4 paginiGlucideAaron CallahanÎncă nu există evaluări
- Glucide 1Document60 paginiGlucide 1Oleg CojocariÎncă nu există evaluări
- Glucide - Curs 1, 2, 3, 4Document55 paginiGlucide - Curs 1, 2, 3, 4Vasilica BoghiuÎncă nu există evaluări
- Referat ChimieDocument6 paginiReferat ChimieFilip CatalinÎncă nu există evaluări
- Glu FinDocument68 paginiGlu FinGheorghiu-Ichimescu Oana-MihaelaÎncă nu există evaluări
- GlucideleDocument24 paginiGlucideler_raoullÎncă nu există evaluări
- 1 GLUCIDE Biochimia Descriptiva 2016Document42 pagini1 GLUCIDE Biochimia Descriptiva 2016Lilia LiliaÎncă nu există evaluări
- GlucideleDocument34 paginiGlucideleromangaidarÎncă nu există evaluări
- Curs Glucide Si Lipide - 9.01.2017Document306 paginiCurs Glucide Si Lipide - 9.01.2017Corina Druta100% (1)
- Biochimie GlucideDocument22 paginiBiochimie GlucideDeny CrÎncă nu există evaluări
- Definitia Si Clasificarea GlucidelorDocument7 paginiDefinitia Si Clasificarea GlucidelorCojocaru LaurențiuÎncă nu există evaluări
- CURS 3 BIOCHIMIE MD GlucideleDocument63 paginiCURS 3 BIOCHIMIE MD GlucideleSimonaBlechschmidtÎncă nu există evaluări
- Casa1 Din BusteniDocument2 paginiCasa1 Din BusteniDorin Hagatis DrancaÎncă nu există evaluări
- Medicina in Egiptul Antic3Document4 paginiMedicina in Egiptul Antic3Dorin Hagatis DrancaÎncă nu există evaluări
- InformaqticaDocument11 paginiInformaqticaDorin Hagatis DrancaÎncă nu există evaluări
- VitamineDocument4 paginiVitamineDorin Hagatis DrancaÎncă nu există evaluări
- Ĺžcoala PostlicealÄ SanitaraDocument1 paginăĹžcoala PostlicealÄ SanitaraDorin Hagatis DrancaÎncă nu există evaluări
- ComunicareDocument6 paginiComunicareDorin Hagatis DrancaÎncă nu există evaluări
- 409 AfumatiDocument1 pagină409 AfumatiDorin Hagatis DrancaÎncă nu există evaluări
- Enzime Digestive Hormoni Estrogeni Prezentare in Farmacii PDFDocument0 paginiEnzime Digestive Hormoni Estrogeni Prezentare in Farmacii PDFDorin Hagatis DrancaÎncă nu există evaluări
- Enzime Digestive Hormoni Estrogeni Prezentare in Farmacii PDFDocument0 paginiEnzime Digestive Hormoni Estrogeni Prezentare in Farmacii PDFDorin Hagatis DrancaÎncă nu există evaluări
- 182 Institutul OncologicDocument1 pagină182 Institutul OncologicAnonymous QX0AmTD2pWÎncă nu există evaluări
- Termostat Computherm 091 - Manual UtilizareDocument7 paginiTermostat Computherm 091 - Manual Utilizareaurel_v100% (1)
- ProiectDocument13 paginiProiectDorin Hagatis DrancaÎncă nu există evaluări
- Buna ZiuaDocument73 paginiBuna ZiuaDorin Hagatis DrancaÎncă nu există evaluări