Documente Academic
Documente Profesional
Documente Cultură
Crestere
Încărcat de
Mădălina Mihalache0 evaluări0% au considerat acest document util (0 voturi)
42 vizualizări12 paginiCrestere
Drepturi de autor
© © All Rights Reserved
Formate disponibile
DOCX, PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentCrestere
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOCX, PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
42 vizualizări12 paginiCrestere
Încărcat de
Mădălina MihalacheCrestere
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOCX, PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 12
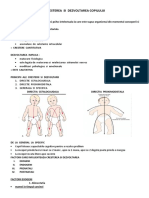
CREŞTEREA ŞI DEZVOLTAREA NORMALĂ
Definiţie. Creşterea este un proces de dezvoltare somatică, un fenomen cantitativ cu acumulare de
masă prin multiplicare celulară, începând din momentul concepţiei şi până la sfârşitul adolescenţei.
Diferenţierea este un fenomen calitativ, dinamic, un proces de maturare legat de diferenţierea
structurilor, celulară şi moleculară, şi de perfecţionarea, de reglarea fiziologică a funcţiilor.
Dezvoltarea însumează ambele fenomene într-un mod armonios, fiind somatică, psihică şi sexuală.
Organismul va atinge norma adultului, fiind capabil să-şi protejeze produsul de concepţie.
Ştiinţa care studiază dezvoltarea organismelor se numeşte auxologie.
Etapele cronologice ale dezvoltării normale:
1. etapa embrionară – implică doar procesul de multiplicare şi diferenţiere celulară în care din celula-ou se
edifică succesiv toate varietăţile celulare, apoi ţesuturile şi organele;
2. etapa fetală – între săptămânile 11 şi 41 de viaţă intrauterină au loc procese de creştere şi maturare
funcţională;
3. etapa postnatală – cuprinde 4 subetape:
a. o creştere rapidă de la naştere (50 cm) până la 4 ani (100 cm);
b. o creştere constantă (5-6 cm/an) până în perioada prepubertară;
c. un salt statural marcat (15-20 cm) în perioada pubertară;
Reglarea creşterii somatice. Este dependentă de intercorelarea funcţională a 4 factori:
1.Genomul - efectul său asupra creşterii este multifactorial şi poligenic; indivizii cu formulă gonozomială XY sunt
mai înalţi decât indivizii XX.
2. Sistemul endocrin - este factorul esenţial al procesului de creştere celulară, proces ce înglobează
diferenţierea, multiplicarea sau transformarea aberantă (cancerogeneza):
a. hormonul de creştere (GH) - eliberarea GH în circulaţie este rezultanta balanţei funcţionale dintre
somatocrinină (GH-RH) cu rol stimulator şi somatostatină (SMS) cu rol inhibitor. GH circulă în plasmă legat de
proteine de transport şi îşi exercită efectul prin intermediul somatomedinelor (SM), factori de creştere de tip
insulinic (IGF–„insulin-like growth factors”), care se sintetizează la nivel hepatic sub controlul GH. Două dintre
somatomedine sunt mai active:
– somatomedina C sau IGF-I, a cărei sinteză şi acţiune este controlată de STH;
– IGF-II, responsabilă şi de reglarea creşterii fetale.
Sistemul GHRH-GH-IGF este mecanismul principal de stimulare a cartilajului de creştere şi a
anabolismului în general. Anomaliile cantitative/calitative ale GH, IGF şi sistemului receptor pot sta la
baza unor tulburări de creştere.
Reglarea secreţiei hormonului somatotrop
b. hormonii tiroidieni - prezintă un efect general permisiv pentru acţiunile multor hormoni, inclusiv GH. Lipsa
hormonilor tiroidieni duce la o diminuare notabilă a conţinutului hipotalamic în GH-RH, cu diminuarea secreţiei
de GH. Deficitul de hormoni tiroidieni are impact în special la nivelul ţesutului osos şi al celui nervos. Ţinta
osoasă este reprezentată de epifiza oaselor lungi. Intervenţia se face asupra pregătirii cartilajului seriat pentru
acţiunea somatomedinelor. Hormonii tiroidieni stimulează apariţia punctelor de osificare, activează procesul de
osificare subperiostală, creşterea în lungime şi lăţime, sudura cartilajelor de creştere. Copiii hipertiroidieni
cunosc o accelerare a creşterii şi maturării osoase.
c. steroizii sexuali - au efect asupra creşterii prin realizarea, odată cu pubertatea, a unui „nivel sexual” de
secreţie a GH, diferit pentru cele 2 sexe, precum şi prin acţiunea directă asupra cartilajului de creştere. Efectul
lor pozitiv asupra creşterii este tranzitor, determinând totodată maturarea accelerată a cartilajelor de creştere
şi încheierea creşterii.
d. glucocorticoizii - au un efect dual asupra secreţiei de GH. În excesul secretor de tip „acut”, glucocorticoizii au
efect de tip stimulator la nivel hipofizar. În excesul cronic (corticoterapie, exces secretor) efectul este de tip
inhibitor, potenţând la nivelul hipotalamusului eliberarea de SMS. De asemenea, glucocorticoizii au efect
inhibitor şi asupra sintezei şi acţiunilor IGF-I.
e. alţi factori hormonali de creştere - sunt substanţe polipeptidice cu greutate moleculară mică. Se mai numesc
şi „factori de creştere tisulară”. Ei operează prin mecanisme autocrine, paracrine şi endocrine asupra creşterii şi
dezvoltării normale, diferenţierii embrionare, cicatrizării, etc.
Factori de crestere tisulara
3. Factorii metabolici - procesul de creştere presupune reglaje metabolice complexe în limitele homeostaziei.
Anumite constante metabolice (glicemia, nivelul acizilor graşi liberi, nivelul unor aminoacizi) devin factori
operaţionali asupra procesului de creştere şi dezvoltare.
4.Mediul bio-psiho-social - efortul fizic dirijat poate fi folosit ca metodă de explorare a secreţiei de GH. Efortul
fizic excesiv este factor de stagnare staturală.
Confortul psihic este o condiţie strict necesară unei dezvoltări somatice corecte. Carenţa afectivă
psihosocială, privarea de afecţiunea maternă, condiţiile improprii de microclimat sunt responsabile de
scăderea amplitudinii „peak-urilor” nocturne ale secreţiei de GH, ducând la apariţia nanismului
psihosocial.
Evaluarea creşterii somatice
Biometria clinică – parametrii măsuraţi sunt:
a. Talia – definirea hipostaturii necesită compararea taliei copilului cu standardele antropometrice de înălţime
pentru fiecare vârstă şi sex (tabel 4.3), luând în calcul şi ritmul normal de creştere staturală (tabel 4.2).
Tabel 4.2 Ritmul normal de creştere staturală
Tabel 4.3 Standarde antropometrice (statura si greutate) la copiii din Romania
Standarde antropometrice (statura si greutate) la copiii din Romania
Aceste standarde includ media aritmetică şi deviaţia standard (DS) ca măsură a abaterii de la medie. O
abatere de 2 DS sub medie este o întârziere staturală ce trebuie investigată. O abatere de 3 DS
defineşte nanismul.
Metoda percentilelor (fig. 4.1) raportează parametrii măsuraţi la curbe grafice reprezentând media
valorilor stabilite statistic în funcţie de vârstă şi sex, pe eşantioane populaţionale. Percentila 10 ar indica
o hipostatură patologică, iar percentila 3 defineşte nanismul.
Curbe grafice de apreciere a dezvoltarii somatice prin metoda percentilelor
Aprecierea periodică a vitezei de creştere are drept scop evidenţierea unei modificări a acesteia (deficit
sau exces).
b. Proporţiile corporale - se apreciază armonia proporţiilor corporale măsurând: segmentul corporal superior
(distanţa vertex–pubis), segmentul corporal inferior (distanţa pubis–sol), perimetrele corporale, diametrele,
greutatea, etc. Tulburarea de creştere poate fi caracterizată ca fiind armonică sau dizarmonică.
c.Aprecierea procesului de maturare – se face cuantificând:
1. maturarea osoasă – prin efectuarea unei radiografii de pumn (fig. 4.2) cu aprecierea vârstei osoase (nucleii
osoşi ai carpului, metacarpului, falangelor, epifizei distale a radiusului, cubitusului, cartilajul de creştere, etc.)
(tabel 4.4; fig. 4.3).
3. maturarea sexuală – cu aprecierea dezvoltării organelor genitale externe, a pilozităţii pubiene şi axilare, a
sânilor la fete; se notează vârsta primei menstre la fete şi volumul testicular la băieţi. Ritmul maturării
pubertare este invers proporţional cu viteza de creştere.
4. Maturarea neuro-psihica - se apreciaza psihologic :
- indicele de inteligenta (IQ)
- ideatia
- capacitatea asociativa
- creativitatea
- afectivitatea.
HIPOTROFIA STATURALĂ
Clasificarea hipostaturii (după C. Rosenfeld - modificat):
I. Deficitul primar de creştere (anormalitatea intrinsecă de creştere a tuturor ţesuturilor):
A.Displazii scheletice:
1. Cu creştere disarmonică:
– Picnodisostoza
– Disostoza cleidocraniană
– Sindromul Kenny
– Osteopetroza (Albers-Schönberg)
– Distrofia triho-rino-falangiană
– Pseudo-pseudo-hipoparatiroidismul
2. Cu creştere disproporţionată:
– Acondroplazia
– Hipocondroplazia
– Nanismul distrofic
– Displazia hipofizară multiplă
– Discondrostenoza
– Sindromul Nievergeit
– Displazia spondiloepifizară
– Disostoza metafizară
– Exostoza multiplă ereditară
– Encondromatoza
– Osteogeneza imperfectă
– Amelia
– Hemimelia
– Focomelia
3. Boli câştigate:
– Cifoza (morbul Pott, etc)
– Scolioza
B. Boli cromozomiale:
– Sindromul Turner
– Sindromul Down
– Deleţia braţului lung al cromozomului 18
– Trisomia 18
– Trisomia 13-15
C. Sindroame dismorfice asociind statură joasă prin deficit primar de creştere:
– Sindrom Aarskorg
– Sindrom Bloom
– Sindrom Cockayne
– Sindrom Cornelia de Lange
– Sindrom Ellis van Creveld
– Leprosonism
– Sindrom Noonan
– Sindrom Prader-Willi
– Progeria (Gillford)
– Sindrom Rubinstein - Taybi
– Sindrom Russel - Silver
– Sindrom Seckel
D. Intârzieri de creştere intrauterină:
– Carenţă nutritivă maternă
– Iradiere pe parcursul sarcinii
– Infecţii (rubeolă, toxoplasmoză, HIV)
– Droguri teratogene (alcool, nicotină, narcotice)
– Alterări placentare
– Cauze necunoscute
E. Iradierea cartilajului de creştere
F. Talie mică familial
II. Deficit secundar de creştere
A. Malnutriţie
1. Aport exogen scăzut cantitativ şi/sau calitativ
2. Malabsorbţie
B. Boli cronice (pulmonare, cardiace, hepatice, hematologice, infecţioase, etc)
C. Privare afectivă
D. Tulburări endocrine:
1. Deficit al hormonului de creştere
a. Deficit izolat, de cauză genetică (genă/gene alterată/alterate, neuroni neurosecretori lezaţi):
Tip I - cu ereditate autozomal recesivă:
– IA - fără GH circulant
– IB - cu GH circulant
Tip II - cu ereditate autozomal dominantă
Tip III - cu ereditate recesivă legată de
cromozomul X
Tip IV - cu prezenţa de GH bioinactiv / polimerizat
b. De cauză organică:
– Leziuni intracraniene:
tulburări de dezvoltare
disgenezie hipofizară
anomalii de structurare anatomică a liniei mediane
– Tumori:
craniofaringiom
gliom de chiasmă optică
pinealom ectopic
adenom hipofizar
– Reticuloendotelioze:
boala Hand-Schuler-Christian
histocitoza X
– Traumatisme
– Radioterapie
– Infecţii
c. De cauză pseudohipofizară (GH normal sau crescut)
– Cu somatomedine scăzute
sindrom Laron cu 2 variante:
– absenţa receptorului GH în ficat
– absenţa proteinei de transport a GH
malnutriţie
defect de generare a IGF dar cu STH normal - pigmeii africani
– Cu somatomedine crescute:
nanism hipersomatomedinic
– sindrom Lanes-Bierrick
– insuficienţă renală - rezistentă la acţiunea somatomedinelor prin acumulare
2. Hipotiroidism
a. Agenezie tiroidiană
b. Disgenezie tiroidiană
c. Vicii congenitale de hormonogeneză
tiroidiană
3. Diabet zaharat - sindrom Mauriac
4. Hipercorticism primar sau iatrogen
– sindrom Cushing ACTH dependent
– corticoterapie prelungită (astm, reumatism cardio-articular, leucoze, sindrom nefrotic)
5. Pubertate şi pseudopubertate precoce:
– Idiopatică
– simptomatică
– sindrom adrenogenital congenital
6. Deficitul hormon-vitaminelor D
– rahitism vitaminorezistent
– rahitism vitaminodependent
– hipofosfatazia
– rahitism comun carenţial
E.Alterări metabolice:
1. Osteodistrofia renală:
– Acidoza tubulară renală
– Fosfoglucoaminoaciduria
2. Hiperfosfatazia
3. Mucopolizaharidoze
– Sindrom Hurler
– Sindrom Hunter
– Sindrom San Filippo
– Sindrom Morquio
– Sindrom Schere
– Sindrom Maroteaux - Lamy
– Gangliozidoza generalizată
4. Erori metabolice congenitale ale:
– Metabolismului proteic
– Metabolismului hidrocarbonat
– Metabolismului lipidic
NANISMUL ENDOCRIN
10% din cazurile de nanism sunt de cauză endocrină, iar jumătate din acestea sunt corelate patologiei
hormonului somatotrop.
Nanism hipotalamo-hipofizar - aspect clinic
Nanism hipotalamo-hipofizar - habitus clinic
Nanism hipotalamo-hipofizar - habitus clinic
Tablou paraclinic
A. Biochimic:
– hipoglicemie;
– balanţă azotată negativă;
– lipide serice normale sau uşor crescute.
B.Radiologic:
– vârstă osoasă întârziată faţă de cea cronologică;
– cartilaje de creştere deschise până la 20-30 ani;
– ţesut osos radiotransparent;
– morfologie selară variată (şa mică / mare / asimetrică);
– calcificări supra- sau intraselare;
– slabă pneumatizare a sinusurilor feţei.
Radiologic
C. Hormonal:
– dozarea bazală a GH seric;
– teste de provocare care explorează rezervele stimulabile de GH;
– măsurarea nivelului IGF-I seric.
Metode de investigare a secreţiei/acţiunii GH
Metode de investigare a secreţiei/acţiunii GH
Metode de investigare a secreţiei/acţiunii GH
Forme de nanism hipotalamo-hipofizar
A. Nanismul somatopenic – deficit izolat de GH sau asociat altor tropi hipofizari. Nivelul bazal al GH este
scăzut şi nu creşte după testele de provocare. IGF-I este scăzut.
B. Nanismul somatogenic – apare prin:
– anomalii de număr şi amplitudine ale pulsurilor secretorii ale somatoliberinei;
– GH bioinactiv (nu este recunoscut de propriul receptor);
– GH polimerizat (cu structură modificată, inactiv).
C. Nanismul pseudohipofizar – prin rezistenţa periferică la efectele GH. Este o patologie de receptor hormonal
(nanismul Laron, nanismul Lanes-Bierich, pigmeii).
Alte nanisme endocrine:
Caracteristic, se pierde armonia proporţiilor corporale.
Nanism disarmonic hipotiroidian
Fig. 4.7. Radiografie nuclei osoşi carpieni la un copil de 5 ani cu mixedem congenital netratat
b.Diabetul zaharat defectuos controlat (sindrom Mauriac).
c. Hipercorticismul metabolic (endogen – Cushing, exogen - iatrogen).
d. Hiperparatiroidismul şi în special pseudohiperparatiroidismul produc deficitul statural dismorfic, cu facies „în
lună plină”, membre scurte, brahidactilie, brahimetacarpie, brahimetatarsie, obezitate centripetă.
e. Pubertatea şi pseudopubertatea precoce (cu închidere precoce a cartilajelor de creştere).
f. Deficitul de vitamina D (de aport, de generare, de recepţie).
Nanism prin deficit al hormon-vitaminelor D
g. Deficitul reversibil de STH (rar - în Cushing-ul iatrogen, după ablaţia unui adenom hipofizar).
ALTE CAUZE DE NANISM
1.Nanismul hipocaloric (de cauze nutriţionale sau digestive).
2.Nanismul din suferinţe cronice (pulmonare, cardiace,renale, anemii, ciroză hepatică).
3.Nanismul din bolile metabolice.
4.Nanismul de origine osoasă.
5.Nanismul psihosocial (de stres cronic).
6.Întârzierea constituţională a creşterii şi dezvoltării:
a) prin pubertate întârziată;
b)esenţial genotipic – componentă genetică familială sau individuală.
7. Nanisme rare cu etiologie neprecizată.
Nanism disarmonic de cauză osoasă
Nanism psihosocial
Exemplu: nanismul progeroid.
Exemplu: nanismul progeroid.
Tratamentul hipotrofiei staturale
Bolile care pot fi influenţate favorabil prin tratament sunt:
unele forme de tulburări secretorii de GH;
întârzierea de maturare şi creştere;
talia mică familială;
sindromul Turner, acondroplazia.
Tratamentul poate fi făcut cu:
1. GH sintetic – obţinut prin recombinare genică;
2. substanţe ce cresc producţia endogenă de GH;
3. medicamente anabolizante.
1.Tratamentul cu GH sintetic
Administrarea este i.m. sau s.c.:
5-20 ui/m2/săptămână, sau
0,1-0,3 ui/kg, administrări zilnice sau intermitente.
După 3-4 ani de tratament, efectul promotor al creşterii diminuă chiar dacă se foloseşte aceeaşi doză.
Efectele secundare ale tratamentului cu GH sunt multiple (abcese locale, HTA, cardiomiopatie
hipertrofică, retenţie hidrică cu albuminurie, stimularea creşterii tumorale, etc.). Nanismul hipofizar de
cauză tumorală reprezintă contraindicaţia majoră a tratamentului cu GH sintetic!
Nanism somatopenic tratat substitutiv
Nanism somatopenic tratat substitutiv
2. Tratamentul cu substanţe ce cresc producţia endogenă de GH
Se folosesc:
GH-RH sintetic
Clonidină
Levo-dopa
Dopamină
Arginină
Propranolol
Rezultatele terapeutice sunt modeste.
3. Tratamentul cu substanţe anabolizante
Substanţele anabolizante sunt steroizi de sinteză cu structură asemănătoare testosteronului. Ele
stimulează sinteza proteică în general, inclusiv în cartilajele de creştere.
Efecte adverse: hirsutism, virilizare somatică (clitoromegalie), precipitarea pubertăţii, avansarea vârstei
osoase spre sudura cartilajelor de creştere.
EXCESUL DE DEZVOLTARE SOMATICĂ
Un exces statural de 2 DS în raport cu media, defineşte o accelerare patologică a creşterii.
Un exces de peste 3 DS faţă de medie defineşte gigantismul.
Entităţi:
A. Statura supranormativă constituţională – este de regulă o caracteristică a întregii familii. Valorile
serice ale factorilor de creştere hormonali sunt normale.
Macrosomie şi fizionomie acromegaloidă constituţional familiale
B. Statura supranormativă patologică:
Gigantoacromegalie prin somatotropinom la un pacien în vârstă de 24 ani
Clinic, gigantismul hipofizar poate fi:
pur – exces numai de GH (rar);
asociat cu: hipogonadism / insuficienţă hipofizară pluritropă.
Paraclinic:
aprecierea GH bazal, după inhibiţie (hiperglicemie provocată) sau stimulare (insulină,
Propranolol);
IGF-I este crescut;
glicemia este crescută;
hidroxiprolina urinară, calciuria şi osteocalcina serică sunt crescute (urmare a intensificării turn-
over-ului osos);
modificări radiologice ale şeii turceşti (balonizare, erodare) şi ale scheletului (osteoporoză).
Tratament:
pentru adenomul secretant de GH: chirurgical / radioterapic / medicamentos (agonişti de
somatostatină);
pentru complicaţiile viscerale şi metabolice (diabet zaharat, hipertensiune arterială, ulcer
varicos, insuficienţă cardiacă);
corecţie ortopedică.
f. Creşteri somatice dispropoţionate - înglobează anomalii constituţionale sau dobândite ce constau în
hipertrofia unui segment mai restrâns (un membru) sau mai extins (hemicorp) al individului:
Sindrom hemihipertrofic
DEZVOLTAREA PUBERTARĂ
Pubertatea este perioada de tranziţie dintre copilărie şi viaţa adultă în dezvoltarea individului.
Procesul cuprinde sudarea epifizelor osoase (cu realizarea taliei finale) şi dezvoltarea capacităţii de
reproducere prin dezvoltarea şi maturarea caracterelor sexuale primare.
Pubertatea fiziologică este urmarea maturării unor structuri hipotalamice afectate acestui proces,
structuri ce alcătuiesc gonadostatul.
Materializarea acestui proces se face prin secreţia pulsatilă a unui neurohormon numit gonadoliberină
(LH-RH sau Gn-RH) care stimulează celulele gonadotrope hipofizare. Secreţia LH-RH este ritmică, la 60-
90 minute.
Gonadotropinele hipofizare, LH – hormonul luteinizant şi FSH – hormonul foliculostimulant, vor stimula
steroidogeneza şi gametogeneza.
Gonada masculină produce testosteron la nivelul celulelor Leydig sub controlul LH. Testosteronul trece
în circulaţia generală şi în celulele Sertoli, prelucrând structurile sensibile şi întreţinând
spermatogeneza. FSH stimulează producerea de spermatozoizi la nivelul tubilor seminiferi şi sinteza
unor compuşi proteici la nivelul celulelor Sertoli.
Pentru ovar, pulsaţiile gonadotropilor iniţiază maturarea unui folicul, cu debutul steroidogenezei care, la
un anumit nivel secretor, produce prima menstră (menarha). Ovulaţia apare ulterior, când nivele
crescute de FSH vor recruta şi matura o serie de foliculi ovarieni, inducând şi apariţia de receptori
pentru LH în celulele granuloase.
Evaluarea somatică a dezvoltării pubertare (după Tanner) (fig. 4.14)
Dezvoltarea pubertară la băiat (după Tanner)
Caracteristicile somatice de dezvoltare pubertară ce definesc adultul, bărbat sau femeie, sunt subliniate
de caracterele sexuale secundare:
Factorii ambientali prelucrează factorii genetici şi realizează un mare polimorfism de expresie. La
ultimele generaţii se observă în Europa o tendinţă de coborâre a vârstei la care apare menarha. În SUA
vârsta de apariţie a menarhăi a scăzut în ultimele 5 decenii de la 15,9 ani la 12,8 ani.
Apariţia pubertăţii înainte de 8 ani la fete şi 9 ani la băieţi defineşte pubertatea precoce.
Debutul pubertăţii între aceste vârste şi vârsta medie fiziologică defineşte “pubertatea precipitată”.
Pubertate precoce adevarata Fată 7 ani cu macromastie
Pubertatea precoce poate fi:
pubertate precoce adevărată (centrală) (fig. 4.15) - în care maturarea sexuală este completă prin
funcţionarea axului hipotalamo-hipofizo-gonadal. Întotdeauna este în acord cu sexul pacientului.
Gametogeneza este prezentă.
pseudopubertate precoce – în care producerea steroizilor sexuali se face la nivel gonadal sau adrenal,
fără maturarea axului hipotalamo-hipofizo-gonadal. Gametogeneza este absentă. Pseudopubertatea
precoce poate fi izo- sau heterosexuală (în acord, respectiv în dezacord cu sexul genetic al pacientului).
Se consideră că 1/10.000 născuţi vii dezvoltă o pubertate precoce. Fenomenul predomină la fete,
raportul faţă de băieţi fiind 3/1 - 4/1.
Cel mai tânăr caz comunicat de pubertate precoce de tip central „idiopatică” s-a descris la un sugar de
sex feminin în vârstă de 6 luni (1991).
Etiologia pubertăţii precoce
1.pubertatea precoce adevărată (centrală):
idiopatică (sporadică sau familială);
organică: tumori (hamartom, gliom, neuroblastom); anomalii congenitale (hidrocefalie); infecţii
(meningită, encefalită, abces cerebral); traumatism cranio-cerebral;
asociată hipotiroidismului;
2. pseudopubertatea precoce:
a. izosexuală (în acord cu sexul genetic al pacientului):
la băieţi:
– secreţie excesivă de androgeni;
– tumori secretante de gonadotropine;
– indusă iatrogen;
– rezistenţă periferică la cortizol;
la fete:
– secreţie excesivă de estrogeni;
– indusă iatrogen.
b. heterosexuală (în dezacord cu sexul genetic al pacientului):
la băieţi:
– secreţie excesivă de estrogeni;
– tumori adrenale feminizante;
– aromatizare periferică excesivă;
– iatrogen (estrogeni);
la fete:
– secreţie excesivă de androgeni;
– rezistenţă primară la cortizol;
– iatrogen (steroizi anabolici, androgeni).
c. asocieri posibile: pseudopubertate precoce cu pubertate precoce de cauză centrală (în cazul sindromului
adrenogenital congenital tratat după atingerea vârstei osoase de 12 ani).
Formele parţiale de pubertate precoce sunt:
adrenarha prematură – dezvoltarea pilozităţii axilare cu caracter pubertar înaintea pubarhăi;
pubarha prematură – apariţia pilozităţii pubiene cu caracter pubertar înaintea vârstei de 7 ani;
telarha prematură – dezvoltarea prematură a sânilor cu caracter pubertar înaintea vârstei de 7 ani;
menarha prematură – apariţia menarhăi înaintea vârstei de 9 ani.
Diagnosticul pozitiv se bazează pe:
1. anamneză
2. somatometrie / examen clinic
3. date de laborator:
– LH / FSH bazal sau după stimulare cu LH-RH
– estradiol / testosteron
– DHEA-S
– androstendion
– 17-hidroxiprogesteron
– T4, TSH
– hCG
– citologie vaginală
4. date imagistice:
– aprecierea vârstei osoase (radiografie mână)
– aprecierea morfologiei selare (radiografie craniană, TC, RMN)
– ecografie abdominală.
Tratament
Tratament
1. Pubertatea precoce adevărată
– Analogi sintetici de LH-RH administraţi continuu – scad producţia hipofizară de LH şi FSH.
– Ciproteron acetat – inhibă steroidogeneza adrenală şi ovariană şi parţial secreţia
gonadotropinelor, precum şi recepţia androgenilor.
– Medroxiprogesteron, Danazol – inhibă secreţia gonadotropă şi deci stimularea gonadelor; sunt
mai puţin folosiţi din cauza efectului inconstant asupra controlului vârstei osoase şi al taliei
finale.
Tratament
2. Pseudopubertatea precoce
– Ciproteron acetat – efect antiandrogenic;
– Tamoxifen – efect antiestrogenic;
– Testolactona – inhibitor de aromatază;
– Ketoconazol – inhibă sinteza de glucocorticoizi şi testosteron;
– Spironolactona – efect antiandrogenic;
– Dexametazona – scade producţia de sexoizi adrenali în sindromul adrenogenital congenital.
PUBERTATEA ÎNTÂRZIATĂ
Termenul de pubertate întârziată defineşte o întârziere în cronologia normală a dezvoltării caracterelor
sexuale secundare.
Pubertatea întârziată este caracterizată de:
– absenţa apariţiei caracterelor sexuale secundare peste 13,5 ani la fete şi 14 ani la băieţi;
– absenţa saltului statural la 13 ani la fete şi 15 ani la băieţi;
– lipsa acestor semne clinice la o vârstă osoasă de 12 ani la fete şi 13 ani la băieţi.
Etiologie
1. hipogonadism hipogonadotrop:
– cauză hipotalamică;
– cauză hipofizară;
2. hipogonadism hipergonadotrop:
a. la fete:
congenital:
– sindrom Turner şi variante de mozaicism;
– agenezie ovariană;
dobândit:
– castrare;
– iatrogen;
– infecţii cronice;
– ooforită autoimună;
b. la băieţi:
congenital:
– sindromul Klinefelter şi variantele sale;
– sindromul poli-Y;
– sindromul Noonan (Turner masculin);
dobândit:
– castrare;
– iatrogen;
– orhită bilaterală;
3. întârziere pubertară constituţională;
4. întârziere pubertară datorată unei boli cronice consumptive.
Diagnostic
1. Tehnici imagistice:
– explorare radiologică convenţională (şa turcă, nuclei osoşi carpieni);
– ecografie (abdominală, pelvină);
– TC (aria supraselară, corticosuprarenale);
– RMN (tija hipofizară, hipotalamus);
2. Studii citologice – în suspicionarea unor cromozomopatii (cariotip, cromatină sexuală).
3. Probe funcţionale – secreţia de GH înainte şi după stimulare.
Tratament
Atitudinea terapeutică este condiţionată de cauza întârzierii pubertare:
1. întârzierea pubertară constituţională
– temporizare terapeutică
– psihoterapie
– anabolizante steroidiene
– hormoni sexoizi naturali sau sintetici
2. pubertatea întârziată din hipogonadismele hipogonadotrope
– steroizi sexuali
– gonadotrofine
I. Steroizi sexuali
a. Sexul masculin
Testosteron depozit 100mg/lună i.m. timp de 3 luni; doza creşte cu
50mg/lună tot la fiecare 6 luni pentru a atinge 200-300 mg/lună
3. întârzierea pubertară secundară unei boli cronice
– tratamentul bolii de bază
4. pubertatea întârziată din hipogonadismele hipergonadotrope
– tratamentul sexoid substitutiv
– capacitatea reproductivă este definitiv alterată.
S-ar putea să vă placă și
- Curs 2Document86 paginiCurs 2Narcisa LazărÎncă nu există evaluări
- C1 - Curs Crestere 2016Document123 paginiC1 - Curs Crestere 2016Alexandra constantinÎncă nu există evaluări
- Hipostatura La CopilDocument21 paginiHipostatura La CopilNatalie KaramanÎncă nu există evaluări
- Conformatia Somatica Si Tipul ConstitutionalDocument49 paginiConformatia Somatica Si Tipul ConstitutionalHallucinogenic ThoughtÎncă nu există evaluări
- Creşterea Şi DezvoltareaDocument86 paginiCreşterea Şi DezvoltareaCosmina GheorgheÎncă nu există evaluări
- Creşterea Şi Dezvoltarea Copilului PRELEGERE-33429Document36 paginiCreşterea Şi Dezvoltarea Copilului PRELEGERE-33429Nicolae-Irina LisnicencoÎncă nu există evaluări
- Curs Deficit Statural FinalDocument16 paginiCurs Deficit Statural FinalMelania OanaÎncă nu există evaluări
- Crestera Si DezvoltareaDocument47 paginiCrestera Si DezvoltareaUmbra MeaÎncă nu există evaluări
- Nanismul HipofizarDocument4 paginiNanismul HipofizarAlexandraIonelaÎncă nu există evaluări
- ProiectDocument43 paginiProiectNicoleta TopalaÎncă nu există evaluări
- Gigantismul Se Caracterizeaza Prin Cresterea Exagerata În ÎnaltimeDocument5 paginiGigantismul Se Caracterizeaza Prin Cresterea Exagerata În ÎnaltimeSava SilviaÎncă nu există evaluări
- Patologia Cresterii 09Document116 paginiPatologia Cresterii 09Tanya Tina100% (1)
- CURS Pediatrie 3 ExDocument136 paginiCURS Pediatrie 3 ExCentru RefillÎncă nu există evaluări
- Hipostatura. (FINALA) Peltec Inesa Gr1401Document51 paginiHipostatura. (FINALA) Peltec Inesa Gr1401Ala Donos Sinciuc100% (2)
- 8 - Genetica DezvoltariiDocument6 pagini8 - Genetica DezvoltariiVlad PerpeleaÎncă nu există evaluări
- Crestere Si DezvoltareDocument50 paginiCrestere Si DezvoltareCezara PinteaÎncă nu există evaluări
- Copil Sanatos Si Endocrin - Tulburări de Creștere La CopiiDocument14 paginiCopil Sanatos Si Endocrin - Tulburări de Creștere La CopiiAndriana GruzinschiÎncă nu există evaluări
- Curs 6 Nanismul HipofizarDocument32 paginiCurs 6 Nanismul HipofizarDaniela ToporauÎncă nu există evaluări
- Fenotip 1Document27 paginiFenotip 1Coco DenÎncă nu există evaluări
- 3 Puericultura Si PediatrieDocument48 pagini3 Puericultura Si PediatrieAndrei PoravÎncă nu există evaluări
- Boli Cauzate de Glandele EndocrineDocument12 paginiBoli Cauzate de Glandele EndocrineCatrina Nicoleta100% (1)
- Distrofia Adipozo - Genitală: EtiologieDocument8 paginiDistrofia Adipozo - Genitală: EtiologieEugenia CosovanÎncă nu există evaluări
- Cresterea-CompletatDocument10 paginiCresterea-CompletatLaila MdalalÎncă nu există evaluări
- Curs 12 Pediatrie PDFDocument13 paginiCurs 12 Pediatrie PDFkidlikid100% (1)
- 2crestere Si DezvoltareDocument24 pagini2crestere Si DezvoltarePruneÎncă nu există evaluări
- Procese Biologice de Dezvoltare Şi ÎmbătrânireDocument33 paginiProcese Biologice de Dezvoltare Şi ÎmbătrânireGrad CameliaÎncă nu există evaluări
- Conov AnaDocument41 paginiConov AnaAnonymous IvZvA2Încă nu există evaluări
- Pipp32 - Puericultura - Igiena-Unitatea 2Document16 paginiPipp32 - Puericultura - Igiena-Unitatea 2Ioana MarinÎncă nu există evaluări
- Curs Pediatrie ConstantaDocument371 paginiCurs Pediatrie Constantadcn100% (1)
- c1 DezvoltareDocument6 paginic1 DezvoltarefundaliÎncă nu există evaluări
- New Microsoft Word DocumentDocument20 paginiNew Microsoft Word Documentallys_1987Încă nu există evaluări
- Endocrine - CursDocument14 paginiEndocrine - CursGlavan ilona nicoletaÎncă nu există evaluări
- Pediatrie Curs I Noțiuni IntroductiveDocument8 paginiPediatrie Curs I Noțiuni IntroductiveMihaela SilviaÎncă nu există evaluări
- Dezvoltarea Fizica A CopiilorDocument70 paginiDezvoltarea Fizica A CopiilorElena ChitoiuÎncă nu există evaluări
- Curs Crestere Si DezvoltareDocument42 paginiCurs Crestere Si DezvoltareEmilia AdrianaÎncă nu există evaluări
- HipostaturaDocument15 paginiHipostaturaIrina Cornilov100% (1)
- Sistemul Muscular Şi OsosDocument6 paginiSistemul Muscular Şi OsosArtiom MinzateanÎncă nu există evaluări
- 5 Nanismul HipofizarDocument55 pagini5 Nanismul Hipofizartasha_french1986Încă nu există evaluări
- Sindromul Adreno - GenitalDocument26 paginiSindromul Adreno - GenitalCarolina TișcencoÎncă nu există evaluări
- PRP CURS NR. 4 Tulburari de CrestereDocument47 paginiPRP CURS NR. 4 Tulburari de CresterePaula Mariana PrelucăÎncă nu există evaluări
- Endocrinologie-Nanismul HipofizarDocument3 paginiEndocrinologie-Nanismul HipofizarIstrati Ana-LoredanaÎncă nu există evaluări
- EndocrinologieDocument20 paginiEndocrinologieBianca PopaÎncă nu există evaluări
- NanismDocument61 paginiNanismAndra Birladeanu SurugiuÎncă nu există evaluări
- Boli EndocrineDocument5 paginiBoli EndocrineAnonymous WUu2apIqIyÎncă nu există evaluări
- PediatrieDocument24 paginiPediatriemaksikÎncă nu există evaluări
- 1-2. Curs Crestere Nov2018 - Varianta PT StudentiDocument83 pagini1-2. Curs Crestere Nov2018 - Varianta PT StudentiPavel Cristian NicolaeÎncă nu există evaluări
- Cresterea Si Dezvoltarea CopiluluiDocument59 paginiCresterea Si Dezvoltarea CopiluluiDiana JelerÎncă nu există evaluări
- Patologie Testiculara 2008Document56 paginiPatologie Testiculara 2008Cristina MihaelaÎncă nu există evaluări
- Cariotipul UmanDocument4 paginiCariotipul UmanBianca100% (1)
- Obiectivele PuericulturiiDocument216 paginiObiectivele PuericulturiiBarbu ValentinÎncă nu există evaluări
- Curs Crestere Si DezvoltareDocument42 paginiCurs Crestere Si DezvoltarepaulyteoÎncă nu există evaluări
- Curs 2 - BOLILE HIPOFIZEIDocument7 paginiCurs 2 - BOLILE HIPOFIZEIRazvi RazvanÎncă nu există evaluări
- Parhon Tulb CrestereDocument12 paginiParhon Tulb CresterestefÎncă nu există evaluări
- Dieta pentru zile senine II: De la durere la echilibru spiritual, psihologic, nutritivDe la EverandDieta pentru zile senine II: De la durere la echilibru spiritual, psihologic, nutritivEvaluare: 5 din 5 stele5/5 (1)
- Depresia: Când Tristețea Devine PatologicăDe la EverandDepresia: Când Tristețea Devine PatologicăEvaluare: 5 din 5 stele5/5 (1)
- Cum sa redescoperi sensul vietii si increderea in sineDe la EverandCum sa redescoperi sensul vietii si increderea in sineÎncă nu există evaluări
- PSICOLOGIA ȘI DISTURBAREA COPIILOR LA VÂRSTĂ EVOLUTIVĂ: ce sunt și cum funcționeazăDe la EverandPSICOLOGIA ȘI DISTURBAREA COPIILOR LA VÂRSTĂ EVOLUTIVĂ: ce sunt și cum funcționeazăEvaluare: 5 din 5 stele5/5 (1)
- Curs 5+6clasificarea InsectelorDocument74 paginiCurs 5+6clasificarea InsectelorMădălina MihalacheÎncă nu există evaluări
- PenicilinaDocument2 paginiPenicilinaMădălina MihalacheÎncă nu există evaluări
- Scala Holmes RaheDocument1 paginăScala Holmes RaheMădălina MihalacheÎncă nu există evaluări
- Tiro IdaDocument11 paginiTiro IdaMădălina MihalacheÎncă nu există evaluări
- Lucrare Practica 19 - Medicatia Aparatului Cardiovascular 5 - Medicatia AntiaritmicaDocument9 paginiLucrare Practica 19 - Medicatia Aparatului Cardiovascular 5 - Medicatia AntiaritmicaMădălina MihalacheÎncă nu există evaluări
- Lista Medicamente 8 Din 10Document24 paginiLista Medicamente 8 Din 10Mădălina MihalacheÎncă nu există evaluări
- PoliomielitaDocument4 paginiPoliomielitaMădălina MihalacheÎncă nu există evaluări
- Punctii, Biopsii, DrenajeDocument25 paginiPunctii, Biopsii, DrenajeMădălina MihalacheÎncă nu există evaluări