Documente Academic
Documente Profesional
Documente Cultură
08 Oxidare Alchene
Încărcat de
Mario Watson0 evaluări0% au considerat acest document util (0 voturi)
159 vizualizări3 paginiOxidare alchene
Titlu original
08 Oxidare alchene
Drepturi de autor
© © All Rights Reserved
Formate disponibile
PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documentOxidare alchene
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
159 vizualizări3 pagini08 Oxidare Alchene
Încărcat de
Mario WatsonOxidare alchene
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 3
1
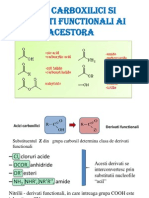
OXIDAREA COMPU}ILOR NESATURA|I (ALCHENE, DIENE, POLIENE) PRIN
RUPEREA LEG~TURII DUBLE
Alchenele sunt compui organici cu formula molecular C
n
H
2n
. Cea mai simpl alchen este
etena sau etilena, CH
2
=CH
2
. (De aici denumirea de etilen pentru gruparea CH
2
CH
2
, cu cte o
valen liber la fiecare atom de carbon).
Exemple de alchene:
1
H
H
H
C C
H
-
1 2
3
2 1
H
2
C=CH
2
H
2
C=CH
CH
3
H
H
C C
H CH
3
CH
3
CH
2
H
2
C=CH
CH
3
CH
2
H
C C
H
H
A
1
A
2
B
1
B
2 C
1
C
2
Eten` Propen`
Buten`
4
3
2 1
Prin urmare structurile A
1
i A
2
reprezint eten, structurile B
1
i B
2
, propen, structurile C
1
i C
2
reprezin 1-buten. Numerele de deasupra atomilor de carbon sunt numere de referin.
{ncepnd cu 2-buten` se realizeaz izomerie cis-trans:
1
2 3
4
C C
H
H
H
3
C CH
3
1
2 3
4
H
C C
H
CH
3
H
3
C
Cis 2-buten`
Trans 2-buten`
(NOT~: se numesc izomeri compui cu aceeai formul molecular dar cu structuri diferite, i
implicit cu proprieti fizico-chimice diferite. Observai la 1-buten, cis-2-buten` i trans-2-
buten` c au aceeai formul molecular, C
4
H
8
).
Oxidarea alchenelor prin ruperea leg`turii duble conduce la localizarea acesteia pe
catena respectiv` dar nu la determinarea configura\iei, cis sau trans; tipul de configura\ie se
determin` prin urm`toarele metode: spectroscopie [n IR (infraro]u), spectroscopie RMN
(rezonan\` magnetic` nuclear`) sau difrac\ie cu raze X. Au fost ob\inute urm`toarele rezultate
prin oxidarea alchenelor:
1
-
3
1 2
H
2
C=CH
2
H
2
C=CH
CH
3
Eten`
Propen`
Buten`
4
3
2 1
1
2 3
4
C C
H
H
H
3
C CH
3
1
2 3
4
H
C C
H
CH
3
H
3
C
+
[O] +
H
2
O CO
2
CO
2 H
2
O
+ [O] + + HOOC
CH
3
CH
3
H
H
C C
H C
H
2
Acid propionic
+
+ [O] +
H
2
O
CO
2
CH
3 C
C
H
2
O
HO
Acid acetic
C
HO
H
3
C
O
C
OH
CH
3
O +
[O]
C
HO
H
3
C
O
OH
C
CH
3
O
+
Acid acetic
+
[O] +
2
2
5
6
5
4
4
Trans 2-buten`
Acid acetic
Cis 2-buten`
Prin urmare, natura chimic` a fragmentelor ob\inute prin oxidare indic` pozi\ia leg`turii duble
pe catena alchenei.
Reac\ii de oxidare similare au condus la elucidarea structurii acizilor gra]i nesatura\i ]i
polinesatura\i. Iat` cteva exemple:
2
Acid pelargonic
Acid azelaic
Acid oleic
+
HOOC
COOH
-
1
COOH
15 24
Acid nervonic
COOH
HOOC
1
9
10 18
[O] 4
Acid pentadecandioic
Acid pelargonic
HOOC COOH COOH +
1
,
15
+
+ 4 [O]
Acizii gra]i -6:
HOOC COOH HOOC
Acid linoleic (acid all cis octadecadienoic) -
Acid azelaic
Acid caproic
Acid malonic
HOOC
HOOC
COOH
2
COOH
COOH
6
1
COOH
COOH
9 10 13 12
18
18
12 13
11
10 9 1
9
,
12 -
-
+
+
COOH
COOH
Acid malonic
7
8
-
9
,
12
,
15 - Acid linolenic (acid all cis octadecatrienoic)
+
+
Acid adipic Acid caproic
Observa\i ni]te regularit`\i:
Leg`turile duble nu sunt conjugate ci izolate, adic` separate printr-o grupare metilen,
CH
2
;
Distan\a dintre gruparea metil, CH
3
, ]i cea mai apropiat` leg`tur` dubl` este de 6
atomi; de aici denumirea de acizi gra]i -6.
Din aceea]i serie -6 face parte ]i acidul arahidonic:
3
15
14
11
8 5 6 9
12
COOH
20
+
+
- 5
,
8
,
11
,
14
1
COOH
COOH
Acid malonic
Acid caproic
Acid glutaric
- Acid arahidonic (acid all cis eikosatetraenoic)
HOOC
HOOC COOH
3
Paleta de produ]i de oxidare a unui alt grup de acizi gra]i polinesatura\i, seria -3, este
deasemenea caracteristic`:
Acid azelaic
2 +
Acid propionic Acid malonic
-
Acid linolenic (acid all cis octadecatrienoic)
COOH
1
9 10
12 13 15 16 18
COOH
HOOC COOH HOOC COOH
9
,
12
,
15-
+
Acid all cis ikosapentaenoic 5
,
8
,
11
,
14
,
17
20
COOH
-
1
5 8
11 14 17
+ HOOC COOH HOOC
Acid malonic
Acid propionic
+
4
Acid glutaric
HOOC COOH
Cele dou` grupuri de acizi gra]i polinesatura\i -6: linoleic, gama-linolenic, arahidonic ]i grupul
-3 constituie vitamina F.
Prepararea reactivului Jones. In 50 mL ap se dizolv 50 g bicromat de potasiu sau, de
preferin, bicromat de sodiu, ultimul avnd o solubilitate mai mare n ap. Peste soluia (sau
suspensia) de bicromat se adaug 1 L acid sulfuric concentrat, sub agitare i rcire. Reactivul
este de culoare rou-brun (culoarea caracteristic compuilor cromului n starea de valen 6 sau
avnd numrul de oxidare 6+) i este stabil luni de zile ntr-o sticl de culoare brun, nchis
ermetic.
Mod de lucru. Se msoar n cinci eprubete diferite cte 0,2 mL de reactiv Jones. Se adaug n
fiecare eprubet o pictur de solu\ie, [ntr-un solvent inert (cloroform, aceton`, eter dietilic,
dimetilformaid`, etc), a unui acid nesaturat: oleic, linoleic, arahidonic, linolenic. Amestecul se
[nc`lze]te la 90
0
C timp de 15 min. Se observ schimbarea culorii de la rou-brun la verde,
aceast ultim culoare fiind caracteristic ionului Cr
3+
. Acizii organici produ]i [n mediu se
separ` cromatografic sau prin antrenare cu vapori de ap` ]i distilare frac\ionat` (v. acolo).
Fiecare acid ob\inut prin fragmentare oxidativ` se identific` prin caracteristicile sale fizico-
chimice, prin spectroscopie IR, spectroscopie RMN ]i prin spectrometrie de mas`.
PROBLEME
1. Scrie\i reac\iile de oxidare de mai sus [n termeni stoechiometrici.
S-ar putea să vă placă și
- Compuşi Organici Cu Două Grupe Funcţionale: 8.1.1. AminoaciziDocument26 paginiCompuşi Organici Cu Două Grupe Funcţionale: 8.1.1. AminoaciziDana CapbunÎncă nu există evaluări
- Acizi Carboxilici EUDocument6 paginiAcizi Carboxilici EUelvira_antib100% (1)
- Acizi CarboxiliciDocument5 paginiAcizi CarboxiliciAdriana TrandafirÎncă nu există evaluări
- Curs 2 - Acizi Carbonilici - Esteri B-CetoniciDocument9 paginiCurs 2 - Acizi Carbonilici - Esteri B-CetonicialexandraÎncă nu există evaluări
- Tema 3. Aciditatea Și Bazicitatea.Document31 paginiTema 3. Aciditatea Și Bazicitatea.Daniel Huntelar100% (1)
- AMINOACIZIDocument19 paginiAMINOACIZIanon_163614935Încă nu există evaluări
- Peniciline de SemisintezaDocument11 paginiPeniciline de SemisintezaAna-Maria PetreÎncă nu există evaluări
- Cursuri de ChimieDocument34 paginiCursuri de ChimieCalin Catalin Cristian100% (1)
- ALCHENEDocument9 paginiALCHENEmanuelbossÎncă nu există evaluări
- Proteine - Curs 8Document56 paginiProteine - Curs 8myaccountonscribdÎncă nu există evaluări
- Proiectarea Unei Instalatii Pentru Fabricarea AcetoneiDocument142 paginiProiectarea Unei Instalatii Pentru Fabricarea AcetoneiAlexandru IonutÎncă nu există evaluări
- I - 03.peptideDocument20 paginiI - 03.peptideStefan MihaelaÎncă nu există evaluări
- Acizi CarboxiliciDocument28 paginiAcizi CarboxiliciAndreea IoanaÎncă nu există evaluări
- Chimie Organica CursDocument17 paginiChimie Organica CursRoxana AlinaÎncă nu există evaluări
- C1 C3 - Acizi CarboxiliciDocument28 paginiC1 C3 - Acizi CarboxiliciAlexandru ViorelÎncă nu există evaluări
- Acidul Glutamic - Proiect FinalDocument94 paginiAcidul Glutamic - Proiect FinalAncu100% (2)
- Oxidarea LipidelorDocument53 paginiOxidarea LipidelorCarmen Damian100% (1)
- Aminoacizi Si ProteineDocument13 paginiAminoacizi Si ProteineRogue Andreea100% (2)
- Acizi Grasi - Izomerie + Propr. - Curs 8Document4 paginiAcizi Grasi - Izomerie + Propr. - Curs 8trisinaÎncă nu există evaluări
- Comp Carbon Ilic IDocument22 paginiComp Carbon Ilic INicoleta PirciulescuÎncă nu există evaluări
- Ntroducere in Chimia Organica Kopiia KopiiaDocument21 paginiNtroducere in Chimia Organica Kopiia Kopiiaepaduraru_4Încă nu există evaluări
- Chimie Clasa A X-ADocument13 paginiChimie Clasa A X-ADelia Melter100% (1)
- Carotenoide PDFDocument30 paginiCarotenoide PDFDana MirceaÎncă nu există evaluări
- CURS 12 Compusi DicarboniliciDocument10 paginiCURS 12 Compusi DicarboniliciMerla OanaÎncă nu există evaluări
- Suport de Curs - Chimie CL X - 2016 - Gheorghe Ilcos PDFDocument20 paginiSuport de Curs - Chimie CL X - 2016 - Gheorghe Ilcos PDFOana FrincuÎncă nu există evaluări
- Subiecte Simulare MG 2015 ClujDocument6 paginiSubiecte Simulare MG 2015 ClujIoana VisanescuÎncă nu există evaluări
- Cursuri de ChimieDocument17 paginiCursuri de ChimieCalin Catalin CristianÎncă nu există evaluări
- 1-305 GrileDocument58 pagini1-305 GrileDragosh Voinea0% (1)
- LaboratorDocument9 paginiLaboratorIvan IvanyshÎncă nu există evaluări
- Compoziţia Proteinelor: Referateok - Ro - Cele Mai Ok ReferateDocument8 paginiCompoziţia Proteinelor: Referateok - Ro - Cele Mai Ok ReferateBuzatu MadalinaÎncă nu există evaluări
- Alchene Alcani Si AlchineDocument23 paginiAlchene Alcani Si AlchinelereniuÎncă nu există evaluări
- C4 AlcooliDocument29 paginiC4 AlcooliMaria DianaÎncă nu există evaluări
- AminoaciziDocument13 paginiAminoaciziToma Alexandru TiberiuÎncă nu există evaluări
- Derivati Functionali Ai Acizilor CarboxiliciDocument50 paginiDerivati Functionali Ai Acizilor CarboxiliciPapillon HeureuseÎncă nu există evaluări
- Chimie Analitica Anul II Sem II LP 10Document4 paginiChimie Analitica Anul II Sem II LP 10Georgiana Cozma FrunzăÎncă nu există evaluări
- Curs 2 Echilibrul OsmoticDocument36 paginiCurs 2 Echilibrul Osmoticmihaela_bondocÎncă nu există evaluări
- AlcaniDocument13 paginiAlcaniirinamelnic96Încă nu există evaluări
- Curs 2. Reactii AnaliticeDocument44 paginiCurs 2. Reactii AnaliticeCezara AxinteÎncă nu există evaluări
- Modele de Probleme de Echilibre Chimice in Apa Si Solutii Apoase1Document14 paginiModele de Probleme de Echilibre Chimice in Apa Si Solutii Apoase1Anonymous W76vMPBRrÎncă nu există evaluări
- Compusi Cu SulfDocument7 paginiCompusi Cu SulfRelu VoloÎncă nu există evaluări
- Biochimie 2016 Curs 8Document32 paginiBiochimie 2016 Curs 8Preda ManuelaÎncă nu există evaluări
- Note de Curs BM 2012-2013 (Bm1-Bm5)Document247 paginiNote de Curs BM 2012-2013 (Bm1-Bm5)Laura NeaguÎncă nu există evaluări
- Sistemul Endocrin Final OlimpiadaDocument54 paginiSistemul Endocrin Final OlimpiadaellamÎncă nu există evaluări
- NUCLEULDocument71 paginiNUCLEULAndrada Raicu100% (1)
- Citologie Animala - Cursul I, Anul IDocument42 paginiCitologie Animala - Cursul I, Anul ICristina CrisÎncă nu există evaluări
- Sistematica Nevertebratelor - BibliografieDocument1 paginăSistematica Nevertebratelor - BibliografieMario WatsonÎncă nu există evaluări
- Curs 1 VertebrateDocument73 paginiCurs 1 VertebrateDaniela Danitzu80% (10)
- Lucrari Practice La Biochimie Generala - BiochimieI - 2013Document41 paginiLucrari Practice La Biochimie Generala - BiochimieI - 2013Mario WatsonÎncă nu există evaluări