Documente Academic
Documente Profesional
Documente Cultură
CURS-nr 12
Încărcat de
George Cioaca0 evaluări0% au considerat acest document util (0 voturi)
67 vizualizări12 paginihhh
Titlu original
CURS-nr.12
Drepturi de autor
© © All Rights Reserved
Formate disponibile
DOC, PDF, TXT sau citiți online pe Scribd
Partajați acest document
Partajați sau inserați document
Vi se pare util acest document?
Este necorespunzător acest conținut?
Raportați acest documenthhh
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOC, PDF, TXT sau citiți online pe Scribd
0 evaluări0% au considerat acest document util (0 voturi)
67 vizualizări12 paginiCURS-nr 12
Încărcat de
George Cioacahhh
Drepturi de autor:
© All Rights Reserved
Formate disponibile
Descărcați ca DOC, PDF, TXT sau citiți online pe Scribd
Sunteți pe pagina 1din 12
CURS nr.
12
Decontaminarea cu ozon in managementul igienei din
industria alimentara
Scurt istoric al ozonului
Ozonul a fost descoperit pentru prima datain Grecia Antica, unde
mirosul sau caracteristic, creat in timpul furtunilor, era cunoscut dar
nu siinteles. In literatura de specialitate, mirosul ozonului este adesea
descris ca fiind “sulfuros”. In 1840 chimistul F.C. Schobein a observat
acelasi miros caracteristic la un gaz format in timpul electrolizei apei.
El a numit acest gaz ozon din cuvantul grecesc óζεiv gr = a mirosi.
Cinci ani mai tarziu, cercetatorii de la Rive si de Marignac au enuntat
teoria conform careia ozonul ar fi o alta forma a oxigenului gaz. Ei au
produs de asemenea ozon, prin aplicarea unei descarcari electrice
oxigenului pur.
Primul generator de ozon, un tub de descarcare electrica pentru
folosirea in laborator, a fost realizat de catre W. von Siemens in 1857.
Acelasi principiu este inca folosit in tehnologiile moderne. In 1865,
J.L. Soret a aratat, printr-o determinare indirecta, ca ozonul este
constituit din trei atomi de oxigen. Efectul bactericid al ozonului, a fost
prima data descoperit de catre Ohlmüllerin 1890, iar pe parcursul
anilor ce au urmat o serie foarte mare de generatoare de ozon au fost
produse de Siemens si Halske.
Ozonul este a doua forma alotropica a oxigenului, fiind constituit
din trei atomi ai acestuia. Formula sa chimica este O 3. Molecula sa
este instabila si se descompune dupa un timp scurt in oxigen
diatomic. El este un oxidant puternic, din care cauza este daunator
omului, producand dureri de cap, fiind iritant, caustic al mucoaselor
respiratorii.
Tocmai datorita faptului ca este instabil, ozonul este foarte rar si
se gaseste in atmosfera (cea mai mare concentratie a sa este stratul
de ozon), la suprafata Pamantului (in procent de 1·10-7%) si la 22 de
km de suprafata Pamantului (in procent de 1·10-6%). Locurile unde
ozonul mai pot aparea sunt cascadele si malurile marilor (rezultat in
urma influentei razelor ultraviolete) si padurile de brazi (produs in
urma oxidarii terebentinei si a altor compusi organici).
Ozonul se obtine cel mai simplu de la oxigen, cu ajutorul unei
energii straine (caldura, lumina, electricitate), dupa reactia:
3O2+ O + 69 kcal = 2O3
Aceasta reactie este endoterma cu concentratie de volum.
Fig. 1.1. Structura chimica a ozonului [36]
Proprietatile ozonului
Ozonul (O3) este un gaz atmosferic cu proprietati antimicrobiene,
incercandu-se, de-a lungul mai multor decenii folosirea sa ca agent
pentru prelungirea valabilitatii unor alimente.
Ozonul este o molecula cu o energie foarte mare si se
descompune inoxigen simplu(O2) astfel putand fi consumate
produsele alimentare tratate cu ozon fara nici o grija din punct de
vedere al sanatatii. S-a dovedit ca acesta este eficient impotriva
diverselor microorganisme, insa datoritafaptului careprezinta un
oxidant puternic, nu poate fi utilizat in cazul alimentelor cu un continut
mare de lipide, deoarece ar provoca o crestere a rancezirii.
Proprietatile fizice ale ozonului
Aspect: gaz incolor
Starea de agregare: gazoasa
Punct de topire: -192,7oC
Punct de fierbere: -12oC ( presiune de 5,5 MPa)
Solubilitate: 494 ml/l apa ( la temperatura de 0 oC)
Miros: intepator
Proprietatile chimice ale ozonului
Masa moleculara: 48,00 g/mol
Densitate: 2,144 kg/m3
Indice de refractie: 1,2226
La concentratii mai mari in aer, ozonul isi schimba culoarea in
albastru, in timp ce la concentratii mai mici, acesta ramane incolor cu
o densitate mai micadecat cea a aerului.
Viata medie a molecule de ozon in aer este relativ lunga avand
valoarea de 30 de minute. Insolutiile apoase, aceasta depinde de
continutul de materie organica. Cu alte cuvinte, cu catconcentratia
materiilor organice este mai mica cu atat este mai mare viata medie a
moleculei de ozon.
Ozonul dizolvat in apa este de zece ori mai puternic decat
oxigenul, iar solubilitatea sa scade odata cu cresterea temperaturii
apei, ceea ce urmeaza afi aratatin tabelul 1.1.
Tabelul 1.1
Relatia dintre temperaturasi solubilitatea ozonului in apa
Temperatura apei (OC) Solubilitatea (concentratie
ozon/concentratie apa)
0 0,640
15 0,456
27 0,270
40 0,112
60 0,000
Toxicitatea ozonului este data de concentratiasain aer, dar si de
perioada de expunere. Aceasta toxicitate este redatain graficul ce
urmeaza.
Concentratia ozonului in aer ( ppm)
Timpul de expunere (min)
Fig1.1. Toxicitatea Ozonului
Legenda: Albastru- Fara simptome; Verde – Fara toxicitate;
Galben – Toxic;
Rosu – Foarte toxic
Ozonul este foarte eficient in distrugerea microorganismelor prin
procesul de oxidare a membranelor celulelor acestora. Ozonul are
proprietatea de a se auto descompunesi de aceea nu va lasa nici un
reziduu toxic. Are un potential de oxidare mai mare de 1,5 ori decat
restul dezinfectantilorsi s-a demonstrat a fi mai eficient peste o
spectru mai larg de microorganisme.
Ozonul este generat in mod natural de radiatiile ultraviolete ( UV)
de la soare dar si de la alte surse de lumina ce utilizeaza UV.
Distrugerea microorganismelor cu ajutorul ozonului
Deoarece ozonul este sigur, un puternic dezinfectant, poate fi
folosit sa controleze cresterea biologica a organismelor nedorite in
produsele alimentare catsi pe suprafata echipamentelor folosite in
industria alimentara. Ozonul este, in special, potrivit pentru industria
alimentara, datoritaabilitatii sale de a distruge microorganismele fara
a adauga chimicale produselor ce sunt tratate sau in apa care se
foloseste la procesarea produselor sau in atmosfera in care
alimentele sunt depozitate.
Aceasta abilitate a ozonului de a distruge microorganismele se
bazeaza pe potentialul sau oxidativ mare, incomparatie cu cel al altor
agenti oxidativi, potential prezentat in tabelul 1.2.
Tabelul 1.2
Potentialul oxidativ (redox) al agentilor de oxidare
Agentul oxidant Potentialul oxidativ (mV)
Fluor (Fl) 2,87
Radicalul Hidroxil (-OH) 2,86
Atomul de oxigen (O) 2,42
Ozonul (O3) 2,07
Peroxidul de hidrogen – Apa 1,78
oxigenata (H2O2)
Permanganatul(- MnO4) 1,67
Dioxidul de clor (ClO2) 1,57
Acidul hipocloros (HClO) 1,49
Clorul (Cl) 1,36
Acidul hipobromhic (HBrO) 1,33
Oxigen (O2) 1,23
Brom (Br) 1,09
Acid hipoiodic ( HIO) 0,99
Hipocloritul (-ClO) 0,94
Iod (I) 0,54
Ozonul este al patrulea cel mai oxidativ agent vreodata
cunoscut. Potentialul sau oxidativ este de 2.07 ( mV – “material
Volts” = volti pe material) incomparatie cu cel al oxidului etilenic
(0.699 mV) si cel al gazului de clor (1,36 mV).
S-a demonstrat ca ozonul este puternic, rapid si are un spectru
larg antimicrobian fata de bacterii, spori ai bacteriilor, virusuri, fungi
catsi sporii acestora. Spre deosebire de ceilaltiagenti de sterilizare,
ozonul distruge destul de repede siusor microorganismele, si pe
langa acestea, ozonul nu lasa reziduuri, urme de miros sau gust.
Un alt avantaj al ozonului este ca poate fi produs pe loc, fie din
aerul inconjurator fie din oxigenul pur. Inactivarea microorganismelor
cu ajutorul ozonului se datoreaza oxidarii acizilor grasi din
membranele celulelor si a macromoleculelor din acestea. Aceste
reactii sunt ireversibile si au ca si rezultat liza celulelor
microorganismelor. Ozonul are de asemeneaefect asupra sporilorsi
virusurilor datoritaoxidarii acidului dezoxiribonucleic (ADN) si a
proteinelor.
Efectul microbiologic al ozonului asupra apei este bine
documentat si s-a raportat a fi mai eficientin comparatie cu aplicatiile
“uscate” ale ozonului, cum ar fi asupra aerului sau a altor gaze. Mai
multe studii au aratat ca ozonul este mai eficient folosit inconditii de
umiditate ridicata.
Avantajele ozonului
Ozonul este cel mai puternic oxidant si dezinfectant pentru
tratamentul solutiilor apoase si a amestecurilor gazoase.
Cu toate ca ozonul este numai partial solubil in apa , solubilitatea
sa este suficientasi ozonul este suficient de stabil, astfel
incatproprietatile sale oxidante si dezinfectante sa fie utilizate pe
deplin. Dupa ce ozonul s-a oxidat, dezinfectand mediul contaminat,
acesta se descompune in oxigen.
Ozonul reactioneaza cu o gama larga de varietati de compusi
organici, facandu-l pe acesta cel mai puternic agent oxidant prezent
pe piata, fiind totodatasi foarte sigur de manevrat. Unul dintre
principalele motive pentru acestea, este ca ozonul nu poate fi
depozitat, de aceea acesta trebuie produs si utilizat pe loc.
Ozonul, in stare gazoasa, este un deodorizant demonstrat pentru
o serie de materiale odorizante.
In tratarea apei potabile si a apei reziduale, ozonul are abilitatea
demonstratade a converti materialele organice biorefractoarein
material biodegradabile. Adaugand ozon oricarui mediu (lichid sau
gazos). Ozonul, singur, nu modifica pH-ul, in schimb oxidarea
microorganismelor contaminante cauzeaza ajustarea ozonului. [26]
Dezavantajele ozonului
Unul dintre dezavantajele ozonului este ca acesta este o
molecula instabila care trec foarte repede in molecula de oxigen.
Timpul necesar pentru ca jumatate din ozon din aer sa se
descompunaeste de 20-60 minute si depinde de temperatura si
umiditatea din aer.
Viata ozonului in apa este aceeasisi este de
asemeneainfluentata de temperatura, pHsi calitatea apei in care se
afla.
Un alt dezavantaj major al ozonului este caacesta nu poate fi
depozitat sau transportat, ceea ce inseamna ca acesta trebuie sa fie
produs pe loc. Rezulta ca este necesar sa existe echipamente ce
produc ozonul side asemenea posibilitatea de a le alimenta cu gaz.
Ar fi fost ideal daca ozonul s-ar putea depozita in containere speciale
care sa poate fi livrate.
Inconcentratii mai mari ozonul poate cauza efecte
asuprasanatatii umane dupa inhalare, prezentandu-se cu simptome
ca iritarea mucoasei nazale si cu dureri de cap. Totusi la concentratii
mai mari de 50 parti pe milion (ppm)si un timp de expunere mai mare
de 30 de minute, ozonul poate fi chiar letal. [26]
Modul deactiune al ozonului
Molecula de ozon, fiind dator sarupa a treia legatura cu atomul
de oxigen, este un foarte puternic oxidant. Aceasta este proprietatea
care il face sa fie foarte eficient in distrugerea microorganismelor.
Este demonstrat ca ozonul poate distruge virusuri ca hepatita A,
virusul gripei A, stomatita veziculoasa, precum si rinotraheita
infectioasa la bovine.
Inactivarea microorganismelor are loc, in principal, ca rezultat al
degradarii proteinelor din capsida virusurilor. Este la fel de eficient
indistrugerea mai multor tulpini de bacteriofagi. Proprietatile
bactericide ale ozonului au fost de asemenea demonstrate in cazul
bacteriilor Gram-pozitive (Listeria Monocytogenes, Staphylococcus
aureus, Enterococcus faecalis) catsi asupra microorganismelor
Gram-negative (Yersinia enterocolitica, Pseudomonas aeruqinosa,
Salmonella typhimurium) atat sub forma de spori catsi a celulelor
vegetative.
La inceput ozonul atacasuprafata celulelor. Au fost identificate
doua mecanisme importante de actiune a ozonului prin care actiunea
bactericida a acestuia este exercitata.
Primul mecanism este acela aloxidarii grupurilor sulfhidrice
siaminoacizilor din enzime, peptide si proteine.
Cel de-al doilea mecanism se bazeaza pe oxidarea acizilor grasi
polinesaturati. In cazul bacteriilor Gram-negative, straturile
lipoproteice sunt principalele tinte ale efectelor distructive ale
ozonului, ceea ce contribuie la crestereapermeabilitatii membranelor
celulelor si, in final, duce la liza acestor celule.
Ozonul actioneaza ca un agent de oxidare general, in timp ce
clorul distruge selectiv anumite enzime.
STADIUL ACTUAL AL CERCETARILOR
Ozonul se utilizeazain industria produselor alimentare in scopul
micsorarii sau chiar a reducerii incarcaturii microbiene (bacterii,
virusuri) a alimentelor sau a produselor alimentare. Aceste tratamente
nu se pot realiza prin contact direct cu produsul ci prin anumiti
intermediari cum ar fi apa si aerul. Tratarea sidezinfectia acestora
sunt prezentate in cele ce urmeaza.
Tratamentul apei cu ajutorul ozonului
Proprietatile fizico-chimice ale ozonului, in special solubilitatea
sarelativ mare in apa si un potential redox crescut ( care distruge
structura microorganismelor), il face pe acesta sa fie un puternic
dezinfectant si dezodorizant.
In decursul ultimilor ani, s-a demonstrat ca apa utilizatain
industria alimentara nu este lipsita de patogeni, asa cum s-a crezut
anterior. In plus, sunt foarte numeroase cazurile cand apa este
contaminatain timpul sau inainte unui proces industrial, prin
fenomenul de croscontaminare. In aceste cazuri, tratamentele de
dezinfectiesi sterilizare trebuie sa fie aplicate pentru a mentine un
nivel scazut de microorganisme care ar putea veni in contact direct
cu produsul. Mai mult decatatat, in apele reziduale existe anumite
pesticide sicompusi organici toxici datoritaactivitatilor industriale care
au crescut considerabil in ultimii ani.
Expunerea populatiei la un mediu contaminat de apele reziduale,
a crescut in ultimii 15-20 de ani, datoritacresterii explozive a
populatieisi a utilizarii acestora a resurselor de apa.
Tratamentul apei reziduale este crucial pentru protectia mediului
inconjuratorsi pentru prelungirea disponibilitatii resurselor de apa. In
ultimii ani s-au dezvoltat noi metode diferite de purificare a apei.
Purificarea sigura a apei necesita sisteme de incredere pentru
dezinfectiadeseurilor, care reprezinta cel mai important proces in
asigurarea sanatatii publice.
Printre organismele ce contamineaza apele reziduale se numara
bacterii enterocolitice, virusuri si multe altele. Cateva microorganisme
gasitein apele reziduale siafectiunile pe care acestea le produc, sunt
prezentate in cele ce urmeaza: Bacterii: Escherichia coli produce
Gastroentorocolita; Salmonella typhi produce Febra tiroida; Vibrio
cholerae produce Holera; Virusuri: Enterovirusuri (72 subspecii)
produc Gastroenterocolita, anomalii la nivelul cordului, Meningita;
Virusul Hepatitei A produce Hepatitainfectioasa. [26]
Este foarte important ca apele reziduale sa fie adecvat tratate
inaintea dezinfectiei astfel incat orice dezinfectant folosit sa fie
eficient.
Nu exista dezinfectantul perfect, totusi sunt catevaproprietati
specifice de care se tine cont la alegerea dezinfectantului potrivit:
abilitatea de a penetra si distruge agentiiinfectiosiinconditii
normale de lucru
lipsa caracteristicilor care ar putea reprezenta pericole
asupra oamenilor sau a mediului inconjuratorin urma dar
siin timpul procesului de dezinfectie
usorsi sigur de manevrat, depozitat si transportat
absenta reziduurilor toxice, mutagenice si carcinogenice
dupadezinfectie
Exista trei metode de dezinfectare a apelor reziduale, si acestea
sunt clorinarea, ozonificarea si tratarea cu ultraviolet (UV) a apelor.
Clorinarea este in continuare cea mai comuna metoda pentru
dezactivarea microorganismelor patogene prezentein apasiindeseuri,
totusi, tehnicile alternative au fost apreciate, datorita unor produse
intermediare indezirabile aparutein urma procesului de clorinare dar
sidatorita ineficientei eliminarii unor microorganisme cu o concentratie
mai mica de clor. Acesta distruge organismele tinta prin oxidarea
materialului celular. Se poate aplica sub forma de gaz, sisolutii
hipoclorice sau sub forma unoralticompusi fie in stare solida fie in
stare lichida.
S-a demonstrat in trecut caozonul este unul dintre cele mai
eficiente substante dezinfectante ce poate inlocui clorul si poate fi
aplicat in vederea distrugerii unei game mai largi de patogeni din apa
potabila.
Ozonul poate distruge produsele secundare formate datorita
clorinarii, pesticidele si compusii organici toxici din apa procesata fara
a contamina apa cu alte reziduuri toxice. Ozonul este de asemenea
folosit pentru a indeparta fierul, magneziul si sulful pentru controlul
mirosului dar si a gustului apei proaspete. [15]
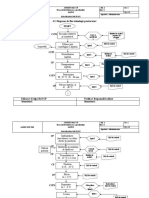
Descrierea Procesului
Ozonul este produs cand asupra moleculei de oxigen (O 2)
actioneaza o sursa de energie, care o distruge in atomi de oxigen (O)
care formeaza imediat legaturi cu moleculele existente generand
astfel un gaz instabil, ozonul (O 3), care este folosit mai departe in
procesul de dezinfectie al apei reziduale.
Acest mecanism are la baza proprietatile oxidative ale ozonului
si cuprinde urmatoarele etape:
oxidarea directa a peretelui celulei rezultand scurgerea
constituentilor celulari in afara celulei
distrugerea constituentilor ai acizilor nucleici din celule
( bazele pirimidinice si purinice)
distrugerea legaturilor carbon-azot din celuleducand la
depolimerizarea acestora
Cand ozonul se descompune in apa, radicalii liberi ce sunt
formati, peroxidul de hidrogen (HO 2) si gruparea hidroxil (OH), au
capacitati mari de oxidare si joaca un rol activin procesul de
dezinfectie. Acesti radicali au rolul de a distruge bacteriile
datoritaoxidarii protoplasmatice ce duc la deteriorarea peretelui
celulei, asa numita liza celulelor. [18]
Tratarea aerului cu ajutorul ozonului
Cel mai periculos sinedorit aspect in ceea ce priveste
contaminarea aerului dintr-o incinta este posibilitatea
dezvoltariiSindromului Respirator Acut Sever, care afecteaza din ce
in ce mai multe persoane. Acesta este o boala globala care s-a
dovedit a fi letalain majoritatea cazurilor.
Cea mai folosita metoda pentru dezinfectia aerului reprezinta
utilizarea radiatiilor ultraviolete (UV) care omoara bacteriile
sivirusurile prin distrugerea AND-ului si a ARN-ului din celulele
microorganismelor. Totusi, dezavantajul acestei metode, constain
faptul caradiatiile puteau sa dezinfecteze aerul numai in zona imediat
apropiatalampilor, deoarece aceste radiatii au o capacitate de
penetrare limitata, ceea ce face ca metoda sa nu fie adecvata pentru
a asigura un mediu sigur si lipsit de virusuri si bacterii.
O alta metoda bine cunoscuta este aceea de a dezinfecta aerul
din incaperi cu ajutorul agentilor chimici. Acestia se folosesc de obicei
prin vaporizare inintreaga incinta. Totusi, acestidezinfectanti chimici
sunt greu de descompus, si astfel acestialasa reziduuri chimice toxice
care sunt periculoase pentru sanatatea omului.
Ultima si cea mai inovativa metoda de a dezinfecta aerul, o
reprezinta utilizarea ozonului, a carorproprietati oxidative puternice
sunt bine cunoscute in distrugerea eficienta a microorganismelor.
Aplicatiile ozonului in tratarea apelor reziduale sunt bine
cunoscute si folosite de catre tehnologiile moderne, in timp ce studiile
pentru folosirea acestui gaz inert indezinfectia aerului sunt limitate,
dar care arataaceasi putere de tratare. Astfel, cercetatorul W. J
Kowalski a studiat efectele bactericide ale ozonului asupra
microorganismelor ce se gasescin aer, Escherichia
colisiStaphilococcus aureus, demonstrand ca rata de distrugere a
acestor doua categorii de bacterii a fost de 99,99%, dupa o
ozonificare inconcentratii mari.
Pe langa puterea oxidativa puternica a ozonului, proprietatile
acestuia l-au facutsa fie un ideal dezinfectant al aerului. Incomparatie
cu radiatiile UV, ozonul este un gaz care poate penetra pana la
fiecare colt al camerei, dezinfectandu-l eficient.
Cum ozonul este un gaz foarte inert, acesta este transformat
rapidin oxigen, nelasand nici un reziduu daunator pentru sanatatea
omului.
Desi ozonul este demonstrat a fi un dezinfectant de succes al
aeruluiin experimentele de laborator, eficacitatea lui insituatii reale
trebuie sa fie mai mult explorata.
Puterea lui de oxidare se bazeaza pe atomii de oxigen care
rezulta in urma degradarii ozonului in moleculediatomicesi mai stabile
de oxigen (O2).
Ozonul este un oxidant mult mai puternic decat clorul, care are un
dezavantaj major, si acela ca are posibilitatea formarii unui compus
carcinogenic secundar ca trihalometan, in special triclorometan
(cloroform – CHCl3), care reprezinta un compus chimic in care trei din
cei patru atomi de hidrogen ai metanului (CH 4) sunt inlocuiti cu atomi
de clor. [35]
Din aceste considerente ozonul este considerat a fi unul dintre
dezinfectantii care nu polueaza mediul exterior in timpul utilizariilui.
Datorita puterii sale superioare si a eficientei sale acesta este
unul dintre mai buni dezinfectanti ai apei in Europa si Statele Unite
ale Americii. Aplicatiile sale indezinfectia aerului nu sunt atat de bine
cunoscute din cauza toxicitatii ozonului. Acesta inconcentratii mai
mari de 1 ppm are efecte adverse asupra sanatatii umane, din
aceasta cauza prezenta umana este nedoritain timpul tratarii aerului
cu ozon dintr-o incapere. [10]
Actiunea ozonului asupra bacteriilor, virusurilor din aer este
bazat pe acelasi principiu ca siin cazul tratarii apei,
principiimentionate mai sus.
S-ar putea să vă placă și
- Igienizarea in Intreprinderile de Industrializare A LapteluiDocument11 paginiIgienizarea in Intreprinderile de Industrializare A LapteluiCami RaduÎncă nu există evaluări
- Reziduuri Anorganice in Produsele Alimentare - Reziduuri de Metale GreleDocument26 paginiReziduuri Anorganice in Produsele Alimentare - Reziduuri de Metale GreleAlexandra RaduÎncă nu există evaluări
- Test de MigrareDocument15 paginiTest de MigrareSinziana FloreaÎncă nu există evaluări
- Final TobaDocument4 paginiFinal TobaAndra AndreeaÎncă nu există evaluări
- Prezentare HaccpDocument19 paginiPrezentare HaccpMezelbrav BrăviceniÎncă nu există evaluări
- Nitrati Si NitratiDocument4 paginiNitrati Si NitratiCristina GheorgheÎncă nu există evaluări
- Conserve Din Carne Curs-9Document27 paginiConserve Din Carne Curs-9GNVÎncă nu există evaluări
- Utilizarea Culturilor Starter În Industria Cărnii Și A Produselor Din CarneDocument14 paginiUtilizarea Culturilor Starter În Industria Cărnii Și A Produselor Din CarneStavilaCristinaÎncă nu există evaluări
- Diagrama de Analiza Si Evaluare A RiscurilorDocument8 paginiDiagrama de Analiza Si Evaluare A RiscurilorRaluca Loredana SemeniucÎncă nu există evaluări
- Metode Moderne de IgienizareDocument28 paginiMetode Moderne de Igienizaregia2204Încă nu există evaluări
- Modalitati de Obtinere Ale OleogelurilorDocument7 paginiModalitati de Obtinere Ale OleogelurilorReinaldogabriel CringaruÎncă nu există evaluări
- Amb. Carne Si ProduseDocument25 paginiAmb. Carne Si ProduseRoxanda Elena SimescuÎncă nu există evaluări
- Tehnologii CarneDocument32 paginiTehnologii CarneŞerban VeronicaÎncă nu există evaluări
- KaizerDocument30 paginiKaizerAlbert BorcosÎncă nu există evaluări
- Caiet de SarciniDocument13 paginiCaiet de SarciniMaftei MariusÎncă nu există evaluări
- Procesare Cu Radiaţii Ionizante PDFDocument52 paginiProcesare Cu Radiaţii Ionizante PDFGeanina SorocanÎncă nu există evaluări
- Logistic ADocument37 paginiLogistic AAndreea MaresÎncă nu există evaluări
- Fabrica de Obtinere A Conservelor Din CarneDocument18 paginiFabrica de Obtinere A Conservelor Din CarneTitus AlexandruÎncă nu există evaluări
- Durata de ValabilitateDocument10 paginiDurata de ValabilitateAlina CormanÎncă nu există evaluări
- Tehnologia de Obtinere A ConservelorDocument48 paginiTehnologia de Obtinere A ConservelorDaniela BădescuÎncă nu există evaluări
- Analiza Senzoriala Si Fizico-Chimica A Branzei de BurdufDocument26 paginiAnaliza Senzoriala Si Fizico-Chimica A Branzei de Burdufneculavali3314Încă nu există evaluări
- CarneDocument16 paginiCarneIspas GeorgianaÎncă nu există evaluări
- Modulul V Distrugerea VitaminelorDocument29 paginiModulul V Distrugerea VitaminelorElena KuhaskÎncă nu există evaluări
- ST-34 - Paine Neagra Cu Seminte 2013Document5 paginiST-34 - Paine Neagra Cu Seminte 2013Iulia Georgescu100% (1)
- Proiect MSADocument764 paginiProiect MSApopaÎncă nu există evaluări
- Managementul Calitatii TotDocument41 paginiManagementul Calitatii TotTinikuVilenkaÎncă nu există evaluări
- Test Conserve Din Carne v2Document2 paginiTest Conserve Din Carne v2Ivan Diana LutaÎncă nu există evaluări
- Ambalat in Vid Si Cu Atmosfera ModificataDocument9 paginiAmbalat in Vid Si Cu Atmosfera ModificataAnonymous DZywhAÎncă nu există evaluări
- Modernizarea Tehnologiei de Fabricare A Salamului "Pâine Din Carne"Document71 paginiModernizarea Tehnologiei de Fabricare A Salamului "Pâine Din Carne"Lidia LunguÎncă nu există evaluări
- Pastrama de PorcDocument21 paginiPastrama de PorcOvidiu CorocaescuÎncă nu există evaluări
- PHG Uleiuri Vegetale ComestibileDocument28 paginiPHG Uleiuri Vegetale ComestibileAngela PelinÎncă nu există evaluări
- Pasul 4 - Diagrama de FluxDocument2 paginiPasul 4 - Diagrama de FluxIonela VișinescuÎncă nu există evaluări
- Microbiologia Carnii de PesteDocument15 paginiMicrobiologia Carnii de Pestee3lenaÎncă nu există evaluări
- T2.Determinarea Aciditatii Totale Din Semiconserve Si Conserve de Peste PDFDocument3 paginiT2.Determinarea Aciditatii Totale Din Semiconserve Si Conserve de Peste PDFIuliaFloreaÎncă nu există evaluări
- Referat Tehnologia de Obtinere A MargarineiDocument26 paginiReferat Tehnologia de Obtinere A MargarineiDany LazarÎncă nu există evaluări
- Ghid de Bune PracticiDocument42 paginiGhid de Bune PracticiBadoi Elena-Adriana100% (1)
- CARNEfinalDocument8 paginiCARNEfinalgeorge_rusuÎncă nu există evaluări
- Amine BiogeneDocument13 paginiAmine BiogeneRaluca Ieremita50% (2)
- 1 Elaborarea Planului HCCPDocument33 pagini1 Elaborarea Planului HCCPAna BurgheleaÎncă nu există evaluări
- Masina de Tocat Carne Proiect de An, Trebuie de ModificatDocument27 paginiMasina de Tocat Carne Proiect de An, Trebuie de ModificatRostislava ZubcoÎncă nu există evaluări
- Prajitura FantaDocument3 paginiPrajitura FantaBianca RotaruÎncă nu există evaluări
- Salam Banatean - BUNDocument38 paginiSalam Banatean - BUNCristian Macovei100% (1)
- Suport de Curs Sem II 2014Document50 paginiSuport de Curs Sem II 2014Daniel BarcanÎncă nu există evaluări
- LabalcDocument27 paginiLabalcElena RotariÎncă nu există evaluări
- CrenvurstiDocument6 paginiCrenvurstiChicheanu Auraş0% (1)
- Utilizarea Hormonilor in Industria AlimentaraDocument15 paginiUtilizarea Hormonilor in Industria AlimentaraК писÎncă nu există evaluări
- Despre Carne Si IgienaDocument65 paginiDespre Carne Si IgienaramonaÎncă nu există evaluări
- Metode Moderne de Monitorizare A Proceselor IndustrialeDocument21 paginiMetode Moderne de Monitorizare A Proceselor Industrialeriderofbikes100% (1)
- ReologiaDocument16 paginiReologiaAndriana Buzadji100% (1)
- Proiect Teh - CarniiDocument21 paginiProiect Teh - Carniiitla_soleÎncă nu există evaluări
- Sistemul de Analiză A Riscurilor În Punctele Critice de ControlDocument15 paginiSistemul de Analiză A Riscurilor În Punctele Critice de ControlDiana GeorgianaÎncă nu există evaluări
- Inspectia Si Controlul Alimentelor IDocument5 paginiInspectia Si Controlul Alimentelor ICosmin ConstantinÎncă nu există evaluări
- Implementarea Sistemului HACCP Pentru Conservele Din CarneDocument38 paginiImplementarea Sistemului HACCP Pentru Conservele Din CarneAlexandru SimaÎncă nu există evaluări
- Laborator 3 Spccpa Decontaminarea Cu Ozon A Produselor AlimentareDocument10 paginiLaborator 3 Spccpa Decontaminarea Cu Ozon A Produselor AlimentareOpreaÎncă nu există evaluări
- Electrotehnologii Cu OzonDocument24 paginiElectrotehnologii Cu OzonmihaiÎncă nu există evaluări
- OzonizareaDocument17 paginiOzonizareacioranu_ionÎncă nu există evaluări
- Dezinfectia Cu OzonDocument2 paginiDezinfectia Cu OzonIulia Darabus100% (1)
- Caracterizarea Generală A OxigenuluiDocument6 paginiCaracterizarea Generală A Oxigenuluidana.iancu2906Încă nu există evaluări
- Ozonul ReferatDocument4 paginiOzonul ReferatDinu ZinveliÎncă nu există evaluări
- Distrugerea Stratului de OzonDocument21 paginiDistrugerea Stratului de OzonGigel FrezatuÎncă nu există evaluări
- Microbiologie GeneralaDocument123 paginiMicrobiologie GeneralaGeorge CioacaÎncă nu există evaluări
- Curs ExpertizaDocument165 paginiCurs ExpertizaGeorge Cioaca100% (1)
- Microbiologie Speciala Curs .Document259 paginiMicrobiologie Speciala Curs .George Cioaca100% (1)
- Referat George - Uleiurile Volatile FinalDocument30 paginiReferat George - Uleiurile Volatile FinalGeorge Cioaca100% (1)
- CursDocument279 paginiCursGeorge CioacaÎncă nu există evaluări
- Plan Haccp LicentaDocument8 paginiPlan Haccp LicentaGeorge CioacaÎncă nu există evaluări
- Referat George - Uleiurile Volatile FinalDocument30 paginiReferat George - Uleiurile Volatile FinalGeorge Cioaca100% (1)
- CONTINUT REFERAT Final PT Curs NutrientiDocument2 paginiCONTINUT REFERAT Final PT Curs NutrientiGeorge CioacaÎncă nu există evaluări